المضادات الحيوية (Antibiotics) أدويةٌ تُستخدم لعلاج العدوى البكتيرية، ولها دور فاعل في زيادة متوسط العمر وتقليل انتشار الأمراض والوفيات الناتجة من الأوبئة المُعدية. تعمل المضادات الحيوية من خلال طرق عديدة، مثل: إيقاف تخليق جدار الخلية، أو تعطيل وظيفة غشاء الخلية، أو منع إنتاج البروتينات أو الحمض النووي البكتيري.
تُصنّف المضادات الحيوية إلى عدة مجموعات بناءً على تركيبها الكيميائي ومصدرها وآلية عملها ونوع نشاطها، وتشمل البيتا لاكتام، والماكروليدات، والسلفوناميدات، والتتراسيكلينات، والأمينوغليكوزيدات، والكينولونات. تختلف مصادر هذه المضادات بين مركبات طبيعية مثل
البنسلين والجنتاميسين، وأخرى شبه اصطناعية مثل الأمبيسيلين والأميكاسين، بالإضافة إلى المضادات الحيوية الاصطناعية مثل الموكسيفلوكساسين والنورفلوكساسين.
تتفاوت فعالية المضادات الحيوية بين تلك ذات النطاق الواسع وأخرى ذات النطاق الضيق. ومع ذلك، أدّى الاستخدام المفرط للمضادات الحيوية إلى مشكلة صحية خطيرة تمثلت في ظهور المقاومة البكتيرية. لذا، من الضروري تطوير علاجات جديدة للتغلب على هذه المقاومة، واستكشاف المركّبات الطبيعية ذات الخصائص المضادة للبكتيريا بصفتها بدائل واعدة للمضادات الحيوية التقليدية.
تعريف المضادات الحيوية
المضادات الحيوية أدويةٌ تُستَخدَمُ لمعالجة العدوى البكتيرية عن طريق القضاء عليها أو منعها من التكاثُر أو تثبيط نموها. تعَدّ المضادات الحيوية من أنجح اكتشافات الأدوية في تاريخ الإنسانية، وأصبحت أساسًا في محاربة الأمراض المعدية، وأسهمت بشكل كبير في التطوّر الصحّي الهائل؛ إذ أنقذت أرواحًا لا حصر لها منذ اكتشافها في أوائل القرن العشرين. وتؤدّي المضادات الحيوية دورًا بارزًا في زيادة متوسط العمر للأفراد عن طريق تقليل انتشار الأمراض والوفيات المرتبطة بالأوبئة السارية. ومنذ ذلك الحين، استمرت المضادات الحيوية بجذب اهتمام الباحثين من مختلف المجالات الطبية بسبب الأدوار المتعددة التي تؤدّيها في مكافحة الأمراض المختلفة التي تهدد صحة الإنسان[1].
تاريخها
في القرن السابع عشر، اكتشف العالم أنطوني فان ليفينهوك (Antonie van Leeuwenhoek، 1632-1723) البكتيريا، ولاحظ وجود علاقة بين هذه الكائنات الحية الدقيقة والأمراض. وقد شجّع ذلك العديدَ من العلماء على البحث لإيجاد مواد جديدة قادرة على قتل البكتيريا أو منع أو تثبيط نمو البكتيريا المسبّبة للعلل. عجزت الإنسانية عن مواجهة الموجات العاتية من الأوبئة عصورًا عدّة، مثل: الكوليرا، والجدري، والطاعون، وحمّى التيفوئيد، والملاريا، والسل، وغيرها، بسبب عدم معرفتها بطبيعة العدوى وعدم توفّر المضادات الحيوية واللقاحات (Vaccines)، وتحسّنَ ذلك تدريجيًّا مع اكتشاف العديد من الكائنات الحية الدقيقة المنتجةِ المضاداتِ الحيويةَ، وهو ما يُعَدّ بداية تطور الطب الحديث[2].
إن اكتشاف المضادات الحيوية والمعرفة الواسعة بمسببات الأمراض أدّى إلى تحسين نوعية الحياة للإنسان، إذ اكتشف العالم بول إرليخ (Paul Ehrlich، 1854-1915) دواءَ الأرسفينامين (Arsphenamine) لمعالجة مرض الزهري في عام 1909، ثم استُبدل بالبرونتوزيل (Prontosil) الذي يُعَدّ عقارًا أوليًّا من السلفوناميد (Sulfonamide)، واكتشفه العالم غيرهارد دوماك (Gerhard Domagk، 1895-1964)، وكان من المضادات الفعّالة للميكروبات واسعة النطاق (Broad spectrum antibiotics)[3] ، ثم توالت بعد ذلك الاكتشافات حتى نجح العالم ألكسندر فليمنغ (Alexander Fleming، 1881-1955) في عزل
البنسلين من فطر البنسيليوم نوتاتوم (Penicillium notatum). وفي عام 1945، طُوِّرَت مشتقات جديدة شبه اصطناعية للتغلب على مقاومة البكتيريا للبنسلين[4].
استطاع العالم سلمان واكسمان (Selman Waksman، 1888-1973)، في عام 1943، عزلَ الستربتوميسين (Streptomycin) من الشّعيات (Actinomycetes)، وهو أول مركب أمينوغليكوزيد (Aminoglycoside) لعلاج مرض السل. بعد ذلك، تعرّف العالم الإيطالي جوزيبي بروتزو (Giuseppe Brotzu، 1895-1976) على مجموعة السيفالوسبورينات (Cephalosporins)، إذ عزل نوعين من السيفالوسبورين P وN من فطر سيفالوسبرينيوم أكريمونيوم (Cephalosporium acremonium)، واستُخدِم بوصفه مضادًا حيويًا فعّالًا
للبكتيريا إيجابية الغرام {{البكتيريا إيجابية الغرام: نوع من البكتيريا تحتفظ بصبغة الغرام البنفسجية أثناء اختبار تلوين غرام (Gram staining)، ويعزى ذلك إلى جدارها الخلوي السميك الغني بالببتيدوغليكان، وتشمل هذه البكتيريا عدة أنواع مثل المكورات العنقودية (Staphylococcus) والمكورات العقدية (Streptococcus).}} (Gram-positive bacteria)
والبكتيريا سلبية الغرام {{البكتيريا سلبية الغرام: نوع من البكتيريا لا تحتفظ بصبغة الغرام البنفسجية أثناء اختبار تلوين غرام، بسبب تركيب جدارها الخلوي. فتتميز بجدار خلوي رقيق يحتوي على طبقة رقيقة من الببتيدوغليكان، وتأخذ اللون الأحمر أو الوردي بعد التلوين بصبغة غرام. ومن الأمثلة عليها الإشريكية القولونية (Escherichia coli) والسلمونيلا (Salmonella).}} (Gram-negative
bacteria) على التوالي[5].
لاحقًا، توالت الأبحاث، ووُجِدَت العديد من أنواع المضادات الحيوية، خصوصًا الطبيعية والمستخرجة من الشّعيات، مثل: الأمينوغليكوزيدات، والتتراسيكلين (Tetracyclines)، والأمفينيكولات (Amphenicols)، والماكروليدات (Macrolides)، والغليكوببتيدات (Glycopeptides)، والأنساميسين (Ansamycins)، واللينكوساميدات (Lincosamides)، والستربتوغرامين (Streptogramins)، والسيكلوسيرين (Cycloserine)، وكذلك المضادات الحيوية المعزولة من الفطريات مثل البنسلينات، والسيفالوسبورينات، بالإضافة إلى المضادات الحيوية الاصطناعية، مثل: السلفونات (Sulfones)، والنيتروفوران (Nitrofurans)، والكينولونات (Quinolones)، والآزولات (Azole)، والفينازينات (Phenazines)، والإيثامبوتول (Ethambutol)، والثيواميدات (Thioamide). ونظرًا إلى زيادة مقاومة الميكروبات لهذه المضادات فقد انخفضت كفاءتها العلاجية[6].
في عام 1980، طُوِّرت علاجات كيميائية واسعة النطاق ومضادة للبكتيريا من نوع البيتا لاكتام (β-lactam)، مثل: الكاربابينيمات (Carbapenems)، والأحادية الباكتام (Monobactams). وبحلول عام 2000، أُنتجت مضادات حيوية جديدة من منتجات طبيعية، مثل: الدابتومايسين (Daptomycin) والريتابامولين (Retapamulin)، وأخرى من مركّبات مشتقة اصطناعيًا تنتمي إلى مجموعة الكوينولون والأوكسازوليدينون (Oxazolidinone)، مثل مركب اللينيزوليد (Linezolid)[7].
تصنيفها
تُصَنَّف المضادات الحيوية إلى عدة مجموعات استنادًا إلى تركيبها الكيميائي، ومصدرها، وآلية عملها ونوعه، وكذلك سعة نطاق نشاطها[8]. أدّى اختلاف تركيب المضادّات من الناحية الكيميائية إلى وجود العديد من الفئات التي تضم البيتا لاكتام، والماكروليدات، والسلفوناميدات، والتتراسيكلينات، والأمينوغليكوزيدات، والكينولونات. وتضم مجموعة البيتا لاكتام: البنسلينات، والسيفالوسبورينات، والكاربابينيمات، وأحادية الباكتام. كما تتنوع مصادر المضادات الحيوية من مركبات حيوية طبيعية تُستَخرَج من الكائنات الحية الدقيقة، مثل: البنزل بنسلين (Benzylpenicillin)، والجنتاميسين (Gentamicin)، إلى مضادات حيوية شبه اصطناعية كالأمبيسيلين (Ampicillin)، والأميكاسين (Amikacin)، ومضادات حيوية اصطناعية كالموكسيفلوكساسين (Moxifloxacin)، والنورفلوكساسين (Norfloxacin)[9].
تتنوع فعالية المضادات بين
المضادات الحيوية ذات النطاق الواسع {{المضادات الحيوية ذات النطاق الواسع: تُعرف أيضًا بالمضادات الحيوية واسعة الطيف، وهي مضادات فعالة ضد البكتيريا إيجابية الغرام وسلبية الغرام. وتستخدم لعلاج مجموعة واسعة من العدوى البكتيرية خاصة عندما لا يكون نوع البكتيريا المسببة للعدوى معروفًا بدقة، أو في حالات العدوى المختلطة والتي تشمل أكثر من نوع من البكتيريا.}} (Broad spectrum antibiotics) وتلك
ذات النطاق الضيق {{المضادات الحيوية ذات النطاق الضيق: نوع من المضادات تستخدم لعلاج العدوى الناتجة عن أنواع محددة من البكتيريا، وتكون فعّالة إما ضد البكتيريا إيجابية أو سلبية الغرام، وليس كلاهما. ويُفضل استخدامها عندما يكون نوع البكتيريا المسببة للعدوى معروفًا، وذلك لتقليل خطر تطوّر المقاومة البكتيرية والحد من التأثير السلبي على البكتيريا النافعة في الجسم.}} (Narrow spectrum antibiotics). تُعدّ المضادات الحيوية واسعة النطاق فعّالة ضد جميع أنواع البكتيريا سواء أكانت إيجابية الغرام أو سلبية الغرام، ومن الأمثلة على ذلك المكوّرات العنقودية (Staphylococci)، والمكورات العقدية (Streptococci)، وبعض أنواع البكتيريا اللاهوائية مثل الليستيريا المستوحدة (listeriaMonocytogenes). في المقابل، تُظهر المضادات الحيوية ذات النطاق الضيّق فعاليةً ضد البكتيريا إيجابية الغرام أو البكتيريا سلبية الغرام فقط، مثل الكليبسيلا (Klebsiella) والإشريكية القولونية (Escherichia coli). يُعدّ استخدام المضادات الحيوية ذات النطاق الضيق أكثر فائدة بسبب خصوصيتها لأنواع معينة من البكتيريا، وتقليل مقاومة البكتيريا لها بالمقارنة مع المضادات واسعة النطاق التي قد تؤثر في البكتيريا الضارة والنافعة على حد سواء[10].
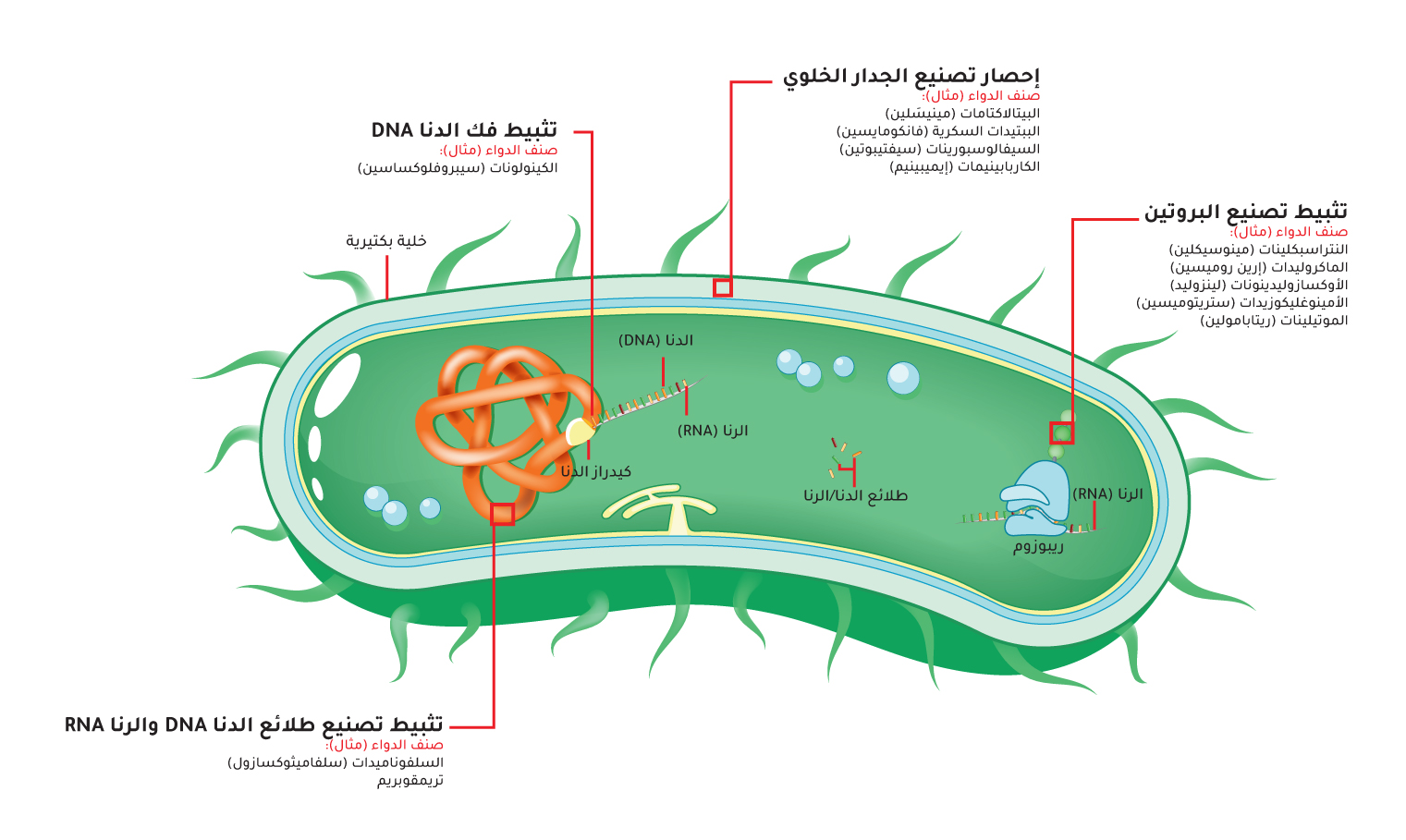
تبيد المضادات الحيوية الجراثيم عن طريق وقف تخليق جدار الخلية، أو إخفاق وظيفة غشاء الخلية، أو إفشال إنتاج البروتين البكتيري أو الحمض النووي (الشكل1). وتشمل مبيدات الجراثيم مجموعة البيتا لاكتام، والأمينوغليكوزيدات، والغليكوببتيدات، والنساميسين (Nsamycins)، والكينولونات، والستربتوغرامين (Streptogramin)، والببتيدات الدهنية (Lipopeptides)، والماكروليدات، في حين تُثبّط أنواع أخرى من المضادات الجراثيمَ عن طريق وقف النشاط الخلوي البكتيري (Bacteriostatic) من دون تحفيز موت الخلية، وتشمل: السلفوناميدات، والتتراسيكلين، والكلورامفينيكول، والأوكسازوليدينونز (Oxazolidinones)، والماكروليدات[11].
تعدّ وظيفة تخليق البروتين البكتيري حيوية ومهمة لبقاء البكتيريا. إذ يمكن إضعاف هذه العملية باستخدام المضادات الحيوية من خلال ارتباطها بوحدات الريبوسوم 30S أو S05. ومن هذه المضادات الحيوية الأمينوغليكوزيدات، والماكروليدات، والتتراسيكلين، والستربتوغرامين، والكلورامفينيكول، والكليندامايسين (Clindamycin)، وغيرها.
يُعَدّ توقيف تخليق الحمض النووي داخل الخلايا البكتيرية أمرًا حيويًا للدور الذي تؤديه المضادات الحيوية. ويتم ذلك عبر تثبيط عمل الإنزيمات المسؤولة عن إنتاج الحمض النووي الريبي منقوص الأكسجين (Deoxyribonucleic Acid, DNA) أو الحمض النووي الريبي (Ribonucleic Acid, RNA).
[الشكل 1]
 المصدر : https://www.shutterstock.com/image-vector/antibiotics-mechanisms-action-antibacterial-drugs-disruption-1966859002
المصدر : https://www.shutterstock.com/image-vector/antibiotics-mechanisms-action-antibacterial-drugs-disruption-1966859002
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
المضادات الحيوية التي تُعرف باسم مثبّطات البوليميراز (Polymerase)، مثل: الريفاميسين (Rifamycin)، والفيداكسوميسين (Fidaxomicin)، والليبيارميسين (Lipiarmycin)، تُحبط عملية تخليق الحمض النووي الريبي (RNA)، ومن ثَمّ تضعف قدرة الخلية على البقاء، في حين تثبّط أنواع أخرى من المضادات كالكينولونات، والميترونيدازول (Metronidazole) تخليق الحمض النووي (DNA) داخل الخلايا البكتيرية عبر التدخل في نشاط النوع الثاني من إنزيمات توبوآيزوميراز (Type II topoisomerase)[12].
تؤثر بعض أنواع المضادات الحيوية، مثل: التريميثوبريم (Trimethoprim) والسلفوناميدات، في
استقلاب (Metabolism) حمض الفوليك، ويتم ذلك من خلال تأثيرها في إنزيم ثنائي هيدروفولات ريدوكتاز (Dihydrofolate reductase) الذي له دور كبير في تخليق الثيميديلات (Thymidylate) ومضاعفة الحمض النووي وبقاء الخلية (الجدول 1)[13].
[الجدول 1]
آلية عمل المضادات الحيوية
مكان العمل |
آلية العمل |
الأمثلة |
|---|
الجدار الخلوي البكتيري | قتل الجراثيم | مجموعة البيتا لاكتام، والأمينوغليكوزيدات، والغليكوببتيدات، والنساميسين، والكينولونات، والستربتوغرامين، والببتيدات الدهنية، والماكروليدات |
تثبيط الجراثيم | السلفوناميدات، والتتراسيكلين، والكلورامفينيكول، والأوكسازوليدينونز، والماكروليدات |
البروتين البكتيري
| قتل الجراثيم | الأمينوغليكوزيدات |
تثبيط الجراثيم | التتراسيكلين، والكلورامفينيكول |
بتراكيز قليلة مثبطة للجراثيم وبتراكيز عالية قاتلة للجراثيم | الماكروليدات والكليندامايسين |
الحمض النووي البكتيري
| تثبيط عملية تخليق الحمض النووي الريبي (RNA) | مثبطات البوليميراز (الريفاميسين، الفيداكسوميسين، والليبيارميسين) |
تثبيط عملية تخليق الحمض النووي (DNA) | مثبطات التوبوآيزوميراز II (الكالكوينولونات والميترونيدازول) |
حمض الفوليك
| التأثير في إنزيم ثنائي الهيدروفولات الذي له دور كبير في تخليق الثيميديلات ومضاعفة الحمض النووي وبقاء الخلية | التريميثوبريم والسلفوناميدات |
آثارها الجانبية
تظهر للمضادات الحيوية آثار جانبية عامة أو خاصة، وقد لوحظت هذه الآثار بشكل محدد على المرضى الذين يعانون من خلل في وظائف الكلى أو الكبد، وكذلك بعد تناول المضادات الحيوية بجرعات عالية ولفترات زمنية طويلة. كما تحتل هذه الأدوية المركز الثاني بوصفها مسببةً للآثار الجانبية المرتبطة بسوء الممارسة الطبية. ومن التأثيرات الجانبية الأكثر شيوعًا
فرط الحساسية (Hypersensitivity)، والآثار السيئة على الجهاز العصبي، والجهاز الهضمي، والكلى، والقلب، والرئة، والكبد. ومن الجدير بالذكر أن معظم هذه الآثار الجانبية لا يمكن التنبؤ بها، وبناء عليه يصبح من الضروري فهم آلية عمل المضادات الحيوية ونوعها؛ فعلى سبيل المثال، أثبت
البنسلين فعاليته في علاج الالتهاب الرئوي، والستربتوميسين في علاج السل، والكلورامفينيكول في علاج حمّى التيفوئيد، وكانت الآثار الجانبية لهذه العلاجات محدودة نسبيًا[14].
مقاومة البكتيريا للمضادات الحيوية
يُقصَد بمقاومة المضادات الحيوية قدرةُ الكائنات الحية الدقيقة على تثبيط فعالية المركّبات المضادة للميكروبات، وتظهر هذه المقاومة عندما تفقد المضادات الحيوية كفاءتها على تقليل نمو البكتيريا. وعلى الرغم من أن الأمراض المعدية حوربت بنجاح فترةً طويلة باستخدام المضادات الحيوية، فإنّ ظهور البكتيريا المقاوِمة فتح فجوة جديدة أصبح من الصعب التغلّب عليها في الوقت الحاضر. تطرأ على البكتيريا بمرور الوقت تغييرات لتتكيف مع التحديات البيئية. ومن الأمثلة على ذلك، المكوّرات العنقودية الذهبية التي كانت في بداية اكتشافها حساسة للبنسلين، ولكن مع مرور الوقت أصبح
البنسلين غير فعّال ضدها، إذ طوّرت السلالات البكتيرية إنزيمات قادرة على تجاوز تأثير
البنسلين. وللحد من هذه المقاومة، طُوِّرت أشكال جديدة من
البنسلين المحصّن ضد تلك الإنزيمات، ولكن بعد بضعة أعوام، تكيّفت البكتيريا وأصبحت مقاوِمة أيضًا للأدوية الجديدة؛ وهكذا زادت نسبة البكتيريا المقاومة للمضادات الحيوية على مر الأعوام[15].
إن الاستخدام المفرط وغير المنظم للمضادات الحيوية بالإضافة إلى عدم صرفها بوصفات طبية أدّى إلى زيادة مستوى مقاومة البكتيريا لها، ومن الضروري إيجاد أساليب تحافظ على فعاليتها، مع العلم أنه لا يوجد فئة من المضادات الحيوية تفتقر إلى المقاومة البكتيرية. كما تمثّل مقاومة المضادات الحيوية مشكلة صحية خطيرة، إذ يتوقع أن تصل حالات الوفاة إلى أكثر من 10 ملايين حالة وفاة سنويًّا بحلول العام 2050. كما أن العديد من المنظمات، مثل
منظمة الصحة العالمية {{منظمة الصحة العالمية: (World Health Organization, WHO) وكالة متخصصة تابعة للأمم المتحدة، تأسست عام 1948. يقع مقرها الرئيسي في جنيڤ، سويسرا. تعمل على مستوى العالم لتنسيق الاستجابات للقضايا والطوارئ الصحية العامة الدولية، وذلك بهدف تعزيز الصحة، ومراقبة الأمراض والوقاية منها، وحماية العالم من الأوبئة، ودعم الدول في تحسين نظامها الصحي.}}، عدّت المقاومة البكتيرية مشكلة كبيرة يتعيّن الحد من انتشارها. ومن المهم اعتماد خطط عالمية فعّالة لمنع حدوث مضاعفات اجتماعية وطبية واقتصادية. لذلك، يجب فهم طريقة عمل المضادات الحيوية مع اعتماد الوصفات الطبية الملائمة بهدف تقليل سمّيتها والحد من مقاومة البكتيريا لها[16].
إن الزيادة المستمرة في مقاومة المضادات الحيوية وارتفاع حصيلة الوفيات الناتجة من ذلك، أدّى إلى ضعف الاهتمام بتطوير أصناف جديدة من المضادات الحيوية، إذ زاد الاهتمام بين العلماء للبحث عن بدائل علاجية جديدة للمضادات الحيوية التقليدية، وذلك باستخدام مركّبات طبيعية(Natural compounds) ، مثل: الفينولات (Phenols) والبوليفينولات (Polyphenols)، وغيرها. تتميز هذه المركبات الطبيعية بفعاليتها في معالجة الالتهابات البكتيرية وقدرتها على التغلب على مقاومة البكتيريا وتقليل الآثار الجانبية. وعلى الرغم من التقدم الكبير في هذا المجال، فإنّ هناك حاجة ملحّة إلى إجراء المزيد من الأبحاث لتوضيح آلية عمل هذه المركّبات والتحقق من تآزرها مع المضادات الحيوية التقليدية بوصفها بديلًا فعّالًا لمكافحة المقاومة البكتيرية[17].
المراجع
Alvarez-Martinez, F. J., Enrique Barrajón-Catalán & Vicente Micol. “Tackling Antibiotic Resistance with Compounds of Natural Origin: A comprehensive Review.” Biomedicines. vol. 8, no. 10 (2020).
Džidić, S., J. Šušković & B. Kos. “Antibiotic Resistance Mechanisms in Bacteria: Biochemical and Genetic Aspects.” Food Technology & Biotechnology. vol. 46, no. 1 (2008).
Ebimieowei, Etebu & Ibemologi Arikekpar. “Antibiotics: Classification and Mechanisms of Action with Emphasis on Molecular Perspectives.”
International Journal of Applied Microbiology and Biotechnology Research. vol. 4 (2016).
Everts, S. “Antibiotic Side Effects Explained.”
Chemical & Engineering News Archive. vol. 91. p. 9 (2013).
Hooper, David C. & George A. Jacoby. “Topoisomerase Inhibitors: Fluoroquinolone Mechanisms of action and Resistance.”
Cold Spring Harb Perspect in Medicine. vol. 6. article no. a025320 (2016).
Hutchings, M. I., Andrew W. T. & Barrie W. “Antibiotics: past, present and Future.” Current Opinion in Microbiology. vol. 51 (2019).
Iyer, Harish V. “History Revisited-Prontosil Red.”
The Journal of Emergency Medicine. vol. 35 (2008).
Kapoor, G., Saurabh S. & Ashok E. “Action and Resistance Mechanisms of Antibiotics: A guide for Clinicians.” Journal of Anaesthesiology Clinical Pharmacology. vol. 33, no. 3(2017).
Kohanski, Michael A., Daniel J Dwyer & James J Collins. “How Antibiotics Kill Bacteria: From Targets to Networks.”
Nature Reviews Microbiology. vol. 8 (2010).
Kumavath, Ranjith (ed.). Antibacterial agents. (London: InTech, 2013).
Ma, Cong, Xiao Yang & Peter J. Lewis. “Bacterial Transcription as a Target for Antibacterial Drug Development.” Microbiology and Molecular Biology Reviews. vol. 80, no. 1 (2016).
Morales-Alvarez, M. C. “Nephrotoxicity of Antimicrobials and Antibiotics.” Advances in Chronic Kidney Disease. vol. 27, no. 1 (2020).
Muteeb, Ghazala et al. “Origin of Antibiotics and Antibiotic Resistance, and Their Impacts on Drug Development: A Narrative Review.” Pharmaceuticals. vol. 16, no. 11 (2023).
Overview of Antibiotics—Infections. Kenilworth, NJ: Merck & Co., 2020
Pancu, Daniel Florin et al. “Antibiotics: Conventional Therapy and Natural Compounds with Antibacterial Activity—a Pharmaco-Toxicological Screening.” Antibiotics. vol. 10, no. 4 (2021).
Putri, cindy Ivana et al. “Literature Review: Kejadian Resistensi Pada Penggunaan Antibiotik.” Medical Profession Journal of Lampung. vol. 13, no. 3 (2013).
Rouveix, B. “Antibiotic Safety Assessment.” International Journal of Antimicrobial Agents. vol. 21 (2003).
StatPearls Publishing. Treasure Island, FL: StatPearls Publishing, 2025. Accessed on:
https://www.ncbi.nlm.nih.gov/books/NBK547678/
Takó, Miklós et al. “Plant Phenolics and Phenolic-enriched Extracts as Antimicrobial Agents Against Food-contaminating Microorganisms.”
Antioxidants. vol. 9, no. 2 (2020).
Waksman, Selman A., Albert Schatz & Donald M. Reynolds. “Production of Antibiotic Substances by Actinomycetes.”
Annals of the New York Academy of Sciences. vol. 1213 (2010).
Wall, Stig. “Prevention of Antibiotic Resistance–an Epidemiological Scoping Review to Identify Research Categories and Knowledge Gaps.” Global Health Action. vol. 12, issue supl. 1 (2019).
Wróbel, A. et al. “Trimethoprim: An Old Antibacterial Drug as a Template to Search for New Targets. Synthesis, Biological Activity and Molecular Modeling Study of Novel Trimethoprim Analogs.”
Molecules. vol. 25, p. 116 (2019).
[1] Daniel Florin Pancu et al., “Antibiotics: Conventional Therapy and Natural Compounds with Antibacterial Activity—a pharmaco-Toxicological Screening,” Antibiotics, vol. 10, no. 4, p. 401 (2021).
[2]
Ibid.
[3] Harish V. Iyer, “History Revisited-Prontosil Red,”
The Journal of Emergency Medicine, vol. 35 (2008), pp. 209-2102.
[4] Pancu et al.
[5] Selman A. Waksman, Albert Schatz & Donald M. Reynolds, “Production of Antibiotic Substances by Actinomycetes,”
Annals of the New York Academy of Sciences, vol. 1213 (2010), pp. 112-124.
[6] Matthew I. Hutchings, Andrew W. Truman & Barrie Wilkinson, “Antibiotics: Past, Present and Future,” Current Opinion in Microbiology, vol. 51 (2019), pp. 72-80.
[7]
Ibid.;
Overview of Antibiotics—Infections, (Kenilworth, NJ: Merck & Co.: 2020).
[8] Hamid Ullah & Saqib Ali, “Classification of Anti-Bacterial Agents and Their Functions,” in: Ranjith Kumavath (ed.), Antibacterial Agents (London: InTech, 2013).
[9] Ullah & Ali; Pancu et al.
[10] Ullah & Ali; Etebu Ebimieowei & Arikekpar Ibemologi, “Antibiotics: Classification and Mechanisms of Action with Emphasis on Molecular Perspectives,”
International Journal of Applied Microbiology and Biotechnology Research, vol. 4 (2016), pp. 90-101.
[11] John Loree & Sarah L. Lappin, “Bacteriostatic Antibiotics,” in:
StatPearls Publishing (Treasure Island, FL: StatPearls Publishing, 2025), accessed on 15/7/2025 on:
https://www.ncbi.nlm.nih.gov/books/NBK547678/; Cong Ma, Xiao Yang & Peter J. Lewis, “Bacterial Transcription as a target for Antibacterial Drug Development,” Microbiology and Molecular Biology Reviews, vol. 80, no. 1 (2016), pp.139-160.
[12] David C. Hooper & George A. Jacoby, “Topoisomerase Inhibitors: Fluoroquinolone Mechanisms of action and Resistance,”
Cold Spring Harb Perspect in Medicine, vol. 6, article no. a025320 (2016).
[13] Michael A. Kohanski, Daniel J. Dwyer & James J. Collins, “How Antibiotics Kill Bacteria: From Targets to Networks,”
Nature Reviews Microbiology, vol. 8 (2010), pp. 423-435; Agnieszka Wróbel et al., “Trimethoprim: An Old Antibacterial Drug as a Template to Search for New Targets, Synthesis, Biological Activity and Molecular Modeling Study of Novel Trimethoprim Analogs,”
Molecules, vol. 25 (2019), p. 116.
[14] Bernard Rouveix, “Antibiotic Safety Assessment,”
International Journal of Antimicrobial Agents, vol. 21 (2003), pp. 215-221; Sarah Everts, “Antibiotic Side Effects Explained,”
Chemical & Engineering News Archive, vol. 91, no. 21 (2013), p. 9; Martha C. Morales-Alvarez, “Nephrotoxicity of Antimicrobials and Antibiotics,” Advances in Chronic Kidney Disease, vol. 27, no. 1 (2020), pp. 31-37.
[15] Garima Kapoor, Saurabh saigal & Ashok Elongavan, “Action and Resistance Mechanisms of Antibiotics: A Guide for Clinicians,” Journal of Anaesthesiology Clinical Pharmacology, vol. 33, no. 3 (2017), pp. 300-305; Ghazala Muteeb et al., “Origin of Antibiotics and Antibiotic Resistance, and Their Impacts on Drug Development: A Narrative Review,” Pharmaceuticals, vol. 16, no. 11 (2023); Cindy Ivana Putri et al., “Literature Review: Kejadian Resistensi Pada Penggunaan Antibiotik,” Medical Profession Journal of Lampung, vol. 13, no. 3 (2013), pp. 219-225.
[16] Francisco J. Alvarez-Martinez, Enrique Barrajón-Catalán & Vicente Micol, “Tackling Antibiotic Resistance with Compounds of Natural Origin: A comprehensive Review,” Biomedicines, vol. 8, no. 10 (2020); Senka Džidić, Jagoda Šušković & Blazenka Kos, “Antibiotic Resistance Mechanisms in Bacteria: Biochemical and Genetic Aspects,” Food Technology & Biotechnology, vol. 46, no. 1 (2008), pp. 11-21.
[17] Miklós Takó et al., “Plant Phenolics and Phenolic-Enriched Extracts as Antimicrobial Agents Against food-contaminating Microorganisms,”
Antioxidants, vol. 9, no. 2 (2020); Stig Wall, “Prevention of Antibiotic Resistance–an Epidemiological Scoping Review to Identify Research Categories and Knowledge Gaps,” Global Health Action, vol. 12, issue supl. 1 (2019).
