المورفين (Morphine) مادة مخدّرة طبيعية ومسكن أفيوني (Opioid analgesic) قوي، يُستخدم لتخفيف الآلام الحادة والمزمنة. استُخلص لأول مرة من بذور الخشخاش (Poppy seeds) عام 1805، وحصل على موافقة إدارة الغذاء والدواء الأمريكية (FDA) عام 1941 (الشكل 1). وعلى الرغم من فاعليته العلاجية العالية، فإنه يُصنف طبيًا وقانونيًا ضمن المواد التي قد تؤدي إلى الاعتماد الجسدي والإدمان في حال سوء الاستخدام.
[الشكل 1]
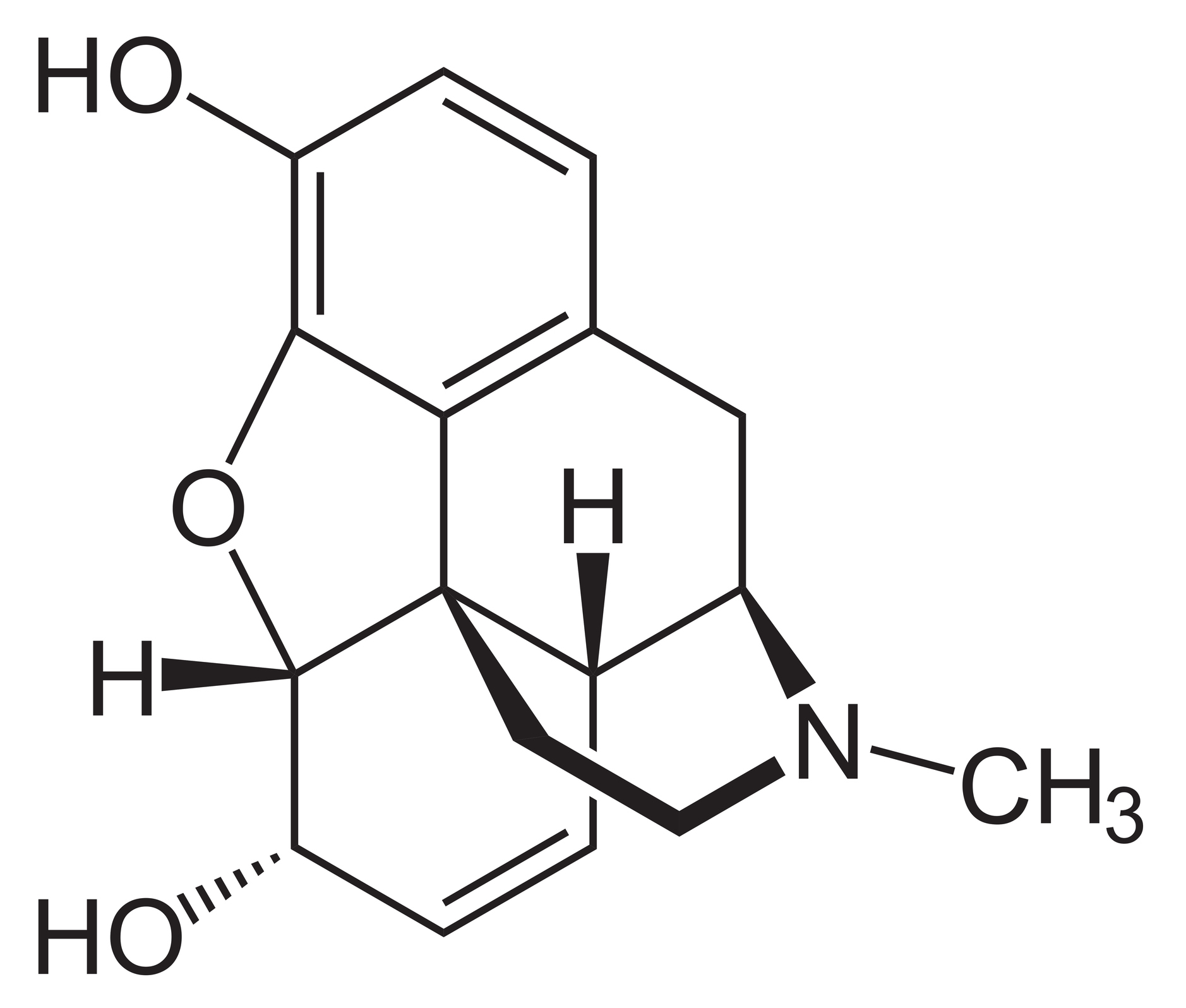 التركيب الكيميائي للمورفين
التركيب الكيميائي للمورفين
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
الاستخدامات وطريقة العمل
يُستخدم المورفين على نطاق واسع في علاج الآلام الحادة والمزمنة، سواء أكانت متوسطة أم شديدة. ويُعدّ من الأدوية الأساسية في الرعاية التلطيفية (Palliative care)، وعلاج آلام السرطان، والآلام الشديدة ما بعد الجراحة والإصابات الخطيرة، وكذلك في تخفيف الألم الناتج من نوبات انسداد الأوعية الدموية. كما يُستخدم لعلاج آلام الجهاز العضلي الهيكلي، وآلام البطن، وألم الصدر، والتهاب المفاصل، والصداع، وخصوصًا عند فشل العلاجات الأخرى. وعلى الرغم من فاعليته في تسكين الألم على المدى القصير، فإن استخدامه قد يؤدي إلى الاعتماد الجسدي والإدمان، مما يستدعي زيادة جرعة الدواء في بعض الحالات للحصول على التأثير نفسه، ويجعل ذلك من الصعب التوقف عن تناوله من دون التعرض لأعراض انسحابية (Withdrawal symptoms) مثل: التعرق، والأرق، والرجفة، والغثيان[1].
يعمل المورفين من خلال ارتباطه بمستقبلات الأفيون (Opioid receptors)، إذ يُعزى نحو 85 في المئة من تأثيراته إلى مُستقلبه النشط مورفين-6-غلوكورونيد (Morphine-6-glucuronide)، الذي يُحفّز مستقبلات الأفيون من النوعين مو (µ) وكابا (κ). ويُعدّ مستقبل مو الأفيوني مسؤولًا بشكل أساسي عن التأثيرات الدماغية للمورفين، إذ يُثبِّط المورفين انتقال إشارات الألم، ويُنشِّط الخلايا العصبية المسؤولة عن تنظيم الألم في النخاع الشوكي، كما يمنع نقل الإشارات من المستقبلات الألم الأولية إلى الخلايا الحسية في القرن الظهري (Dorsal horn sensory cells)، مما يقلل من الإحساس بالألم[2].
يُعطى المورفين عبر عدة طرق، منها الإعطاء الفموي سواء بإطلاق فوري أو ممتد، أو من خلال
الحقن الوريدي (Intravenous injection)، أو
الحقن العضلي (Intramuscular injection)، أو
الحقن فوق الجافية (Epidural injection)، أو
الحقن داخل النخاع الشوكي (Intrathecal injection).
ونظرًا إلى ارتفاع معدل الأيض الكبدي الأولي (Primary hepatic metabolism)، يجب أن تكون الجرعات الفموية أكبر بنحو ست مرات من الجرعات الوريدية لتحقيق التأثير العلاجي نفسه[3].
الأشكال الدوائية
يتوفر المورفين في عدة أشكال دوائية، مثل التحاميل (Suppositories)، والمحاليل الفموية (Oral solutions)، والأقراص تحت اللسان (Sublingual tablets). وتتراوح الجرعة الأولية للمورفين الوريدي للبالغين بين 2 و10 ملّيغرامات لكل 70 كيلوغرامًا من وزن الجسم، مع التأكيد على ضرورة استخدام أقل جرعة فاعلة لتسكين الألم. وتُعدَّل الجرعة تدريجيًا بناءً على استجابة المريض السريرية.
أما في حال الاستخدام الفموي للبالغين غير المعتادين على الأفيونات (Opioid-naive adults)، فتكون الجرعة المبدئية بين 15 و30 ملّيغرامًا كل أربع ساعات حسب الحاجة. وبالنسبة إلى الأطفال الذين يزيد وزنهم على 50 كيلوغرامًا، تبدأ الجرعة بـ15 ملّيغرامًا كل أربع ساعات، ولا يُنصح بتجاوز 30 ملّيغرامًا في الجرعة الأولى.
الآثار الجانبية
يُعدّ كلٌّ من الإمساك (Constipation)، والغثيان، والتقيؤ، والنعاس، واحتباس البول آثارًا جانبيةً شائعةً لاستخدام المورفين، إضافة إلى أنه قد يؤدي إلى انخفاض ضغط الدم وتباطؤ ضربات القلب؛ الأمر الذي يُسبِّب دوارًا شديدًا أو حتى فقدانًا للوعي في بعض الحالات. إضافة إلى ذلك، يُحدث المورفين تأثيرات غير مرغوب فيها في الجهاز العصبي المركزي، مثل النعاس الشديد والدوخة، مما يؤثر سلبيًا في قدرة الشخص على أداء أنشطته اليومية.
يُعدّ تثبيط الجهاز التنفسي (Respiratory depression) من بين أكثر الآثار الجانبية خطورةً للمورفين، إذ قد يُسبِّب تباطؤًا خطيرًا في التنفس، وقد يصل الأمر إلى توقفه تمامًا في حالات الجرعة الزائدة، مما يُشكّل خطرًا حقيقيًا على حياة المريض. وتشمل المخاطر الأخرى المرتبطة باستخدام المورفين احتمالية حدوث هلوسة أو تغيرات نفسية، تتراوح بين اضطرابات المزاج، والشعور بالارتباك أو القلق. وفي حالات نادرة، قد يُسبِّب تغيرات معرفيةً أو إدراكيةً، تؤثر في قدرة المريض على اتخاذ قرارات سليمة[4].
عند تناول المورفين بجرعات زائدة، قد يؤدي ذلك إلى الشعور بالنشوة (Euphoria)، والتهدئة (Sedation)، وتثبيط التنفس (Respiratory depression)، والنعاس (Somnolence)، وارتخاء عضلات الهيكل العظمي، وبرودة الجلد ورطوبته. كما قد يُسبِّب تضيّق حدقة العين (Miosis) أو توسّعها (Mydriasis) وفي الحالات الشديدة، قد تتطور الأعراض إلى وذمة رئوية (Pulmonary edema)، وبطء في ضربات القلب (Bradycardia)، وانخفاض ضغط الدم (Hypotension)، وتوقف القلب (Cardiac arrest)؛ الأمر الذي قد ينتهي بالوفاة[5].
لعلاج الجرعة الزائدة من المورفين، يُعطى الأكسجين لدعم التنفس، كما تُستخدم قابضات الأوعية الدموية (Vasopressors) في حال حدوث انخفاض في ضغط الدم، ويُعدّ
النالوكسون (Naloxone) العلاج النوعي لعكس تأثير المورفين، إذ يعمل مضادًا لمستقبلات الأفيونات[6].
وعلى الرغم من فاعلية المورفين، فإنه يجب استخدامه بحذر لدى المرضى الذين يعانون من تثبيط التنفس الشديد، أو الربو، أو مرض الانسداد الرئوي المزمن (Chronic obstructive pulmonary disease - COPD)، كما يُمنع استخدامه في حالات انسداد الأمعاء.
من الواجب كذلك تجنّب استخدام المورفين مع الأدوية الأخرى التي تسبب تثبيط التنفس، مثل الكحول، والمواد الأفيونية الأخرى، والبنزوديازيبينات (Benzodiazepines)، والباربيتورات (Barbiturates). يُنصح أيضًا بعدم استخدامه لدى المرضى الذين لديهم تاريخ من ردود الفعل التحسسية تجاهه، إضافة إلى توخي الحذر عند تناوله مع مثبطات أوكسيداز أحادي الأمين (monoamine Oxidase inhibitors - MAOIs)، إذ تُعزز هذه الأدوية تأثيره بشكل ملحوظ.
قد يُعزِّز المورفين تأثير مرخيات العضلات الهيكلية (Skeletal muscle relaxants)، مما يزيد احتمالية حدوث تثبيط في التنفس. وقد يؤدي الاستخدام المتزامن للمورفين مع مضادات الكولين (Anticholinergics)، أو الأدوية التي تمتلك خصائص مضادة للكولين إلى زيادة خطر احتباس البول والإمساك الشديد الذي قد يتطور إلى انسداد معوي شللي (Paralytic ileus)[7].
يُوصى باستخدام المورفين تحت إشراف طبي دقيق، مع ضرورة تحديد الجرعة بعناية، ومراقبة الحالة الصحية للمريض بشكل مستمر. كما يُنصح بعدم التوقف عن استخدامه فجأةً إذا كان قد استُخدِم فترات طويلة، بل يجب تقليل الجرعة تدريجيًا لتجنب أعراض الانسحاب.
المراجع
Boom, Merel et al. “Non-Analgesic Effects of Opioids: Opioid-Induced Respiratory Depression.”
Current Pharmaceutical Design. vol. 18, no. 37 (2012). pp. 5994-6004. doi: 10.2174/138161212803582469
Hess, Shane R. et al. “Safety and Side-Effect Profile of Intrathecal Morphine in a Diverse Patient Population Undergoing Total Knee and Hip Arthroplasty.”
European Journal of Orthopaedic Surgery & Traumatology. vol. 29, issue 1 (2019). 125-129. doi:
10.1007/s00590-018-2293-9
Junior, Joaquim Barbosa Leite et al. “Reversal of Morphine Conditioned Behavior by an Anti-Dopaminergic Post-Trial Drug Treatment During Re-consolidation.”
Behavioural Brain Research. vol. 359, (2019) 771-782. doi:
10.1016/j.bbr.2018.08.009
Nosek, Krzysztof et al. “Efficacy and Safety of Topical Morphine: A Narrative Review.”
Pharmaceutics. vol 14, issue 7, article 1499 (2022). doi:
10.3390/pharmaceutics14071499
Pacifici, Gian Maria. “Metabolism and Pharmacokinetics of Morphine in Neonates: A Review.”
Clinics. vol. 71, issue 8 (2016). pp. 474-480. doi:
10.6061/clinics/2016(08)11
Renard, Yves et al. “Non-Pulmonary Complications of Intrathecal Morphine Administration: A Systematic Review and Meta-Analysis with Meta-Regression.”
British Journal of Anaesthesia. vol. 133, issue 4 (2024). pp. 823-838. doi:
10.1016/j.bja.2024.05.045
Tylleskar, Ida et al. “Naloxone Nasal Spray–Bioavailability and Absorption Pattern in a Phase 1 Study.”
Tidsskrift for Den norske legeforening. vol. 139, no. 13 (2019). pp. 1-8. doi:
10.4045/tidsskr.19.0162
[1] Krzysztof Nosek et al., “Efficacy and Safety of Topical Morphine: A Narrative Review,”
Pharmaceutics, vol 14, issue 7, article 1499 (2022), pp. 1-11, doi:
10.3390/pharmaceutics14071499; Gian Maria Pacifici, “Metabolism and Pharmacokinetics of Morphine in Neonates: A Review,”
Clinics, vol. 71, issue 8 (2016), pp. 474-480, doi:
10.6061/clinics/2016(08)11
[2] Pacifici,
op. cit.; Joaquim Barbosa Leite Junior et al., “Reversal of Morphine Conditioned Behavior by an Anti-Dopaminergic Post-Trial Drug Treatment During Re-consolidation,”
Behavioural Brain Research, vol. 359 (2019), 771-782, doi:
10.1016/j.bbr.2018.08.009
[3] Shane R. Hess et al., “Safety and Side-Effect Profile of Intrathecal Morphine in a Diverse Patient Population Undergoing Total Knee and Hip Arthroplasty,”
European Journal of Orthopaedic Surgery & Traumatology, vol. 29, issue 1 (2019), pp. 125-129, doi:
10.1007/s00590-018-2293-9
[4] Merel Boom et al., “Non-Analgesic Effects of Opioids: Opioid-Induced Respiratory Depression,”
Current Pharmaceutical Design, vol. 18, no. 37 (2012), pp. 5994-6004, doi:
10.2174/138161212803582469
[5] Pacifici,
op. cit.; Yves Renard et al., “Non-Pulmonary Complications of Intrathecal Morphine Administration: A Systematic Review and Meta-Analysis with Meta-Regression,”
British Journal of Anaesthesia, vol. 133, issue 4 (2024), pp. 823-838, doi:
10.1016/j.bja.2024.05.045
[6] Ida Tylleskar et al., “Naloxone Nasal Spray–Bioavailability and Absorption Pattern in a Phase 1 Study,”
Tidsskrift for Den norske legeforening, vol. 139, no. 13 (2019), pp. 1-8, doi:
10.4045/tidsskr.19.0162
[7] Pacifici,
op. cit.