استئصال القناة الدافقة إجراء جراحيّ صغير ودائم، يهدف إلى منع مرور الحيوانات المنوية من الخصيتين إلى السائل المنوي. يوفر هذا الإجراء وسيلة موثوقة للتعقيم دون التأثير في الوظيفة الجنسية أو الإنتاج الهرموني، وهو الإجراء الأكثر فعالية وديمومة لمنع الحمل الذكري، ويتميز بالبساطة النسبية وارتفاع معدل النجاح. تنقل القناة الحيوانات المنوية من الخصيتين إلى الإحليل، بينما الخصيتان تنتجان الحيوانات المنوية وتفرزان التستوستيرون المسؤول عن الصفات الجنسية والرغبة الجنسية. تشمل الأساليب الجراحية التي يكون بها استئصال القناة الدافقة الطريقة التقليدية بلا مشرط، وأساليب حديثة مثل الكي الحراري، والفصل الطبقي، والسدادات الجراحية، مع اختلاف نسب الأمان والفعالية لكل تقنية. تؤثر المضاعفات المحتملة، قصيرة المدى وبعيدة المدى وانعكاساتهما في الوظيفة الجنسية والهرمونية، وإمكانية عكس العملية لإعادة الوظيفة الإنجابية وتقنيات المساعدة في الإنجاب، في قرار اختيار هذه الوسيلة. إضافة إلى ذلك، يحمل القرار أبعادًا نفسية واجتماعية مهمة، ما يجعل التقييم الشامل قبل العملية أمرًا ضروريًّا لضمان أفضل النتائج الصحية والنفسية.
تعريفه
استئصال القناة الدافقة (Vasectomy) هو إجراء جراحي صغير ودائم، يهدف إلى منع مرور الحيوانات المنوية من الخصيتين إلى السائل المنوي، ما يعني توفير وسيلة فعّالة وطويلة الأمد لمنع حدوث الحمل من جهة الذكور. يتميز هذا الإجراء ببساطته مقارنةً بالإجراءات الجراحية التناسلية الأخرى، مع معدلات نجاح عالية وخطر منخفض للمضاعفات. يمثل استئصال القناة الدافقة نهجًا متقدمًا في تنظيم النسل، إذ يجمع بين الأمان، والفعالية، والقدرة على الاستقلالية في التخطيط الأسري، مع الحفاظ على الوظيفة الجنسية الطبيعية[1] (الشكل 1).
وظائفه التشريحية والهرمونية
تؤدي الخصيتان دورًا محوريًّا في الجهاز التناسلي الذكري، إذ تُعدّان الموقع الأساسي لإنتاج الخلايا المنوية ضمن
الأنابيب المنوية الملتفة {{الأنابيب المنوية المتلفة: (Seminiferous Tubules) هي أنابيب دقيقة ملتفة داخل الخصية، تشكل الموقع الأساسي لإنتاج النطاف، إذ تنضج الخلايا الجرثومية ضمن بيئة محمية وخاضعة لتنظيم هرموني دقيق.}}، وهي هياكل دقيقة مغطاة بخلايا سيرتولي {{خلايا سيرتولي: (Sertoli cells) خلايا داعمة داخل الأنابيب المنوية، توفر الغذاء والحماية للخلايا الجرثومية، وتنسق عملية تكوين النطاف من خلال إشارات كيميائية دقيقة.}} التي توفر الدعم الغذائي والهيكلي لتطوير النطاف {{تطوير النطاف: (Spermatogenesis) عملية متسلسلة تتحول فيها الخلايا الجرثومية الأولية إلى حيوانات منوية ناضجة، تتم داخل الأنابيب المنوية تحت إشراف الخلايا الداعمة والهرمونات}}.
تُعرف عملية إنتاج الحيوانات المنوية باسم تكوين النطاف (Spermatogenesis)، وهي سلسلة معقدة من الانقسامات الخلوية والتحولات الشكلية التي تستغرق عادةً بين 64 و72 يومًا لإنتاج حيوان منوي ناضج قادر على التخصيب؛ وخلال هذه العملية، تنتقل الخلايا الجرثومية الأولية من مرحلة الانقسام المتساوي إلى المنصّف، ثم إلى مرحلة النضج، إذ يكتسب الحيوان المنوي ذيله ويصبح قادرًا على الحركة المستقلة.
بعد إتمام تكوينها، تنتقل الحيوانات المنوية إلى
البربخ {{البربخ: (Epididymis) هو أنبوب طويل ملتف فوق الخصية، يعمل كمستودع ونقطة نضج للحيوانات المنوية، إذ تكتسب القدرة على الحركة والخصوبة قبل انتقالها إلى الأسهر.}}، وهو هيكل ملتف يقع على طول الحافة الخلفية للخصية، إذ تكمل الحيوانات المنوية نضجها الوظيفي، وتكتسب القدرة على الحركة والإخصاب. يعمل البربخ مخزنًا فعالًا للحيوانات المنوية حتى لحظة القذف، مع توفير بيئة غنية بالبروتينات ونظام أيوني متوازن يحافظ على حيويتها.
عند حدوث القذف، تسلك الحيوانات المنوية مسار القناة الدافقة (Vas deferens)، وهي أنبوب بطول 30 إلى 35 سنتيمرًا يمر ضمن الحبل المنوي، ويحمل الحيوانات المنوية من البربخ نحو الحويصلات المنوية والبروستاتا (الشكل 1). في هذه المرحلة، تختلط الحيوانات المنوية بإفرازات الحويصلات المنوية والبروستاتا، التي تحتوي على سكريات، مثل الفركتوز، وبروتينات وإنزيمات ضرورية لتغذية الحيوانات المنوية وحماية الحمض النووي فيها، وتعزيز قدرتها على الحركة داخل البيئة النسائية.
على المستوى الهرموني، تحتوي الخصيتان على
خلايا لايديغ {{خلايا لايديغ: (Leydig cells) خلايا تقع بين الأنابيب المنوية، مسؤولة عن إنتاج هرمون التستوستيرون الذي يحفز نمو الخصية وتكوين النطاف والصفات الجنسية الثانوية.}} الموجودة في الفراغات بين الأنابيب المنوية، والتي تفرز هرمون التستوستيرون. يُعدّ التستوستيرون الهرمون الأساسي المسؤول عن تطوير الصفات الجنسية الثانوية للذكور، مثل نمو الشعر الخشن، وزيادة كتلة العضلات، والصوت الأعمق، كما يحفز الرغبة الجنسية ويدعم مسار تكوين النطاف. يضمن هذا التكامل بين الوظيفة التشريحية والإفراز الهرموني إنتاج حيوانات منوية ذات قدرة عالية على الإخصاب، ويبرز الدور الحيوي للقناة الدافقة بوصفها حلقةً محوريةً في سلسلة معقدة تبدأ بإنتاج النطاف وتنتهي بوصولها إلى البويضة لتفعيل عملية الإخصاب[2].
الأساليب الجراحية لاستئصال القناة الدافقة
تتباين الأساليب الجراحية لاستئصال القناة الدافقة بشكل ملحوظ بهدف تحقيق أعلى درجات الفعالية التعقيمية مع أدنى معدلات المضاعفات. وتختلف هذه الأساليب بحسب طريقة الوصول إلى القناة الدافقة وتقنيات إغلاقها، مع مراعاة التوازن بين البساطة التقنية والأمان الجراحي.
[الشكل1]
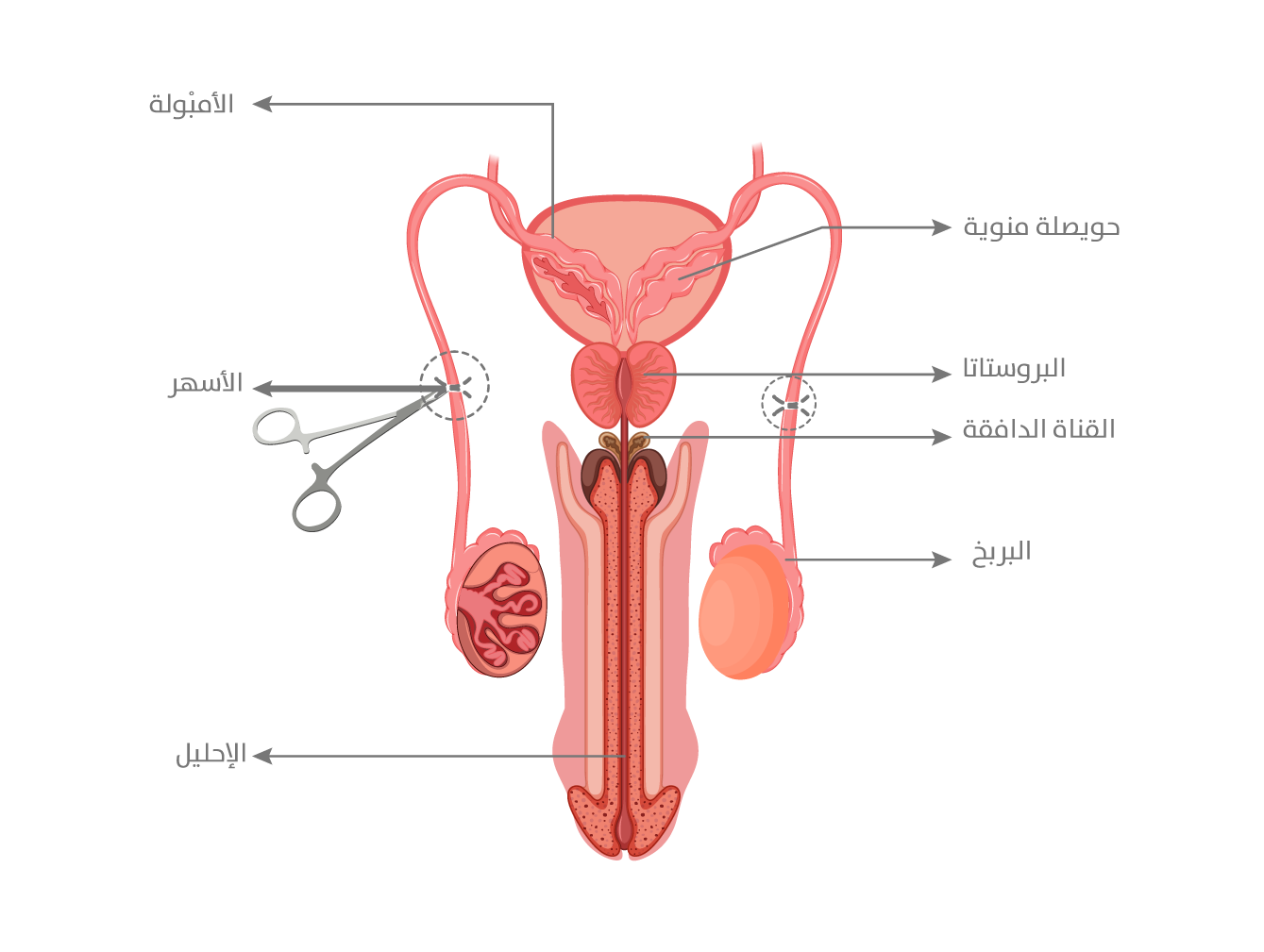 رسم توضيحي لتشريح الجهاز التناسلي الذكري
رسم توضيحي لتشريح الجهاز التناسلي الذكري
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تعتمد الطريقة التقليدية على شقين صغيرين في كيس الصفن باستخدام مشرط دقيق، إذ تُحدد القناة الدافقة بعناية، ثم تُقطع ويُربط طرفاها بخيوط جراحية. تتميز هذه الطريقة بالفعالية العالية، لكنها ترتبط بمعدلات أكبر نسبيًّا للنزيف، والتورم، والكدمات ما بعد العملية، خاصة في حال عدم استخدام أساليب ميكروسكوبية دقيقة أو مراقبة دقيقة للأنسجة المحيطة.
[الشكل2]
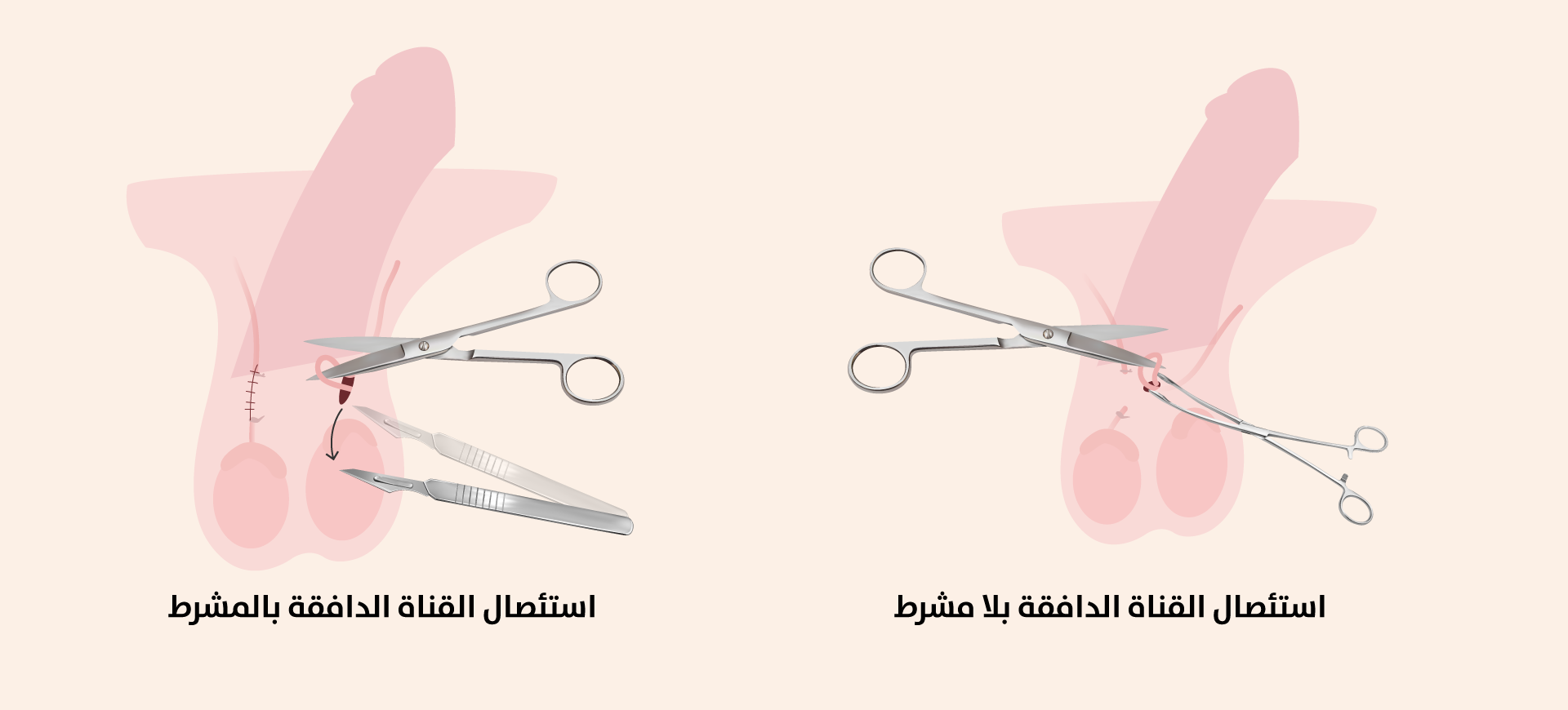 صورة توضيحية تُبين الفرق بين استخدام المشرط وبلا مشرط في استئصال القناة الدافقة
صورة توضيحية تُبين الفرق بين استخدام المشرط وبلا مشرط في استئصال القناة الدافقة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تقدم الطريقة الأخرى، وهي من دون مشرط (No-scalpel vasectomy)، نهجًا أكثر حداثة، إذ تُستخدم أداة خاصة لعمل ثقب صغير بدل الشق التقليدي، ما يقلل من النزيف، والألم، والتورّم، ويسرع من فترة التعافي (الشكل 2). أثبتت الدراسات أن هذه الطريقة توفر معدلات مضاعفات منخفضة، مع فاعلية تتجاوز 99 في المئة، ما جعلها الأكثر شيوعًا عالميًّا واعتمادًا في المراكز المتقدمة[3].
كما ظهرت أساليب حديثة ومتقدمة لتعزيز أمان العملية ومنع إعادة الاتصال العفوي للقناة، منها: الكي الحراري (Thermal Cautery) لإغلاق نهايات القناة بالحرارة الدقيقة، والسدادات الجراحية (Clips/ Plugs) التي توفر إغلاقًا ميكانيكيًّا مستقرًا، وتقنية الفصل الطبقي (Fascial Interposition) (الشكل 3) التي تقوم على دفن أحد طرفي القناة في طبقة نسيجية منفصلة لمنع إعادة الاتصال العفوي.
[الشكل3]
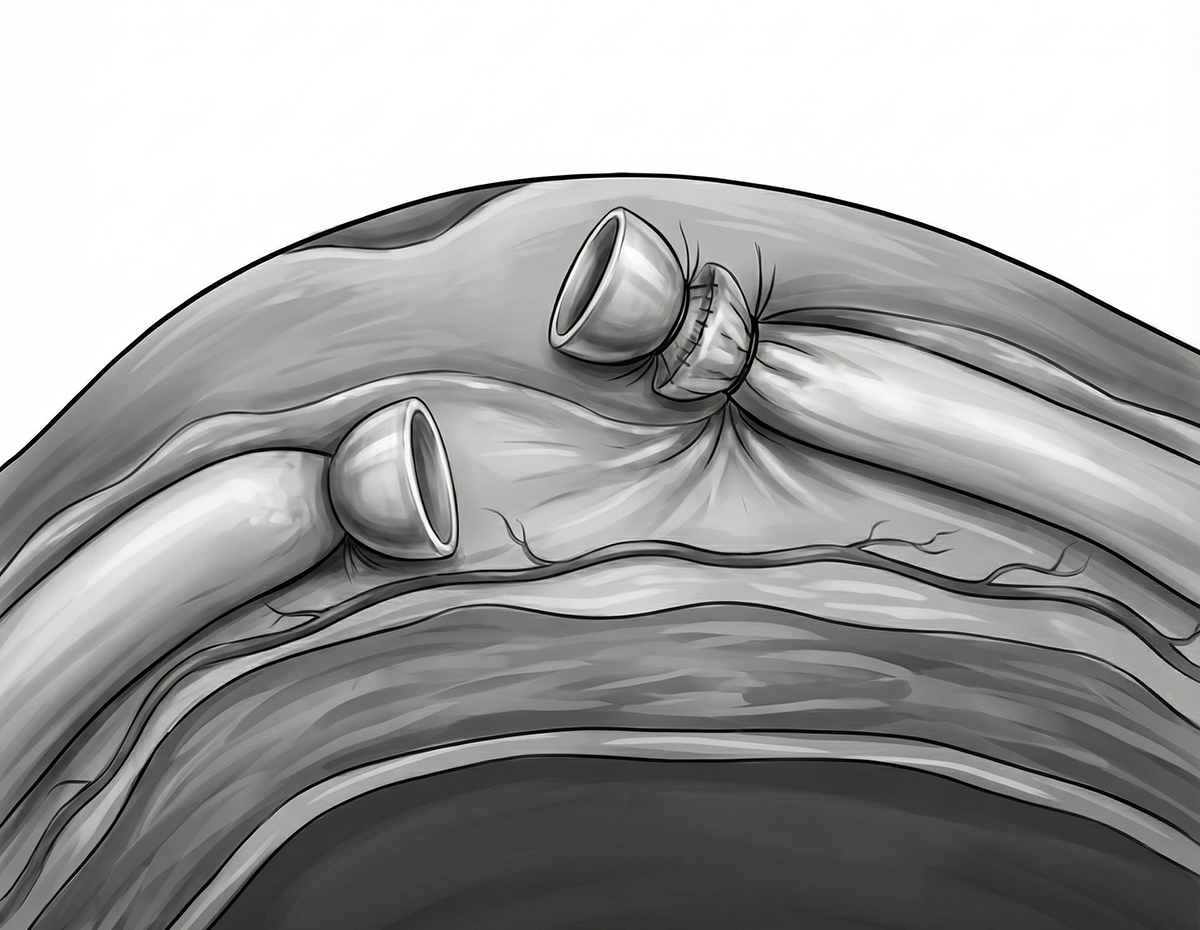 تقنية الفصل الطبقي
تقنية الفصل الطبقي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تشير الدراسات إلى أن الأساليب الحديثة مثل الكي الحراري، والسدادات الجراحية، والفصل الطبقي، وطريقة الجراحة بلا مشرط، ترتبط بمستويات أمان أعلى ومعدلات تعافي أسرع، مع انخفاض احتمالات فشل العملية مقارنة بالطريقة التقليدية، ورغم أن جميع الأساليب الجراحية تحقق نسبة نجاح تتجاوز 99 في المئة، غير أن الطريقة التقليدية تبقى خيارًا فعالًا في المراكز محدودة الإمكانات، فهي تقنية بسيطة قابلة للتنفيذ بكفاءة ضمن نطاق الموارد المتاحة[4].
التحضيرات قبل الإجراء الجراحي
تبدأ عملية استئصال القناة الدافقة بمرحلة تحضيرية دقيقة لضمان نجاح التدخّل وتقليل المضاعفات. يشمل الفحص الطبي ما قبل العملية تقييم التاريخ الطبي للمريض، والتحرّي عن أمراض مرافقة، مثل اضطرابات النزف أو العدوى التناسلية، إضافة إلى مناقشة الحالة الإنجابية والتأكد من رغبة المريض النهائية في التعقيم. كما يُنصح بإجراء استشارة شاملة تتناول الجوانب الطبية والنفسية والاجتماعية. أما الإجراءات التحضيرية فتتضمن حلاقة منطقة الصفن أو تنظيفها جيدًا، وارتداء ملابس فضفاضة، والتوقف عن تناول مضادات التخثّر في حال كان المريض يتلقاها بناءً على وصفة طبيّة.
خطوات الإجراء الجراحي
خلال خطوات العملية الجراحية، يُطبَّق التخدير الموضعي على جلد الصفن، ثم تُكشف القناة الدافقة إما عبر شق صغير (الطريقة التقليدية) أو ثقب دقيق (طريقة دون مشرط). وبعد عزل القناة تُقطع وتُغلق باستخدام الربط، أو الكي الحراري، أو تقنيات حديثة مثل الفصل الطبقي. تستغرق الجراحة عادة ما بين 15 و30 دقيقة، وتُجرى في العيادة الخارجية من دون حاجة للإدخال إلى المستشفى. أما الرعاية المباشرة بعد العملية فتشمل وضع كمادات باردة لتخفيف التورم، ارتداء داعم للصفن عدة أيام، وتجنب الجهد البدني أو الجماع مدة تتراوح بين 48 و72 ساعة. يُنصح المريض بمراقبة أي علامات نزيف، أو التهاب، أو تورّم زائد، إضافة إلى الالتزام بالمتابعة المخبرية لفحص السائل المنوي بعد أسابيع للتأكد من نجاح التعقيم (الشكل 4).[5]
الشكل [4]
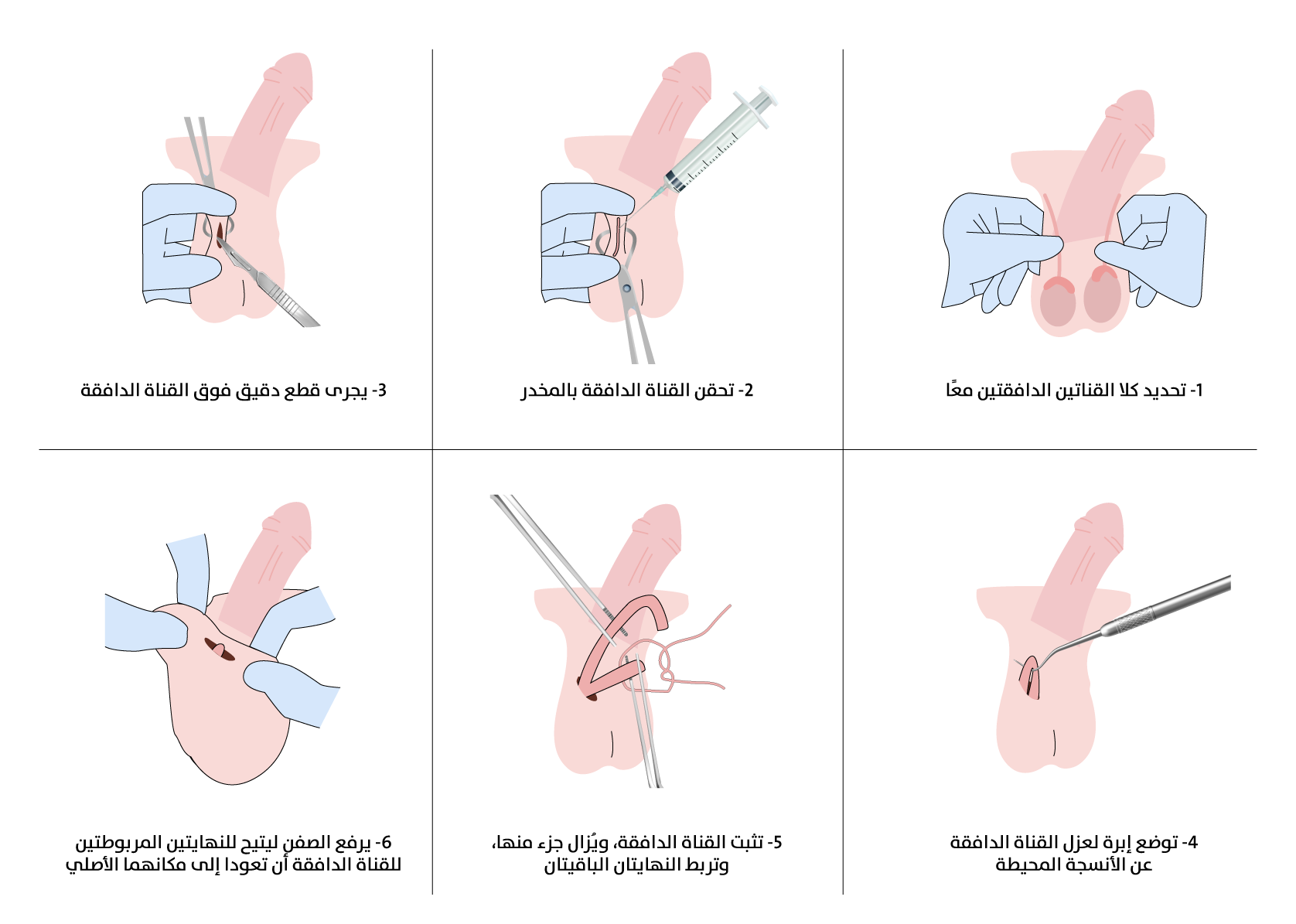 خطوات استئصال القناة الدافقة
خطوات استئصال القناة الدافقة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
النتائج والفعالية
تشير الأدلة السريرية والمراجعات المنهجية، واسعة النطاق، إلى أن استئصال القناة الدافقة يمثل واحدة من أكثر وسائل التعقيم الذكري فعالية وموثوقية؛ إذ تتجاوز معدلات النجاح في منع الحمل 99.5 في المئة عند تطبيق التقنيات الجراحية الحديثة والالتزام الصارم بمتابعة الفحوص المخبرية بعد العملية. أظهرت الدراسات متعددة المراكز، التي شملت آلاف المرضى على مدى عقود، أن حالات فشل العملية نادرة للغاية، إذ لا تتجاوز نسبة الفشل 1 إلى 2 حالة لكل 2000 عملية تقريبًا. غالبًا ما تُعزى حالات الفشل هذه إلى إعادة الاتصال التلقائي للقناة الدافقة (Recanalization)، أو إلى عدم الالتزام بإجراء الفحوص الدورية الموصى بها بعد العملية، وهو ما يبرز أهمية التوجيه الدقيق للمرضى حول متابعة نتائج الفحوص المخبرية[6].
رغم أن الفعالية العالية للعملية تجعلها وسيلة دائمة لمنع انتقال الحيوانات المنوية، فإن هناك مرحلة انتقالية حرجة تمتد عادة فترة تتراوح بين 8 و12 أسبوعًا بعد العملية، أي ما يعادل نحو 15 إلى 20 دورة قذف، تظل خلالها بعض الحيوانات المنوية متواجدة في الأقسام القريبة من الإحليل أو في الحويصلات المنوية. في خلال هذه الفترة، قد يحدث الحمل إذا لم تُستخدم وسائل منع حمل إضافية، ما يؤكد ضرورة توجيه المرضى نحو استخدام وسائل حماية مؤقتة حتى التأكد الكامل من التعقيم من خلال فحوصات السائل المنوي المتتابعة.
يُعدّ فحص السائل المنوي بعد استئصال القناة الدافقة خطوة محورية وموضوعية لتقييم نجاح التعقيم. تحلل في خلال هذا الفحص العينة مجهريًّا للتحقق من انعدام الحيوانات المنوية تمامًا (Azoospermia)، أو وجود أعداد قليلة غير متحركة (Rare Non-motile Sperm). وفي كلا الحالتين، يُصنَّف المريض عقيمًا وظيفيًّا، مع العلم أن وجود أعداد قليلة من الحيوانات المنوية غير المتحركة لا يقلل من فعالية التعقيم بشكل كبير إذا تُحقق من عدم وجود حيوانات منوية متحركة.
تجاهل هذا الفحص أو تأجيله قد يؤدي إلى اعتقاد زائف بنجاح العملية، ما يزيد خطر حدوث حمل غير مخطط له، ويقلل من الموثوقية الفعلية للعملية وسيلةً دائمة لمنع حمل. لذلك، يُوصى بشدة بإجراء فحصين متتاليين للسائل المنوي بعد العملية، عادة بفاصل أسبوعين على الأقل، لضمان التأكد من انعدام أي نشاط حيوي للحيوانات المنوية، وهو ما يعزز الثقة لدى المرضى ويضمن الالتزام بإرشادات منع الحمل المؤقتة خلال المرحلة الانتقالية.
إضافة إلى ذلك، تشير الأدلة إلى أن التقنيات الجراحية الدقيقة، مثل الطريقة من دون مشرط (No-scalpel Vasectomy)، والكي الحراري (Thermal Cautery)، والسدادات الجراحية (Clips/Plugs)، تزيد من معدلات النجاح وتقلل بشكل ملموس من احتمالية الفشل مقارنة بالطرق التقليدية، مع تقليل المضاعفات المؤقتة مثل الألم أو التورم، ما يعكس التكامل بين الأمان الجراحي والدقة العلمية في تحقيق التعقيم الأمثل[7].
المضاعفات المحتملة
رغم أن استئصال القناة الدافقة يُعدّ إجراءً آمنًا وبسيطًا نسبيًا، فإن بعض المرضى قد يعانون من مضاعفات قصيرة المدى أو طويلة المدى. على المدى القصير، قد تظهر أعراض شائعة مثل الألم الموضعي، أو النزيف البسيط، أو التورم في كيس الصفن، وتُعزى هذه التظاهرات غالبًا إلى الرضة الجراحية أو
تجمع دموي صغير {{تجمع دموي صغير: (Hematoma) هو تراكم محلي للدم خارج الأوعية الدموية نتيجة تمزقها، وغالبًا ما يحدث بعد إصابة مباشرة أو إجراء جراحي بسيط. يؤدي هذا التراكم عادةً إلى تورم موضعي وألم محدود في المنطقة المصابة، وقد يسبب شعورًا بعدم الراحة. على الرغم من ذلك، فإن التجمع الدموي الصغير غالبًا ما يزول تدريجيًّا مع مرور الوقت من دون مضاعفات خطيرة، مع إمكانية استخدام تدابير داعمة لتخفيف الانزعاج وتسريع التعافي.}} في موقع العملية، وتُعالج عادة بالراحة، ووضع كمادات باردة، ومسكنات الألم البسيطة، ونادرًا ما تتطلب تدخلًا إضافيًّا. أما المضاعفات طويلة المدى فتشمل تكوّن الحبيبات المنوية (Sperm Granulomas)،وهي تكتلات صغيرة ناتجة من تسرب الحيوانات المنوية من طرف القناة المقطوعة إلى الأنسجة المحيطة، وتكون غالبًا غير مؤلمة ولكنها قد تسبب انزعاجًا عند بعض المرضى. إضافة إلى ذلك، تعدّ متلازمة الألم الصفني المزمن {{متلازمة الألم الصفني: (Post-vasectomy Pain Syndrome) هي حالة مؤلمة تستمر بعد عملية قطع الأسهر، قد تنتج من التهاب، أو توتر عصبي أو تجمع دموي، وتؤثر في جودة الحياة والنشاط الجنسي.}} من أبرز المخاوف، إذ يعاني نسبة قليلة (حوالي 1 إلى 2 في المئة) من ألم مستمر أو متقطع في الخصية أو البربخ يستمر أشهرًا أو سنوات، وقد يؤثر في جودة الحياة. وتشير الدراسات إلى أن معظم هذه الحالات تستجيب للتدبير الدوائي أو الجراحي المحدود. إجمالًا، تبقى معدلات المضاعفات منخفضة نسبيًّا، ما يجعل العملية آمنة وذات نسبة نجاح مرتفعة، خاصة عند الالتزام بالمعايير الجراحية الدقيقة والرعاية الطبية بعد العملية[8].
الانعكاسات على الوظيفة الجنسية والهرمونية
لا يغيّر استئصال القناة الدافقة الوظيفة الجنسية أو الهرمونية للذكر؛ إذ تبقى الرغبة الجنسية والانتصاب والقذف والنشوة على حالها، وذلك لأن مسار الأعصاب والأوعية الدموية والآلية الوعائية-العصبية للانتصاب لا تُمسّ بالجراحة. ويكون أي تذبذب عابر في الرغبة بعد العملية عادةً نفسيَّ المنشأ (قلق أو توتر) وليس عضويًّا، ويتحسّن مع الاطمئنان وغياب الألم.
يظل حجم السائل المنوي بعد الإجراء شبه ثابت؛ فالحيوانات المنوية تمثّل قرابة 2 إلى 5 في المئة فقط من الحجم، في حين يأتي أغلب السائل من الحويصلات المنوية والبروستاتا، لذا قد يلاحظ البعض فرقًا طفيفًا أو غير ملحوظ في الكمية أو القوام من دون تغير في اللون أو اللزوجة أو الرائحة. كذلك لا يحدث قذف راجع ولا تتأثر قوة الدفق، لأن الإحليل والبروستاتا سليمان. هرمونيًّا، يبقى محور تحت المهاد–النخامى–الخصية سليمًا؛ فخلايا لايديغ تستمر في إنتاج التستوستيرون بالمستويات نفسها، ما يعني ثبات الصفات الجنسية الثانوية، والكتلة العضلية وكثافة العظام والمزاج.
قد يظهر في الأسابيع الأولى انزعاج بعد القذف بفعل ارتفاع الضغط داخل البربخ، لكنه يزول تدريجيًّا مع الالتحام النسيجي. ومن الممكن تكوّن أضداد ضد النطاف بعد الاستئصال، لكنه لا يؤثر في الأداء الجنسي ولا على الهرمونات، وتقتصر أهميته على اعتبارات الإخصاب المستقبلي في حال التفكير بالعكس أو إجراءات المساعدة في الإنجاب[9].
الاعتبارات النفسية والاجتماعية
يمثل قرار إجراء استئصال القناة الدافقة خطوة كبيرة ذات أبعاد نفسية واجتماعية مهمة. ويعدّ الاستعداد النفسي لاتخاذ قرار دائم من أهم العوامل لضمان رضا المريض على المدى الطويل، إذ يتطلب وعيًا تامًا بأن العملية تُعدّ وسيلة منع حمل دائمة، وأن التراجع عنها قد يكون معقدًا ويحتاج إلى جراحة دقيقة أو تقنيات مساعدة في الإنجاب. يؤدي دور الشريكة في القرار أيضًا دورًا محوريًّا، فموافقة الزوجة أو الشريكة تسهم في تقليل القلق النفسي وتعزيز شعور الأمان والثقة، في قد يؤدي غياب النقاش إلى توتر وصراعات عاطفية. يمكن أن تظهر احتمالية الندم وتغير الظروف الحياتية في حالات تغيّر الرغبة الإنجابية مستقبلًا، مثل فقدان الأطفال أو الرغبة في إنجاب أطفال إضافيين، ما يجعل من الضروري التفكير مليًا قبل اتخاذ القرار النهائي؛ لذلك، تُعدّ الاستشارة والدعم النفسي قبل العملية جزءًا أساسيًّا من التحضير، وتشمل مناقشة البدائل المتاحة، وتوضيح المضاعفات، والمعلومات حول إمكانات العكس أو المساعدة في الإنجاب في المستقبل، ما يساعد في تقليل القلق وتحقيق رضا المريض على المدى الطويل[10].
إمكانية العكس والخيارات المستقبلية
على الرغم من أن استئصال القناة الدافقة يُسوَّق باعتباره وسيلة دائمة لمنع الحمل، فإن التطور الجراحي والتقني أتاح خيارات لعكس الإجراء لدى الراغبين بالإنجاب مستقبلًا. تتضمن جراحة إعادة التوصيل (Vasovasostomy) وإعادة ربط طرفي القناة الدافقة المقطوعة باستخدام تقنيات ميكروسكوبية دقيقة لضمان مرور الحيوانات المنوية مرة أخرى. في الحالات التي يكون فيها الانسداد طويل المدى أو عند تلف البربخ، يُلجأ إلى التوصيل بالبربخ (Vasoepididymostomy)، إذ يُربط البربخ مباشرة بالقناة الدافقة، وهي عملية أكثر تعقيدًا وتتطلب خبرة جراحية عالية. بإضافة إلى ذلك، توفر تقنيات المساعدة في الإنجاب، مثل
الحقن المجهري بالحيوانات المنوية (ICSI) أو
التلقيح الصناعي (IVF) بدائل للمرضى الذين تعذر عليهم تحقيق الحمل عبر الطرق الجراحية التقليدية؛ إذ يمكن استخراج الحيوانات المنوية مباشرة من الخصية أو البربخ واستخدامها للتلقيح في المختبر.
تعتمد نسب النجاح على عدة عوامل، أبرزها مدة الزمن منذ استئصال القناة الدافقة، ومهارة الجراح، وجودة الحيوانات المنوية، وعمر الزوجة، إذ تتراوح معدلات استعادة الخصوبة بعد إعادة التوصيل (Vasovasostomy) بين 70 و95 في المئة في خلال السنوات العشر الأولى، بينما تقل تدريجيًّا بعد مرور فترات أطول. ترفع العوامل التقنية، مثل استخدام المجهر الجراحي، والفصل الطبقي للقناة، وعزل الطرفين في أنسجة منفصلة، احتمالية النجاح وتقلل عناصر الفشل؛ وبذلك، تظل الخيارات المستقبلية واسعة، لكنها تتطلب تقييمًا فرديًّا دقيقًا لضمان أفضل النتائج الممكنة[11].
المراجع
Anderson, Danyon et al. "Vasectomy Regret or Lack Thereof."
Health Psychology Research. vol. 10, no. 3 (2022).
Borrell, Joseph A. et al. “Comparing Vasectomy Techniques, Recovery and Complications: Tips and Tricks.”
International Journal of Impotence Research (2025). pp. 1-7.
Cook, Lynley et al. "Vasectomy Occlusion Techniques for Male Sterilization."
Cochrane Database of Systematic Reviews (2014). pp. 1-26.
Dohle, Gert et al. "European Association of Urology Guidelines on Vasectomy."
European Urology. vol. 61, no. 1 (2012). pp. 159-163.
Johnsonbaugh, Roger, Carol Czerwinski & M. Edson. “Serum Hormone Levels before and Two Years after Vasectomy.”
Contraception Journal. vol. 6, no. 6 (1977). pp. 563-567.
Khalafalla, Kareim et al. “Post-Vasectomy Semen Analysis: What’s All the Fuss About?”
Diagnostics. vol. 14, no. 20 (2024).
Kolettis, Peter et al. “Outcomes for Vasectomy Reversal Performed after Obstructive Intervals of at Least 10 Years.”
Urology. vol. 60, no. 5 (2002). pp. 894–898.
Mbizvo, Michael T. & Tendai M. Chiware. "Male Reproductive Function and Fecundity."
Oxford Research Encyclopedia of Global Public Health (2020).
Fang Yang et al. "Review of Vasectomy Complications and Safety Concerns."
The World Journal of Men's Health. vol. 39, no. 3 (2020). pp. 406-418.
Zeitler, Matthew R. & Brian Z. Rayala. "Outpatient Vasectomy: Safe, Reliable, and Cost-effective."
Primary Care: Clinics in Office Practice. vol. 48, no. 4 (2021). pp. 613-625.
[1] Matthew R. Zeitler & Brian Z. Rayala, "Outpatient Vasectomy: Safe, Reliable, and Cost-effective,"
Primary Care: Clinics in Office Practice, vol. 48, no. 4 (2021).
[2] Michael T. Mbizvo & Tendai M. Chiware, "Male Reproductive Function and Fecundity,"
Oxford Research Encyclopedia of Global Public Health (2020).
[3] Joseph A. Borrell et al., “Comparing Vasectomy Techniques, Recovery and Complications: Tips and Tricks,”
International Journal of Impotence Research (2025).
[4] Lynley Cook et al.,“Vasectomy Occlusion Techniques for Male Sterilization,”
Cochrane Database of Systematic Reviews (2014).
[5] Borrell et al.
[6] Kareim Khalafalla et al., “Post-Vasectomy Semen Analysis: What’s All the Fuss About?”
Diagnostics, vol. 14, no. 20 (2024).
[7] Gert Dohle et al., "European Association of Urology Guidelines on Vasectomy,"
European Urology, vol. 61, no. 1 (2012), pp. 159-163.
[8] Fang Yang et al., "Review of Vasectomy Complications and Safety Concerns,"
The World Journal of Men's Health, vol. 39, no. 3 (2020), pp. 1–13.
[9] Roger Johnsonbaugh, Carol Czerwinski & M. Edson, “Serum Hormone Levels before and Two Years after Vasectomy,”
Contraception Journal, vol. 6, no. 6 (1977).
[10] Danyon Anderson et al., “Vasectomy Regret or Lack Thereof,”
Health Psychology Research, vol. 10, no. 3 (2022).
[11] Peter Kolettis et al., “Outcomes for Vasectomy Reversal Performed after Obstructive Intervals of at Least 10 Years,”
Urology, vol. 60, no. 5 (2002), pp. 894–898.
✓ تم النسخ
Peter Kolettis et al., “Outcomes for Vasectomy Reversal Performed after Obstructive Intervals of at Least 10 Years,”
Urology, vol. 60, no. 5 (2002), pp. 894–898.
.