دورة اليوريا (Urea cycle)، المعروفة أيضًا باسم دورة الأورنيثين (Ornithine cycle)، هي مسار استقلابي في الكبد مسؤول عن إزالة سُميّة الأمونيا {{الأمونيا: (NH₃) غاز عديم اللون، لاذع الرائحة، يتكون من النيتروجين والهيدروجين. يذوب في الماء بدرجة عالية، مكونًا هيدروكسيد الأمونيوم (NH₄OH) الذي يعدّ قاعدة ضعيفة. يُنتَج طبيعيًّا عن طريق تحلل المواد العضوية، وهو ناتج ثانوي لعملية أيض البروتين في الجسم، ويعدّ سامًا في التراكيز العالية.}}، وهو منتج ثانوي لاستقلاب البروتين، من خلال تحويله إلى يوريا، لإفرازه مع البول. تساعد دورة اليوريا في الحفاظ على توازن النيتروجين في الجسم، إذ تحوِّل الخلايا الكبدية الأمونيا السامة إلى مركّب اليوريا، فتحيّد الآثار السلبية لزيادة مستويات الأمونيا في الدم.
أما عندما لا تعمل هذه الدورة بكفاءة، فتتراكم الأمونيا السامة داخل الجسم، وقد تؤدي إلى علل سريرية مختلفة، مثل: الخمول، وتداخل الكلام، والوذمة الدماغية، والارتعاش الخافق وغيرها.
يُعدّ فهم الآليات البيوكيميائية لدورة اليوريا وضوابطها التنظيمية، والاضطرابات المرتبطة بها، أمرًا ضروريًا لدراسة عمليات الاستقلاب في الصحة والمرض.
اكتشافها
اكتشف دورة اليوريا، في عام 1932، عالم الكيمياء الحيوية والطبيب الألماني هانز أدولف كرِبس (Hans Adolf Krebs)، وطالبه كورت هنسلايت (Kurt Henseleit)، الباحثان في جامعة فرايبورغ[1]. كما اكتشف كرِبس لاحقًا دورة حمض الستريك أو حلقة كرِبس (Citric acid cycle / Krebs cycle)، خلال إقامته في جامعة شيفيلد في إنكلترا[2]. يُعتبر اكتشاف دورة اليوريا أول توضيح لمسار استقلابي حلقي {{مسار استقلابي حلقي: المسار الأيضي الدائري أو المسار الاستقلابي الحلقي هو سلسلة من التفاعلات الإنزيمية تُعيد إنتاج الركيزة الأولى في المسار مُنشئةً دورةً مستمرةً. ومن الأمثلة الرئيسة على ذلك دورة حمض الستريك (حلقة كرِبس) التي تؤكسد أسيتيل مرافق الإنزيم أ لإنتاج الطاقة (ATP، NADH). تبدأ الحلقة بالأوكسالوأسيتات وتنتهي به بعد سلسلة من 8 تفاعلات.}} (Cyclic metabolic pathway) في تاريخ الكيمياء الحيوية، وهو ما سلّط الضوء على أهمية إزالة سموم الأمونيا في الثدييات. لقد وضع عمل كرِبس الأساس للكيمياء الحيوية الحديثة، وتحديدًا التمثيل الغذائي الخلوي وفهم مسارات الاستقلاب وتنظيمها.
وظيفتها
يُنتج الجسم جزيء الأمونيا نتيجة لاستقلاب البروتينات والأحماض الأمينية والمواد المحتوية على نيتروجين. وهو جزيء له تأثير سام إن وُجد تراكيز مرتفعة. ينتج الجسم كميات كبيرة من الأمونيا إذا كان الشخص يتّبع نظامًا غذائيًا عالي البروتين (High-protein diet)، كما يمكن أن تزيد كميتها خلال فترة المجاعة الطويلة، حين يعمل الجسم على استخدام البروتينات الخلوية لإنتاج الطاقة بسبب غياب مصادر أخرى لها. كذلك يُنتج جزيء الأمونيا بشكل طبيعي بواسطة ميكروبات الأمعاء {{ميكروبات الأمعاء: هي مجتمع واسع ومتنوع من تريليونات البكتيريا والفيروسات والفطريات التي تعيش في أمعاء الإنسان، وهي ضرورية للهضم والمناعة والصحة العامة.}} (Gut microbiota). وهناك طرق عدة للتخلّص من هذا المركّب، تختلف من كائن حي إلى آخر، فالأسماك مثلًا تفرزه مباشرة في الماء، أما الطيور والزواحف فتحوّله إلى حمض اليوريك {{حمض اليوريك: هو مركب نيتروجيني ناتج عن استقلاب البيورين يُطرح في البول. ارتفاع مستوياته قد تُسبب حالات مؤلمة مثل النقرس وحصوات الكلى.}} (Uric acid)، والثدييات تستقلب الأمونيا إلى يوريا (Urea) وحمض اليوريك. تحوَّل الأمونيا السامة إلى جزيء يوريا من خلال دورة اليوريا (أو كما كانت تسمّى دورة الأورنيثين) لدى بعض الكائنات الحية، ومن ضمنها البشر. ومركّب اليوريا هو جزيء صغير قابليته للذوبان في الماء عالية جدًا، ما يعني سهولة إخراجه من الجسم في عملية التبوّل[3].
تحتوي جميع الأحماض الأمينية على مجموعة وظيفية (Functional group) من نوع أمين (Amine)، إضافة إلى الهيكل الكربوني للمركّب. تستوجب عملية استقلاب الهيكل الكربوني في مسارات الأيض الوسيطة (Intermediary metabolism) بدايةً إزالة مجموعة الأمين. ولتنفيذ هذه العملية بكفاءة، تُحوّل جميع الأحماض الأمينية إلى نوع واحد منها، وهو الغلوتامات (Glutamate) عن طريق نقل مجموعتها الأمينية إلى جزيء ألفا كيتوغلوتارات (Alpha-ketoglutarate). تؤدي هذه العملية إلى تجميع المجموعات الأمينية في حمض أميني واحد، ليُنقل إلى الكبد، حيث يُتخلّص من مجموعة الأمين هناك. إضافة إلى ذلك، في الأنسجة العضلية والمحيطية، فإن الغلوتامات يمكنه أن يستقبل جزيء الأمونيا الناتج من استقلاب البروتين، ويضيفها عليه، ما يؤدي إلى تكوين الحمض الأميني الغلوتامين (Glutamine). يتم هذا التفاعل بواسطة إنزيم غلوتامين سينثاتاز (Glutamine synthatase). يُصدَّر الغلوتامين المنتَج من الأنسجة المكوّنة له عبر الدم إلى الكبد ويدخل إلى الميتوكوندريا (Mitochondria)، حيث يُكسّر إنزيم الغلوتاميناز (Glutaminase) الغلوتامين إلى مكوّناته؛ الغلوتامات والأمونيا. يتحوّل الغلوتامات إلى ألفا كيتوغلوتارات وجزيء أمونيا آخر، عن طريق إنزيم ديهيدروجيناز الغلوتامات (Glutamate dehydrogenase)[4]. من هنا، يبدأ مسار دورة اليوريا، إذ تُدمج الأمونيا مع أيون البيكربونات (Bicarbonate) لتكوين كاربامويل فوسفات (Carbamoyl phosphate)، وهو المركَّب الأول في هذه الدورة. تنتهي الدورة بتكوين جزيء يوريا في سيتوبلازم (Cytoplasm) الخلية الكبدية، ومن ثم تخرج اليوريا من الخلية، وتنتقل عبر الدم إلى الكلى، حيث تُفرز نهايةً مع البول[5].
[الشكل 1]
 الخطوات الإنزيمية لدورة اليوريا
الخطوات الإنزيمية لدورة اليوريا
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تفاعلاتها
في الثدييات، الكبد هو الموقع الوحيد الذي تُصنّع فيه اليوريا، وتتم هذه العملية من خلال المسار الأيضي، دورة اليوريا. تشمل دورة اليوريا خمسة تفاعلات إنزيمية متعاقبة في الخلايا الكبدية، يبدأ جزء منها في الميتوكوندريا، ثم يحدث الآخر في السيتوبلازم[6]، لتكتمل الخطوات الإنزيمية لدورة اليوريا (الشكل 1).
التفاعل الأول
تفاعل تحضيري يتكوّن به الكاربامويل فوسفات، عن طريق إضافة ثاني أكسيد الكربون الذائب (أيون البيكربونات) إلى الأمونيا، بواسطة إنزيم كاربامويل فوسفات سينثاتاز 1 (Carbamoyl phosphate synthetase 1, CPS1) الذي يستهلك طاقة بشكل أدينوسين ثلاثي الفوسفات (ATP). يعتبر هذا التفاعل الخطوة المحددة لسرعة التفاعل (Rate-limiting step) للمسار كاملًا. في هذه الخطوة، يشكّل جزيء الأمونيا مصدر المجموعة الأمينية الأولى في جزيء اليوريا. ولإتمام هذه العملية، يتطلب إنزيم CPS 1 منشطًا إلزاميًا، وهو إن-أسيتيل غلوتامات (N-acetyl-glutamate)[7].
ATP + Bicarbonate + Ammonia → Carbamoyl phosphate + ADP (in mitochondria)
التفاعل الثاني
يتيح هذا التفاعل الذي يحفّزه إنزيم الأورنيثين ترانسكاربامويلاز (Ornithine transcarbamoylase) البدء في دورة اليوريا. ففي تفاعل دمج يتّحد الكاربامويل فوسفات مع الأورنيثين، وهو حمض أميني غير مولِّد للبروتين (Non-proteinogenic amino acid)، مكوّنًا حمضًا أمينيًا آخر غير مولِّد للبروتين، وهو السيترولين (Citrulline) في الميتوكوندريا. وبعد تكوين السيترولين، يُنقل إلى السيتوبلازم بواسطة البروتين الناقل أورنيثين ترانسلوكاز (Ornithine translocase)[8].
Carbamoyl phosphate + Ornithine → Citrulline (in mitochondria)
Citrulline (in mitochondria) → Citrulline (in cytosol)
التفاعل الثالث
[الشكل 2]
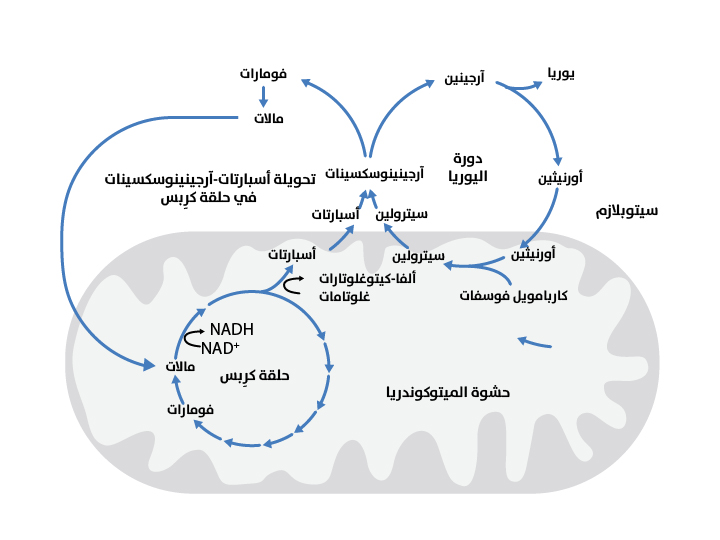 حلقتا كرِبس: التفاعلات التي اكتشفها هانز كرِبس المُشَكِّلة لدورتي اليوريا وحمض الستريك
حلقتا كرِبس: التفاعلات التي اكتشفها هانز كرِبس المُشَكِّلة لدورتي اليوريا وحمض الستريك
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
في السيتوبلازم، يدمج إنزيم آرجينينوسكسينات سينثاتاز (Argininosuccinate synthetase)، الذي يحتاج إلى طاقة ATP، السيترولين مع الحمض الأميني الأسبارتات، لتكوين مركّب آرجينينوسكسينات. من الجدير ذكره أن الحمض الأميني الأسبارتات في هذا التفاعل هو مصدر المجموعة الأمينية الثانية في مركّب اليوريا[9].
Citrulline + Aspartate + ATP → Argininosuccinate + AMP + PPi (in cytosol)
التفاعل الرابع
في التفاعل قبل الأخير من الدورة، يكسَّر مركّب الآرجينينوسكسينات إلى الحمض الأميني آرجينين وجزيء فومارات (Fumarate) عن طريق إنزيم آرجينينوسكسينات لياز (Argininosuccinate lyase). تجدر الإشارة إلى أن جزيء الفومارات المنتَج يمكن نقله إلى الميتوكوندريا، حيث يشارك في تصنيع الطاقة الحيوية على شكل ثنائي نوكليوتيد الأدنين وأميد النيكوتين (NADH)، عبر دورة حمض الستريك. يُعتبر جزيئا الأسبارتات والفومارات الرابطين بين دورتي اليوريا وحمض الستريك، وكلا الدورتان اكتشفهما هانز كرِبس، لذا يُطلق عليهما معًا "حلقتي كرِبس"[10] (Krebs’ bicycle) (الشكل 2).
Argininosuccinate → Arginine + Fumarate
التفاعل الخامس
في التفاعل الأخير من هذه الدورة، يخضع الآرجينين للتحلل المائي (Hydrolysis) بواسطة إنزيم آرجيناز (Arginase)، مكوّنًا اليوريا، ويعيد إنتاج الأورنيثين، الذي يدخل الميتوكوندريا عن طريق ناقل الأورنثين، ثم يبدأ دورة جديدة مرة أخرى[11].
Arginine → Urea + Ornithine (in cytosol)
Ornithine (in cytosol) → Ornithine (in mitochondria)
تنظيمها
تنظَّم دورة اليوريا في الخلية، مثل مختلف المسارات الاستقلابية، من خلال مستويات متعددة لضمان إزالة سموم الأمونيا بكفاءة وفعالية[12]. وهنا بعض هذه الطرق التنظيمية:
أ. التنظيم التفارغي (Allosteric regulation): يعمل جزيء إن-أسيتيل غلوتامات منشطًا أساسيًا للإنزيم المتحكّم بتدفّق المسار (كاربامويل فوسفات سينثاتاز). يحفّز إنزيم إن-أسيتيل غلوتامات سينثاز (N-Acetylglutamate synthase) دمج الغلوتامات مع جزيء أسيتيل مرافق الإنزيم أ (Acetyl CoA)، لإنتاج جزيء إن-أسيتيل غلوتامات. ويحفَّز هذا الإنزيم بواسطة الحمض الأميني آرجينين. وفي حال وجود كمية عالية من الأرجينين والغلوتامات في الخلية (بسبب زيادة في تكسير البروتينات)، تُحفّز دورة اليوريا للتخلّص من الأمونيا.
ب. التعبير الجيني (Gene expression): يتأثر إنتاج إنزيمات دورة اليوريا بالحِمية المتّبعة لدى الشخص، وتحديدًا تلك المعتمدة على البروتين، إضافة إلى الإشارات الهرمونية المختلفة؛ إذ إن تناول كميات كبيرة من البروتين يحفّز تخليق هذه الإنزيمات، في حين أن ظروف الصيام والتوتر التي تؤثر فيها هرمونات الغلوكاغون (Glucagon) والقشريات السُّكرية (غلوكوكورتيكويدات، Glucocorticoids)، تعمل أيضًا على تنظيم تعبيرها الجيني. تعمل هذه الهرمونات على زيادة نسخ الجينات التي تشفّر إنزيمات دورة اليوريا، ما يضمن قدرة الكبد على التعامل مع مستويات الأمونيا المتزايدة من تقويض البروتين خلال فترات الصيام أو التوتر.
اضطراباتها
اضطرابات دورة اليوريا (Urea cycle disorders) هي حالات استقلابية موروثة ناجمة عن طفرات في الجينات التي تشفّر الإنزيمات اللازمة لهذه الدورة، أو البروتينات الناقلة المساعدة لها. تحدث اضطرابات دورة اليوريا لدى 1 من بين 35,000 مولود جديد تقريبًا. هناك ثمانية اضطرابات سريرية مرتبطة بشكل مباشر أو غير مباشر باستقلاب اليوريا، تؤدي جميعها إلى زيادة الأمونيا وانخفاض اليوريا في الدم، ما يجعل لكل منها أعراضًا سريرية متشابهة، وإن اختلف المسبب[13].
إن زيادة الأمونيا في الدم سامة للأعضاء، وخاصة الدماغ، ما قد يؤدي إلى اعتلالات دماغية (Encephalopathy). يمكن لهذه الاعتلالات أن تظهر على المريض على شكل وذمة دماغية (Cerebral edema)، وتقيّؤ، وعدم وضوح الرؤية، ونوبات عصبية (Seizures). كما تؤدي زيادة الأمونيا إلى زيادة تكوين الغلوتامين وانخفاض الغلوتامات، بسبب تحويل الغلوتامات إلى غلوتامين. تُعدّ الغلوتامات من النواقل العصبية {{النواقل العصبية: مواد كيميائية مخزّنة في حويصلات الشق التشابكي للخلايا العصبية. تنطلق هذه المواد من الخلية العصبية عند وصول النبضة العصبية من الخلية الأولى وترتبط بمستقبِلات تتأثر بها فقط وتسبب تغييرًا في الجهد الكهربي لغشاء الخلية اللاحقة. يتكسّر الناقل العصبي بعد ارتباطه بالمستقبِل أو يُعاد امتصاصه بوساطة الخلايا الدبقية أو الخلية الأولى ليعاد استخدامه.}} محفّزًا (Excitatory neurotransmitter)، وانخفاض مستوياته يسبب تثبيط النشاط العصبي بشكل عام، ما يظهر على شكل خمول كبير، أو غيبوبة في بعض الحالات الصعبة. إضافة إلى ذلك، تعيق الأمونيا الزائدة دورة حمض الستريك بسحب مكوّن مهم، وهو ألفا كيتوغلوتارات، بتحويله إلى غلوتامات[14]. يمثّل الجدول (الجدول 1) الآتي اضطرابات دورة اليوريا المختلفة والجينات الذي تسببت طفرتها في حدوث الاضطراب:
[الجدول 1] - اضطرابات دورة اليوريا
[15]الاضطراب | الجين المتسبِّب | الوظيفة المتأثرة |
عَوَز إن-أسيتيل غلوتامات سينثاز | NAGS | التحفيز الأولي لدورة اليوريا |
عَوَز كاربامويل فوسفات سينثاتاز 1 | CPS1 | التفاعل البادئ للدورة |
عَوَز أورنيثين ترانسكارباميلاز | OTC | التفاعل الثاني في الدورة |
عَوَز آرجينينوسكسينات سينثاتاز | ASS1 | التفاعل الثالث في الدورة |
عَوَز سيترين (Citrin deficiency) | SLC25A13 | نقل الأسبارتات من الميتوكوندريا إلى السيتوبلازم، وعليه، عدم قدرة دورة اليوريا على الاستمرار |
عَوَز آرجينينوسكسينات لياز | ASL | التفاعل الرابع في الدورة |
عَوَز آرجيناز | ARG | التفاعل الخامس في الدورة |
عَوَز أورنيثين ترانسلوكاز | SLC25A15 | نقل السيترولين إلى السيتوبلازم، ونقل الأورنيثين إلى الميتوكوندريا |
التشخيص والأهمية السريرية
عادة ما يتضمن تشخيص اضطرابات دورة اليوريا قياس ارتفاع مستويات الأمونيا والأحماض الأمينية المختلفة في دم المريض، واختبارات وظائف الكبد. كذلك، تساهم الاختبارات الجينية في التأكد من الجينات المسببة لهذه الاضطرابات. لا يوجد علاج شامل وتام لهذه الاضطرابات، غير أنه من الممكن السيطرة على المرض بواسطة بعض المحدِّدات الغذائية (نظام غذائي منخفض البروتين)، والأدوية المزيلة للأمونيا الزائدة (على سبيل المثال، فينيل بوتيرات الصوديوم). وفي الحالات الصعبة التي تفاقم فيها المرض، يمكن اللجوء إلى زراعة الكبد. مع الكشف المبكّر عن نقص فاعلية دورة اليوريا، يمكن حماية المرضى (غالبًا من حديثي الولادة والرضع) من العواقب العصبية المحتملة من خلال تحديد نظام غذائي مدى الحياة[16].
المراجع
“Hans Krebs Facts,” The Nobel Prize. 3/7/2025. Accessed on 7/3/2025, at: https://acr.ps/1L9F34O
Haussinger, Dieter. “Nitrogen Metabolism in liver: Structural and Functional Organization and Physiological Relevance.” Biochemical Journal. vol. 267, no. 2 (1990). pp. 281-290.
Grasshoff, Gerd. “Discovery of the Urea Cycle.” Mpiwg-Berlin. Accessed on 7/3/2025, at: https://acr.ps/1L9F2E9
Jez, Joseph (ed.). Encyclopedia of Biological Chemistry III. vol. 1 .3rd ed. Amesterdam: Elsevier, 2021.
Nelson, David L. & Michael Cox. Lehninger Principles of Biochemistry: International Edition. [New York]: Freeman & Company, 2021.
Simpson,Kara L.et al. “Urea Cycle Disorders Overview.”GeneReviews (2025). Accessed on 3/7/2025, at: https://acr.ps/1L9F32F
“Urea Cycle Disorder.” Cleveland Clinic. Accessed on 24/10/2024, at: https://acr.ps/1L9F2YI
[1] Gerd Grasshoff, “Discovery of the Urea Cycle,” Mpiwg-Berlin, accessed on 7/3/2025, at: https://acr.ps/1L9F2E9
[2]“Hans Krebs Facts,” The Nobel Prize, 3/7/2025, accessed on 7/3/2025, at: https://acr.ps/1L9F34O
[3] Dieter Haussinger, “Nitrogen Metabolism in Liver: Structural and Functional Organization and Physiological Relevance,” Biochemical Journal, vol. 267, no. 2 (1990), pp. 281-290.
[4] David L. Nelson & Michael Cox, Lehninger Principles of Biochemistry: International Edition ([New York]: Freeman & Company, 2021).
[5] Malcom Watford, “Amino Acids: Ornithine Cycle,” in: Joseph Jez (ed.), Encyclopedia of Biological Chemistry III, vol. 1, 3rd ed. (Amesterdam: Elsevier, 2021), pp. 79-87.
[6] Nelson & Cox, op. cit.
[7] Ibid.
[8] Ibid.
[9] Ibid.
[10] Ibid.
[11] Ibid.
[12] Ibid.
[13]Kara L.Simpson et al., “Urea Cycle Disorders Overview,”GeneReviews (2025), accessed on 3/7/2025, at: https://acr.ps/1L9F32F
[14] “Urea Cycle Disorder,” Cleveland Clinic, accessed on 24/10/2024, at: https://acr.ps/1L9F2YI
[15] Simpson et al, op. cit.
[16] Can Ficicioglu, Marc Yudkoff & Sarah C. Stainbrook, “Diseases & Disorders: Urea Cycle: Disease Aspects,” in: Jez (ed.), pp. 462-471.