النزف تحت العنكبوتية (Subaracnoid hemorrhage) تجمّع الدم في الحيز الفاصل بين غشاءَيْ الأم الحنون والأم العنكبوتيّة من أغشية السحايا المحيطة بالدماغ، ويُعد من الحالات الطبية الطارئة التي تتطلب تدخلًا فوريًا، إذ قد يؤدي إلى تدهور سريع في مستوى الوعي، والدخول في غيبوبة، واختلال في وظائف الدماغ، وقد ينتهي بالوفاة إذا لم يُعالج على نحو عاجل.
تشير الإحصاءات إلى أن نحو 85 في المئة من حالات النزف تحت العنكبوتيّة تعود إلى أسباب غير رضحيّة، وعادة ما تنجم عن انفجار أحد الأوعية الدموية الدماغية ولا سيما في حالات أم الدم، أما النسبة المتبقية فترتبط بإصابات رضحية مباشرة. تبدأ الأعراض عادةً بصداع رعديّ مفاجئ وشديد، ويُعد من أبرز علامات الحالة، ويرافقه غالبًا غثيان وقيء قذفيّ. ويؤدي النزف أيضًا إلى تهيّج السحايا، مسببًا ما يعرف بالحالة السحائية، التي تتظاهر بأعراض تشبه التهاب السحايا. يبدأ تشخيص مصابي النزف تحت العنكبوتيّة من خلال تقييم الأعراض المصاحبة والفحص السريريّ، ثم يُستكمل عبر الفحوصات المخبرية والتصويرية، التي تُجرى بصورة متكررة خلال مدة العلاج لمتابعة تطوّر الحالة وضمان الاستجابة المناسبة للعلاج.
يعتمد العلاج على المراقبة الدقيقة، والتدخّل الدوائي للسيطرة على النزف وخفض ضغط الدم والوقاية من تشنج الأوعية الدموية الدماغية. وقد يتطلّب الأمر أيضًا تدخلًا جراحيًا لإغلاق أم الدم، إما عن طريق الاستئصال الجراحي المباشر وإما من خلال تقنية اللفّ داخل الوعائي التي تُعد من الخيارات الفعالة والآمنة.
تعريفه
النزف تحت العنكبوتية نوع من أنواع
السكتات النزفية، يحدث نتيجة تجمّع الدم داخل الحيّز الموجود بين الطبقة العنكبوتية والأم الحنون من أغشية السحايا المحيطة بالدماغ، يؤدي إلى تراكم الدم في المسافة تحت العنكبوتية، ما قد يسبب ارتفاع الضغط داخل الجمجمة، وتلف أنسجة الدماغ، واضطرابًا في الوظائف العصبية. يصاب من 6 إلى 7 أشخاص من كل 100 ألف شخص بالنزف تحت العنكبوتيّة سنويًا، إلا أنّ المعدّل يرتفع لأسباب غير معروفة إلى نحو 20 حالة لكل 100 ألف سنويًا في اليابان وفنلندا. ورغم أن التقدّم في السن يزيد من فرص الإصابة بالنزف، فإن نصف المرضى المشخّصين تحت سن الـ 55 عامًا. يموت نحو 15 في المئة من مصابي النزف تحت العنكبوتيّة في منازلهم أو خلال نقلهم إلى المستشفيات، وتصل معدلات الوفاة العامّة لهذا النوع من النزف إلى 50 في المئة[1].
أغشية الدماغ أو السحايا
تعرف أغشية الدماغ (Brain membranes) باسم "السحايا" (Meninges)، وهي ثلاث طبقات تحيط بالدماغ والحبل الشوكي لحمايتهما. تتكون السحايا من: الطبقة الخارجية وتسمى الأم الجافية (Dura mater)، وهي الطبقة الأصلب، تليها الطبقة الوسطى المعروفة بالأم العنكبوتية (Arachnoid mater)، وقد سُميت بذلك لتشابه شكلها مع نسيج العنكبوت. أما الطبقة الداخلية فتسمى بالأم الحنون (Pia mater)، وتلتصق مباشرة بسطح الدماغ وتتبعه في تعرجاته جميعها. يفصل بين الأم العنكبوتية والأم الحنون حيّز يعرف بالحيز تحت العنكبوتيّة (Subarachnoid space) الذي يملؤه
السائل الدماغي النخاعي (Cerebro-spinal fluid) ويؤدي دورًا مهمًا في حماية الدماغ وامتصاص الصدمات (الشكل 1).
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
أسبابه
[الشكل2]
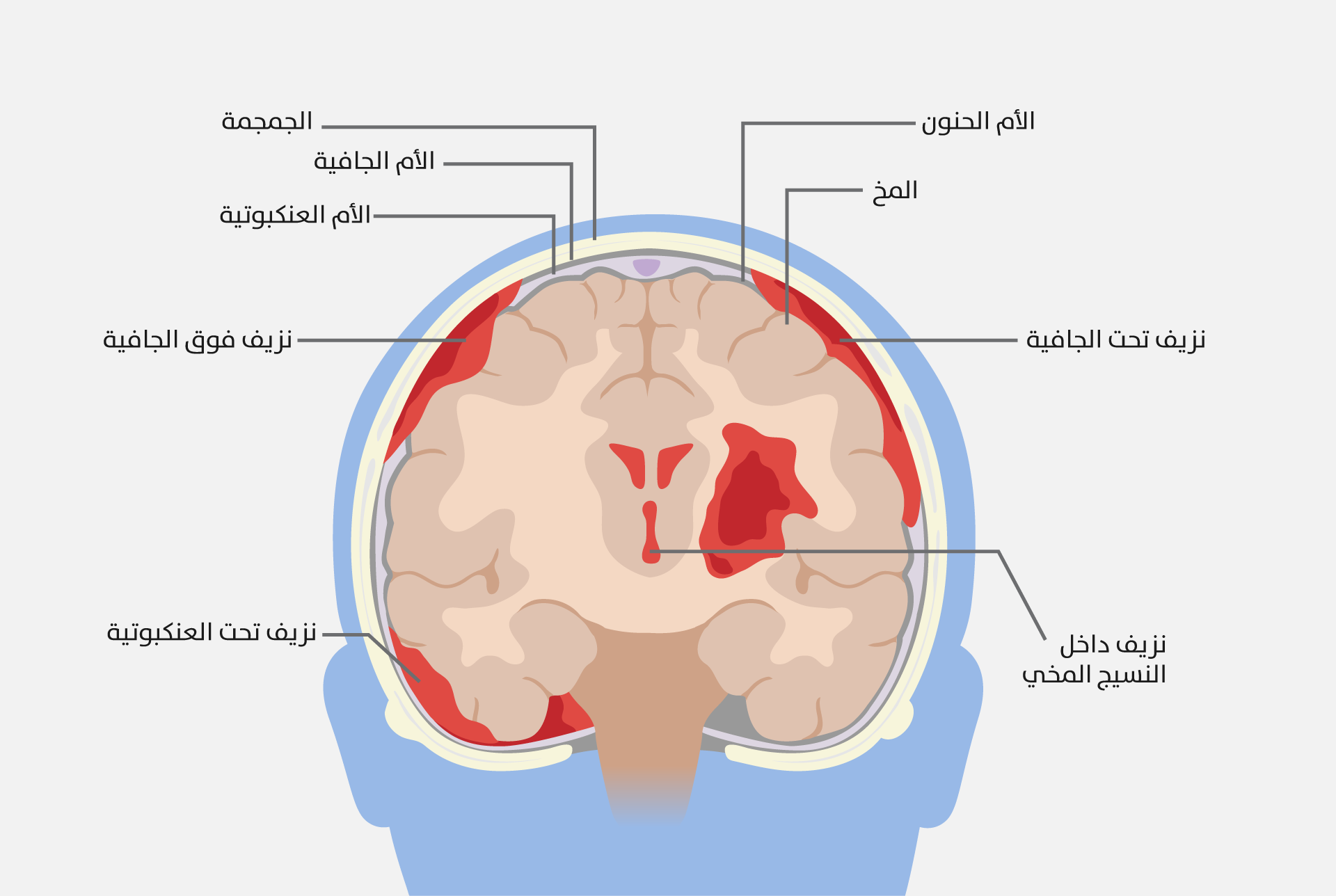 رسم توضيحي لأنواع النزف الدماغي
رسم توضيحي لأنواع النزف الدماغي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
عند تضرر الأوعية الدموية في الدماغ، قد يحدث نزف في مناطق مختلفة بين طبقات السحايا (الشكل 2)، وتحدث السكتات الدماغيّة (Stroke) نتيجة نزف داخل نسيج المخ مباشرة (Intracerebral hemorrhage) أو في الحيز الموجود تحت الطبقة العنكبوتيّة، وذلك ما يعرف بالنزف تحت العنكبوتيّة (Subarachnoid hemorrhage). يؤدي هذا النزف إلى تجمع الدم في الحيّز الفاصل بين الأم الحنون والأم العنكبوتيّة، ويُعد من الحالات الطبية الطارئة التي تتطلب تدخلًا فوريًا، وغالبًا ما يظهر هذا النوع من النزف على شكل صداع مفاجئ شديد يُوصف بالصداع الرعدي (Thunderclap headache). كذلك يهدد هذا النزف حياة المصاب، إذ قد يؤدي إلى تدهور سريع في الوعي، والغيبوبة، وتعطل في وظائف الدماغ، وقد ينتهي بالوفاة إذا لم يُعالج فورًا[2].
[الشكل3]
/أم-الدم-(Aneurysm).png) أم الدم (Aneurysm)
أم الدم (Aneurysm)
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يُعد تحديد طبيعة النزف تحت العنكبوتية أمرًا صعبًا في كثير من الحالات، إلا أن تشخيص السبب الدقيق للنزف يُعد خطوة أساسية قبل البدء بالعلاج، نظرًا إلى اختلاف خطة العلاج بشكل كبير وفقًا للمسبب. وتشير الإحصاءات إلى أن 85 في المئة من حالات النزف تحت العنكبوتيّة تعود إلى أسباب غير رضحيّة (Nontraumatic)، وتكون عادة نزفًا ثانويًا ناجمًا عن انفجار في مكان تمدد أحد الأوعيّة الدمويّة الدماغية، أو ما يعرف بأمّ الدم (Aneurysm) (الشكل 3). في حين ترتبط نسبة 15 إلى 20 في المئة من الإصابات بأسباب متنوعة، من ضمنها الإصابات الرضحيّة. وتصنّف مسببات النزف تحت العنكبوتيّة غير الرضحيّة إلى مجموعتين رئيستين:
النزف تحت العنكبوتية الناتج من أم الدم
يحدث النزف تحت العنكبوتية الناتج من أم الدم (Aneurysmal Subarachnoid hemorrhage) عند انفجار أم الدم الدماغية، وتعد خللًا خلقيًا أو مكتسبًا في جدران الأوعية الدمويّة الدماغيّة، يجعلها أكثر عرضة للانهيار تحت ضغط الدم المتدفّق. وتعد العوامل الصحيّة المرتبطة بحدوث أم الدم في الدماغ هي ذاتها العوامل المرتبطة بزيادة فرصة انفجارها لاحقًا، مثل ارتفاع ضغط الدم (Hypertension) والتدخين المستمر، وتناول المشروبات الكحوليّة، أو وجود تاريخ عائلي للإصابة بهذا النوع من الأمراض. وتزداد فرصة انفجار أم الدم الدماغيّة لدى الأشخاص الذين تزيد أعمارهم على 60 عامًا، أو في حال ازدياد حجم أم الدم بقطر يتجاوز 5 سنتميترات. علاوة على ذلك، قد يُحفَّز انفجارها نتيجة نشاط بدني عنيف، كأداء التمارين الرياضية أو التعرّض لانفعال شديد، غير أن هذا يعتمد أساسًا على مدى استقرار جدران الأوعية الدموية المحيطة بأم الدم[3].
النزف تحت العنكبوتيّة غير الناتج من أم الدم
ينقسم النزف تحت العنكبوتيّة غير الناتج عن أم الدم (Nonaneurysmal Subarachnoid Hemorrhage) إلى خمسة أقسام رئيسة:
النزف حول الدماغي غير الناتج من أم الدم تحت العنكبوتية
يعدّ النزف حول الدماغي غير الناتج من أم الدم تحت العنكبوتية (Perimesencephalic nonaneurysmal subarachnoid hemorrhage) غير مؤذٍ، إذ ينساب الدم ويتجمّع في الصهاريج الدماغية (Cisterns) المحيطة بالدماغ الأوسط (Midbrain). ويحدث هذا النوع عادة نتيجة لنزف في المنطقة الأمامية للدماغ الأوسط أو جسر جذع الدماغ، ويتميّز بتوزيع الدم بشكل محدد يظهر عند التصوير بالأشعة المقطعيّة (Computed tomography (CT) scan, CT scan)، إذ يظهر الدم محصورًا في الصهاريج الدمويّة حول الدماغ، وأمام جذع الدماغ. ويُشخص هذا النوع من النزف عند مشاهدة النمط الخاص به في صور الأشعة، علاوة على تصوير وعائيّ دماغي طبيعي، وأعراض محدودة، نظرًا إلى الطبيعة البطيئة والمستمرة للنزف.
أم الدم الغامضة
قد يعجز التصوير الوعائي الأوليّ عن تشخيص مرضى النزف تحت العنكبوتيّة وتحديد سبب النزف، ومع ذلك، فقد يظهر السبب لاحقًا عند إجراء تصوير متكرر، ففي هذه الحالة، يُوصف النزف بـ"الغامض" أو ما يعرف بأم الدم الغامضة (Occult aneurysm)، إذ تظهر أعراض النزف تحت العنكبوتية على المرضى، ولكن التصوير الإشعاعي لا يحدد مكان أم الدم أو يلاحظها فورًا، بل يظهرها بعد مدة من الزمن، وذلك يحدث أحيانًا بسبب أخطاء تقنيّة في التصوير أو في تفسيره، أو عندما تكون أم الدم صغيرة الحجم. كذلك قد يسبب وجود تشنّج دموي أو جلطات في أم الدم حجبَ الأشعة التصويريّة عن مكان النزيف، ما يجعل التشخيص أصعب.
تشوه الأوعية الدموية
تحدث تشوّهات الأوعية الدموية (Vascular malformations) في مواقع متعددة من الجهاز العصبي ونظام التروية الدموية، إلا أن التشوّهات الوعائية التي قد تؤدي إلى نزف تحت العنكبوتية تكون غالبًا داخل الدماغ أو النخاع الشوكي. وتشمل هذه الحالات عادةً التحوّلات الشريانية الوريدية(Arteriovenous malformations, AVMs)، أو الناسور الشرياني الوريدي الجافي (Dural Arteriovenous Fistula). تُكتشف هذه التشوّهات بوضوح من خلال التصوير الوعائي للدماغ، ويُعالج معظمها إما جراحيًا بشكل مباشر وإما من خلال التداخلات الوعائية باستخدام المناظير.
تسلّخ شريانيّ دماغيّ
يحدث هذا النوع من النزف تحت العنكبوتيّة عند حدوث تسلّخ في أحد الشرايين داخل الدماغ (Intracranial arterial dissection) وامتداده إلى الغلالة البرانيّة (Tunica Adventitia) مسببًا نزفًا حادًا وشديد الخطورة. يُشخّص هذا النوع من النزف عبر التصوير الوعائي التقليديّ، ويعالج إما جراحيًا وإما عبر التدخّل الوعائي باستخدام التنظير (Endovascular intervention).
أسباب أخرى
تحدث بعض حالات النزف تحت العنكبوتيّة لأسباب نادرة، مثل استخدام الأدوية المضادّة للتخثّر (Anticoagulants)، أو تعاطي الكوكايين (Cocaine)، أو الإصابة بفقر الدم المنجليّ (Sickle cell anemia). كذلك تتسبب بعض الأورام الدماغيّة في هذا النوع من النزف، إلى جانب أمراض الأوعية الدمويّة كمرض بهجت {{مرض بهجت (Behçet’s disease): اضطراب مناعي ذاتي نادر يُسبب التهابات في الأوعية الدموية قد تصيب مختلف أنحاء الجسم. يتميّز هذا المرض بظهور أعراض متفرقة ومتفاوتة من شخص إلى آخر، وتشمل تقرحات مؤلمة في الفم والأعضاء التناسلية، وطفحًا جلديًا أو بقعًا مؤلمة عادةً في أسفل الساقين، إلى جانب التهابات في العينين، وآلام في المفاصل، وقد تمتد الأعراض لتشمل الجهاز الهضمي أو الجهاز العصبي المركزي.}} والتهاب الشرايين العُقدي (Polyarteritis nodosa)[4].
الفيزيولوجيا المَرَضية في نشوء أم الدم الدماغية
تشير الأبحاث إلى أنّ الالتهابات التي تصيب جدران الأوعيّة الدمويّة تعدّ عاملًا أساسيًا في تطور أم الدم، إذ تتكون نتيجة إصابة أو تلف تتعرض له جدران الأوعية الدمويّة، وتنجم من ذلك سلسلة من التفاعلات الالتهابية تسبب موتًا مبرمجًا (Apoptosis) في الخلايا العضليّة الملساء (Smooth muscle cells)، وتحلل النسيج الخلويّ الخارجيّ بوساطة إنزيمات الميتالوبروتيناز الخاصة بالمادة الخلاليّة (Matrix metalloproteinases). ونتيجة لذلك، تضعف بنية جدران الأوعية الدمويّة بشكل كبير، ما يؤدي إلى تمددها بفعل ضغط الدم المتدفّق، ونشوء أم الدم أو كيس دمويّ الذي قد ينفجر في ما بعد.
ورغم التقدم في فهم آلية نشوء أم الدم الدماغيّة، فإنه لا تزال ثمة كثير من الثغرات المعرفية، ولا سيما في ما يتعلق بالعوامل المؤدية إلى انفجارها، إلا أنّ الضغط الديناميكي الدموي يُعدّ العامل الأساسي المسهم في نشأتها، إذ تتركز هذه التشوّهات عادة في المناطق التي يتعرّض فيها جدار الوعاء لضغط زائد، مثل نقاط تفرّع الشرايين أو التقائها في زوايا حادة. ومن أبرز المواقع التي تظهر فيها هذه التشوّهات نقطة تشعّب الشريان القاعديّ (Basilar artery) عند نقطة تفرّع الشريان المخيخي السفلي الخلفي (Posterior inferior cerebellar artery)، أو عند الشريان الفقاري (Vertebral artery)، وكذلك الشريان الواصل الأمامي (Anterior communicating artery).
يتضخّم حجم أم الدم إلى درجة تضغط فيها على أنسجة الدماغ المحيطة، ما يؤدي إلى علامات سريريّة عصبيّة موضعيّة. أما في حال انفجارها، فإنها تعوق تدفق الدم إلى الأنسجة الدماغيّة الواقعة خلفها، مسببةً تشنّجًا وعائيًا يعقبه
نقص تروية دماغي (Cerebral ischemia).
[الشكل4]
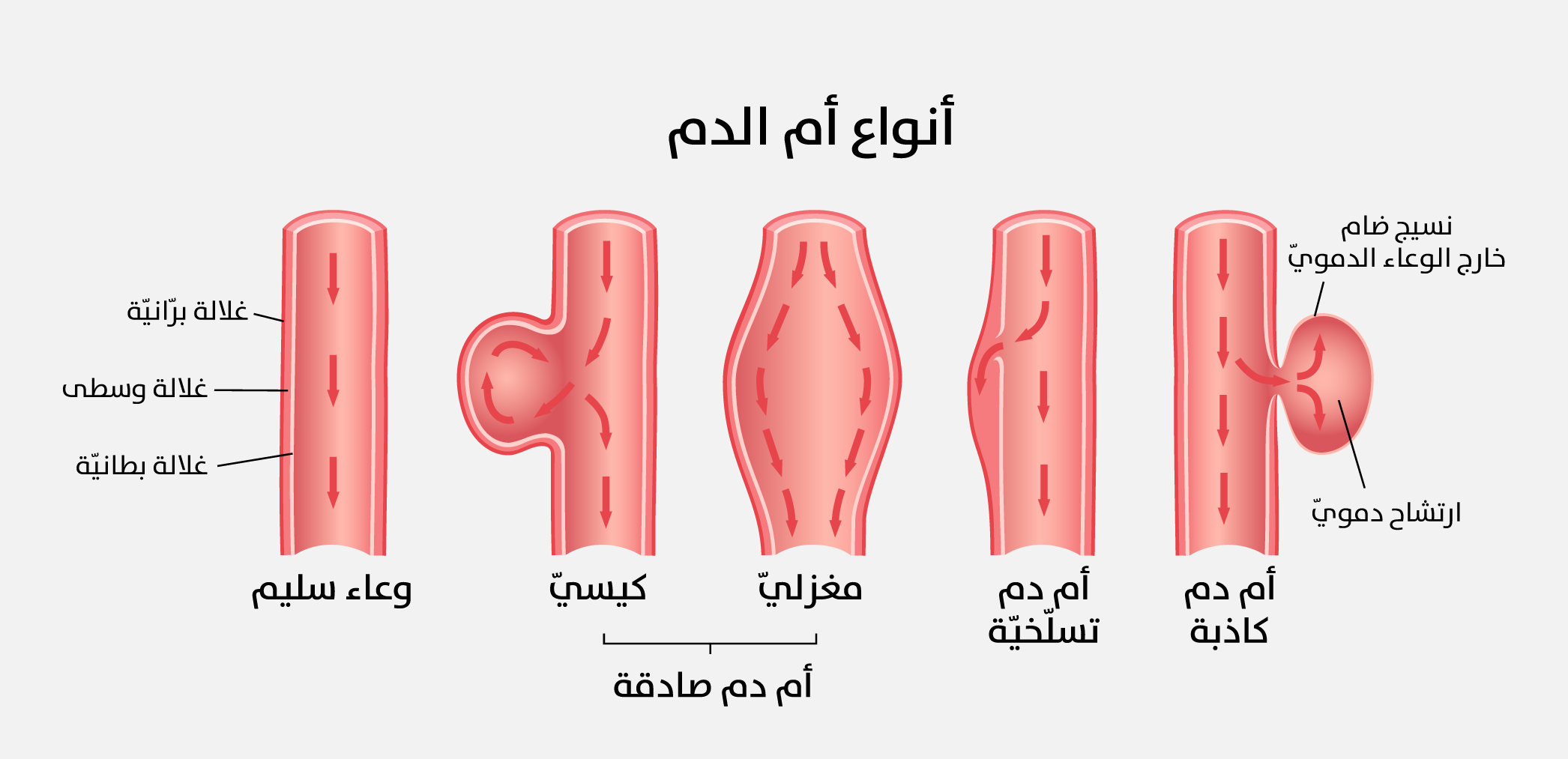 أنواع أم الدم
أنواع أم الدم
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تُصنّف أم الدم من الناحية البنيويّة وفقًا للتشريح النسيجي المرضي إلى ثلاثة أنواع رئيسة: النوع الأول هو أم الدم الكيسيّة (Saccular aneurysm)، التي تظهر على شكل زوائد أو حويصلات بارزة من جدار الوعاء الدموي، وغالبًا ما توجد عند تفرّعات الشرايين الدماغيّة. أما النوع الثاني فهو أم الدم المغزليّة (Fusiform aneurysm)، إذ يحدث توسّع موضعي في مقطع من الوعاء الدموي من دون تشكّل جيوب أو حويصلات. وأما النوع الثالث فهو التمدد أو التطاول الوعائي الدموي (Vascular elongation (dolichoectasia))، ويتميّز بتطاول أجزاء من الوعاء الدموي والتوائها، مع احتمالية حدوث توسّع في بعض المواضع. وثمة نوع رابع يُشار إليه أحيانًا بعد التسلّخ الشرياني (Arterial dissection)، ويُعدّ من الناحية التشريحية قريبًا من الشكل المغزلي (الشكل 4)[5].
العلامات والأعراض
تبدأ أعراض النزف تحت العنكبوتيّة عادةً بصداع رعديّ (Thunderclap headache) مفاجئ وشديد يصفه المريض عادّة بأنّه "أسوأ صداع شعر فيه بحياته"، ويصحبه غالبًا غثيان وقيء قذفيّ، ويحدث أيضًا تهيّج في أنسجة الدماغ والنخاع الشوكيّ بسبب انتشار الدم تحت العنكبوتيّة واختلاطه بالسائل الدماغي الشوكي (Cerebrospinal fluid, CSF). وينتشر الدم في البطين الدماغي الرابع مسببًا ما يعرف بالحالة السحائيّة (Meningismus)، وهي حالة تؤدي إلى أعراض شبيهة بالتهاب السحايا (Meningitis)، مثل تيبّس الرقبة، وألم في مؤخرة الرأس، ورهاب الضوء، ولكنها لا تكون مصحوبة بالحمى أو علامات العدوى.
يستدعي ظهور هذه الأعراض إجراء فحص سريريّ دقيق وتقييم إشعاعيّ للمريض لتحديد موقع الإصابة ومدى شدّتها، إذ يُسهم الفحص العصبي في الكشف عن
العجز العصبي البؤري (Focal neurological deficit)، ويوفّر أيضًا قاعدة مرجعيّة لتقييم تحسّن حالة المريض بعد العلاج. وفي بعض الحالات، قد يؤدي النزف إلى تدهور في مستوى الوعي أو غيبوبة، ما يستدعي تدخّلًا عاجلًا لتجنّب التلف العصبي الدائم.
وفي بعض الحالات، تظهر الأعراض العصبيّة في مراحل مبكرة نتيجة الضغط الذي تسببه أم الدم المتوسعة على الأنسجة المحيطة، أو بسبب ارتفاع الضغط داخل القحف بعد انفجارها، ما قد يؤدي إلى
شلل في الأعصاب القحفية (Cranial nerve palsies)، ولا سيما العصبان الثالث والسادس، أو قد يظهر بشكل نوبات صرعية[6].
التشخيص
يبدأ تشخيص مصابي النزف تحت العنكبوتيّة من الأعراض المصاحبة والفحص السريريّ، لتبدأ بعدئذٍ مرحلة التقييم والتشخيص المخبري والإشعاعي، وتتضمن الفحوصات ما يأتي:
- فحص قاع العين
عند الشك في نزف تحت العنكبوتيّة، لا بد من إجراء فحص لقاع العين، للتأكد من عدم حدوث نزف داخل العين (Intraocular hemorrhage). ويحدث النزف داخل العين بنسبة عالية لدى مرضى النزف تحت العنكبوتية الذين تراجع مستوى الوعي عندهم. ويظهر النزف داخلها في ما وراء الشبكيّة كخطوط طوليّة من الدم، أو كنزف على شكل ألسنة اللهب، ويكون عادة قرب القرص البصري (Optic disc). وعندما يكون النزف شديدًا، يمتد نزف ما وراء الشبكيّة حتى الجسم الزجاجي للعين، مسببًا نقاطًا أو بقعًا حمراء للمريض، في ما يعرف بمتلازمة تيرسون (Terson’s syndrome).
- تصوير الأشعة المقطعيّة (CT)
يُعد التصوير الطبقي للدماغ الخطوة الأولى في تقييم حالات النزف تحت العنكبوتية، إذ يُستخدم لتحديد وجود النزف وتقدير موقعه وحجمه بدقة في حال جرى الكشف عن أم دم نازفة. أما إذا كانت نتيجة التصوير المقطعي سلبية، فيُوصى باللجوء إلى وسائل تشخيصية أدق للتأكد من عدم وجود نزف خفي. ويشار إلى أن الأشعة المقطعية قادرة على كشف النزف تحت العنكبوتية في نحو 95 في المئة من الحالات خلال أول 24 ساعة من حدوثه، إلا أن حساسيتها تنخفض مع مرور الوقت نتيجة تَوزُّع الدم داخل الأنسجة، ما يزيد من صعوبة اكتشافه (الصورة 1).
[الصورة1]
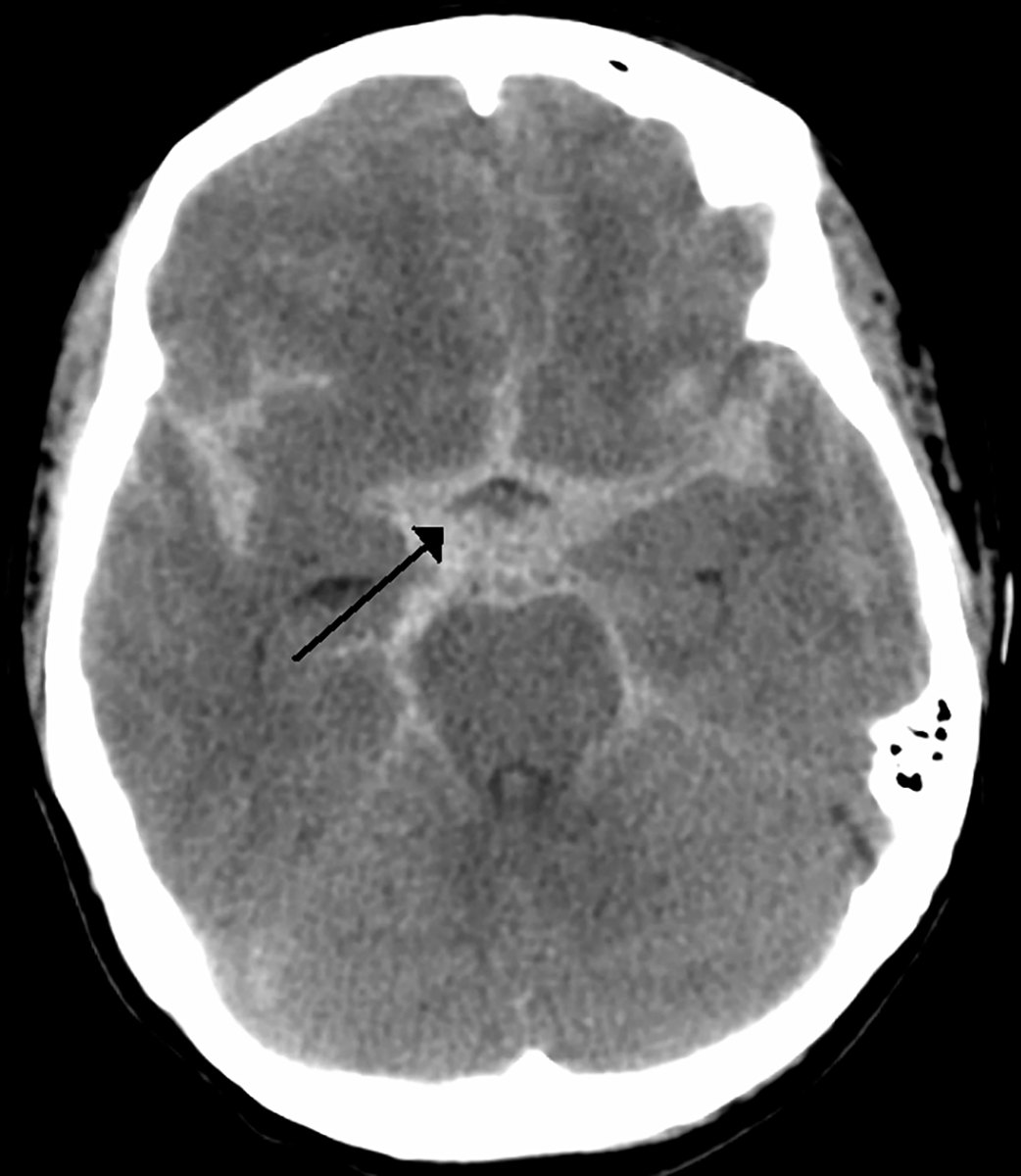 صورة أشعة مقطعيّة لمريض يعاني نزفًا تحت العنكبوتيّة
صورة أشعة مقطعيّة لمريض يعاني نزفًا تحت العنكبوتيّة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
- البزل القَطَني
عند الاشتباه في وجود نزف تحت العنكبوتية مع نتيجة سلبية للتصوير المقطعي، يُعد البزل القطني القَطَني (Lumbar puncture) ضروريًا لتحليل السائل الدماغي النخاعي (CSF) ويُفضل إجراء هذا الفحص بعد مرور 6 ساعات على التصوير المقطعي، أو بعد 12 ساعة منذ بدء الأعراض، ولا سيما الصداع، إذ إن وجود الدم الطازج في السائل قد يربك التشخيص ويصعّب التمييز بين النزف الحقيقي والنزف الناتج من عملية البزل نفسها. وبعد مرور هذه المدة، تكون كريات الدم الحمراء - في حال وجود نزف - قد تحللت، محررة الهيموغلوبين الذي يتحول إلى أصباغ تسبب اصفرار السائل الدماغي النخاعي، وهي ظاهرة تُعرف بالزنخة (Xanthochromia)، وتُعد علامة مميزة للنزف تحت العنكبوتية (الصورة 2).
[الصورة2]
 صورة توضيحية يظهر في يسارها سائل عصبي نخاعي سليم، وفي يمينها سائل عصبيّ مصفرّ
صورة توضيحية يظهر في يسارها سائل عصبي نخاعي سليم، وفي يمينها سائل عصبيّ مصفرّ
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
وإذا كان السائل المستخرج صافيًا وخاليًا من علامات النزف، فيجب حينئذٍ قياس ضغطه لتقييم وجود اضطرابات أخرى مثل الجلطات الدماغية أو انخفاض الضغط داخل القحف، علاوة على ضرورة زراعته مخبريًا لاستبعاد العدوى أو التهاب السحايا.
- الرنين المغناطيسي
نظرًا إلى ارتفاع تكلفة التصوير بالرنين المغناطيسي (Magnetic resonance imaging, MRI) وصعوبة توفره في بعض المراكز، يُعتمد عادةً على التصوير الطبقي بوصفه وسيلة أوليّة لتشخيص النزف تحت العنكبوتية، ولا سيما خلال الأيام الأولى من حدوثه. ومع مرور الوقت وتراجع قدرة التصوير الطبقي على كشف النزف نتيجة لتوزع الدم وتغير كثافته، يُصبح التصوير بالرنين المغناطيسي (MRI) الخيار الأدق والأكثر كفاءة لتحديد وجود النزف ومكانه بدقة أكبر.
- التصوير الوعائي
يُعد التصوير الوعائي (Angiography) أداة أساسية في تشخيص أم الدم، ويُستخدم أيضًا في حالات النزف تحت العنكبوتية لتحديد موضع النزف والكشف عن أم الدم المسببة، مع تقديم تفاصيل دقيقة بشأن حجمها وعلاقتها التشريحية بالبنى المحيطة، ما يُساعد في اختيار التدخل العلاجي الأنسب. ويمكن إجراء هذا النوع من التصوير باستخدام الأشعة الطبقية أو الرنين المغناطيسي، ويمكن تنفيذه أيضًا من خلال تنظير الأوعية الدموية مباشرة. ومع ذلك، يجب توخي الحذر عند استخدام هذه التقنية، إذ قد تؤدي في بعض الحالات إلى تمزق أم دم غير منفجرة، لذا يُفضل تجنبها عندما تتوفر بدائل تشخيصية آمنة وفعالة.
- فحوصات أخرى
تُستخدم بعض الفحوصات المساندة للمساعدة في تشخيص النزف تحت العنكبوتية، ومنها تخطيط القلب (Electrocardiogram)، ولا سيما في الحالات التي يحدث فيها انخفاض في ضغط الدم نتيجة النزف، إذ قد يُظهر التخطيط تغيرات تشبه تلك المصاحبة للذبحة الصدرية. كذلك تُجرى تحاليل الدم في المراحل الأولى من التشخيص بوصفها أداة داعمة للتصوير الطبقي، إلا أن فاعليتها في الكشف عن النزف تقل تدريجيًا مع مرور الوقت وظهور الأعراض[7].
المقاييس التصنيفية للنزف تحت العنكبوتية
من الناحية السريرية، يعتمد الأطباء على معايير ومقاييس موحّدة لتقييم تحسّن المرضى المصابين بالنزف تحت العنكبوتية، وتعتمد هذه المقاييس بصورة رئيسة على نتائج الفحص العصبي السريري الأولي، ومدى وجود الدم في أول صورة للأشعة المقطعية. ومن أبرز هذه المقاييس التصنيفيّة:
- مقياس غلاسغو للغيبوبة
طُوِّر مقياس غلاسغو للغيبوبة (Glasgow Coma Scale, GCS) عام 1974 لتقييم مستوى الوعي والإدراك لدى المرضى، ويستخدم لتحديد الحالة العصبية العامة للمريض، ولا سيما في حالات إصابات الدماغ. يعتمد هذا المقياس على ثلاثة مؤشرات رئيسة، وهي: الاستجابة اللفظية، والاستجابة الحركيّة، والاستجابة البصريّة في حالة اليقظة التامة. ويُقيَّم كل محور من محاور المقياس بنظام نقاط تُجمع للحصول على النتيجة النهائية، إذ تُعدّ الدرجة 3 الأدنى، وتشير إلى غيبوبة عميقة، في حين تمثّل الدرجة 15 الحد الأعلى، وتدلّ على يقظة تامة.
- المقياس التدرّجي للاتحاد العالمي لجمعيات جراحة الأعصاب
يعتمد المقياس التدرّجي للاتحاد العالمي لجمعيات جراحة الأعصاب (The World Federation of Neurosurgical Societies (WFNS) Grading Scale) على مقياس غلاسغو للغيبوبة، علاوة على وجود العجز العصبي البؤري أو غيابه. ويعد هذا المقياس فعّالًا في قياس التحسّن في حالات النزف تحت العنكبوتيّة، ويساعد في تصنيف المرضى إلى درجات من الأولى (الأخف) حتى الخامسة (الأشد)، بناءً على مستوى الوعي والعلامات العصبية.
- مقياس هانت وهيس التدرجيّ
طُوِّر مقياس هانت وهيس التدرجيّ (Hunt and Hess grading scale) عام 1968، ويهدف إلى تقدير مآلات الحالة ونتائجها الصحيّة النهائية، وذلك من خلال تصنيف المرضى إلى خمس درجات وفقًا لشدة الحالة العصبية ومستوى الوعي.
- مقياس فيشر التدرّجي
يُستخدَم مقياس فيشر التدرّجي (Fisher Grading Scale) لتقدير كميّة الدم في المساحات تحت العنكبوتية كما تُظهرها الصورة المقطعيّة، ويُصنِّف الحالة ضمن درجات من 1 إلى 4 تعكس شدة النزف، والحالة السريريّة لأعراض أم الدم، والتشنّج الوعائي الدمويّ، ولا سيما في ما بعد النزف تحت العنكبوتيّة. وفي عام 2001، حُدِّث هذا المقياس ليُعرَف باسم مقياس فيشر التدرجيّ المعدّل (Modified Fisher Grading Scale)[8].
العلاج
يعد النزف تحت العنكبوتيّة حالة طارئة تستوجب المراقبة المستمرّة والعلاج المباشر. يبدأ العلاج لمرضى النزف تحت العنكبوتيّة بالتقييم الأوليّ، وتحديد النقطة المرجعيّة للحالة سريريًا، ويستخدم لذلك أساليب كمقياس غلاسغو، وتخطيط القلب، والتصوير الطبقيّ المتكرر، وفحوصات العيون، والفحوصات العصبيّة السريريّة العامة والبؤريّة. وتتكرر هذه الفحوصات دوريًا للتأكد من استقرار حالة المريض وتلقيه العلاجَ المناسب. ومن الجدير بالذكر أن العلاج الدوائي يختلط بالعلاج التدخلي في حالات النزف تحت العنكبوتيّة.
وفي العلاج الدوائي، يفضل استشارة الصيادلة بشأن استخدام الأدوية وتحديد جرعاتها، مثل مضادات الصرع (Antiepileptics)، ومضادات التخثر (Anticoagulants)، والمضادات الحيوية (Antibiotics)، ومسكنات الألم، وغيرها، وذلك وفقًا للاحتياجات والتقييم السريري لكل حالة. علاوة على ذلك، يحتاج مرضى النزف تحت العنكبوتيّة إلى السيطرة على ضغط الدم بدقة، منعًا لتكرار النزف، أو ارتفاع الضغط داخل الجمجمة، أو حدوث استسقاء دماغيّ (Hydrocephalus)، سواء نتيجة وجود أم الدم أم بسبب العلاجات الوريديّة المتكررة. ويضاف إلى ذلك أيضًا فرط تحفيز الجهاز العصبي السمبثاوي (Sympathetic nervous system) الذي يؤدي بدوره إلى رفع ضغط الدم.
تستخدم عدة علاجات للسيطرة على ضغط الدم، منها حاصرات البيتا (Beta-blockers) مثل لابيتولول (Labetalol)، وحاصرات قنوات الكالسيوم (Calcium channel blockers) مثل نيكاريدبين (Nicardipine)، كذلك تسهم مسكنات الألم الأفيونية (Opioid analgesics)، التي تُعطى غالبًا للمرضى، في ضبط ضغط الدم أيضًا.
يتطلب علاج النزف تحت العنكبوتيّة أيضًا التركيز على منع حصول تشنّج وعائي، وعلاجه في حال حدوثه، باستخدام عدة علاجات كحاصرات قنوات الكالسيوم، والمغنيسيوم، ومضادات الإندوثيلين (Endothelin antagonist)، والستاتينات (Statins).
علاوة على العلاج الدوائي، يحتاج مرضى النزف تحت العنكبوتيّة إلى التدخّل الجراحي، ولا سيما لمعالجة أم الدم المنفجرة، إذ تكون هذه المعالجة إمّا عبر الاستئصال الجراحي المباشر، وإما عبر اللف داخل الوعائي (Endovascular coiling) الذي يعد العلاج الأنجع. ويُنصح بإجراء التدخلات الجراحية العاجلة خلال 24 ساعة من انفجار أم الدم[9].
المآلات
يرتبط النزف تحت العنكبوتية عمومًا بمعدل وفيات مرتفع، حتى بين المرضى الذين يصلون إلى المستشفى أحياء، ويحدث ذلك بسبب النزف الأولي نفسه أو نتيجة تكرار النزف، أو بسبب تشنّج الأوعية الدمويّة مسببًا اختناقًا لأنسجة الدماغ، أو الاستسقاء الدماغي، أو ارتفاع ضغط الدماغ، أو نوبات الصرع والنوبات القلبيّة[10]. ويموت 45 في المئة من مرضى النزف خلال الـ 30 يومًا الأولى[11].
قد ينتج من الإصابة بالنزف فوق العنكبوتيّة عدة مضاعفات على المديين القصير أو البعيد. أما مضاعفات المدى القصير، فقد يصاب المريض بسكتة قلبيّة، أو فشل في عضلة القلب، بسبب هبوط الضغط المفاجئ أو بسبب اضطراب نبضات القلب، علاوة على الاستسقاء الرئوي والتهابات الرئة. أمّا مضاعفات المدى البعيد، فقد يصاب المرضى بمضاعفات عصبيّة أو إدراكيّة، علاوة على نوبات الصرع وغيرها من أنواع العجز العصبيّ البؤري[12].
المراجع
Abraham, Michael K. & Wan-Tsu Wendy Chang. “Subarachnoid Hemorrhage.”
Emergency Medicine Clinics of North America. vol. 34, no. 4 (2016). pp. 901-916.
Christopher R. Carpenter, “Spontaneous Subarachnoid Hemorrhage: A Systematic Review and Meta‐analysis Describing the Diagnostic Accuracy of History, Physical Examination, Imaging, and Lumbar Puncture with an Exploration of Test Thresholds,”
Academic Emergency Medicine, vol. 23, no. 9 (2016), pp. 963-1003.
Etminan, Nima. “Worldwide Incidence of Aneurysmal Subarachnoid Hemorrhage According to Region, Time Period, Blood Pressure, and Smoking Prevalence in the Population: A Systematic Review and Meta-Analysis.”
JAMA Neurology. vol. 76, no. 5 (2019). pp. 588-597.
Gijn, Jan Van. “Subarachnoid Haemorrhage.”
Lancet. vol. 369, no. 9558 (2007). pp. 306-318.
Hine, Jason. “Approach to the Diagnosis and Management of Subarachnoid Hemorrhage.”
The Western Journal of Emergency Medicine. vol. 20, no. 2 (2019). pp. 203-211.
Lindbohm, Joni Valdemar. “Risk Factors of Sudden Death From Subarachnoid Hemorrhage.”
Stroke. vol. 48, no. 9 (2017). pp. 2399-2404.
Vlak, Monique H. M. “Trigger Factors for Rupture of Intracranial Aneurysms in Relation to Patient and Aneurysm Characteristics.”
Journal of Neurology. vol. 259, no. 7 (2012). pp. 1298-1302.
Wee, N. Van der et al. “Detection of Subarachnoid Haemorrhage on Early CT: Is Lumbar Puncture Still Needed after a Negative Scan?”
Journal of Neurology, Neurosurgery, and Psychiatry. vol. 58, no. 3 (1995). pp. 357-359.
Ziu, Endrit, Mahammed Z. Khan Suheb & Fassil B. Mesfin. “Subarachnoid Hemorrhage.” in:
StatPearls. Treasure Island, FL: StatPearls Publishing, 2023. at: https://acr.ps/1L9F2b5
[1] Christopher R. Carpenter, “Spontaneous Subarachnoid Hemorrhage: A Systematic Review and Meta‐analysis Describing the Diagnostic Accuracy of History, Physical Examination, Imaging, and Lumbar Puncture with an Exploration of Test Thresholds,”
Academic Emergency Medicine, vol. 23, no. 9 (2016), pp. 963-1003.
[2] Joni Valdemar Lindbohm, “Risk Factors of Sudden Death From Subarachnoid Hemorrhage,”
Stroke, vol. 48, no. 9 (2017), pp. 2399-2404.
[3] Monique H. M. Vlak, “Trigger Factors for Rupture of Intracranial Aneurysms in Relation to Patient and Aneurysm Characteristics,”
Journal of Neurology, vol. 259, no. 7 (2012), pp. 1298-1302.
[4] Nima Etminan, “Worldwide Incidence of Aneurysmal Subarachnoid Hemorrhage According to Region, Time Period, Blood Pressure, and Smoking Prevalence in the Population: A Systematic Review and Meta-Analysis,”
JAMA Neurology, vol. 76, no. 5 (2019), pp. 588-597.
[5] Vlak.
[6] Lindbohm; Jan Van Gijn, “Subarachnoid Haemorrhage,”
Lancet, vol. 369, no. 9558 (2007), pp. 306-318.
[7] N. Van der Wee et al., “Detection of Subarachnoid Haemorrhage on Early CT: Is Lumbar Puncture Still Needed after a Negative Scan?”
Journal of Neurology, Neurosurgery, and Psychiatry, vol. 58, no. 3 (1995), pp. 357-359; Jason Hine, “Approach to the Diagnosis and Management of Subarachnoid Hemorrhage,”
The Western Journal of Emergency Medicine, vol. 20, no. 2 (2019), pp. 203-211.
[8] Endrit Ziu, Mahammed Z. Khan Suheb & Fassil B. Mesfin, “Subarachnoid Hemorrhage,” in:
StatPearls (Treasure Island, FL: StatPearls Publishing, 2023), accessed on 9/9/2025, at:
https://acr.ps/1L9F2XL
[9] Hine.
[10] Gijn.
[11] Michael K. Abraham & Wan-Tsu Wendy Chang, “Subarachnoid Hemorrhage,”
Emergency Medicine Clinics of North America, vol. 34, no. 4 (2016), pp. 901-916.
[12] Gijn.