الدهون (الشحميّات) السفينغولية (Sphingolipids) هي فئة رئيسة من الدهون إلى جانب الفئات الرئيسة الأخرى منها، هي:
الدهون الفسفورية والستيرولات والدهون الثلاثية. تُوجَد الدهون السفينغولية في جميع
خلايا الكائنات
حقيقية النواة، بما فيها
خلايا الإنسان، وفي
الدورة الدموية أيضًا. تشكِّل القواعد السفينغولية نواةَ الدهون السفينغولية، ويعتبر جزيء
السفينغوسين القاعدةَ السفينغولية الأوسع انتشارًا في جسم الإنسان، إذ هو الوحدة البنائية الأساسية لتكوين المئات، إن لم يكن الآلاف، من الجزيئات الدهنية السفينغولية المختلفة. ولهذه الدهون وظائف متعدّدة ومتميّزة في الخلية، إذ تُعتبر مكوناتٍ هيكلية للأغشية الخلوية، وجزيئاتٍ تنظيمية، ومركباتِ إشارة. وقد ولّدت هذه الجوانب المتعددة اهتمامًا كبيرًا بهذه الفئة من الدهون، إذ تشير وظائفها إلى عمليات بيولوجية مهمة، في حين توجد اختلالات
استقلابها في العديد من الأمراض، بما في ذلك الأمراض الوراثية، والسرطان، والأمراض التنكسية العصبية، والأمراض المُعدِية، وأمراض القلب والأوعية الدموية، والأمراض الاستقلابية.
اكتشاف الدهون السفينغولية
 أبو الهول اليوناني مع أوديب
أبو الهول اليوناني مع أوديب يوهان ثوديكوم
يوهان ثوديكوم
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
عُزِلت الدهون (الشحميّات) السفينغولية (Sphingolipids) لأول مرة عن أنسجة
الدماغ بجهود الطبيب الألماني
يوهان لودفيغ ثوديكوم (Johann Ludwig Thudichum، 1829-1901)، وهو عالم كان يعمل في لندن بالمملكة المتحدة في منتصف القرن التاسع عشر، وشملت اهتماماته البحثية تحليلَ التركيب الكيميائي للدماغ. وأثناء دراساته هذه، عزل بعض المواد الدهنية عن
الدماغ، ولكنه لم يستطع عزل جميع المواد الدهنية، إذ ظلّ بعضها غير قابل للذوبان حسب أساليب العزل التي اتبعها آنذاك. ونظرًا إلى حيرته بشأن ما يمكن أن تكون عليه هذه المركّبات، أطلق على المادة اسم "سفينغوسين" (Sphingosine)، نسبة إلى اسم أبي الهول اليوناني (Sphinx) المشهور في الميثولوجيا اليونانية بسبب اللغز المحيِّر الذي عرضه على أوديب[1]. كما استطاع ثوديكوم عزل
السفينغوميالين (Sphingomyelin)، والسولفاتيد (Sulfatide)، وغالاكاتوزيل سيراميد (Galactosylceramide)[2]، وجميعها دهون سفينغولية مهمة[3].
ظلّ مجال الدهون السفينغولية وأبحاث
السفينغوسين خاملًا نسبيًّا حتى أوائل القرن العشرين، عندما بُدِئَ باستعمال الأساليب الكيميائية الحديثة في توضيح تركيب
السفينغوسين والدهون السفينغولية الأخرى وأشكالها، فاكتُشِف التركيب الكيميائي للسفينغوميالين في عشرينيات القرن العشرين، وتركيب
السفينغوسين في أربعينيات القرن نفسه[4]. وخلال منتصف القرن العشرين وأواخره، أُرسِيت أشكال معظم الدهون السفينغولية والكيمياء الفراغية الخاصة بها، خصوصًا للفئة الفرعية المسماة
الدهون السفينغولية السكريّة (Glycosphingolipids). لفَتَ العمل الذي بدأه العالم الياباني سن إيتيروه هاكوموري الانتباه إلى هذه الفئة من الدهون السفينغولية من خلال اكتشاف هياكلها ووظائفها في تفاعلات ما بين الخلايا، وبوصفها
مستضداتٍ على
غشاء الخلية (Cell membrane antigens)[5]. وفي منتصف الثمانينيات من القرن نفسه، أسهمت الدراسات التي بدأها الطبيب والعالم الفلسطيني الأميركي،
يوسف عوني حنون، في تحديد أدوار مهمة للسفينغوسين والسيراميد (Ceramide) بوصفهما
جزيئات إشارة لها وظائف تنظيمية. ومن ثَمَّ، آذنت هذه الأبحاث بولادة مجال
الدهون السفينغولية النشطة بيولوجيًّا (Bioactive sphingolipids)[6].
أشكالها وهياكلها
تعتبر القواعد السفينغولية (Sphingoid bases) وحدة البناء الهيكلية الأساسية للدهون السفينغولية، وهي كحولات أمينية أليفاتية (Aliphatic amino alcohols)، فالاسم الكيميائي للسفينغوسين هو 2-أمينو-4-ترانس-أوكتاديكين-1,3-ديول (2-amino-4-trans-octadecene-1,3-diol)، وهو يحتوي على ذرتَي كربون
كيرالية {{كيرالية (Chiral carbons): تكون ذرة الكربون كيرالية إذا ارتبطت بها 4 ذرات مختلفة.}}، وهما ذرتا الكربون الثانية والثالثة. والتكوين الكيميائي الفراغي للآيزومر الطبيعي للسفينغوسين هو (2S، 3R) D-إريثرو-سفينغوسين. تختلف القواعد السفينغولية الأخرى من حيث وجود
الرابطة المزدوجة المفروقة (Trans double bond) بين ذرتَي الكربون الرابعة والخامسة أو عدمه، ووجود مجموعة الهيدروكسيل على الكربون الأول أو عدمه، ووجود
روابط مزدوجة أخرى، إضافة إلى طول السلسلة الأليفاتية (العمود الفقري الكربوني) وتفرعها. وينتج من هذه الاختلافات عدد كبير من القواعد السفينغولية المتميزة[7].
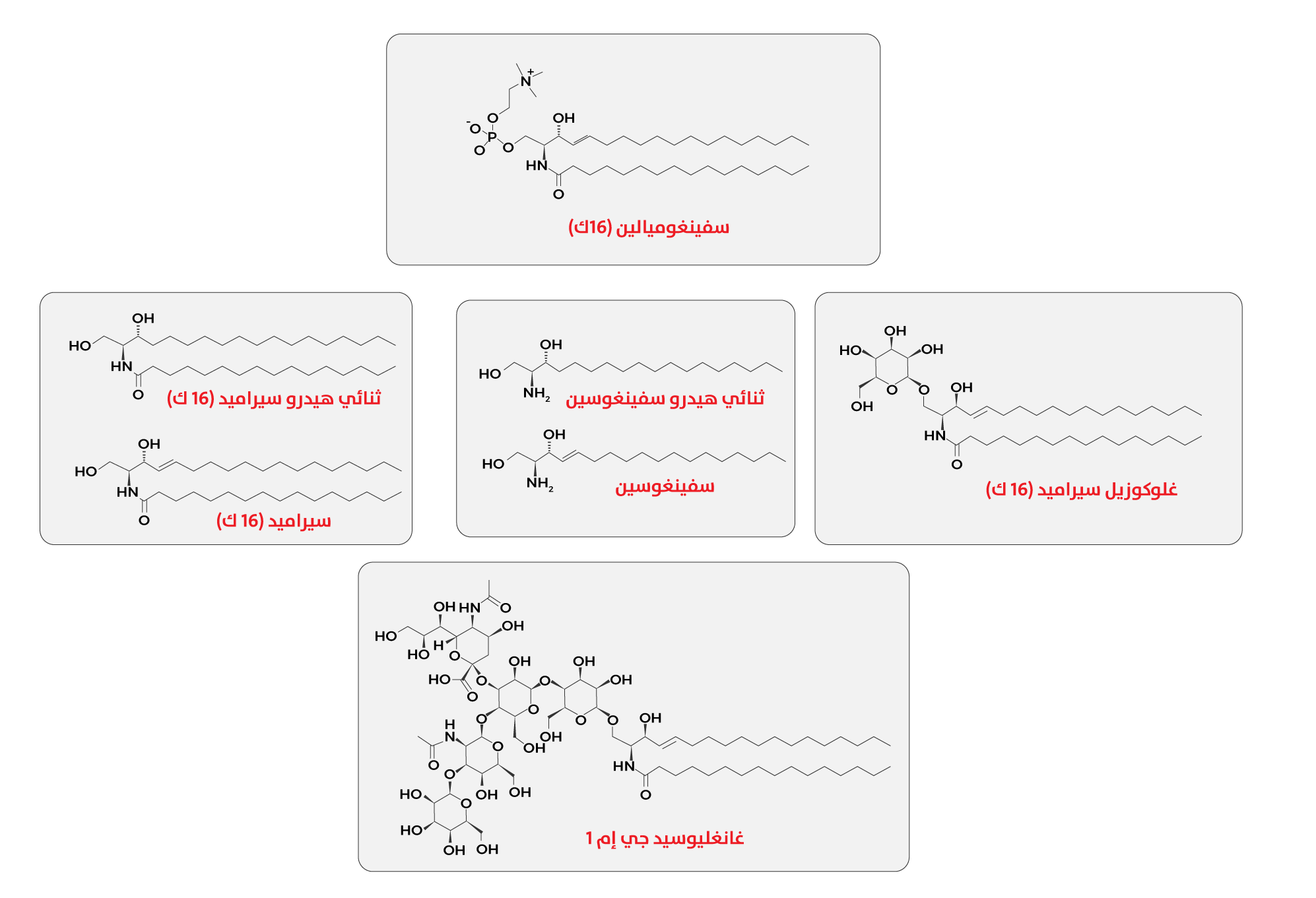 أشكال الدهون السفينغولية المختلفة
أشكال الدهون السفينغولية المختلفة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تُنتِج القواعد السفينغولية، مثل
السفينغوسين، مركبات
السيراميد المختلفة بوساطة عملية
الأَسْيَلَة {{الأسيلة (Acylation): عملية كيميائية حيوية، تتضمّن إضافة مجموعة أسيل (-R(C=O)) إلى جزيء عضوي يحتوي على مواقع نيوكليوفيلية، مثل مجموعات الأمين أو الهيدروكسيل. يُحفَّز هذا التعديل الكيميائي بوساطة إنزيمات الأسيل ترانسفيراز التي تنقل مجموعة الأسيل من جزيء مانح الأسيل إلى موقع محدد على الجزيء المستهدف.}} على النيتروجين الموجود على الكربون الثاني. وتتميز
السيراميدات باختلاف طول سلسلة الأسيل (Acyl chain) المدخلة، و/أو عدد
الروابط المزدوجة، و/أو عدد جزيئات الهيدروكسيل الإضافية، ما يؤدي إلى إنتاج مركبات أكثر تنوعًا من
السيراميد. ويمكن تعديل
السيراميد في الثديّات، بما في ذلك الإنسان، بشكل أكبر عند موضع الهيدروكسيل على الكربون الأول لتكوين فئات فرعية إضافية من الدهون السفينغولية، بما في ذلك
السفينغوميالين، والسيراميد 1-فوسفات (Ceramide 1-phosphate)، و1-O-أسيل سيراميد (1-O-acylceramide)، ومختلف
الدهون السفينغولية السكرية. وباعتبار كل كيان كيميائي جزيئًا مختلفًا محدّدًا، يُقدَّر تنوّع هياكل الدهون السفينغولية بالآلاف، إن لم يكن بعشرات الآلاف[8].
استقلابها والإنزيمات الرئيسة
تتكون الدهون السفينغولية في
الخلايا باستخدام مسارات مختلفة، ويعتبر مسار التخليق الحيوي دي نوفو (De novo biosynthesis) المسار الرئيس، وفيه يبدأ
إنزيم سيرين بالميتويل ترانسفيراز (Serine palmitoyltransferase) في تنفيذ الخطوة الأولى في التخليق الحيوي (Biosynthesis) للدهون السفينغولية، وهذا
الإنزيم هو
بروتين مركّب من عدة وحدات ببتيدية فرعية تحفيزية (Catalytic subunits) وتنظيمية (Regulatory subunits). يجري هذا الإنزيم تفاعلَ تكثيفٍ (Condensation reaction) للحمض الأميني سيرين (Serine) مع جزيء بالميتويل مرافق الإنزيم أ (Palmitoyl CoA) (وهو "المتبرع" بالحمض الدهني المكون من 16 ذرة كربون "البالميتات")؛ لتكوين جزيء 3-كيتو ثنائي هيدرو سفينغوسين (3-ketodihydrosphingosine)، ولكن يمكن لهذا
الإنزيم أيضًا دمج
الأحماض الأمينية ألانين (Alanine) وغلايسين (Glycine) بوصفها
أحماضًا أمينية بديلة، وأحماضًا دهنية أخرى أيضًا ذات أطوال سلسلة مختلفة، مثل الستيرات (Stearate) (18 ذرة كربون)، والميريستات (Myristate) (14 ذرة كربون). وبعد هذا التفاعل، يُختزَل مركّب 3-كيتو ثنائي هيدرو سفينغوسين بوساطة
إنزيم مختزِل يُدعى 3-كيتو ثنائي هيدرو سفينغوسين ريدكتاز (3-ketodihydrosphingosine reductase) مكونًا ثنائي هيدرو سفينغوسين (Dihydrosphingosine). وفي الثديّات، يجري أحد
إنزيمات سيراميد سينثاز (Ceramide synthase) الستة عملية
أَسْيَلَة ثنائي هيدرو سفينغوسين مكونًا ثنائي هيدرو سيراميد (Dihydroceramide) بأحماض دهنية ذات أطوال مختلفة بحسب
إنزيم السيراميد سينثاز المستعمل. وبعد ذلك، يصنّع أحد إنزيمَي ثنائي هيدرو سيراميد ديساتوراز (Dihydroceramide desaturase)، ديس1 أو ديس2،
السيراميدَ (برابطة مزدوجة مفروقة بين ذرتَي الكربون الرابعة والخامسة) أو 4-هيدروكسي سيراميد (فيتوسيراميد، Phytoceramide)[9].
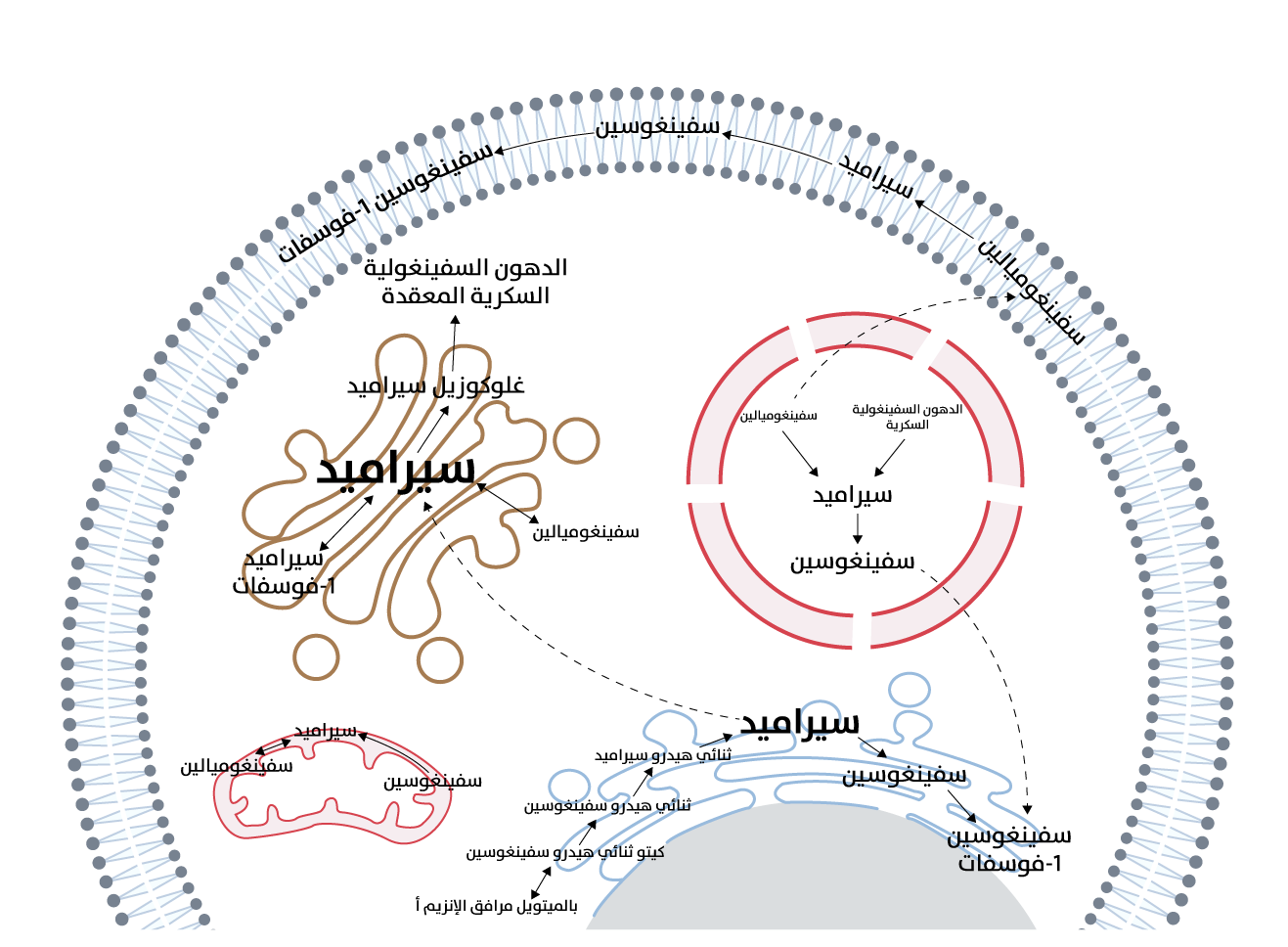 استقلاب الدهون السفينغولية في الخلية
استقلاب الدهون السفينغولية في الخلية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تؤدي هذه
السيراميدات الناتجة وظيفتها بوصفها مركزًا أيضيًّا لدمج
السيراميد في فئات فرعية أكثر تعقيدًا، فينقل
إنزيم سفينغوميالين سينثاز (Sphingomyelin synthase) جزيءَ فوسفوكولين (Phosphocholine) إلى
السيراميد مكونًا
السفينغوميالين، في حين يُكوِّن نقلُ جزيء
غلوكوز أو غالاكتوز بوساطة
إنزيمات غلوكوزيل سيراميد سينثاز (Glucosylceramide synthase) أو غالاكتوزيل سيراميد سينثاز (Galactosylceramide synthase) غلوكوزيلَ سيراميد وغالاكاتوزيلَ سيراميد، على التوالي. كما يمكن لغالاكتوزيل سيراميد أن يتَكَبْرَت (Sulfated) لتصنيع السولفاتيد بوساطة
إنزيم سولفو ترانسفيراز (Sulfotransferase)، أو أن
يتَسَيْلَل[10] (Sialylated) بوساطة
إنزيم سيَالِيلْ ترانسفيراز (Sialyltrasnferase) لتكوين
غانغليوسيد {{الغانغليوسيدات (Ganglioside): دهون سفينغولية سكرية مُتَسَيْلِلَة (تحتوي على حمض السياليك).}}. ومن ناحية أخرى، يتكوّن اللاكتوزيل سيراميد (Lactosylceramide) بوساطة إضافة غالاكتوز على الغلوكوزيل سيراميد بوساطة
إنزيم غالاكتوزيل ترانسفيراز (Galactosyl transferase). أما اللاكتوزيل سيراميد، فيصبح بدوره موضوعًا لتعديلات متعددة ومتسلسلة مع مجموعات السكريات والسياليل، ما يكوّن العديد من
الدهون السفينغولية السكرية والغانغليوسيدات. ويمكن أن يصل عدد
الدهون السفينغولية السكرية إلى نحو 300 جزيء تتميز بمجموعاتها الرئيسة من السكر (من دون احتساب الاختلافات في عمودها الفقري السفينغولي)، كما يمكن أيضًا
فسفرةالسيراميد بوساطة
إنزيم سيراميد كيناز (Ceramide kinase) لإنتاج سيراميد 1-فوسفات، أو أَسْيَلَته بوساطة
إنزيم ديغات 2 (DGAT2) لتصنيع 1-O-أسيل-سيراميد[11].
عندما يَستخدِم
إنزيمُ سيرين بالميتويل ترانسفيراز
الحمضَ الأميني ألانين بوصفه ركيزة بدلًا من سيرين، فإنه ينتج فئةً فرعيةً تفتقر إلى مجموعة الهيدروكسيل على الكربون الأول، تُسمَّى الدهون السفينغولية المنزوعة الأكسجين (Deoxysphingolipids)، وتشتمل هذه الفئة الفرعية على القواعد السفينغولية المنزوعة الأكسجين والسيراميدات المنزوعة الأكسجين (Deoxyceramides)[12]. إن غياب الهيدروكسيل على الكربون الأول يمنع المزيد من التعديل إلى
السفينغوميالين أو
الدهون السفينغولية السكرية، ويمنع الفسفرة إلى سيراميد 1-فوسفات. أما في الخميرة والنباتات، فتعتمد الأشكال الرئيسة للدهون السفينغولية على فيتوسيراميد لا على
سيراميد. كما تعتمد الدهون السفينغولية المعقدة الرئيسة أيضًا على فوسفات الإينوسيتول (Inositol phosphate) لإنتاج إينوسيتول فوسفو فيتوسيراميد (Inositol phosphophytoceramide). ويمكن أن يكون هذا أيضًا بمنزلة
ركيزة لمزيد من التعديلات، ولا سيّما إدخال وحدات سكر المانّوز (Mannose)[13].
تحدث الخطوات الأولى في التخليق الحيوي للدهون السفينغولية في
الخلايا حقيقية النواة في
الشبكة الإندوبلازمية (Endoplasmic reticulum)، ويمكن بعد ذلك نقل
السيراميد إلى
جهاز غولجي (Golgi apparatus) إما من خلال
النقل الحويصلي (Vesicular trafficking)، وإما بوساطة
بروتين نقل
السيراميد (سيرت، CERT). يؤدي
السيراميد الذي يُنقَل غالبًا عبر سيرت إلى تصنيع
السفينغوميالين، في حين يوجّه
النقلُ الحويصليالسيراميدَ إلى
استقلابالدهون السفينغولية السكرية بشكل تفضيلي. كما يخضع الغلوكوزيل سيراميد أيضًا لتأثير بروتين النقل فاب 2 (FAPP2) الذي يربط الغلوكوزيل سيراميد بتكوين اللاكتوزيل سيراميد، ومن ثَمّ إلى
الدهون السفينغولية السكرية الأخرى[14]. وتؤدي عمليات
النقل الحويصلي الإضافية إلى نقل هذه الدهون السفينغولية المعقدة (السفينغوميالين والدهون السفينغولية السكرية) إلى
الغشاء البلازمي[15].
يعتبر
تقويض (هدم، Catabolism) الدهون السفينغولية عملية أساسية، إذ تتكسّر هذه المركبات أولًا في
الأجسام الحالّة)الليسوسومات( {{الليسوسومات: عضيّات خلوية حمضية تحتوي على إنزيمات حالّة لجميع الجزيئات الخلوية الكبيرة المعقدة.}}، فيُكوِّن السفينغومياليناز الحمضي السيراميدَ عن طريق هدم
السفينغوميالين، في حين تتحلل
الدهون السفينغولية السكرية المعقدة تدريجيًّا بفعل تعاقب
إنزيمات الغليكوسيداز (Glycosidases) والهيدرولاز (Hydrolases) مكوّنة غلوكوزيل سيراميد وغالاكتوزيل سيراميد، فيتحول هذان المركبان بعد ذلك بوساطة الغليكوسيداز الحمضي (Acid glycosidases) ليكونا
السيراميد. تتضمن الخطوة الإنزيمية النهائية في
الليسوسوم السيراميدازَ الحمضي (Acid ceramidase) الذي يكسر
السيراميد مكونًا
السفينغوسين والحمض الدهني. وعلى الرغم من أن
السفينغوسين، بفضل شحنته الموجبة (على مجموعة الأمين)، يتركّز في
الليسوسوم، فيُعتقد أن جزيئات
السفينغوسين التي تخرج من
الليسوسوم يمكن أن تُحْجَز في
السيتوبلازم {{السيتوبلازم: (أو الوسط الخلوي) هو ما يوجد داخل الخلية باستثناء النواة في الخلايا حقيقية النوى (Eukaryotic cells)، وكل ما يوجد داخل الخلية في الخلايا غير حقيقية النوى (Prokaryotic cells).}} بوساطة
إنزيمات سفينغوسين كيناز و/أو سيراميد سينثاز لتكوين سفينغوسين 1-فوسفات وسيراميد، على التوالي. وبناءً عليه، تتيح هذه العملية قوةً دافعةً لإزالة
السفينغوسين من
الليسوسوم واستعادته لتجديد تكوين
السيراميد والمركبات السفينغولية المعقدة.
كما يمكن للدهون السفينغولية أن تخضع للتكسير في أماكن غير
الليسوسوم، إذ يكون مختلف أنواع السفينغومياليناز والسيربروسيداز والسيراميداز
السيراميدَ، ومن ثمّ
السفينغوسين. ولهذه
الإنزيمات أشكال آيزوميرية مختلفة، وتوجد في حُجيرات خلوية محددة تشمل
الشبكة الإندوبلازمية، وجهاز غولجي، والغشاء البلازمي، والميتوكوندريا، وحتى
النواة. وعند تكوينه،
يتفسفرالسفينغوسين بوساطة
إنزيمات سفينغوسين كيناز لتكوين سفينغوسين 1-فوسفات، وهو
دهن سفينغولي نشط بيولوجيًّا. ينتهي
المسار الأيضي للدهون السفينغولية عندما يحلّل
إنزيم لياز (lyase) السفينغوسين 1-فوسفات إلى إيثانول أمين فوسفات (Ethanolamine phosphate) وألديهايد دهني (Fatty aldehyde)[16].
آليات عملها
تؤثّر الشحميّات السفينغولية في وظائف الخلايا عن طريق التفاعل مع أهداف بروتينية محددة و/أو عن طريق تعديل خصائص
الأغشية. وتُعرف بعض
الدهون السفينغولية السكرية بأنها أهداف مباشرة للسموم أو
مستضدات ذاتية (Autoantigens). وتؤدي
الدهون السفينغولية السكرية الأخرى وظيفتها بوصفها مستضدات
لأجسام مضادة (Antibodies) محددة، بما في ذلك
مستضدات خلايا الدم الحمراء المشاركة في تفاعلات نقل الدم[17]. وقد بيّنت دراسات متعددة أن جزيئات
السفينغوميالين، باعتبارها مكوّنًا مهمًّا في القشرة الخارجية
للغشاء البلازمي، تتجمّع معًا (وتتخللها جزيئات
كوليسترول) في مناطق/ مجالات صغيرة جدًا (Microdomains)؛ ما يؤدي إلى تنظيم الإشارات العابرة للغشاء، إضافة إلى تنظيم وظائف
بروتيناتغشاء البلازما المختلفة[18].
من بين الشحميّات السفينغولية النشطة بيولوجيًّا، يرتبط السفينغوسين 1-فوسفات بخمسة مستقبلات خلوية متميزة من عائلة المستقبلات المقترنة بالبروتين ج (G protein-coupled receptors)[19]. كما قد يرتبط السفينغوسين 1-فوسفات أيضًا ببروتينات محددة داخل
الخلايا مثل هيستون دياسيتيلاز (Histone deacetylase). أما
السفينغوسين، فقد ثبت أنه يثبّط أولًا
بروتين كيناز سي (Protein kinase C)، وقد يكون هذا سببًا في الوظائف المَرَضيّة للسفينغوسين والسايكوسين (Psychosine) وغيرها من الدهون السفينغولية المنقوصة الحمض الدهني (Lysosphingolipid). وتبيّن أيضًا أن
السفينغوسين ينظم بروتين كيناز بي (Protein kinase B or Akt)، ربّما من خلال فوسفاتاز السيرين (Serine phosphatase). أما
السيراميد، فيرتبط بإنزيم سيرين/ ثريونين فوسفاتاز (Serine/Threonine phosphoprotein phosphatase) وينشّطه. وتزيل هذه
الإنزيمات الفوسفات من جزيئات معينة في
الخلية، محدثةً توسطًا في استجابات خلوية محددة. وقد ثبت أيضًا أن
السيراميد يرتبط ببروتين كاثيبسين د (Cathepsin D) في
الليسوسوم وينشطه، وربما ينظّم عمل بروتين كيناز سي زيتا (Protein kinase Cz). كما أثبتت دراسات متعددة قدرة جزيئات
السيراميد على التجمع معًا لإنشاء قنوات ديناميكية في الغشاء الخارجي
للميتوكوندريا تسهم في مرور
البروتينات إلى
السيتوبلازم إيذانًا ببدء
الموت الخلوي المبرمج،
الاستماتة الخلوية (Apoptosis)[20]. أما السيراميد 1-فوسفات، فقد أشارت بعض الأبحاث إلى وجود
مستقبِلات له على سطح
الخلية، وأظهرت دراسات أخرى تنشيطه لإنزيم فوسفوليباز أ2 (Phospholipase A2) الذي قد يربط عمل سيراميد 1-فوسفات بمسار
الأيكوسانويد {{الأيكوسانويد (Eicosanoid) :جزيئات دهنية نشطة بيولوجيًا، تُصنَّع من حمض الأراكيدونيك (Arachidonic acid) بوساطة تفعيل إنزيم فوسفوليباز أ2. تنظم الأيكوسانويدات العديد من العمليات الفيزيولوجية المتنوعة، بما في ذلك الالتهابات ورفع درجة حرارة الجسم، والاستجابة المناعية، وتوازن الأوعية الدموية.}}.
آليات تنظيم استقلابها وإنزيماتها
تخضع
مسارات استقلاب الدهون السفينغولية لتنظيم كبير على المستوى الكلّي، إضافة إلى تنظيم
إنزيمات معيّنة في هذه المسارات، إذ يوفّر
إنزيم سيرين بالميتويل ترانسفيراز الخطوة الأولى المُلزمة في التخليق الحيوي للدهون السفينغولية، ويُنظَّم هذا
الإنزيم استجابةً لمستويات
السيراميد في
الخلية؛ فيرتبط
السيراميد بشكل مباشر بهذا
الإنزيم المتعدد الوحدات ويثبطه. وإضافة إلى ذلك، تؤدي الوحدات الفرعية لإنزيم سيرين بالميتويل ترانسفيراز المسمّاة "أورم" (Orm) دورًا مثبطًا. أما وظيفة أورم نفسها، فتُنَظَّم عن طريق تعديل
التعبير الجيني (Gene expression) أو التعديل اللاحق للترجمة (Post-translational modification)، فعلى سبيل المثال، تعتبر
الفسفرة آلية رئيسة في تنظيم عمل أورم في الخميرة، وتؤثر وحدتان صغيرتان من مُعقَّد سيرين بالميتويل ترانسفيراز في انتقائيته
للركائز (الأحماض الدهنية والأحماض الأمينية). ومن الجدير ذكره أن نتاج تفاعل سيرين بالميتويل ترانسفيراز يعتمد بقوة على توفّر
ركائزه الرئيسة؛ سيرين وبالميتويل مرافق الإنزيم أ. وعلى الرغم من أن العديد من المحفّزات، مثل عامل نخر الورم (Tumor necrosis factor) وبعض عوامل
العلاج الكيميائي (Chemotherapy)، معروفة بتشغيل مسار تخليق السيراميد دي نوفو، فإنه لا يُعرف سوى القليل عن الآليات الجزيئية التي تؤدي هذا التنشيط[21].
إن الدراسات عن تنظيم الإنزيم التالي في السلسة، 3-كيتو ثنائي هيدرو سفينغوسين ريدكتاز، قليلة جدًا. أما الخطوة الموالية، التي يؤديها أحد
إنزيمات سيراميد سينثاز الستة، فإنها تخضع للتنظيم بطرق متعددة، مثل
التحلل البروتيني {{التحلل البروتيني (Proteolysis): التحلل الممنهج للبروتينات بوساطة إنزيمات خاصة مكونًا ببتيدات أصغر و/أو أحماض أمينية. هذه العملية أساسية في الهضم والتنظيم وإعادة التدوير الخلوي.}}، والفسفرة (بوساطة كيزين كيناز (Casein kinase) وYpk1 في الخميرة)، والدَيْمَرَة {{الديمرة (Dimerization) : (أو التَّثْنِيَة) عملية ارتباط جزيئين بروتينيين معًا لتكوين بروتين معقَّد يحتوي على وحدتين. يمكن أن تحدث هذه التفاعلات بين جزيئات بروتينية متماثلة (تثنية متماثلة) أو بين جزيئات بروتينية مختلفة (تثنية غير متماثلة). تؤدي عملية تثنية البروتين أدوارًا مهمة في العمليات الخلوية، مثل انتقال الإشارة، وتنظيم الإنزيمات، وثبات البروتينات. ويمكن أن تؤدي أيضًا إلى تغيرات في وظيفة البروتينات أو نشاطها.}}، وكذلك تفاعلاتها مع
البروتينات الأخرى التي تشمل منظِّمات
موت الخلايا المبرمج باك (Bak) وبي سي إل 2 إل 13 (Bcl2L13)، وإنزيم سينثاز الحمض الدهني مرافق الإنزيم أ (Fatty acyl CoA synthase). كما يُنظَّم عمل بعض من هذه
الإنزيمات الستة عن طريق تنظيم
التعبير الجيني بوساطة الأحماض النووية الريبية غير المشفِّرة الطويلة (Long non-coding RNAs) وعمليات الأسْتَلة (Acetylation)[22]. وفي الخطوة الأخيرة، يحوّل
إنزيمَا ديساتوراز ثنائيَّ هيدرو سيراميد المتكوِّن في الخطوة السابقة إلى
سيراميد. إن هذين
الإنزيمين حساسان لحالة الأكسدة والاختزال (Redox state) في
الخلايا، وكذلك لتراكيز مركّب النيكوتيناميد أدينين ثنائي النوكليوتيد فوسفات (NADPH)، وهو عامل مساعد رئيس لنشاطها، ويؤدي دورًا مهمًّا في حالة اختزال
الخلايا.
أما
بروتين النقل سيرت الذي ينقل
السيراميد من
الشبكة الإندوبلازمية إلى
جهاز غولجي، فيُنظَّم بصورة أساسية عن طريق
الفسفرة في مواقع مختلفة[23]. وتُنشِّط
فسفرة بعض المواقع بروتين النقل، بينما تعتبر فسفرة مواقع أخرى مثبِّطةً عن طريق تحسين التغذية الراجعة السلبية (Feedback inhibition) استجابةً لتركيزالسفينغوميالين. وعندما يصل
السيراميد إلى
جهاز غولجي بوساطة سيرت، تُعدِّل عليه
إنزيمات سفينغوميالين سينثاز التي تُنظَّم على مستوى
التعبير الجيني، على سبيل المثال، بوساطة الأحماض الريبية النووية الميكروية (Micro RNAs)، وكذلك بوساطة
الجين الورمي (Oncogene) بي سي آر-أبل (bcr-abl). كما تُنظَّم مستويات سيرت أيضًا بوساطة إنزيمات البروتياز (Proteases)، بما في ذلك الكاسبيزات المؤازرة للاستماتة الخلوية (Pro-apoptotic caspases). ومن جهة أخرى، يحوّل
إنزيمَا غلوكوزيل سيراميد سينثاز وغالاكتوزيل سيراميد سينثاز
السيراميدَ في
جهاز غولجي إلى غلوكوزيل سيراميد وغالاكتوزيل سيراميد، على التوالي. وعلى الرغم من أن هذين
الإنزيمين يؤديان دورَ حُرّاس البوابة لتخليق معظم مكوّنات عائلة الدهون السفينغولية، فإن ما يُعرَف عن عمليات تنظيم عملهما قليل. وأوضحت الأبحاث أن
إنزيم غلوكوزيل سيراميد سينثاز يرتبط بالدهن الفسفوري الأنيوني فوسفاتيديل إينوسيتول 4-فوسفات، ما ينظم التفاعل مع غلوكوز ثنائي فوسفات اليوريدين (UDP-glucose) ويعدّل مستوى
التعبير الجيني بصورة فوق جينية (Epigenetically).
وظائفها في بيولوجيا الخلية
للدهون السفينغولية أدوار كبيرة جدًّا ومتخصصة في حياة
الخلايا وموتها، وهناك أدبيات كثيرة عن الأنشطة البيولوجية لمختلف فصائل الدهون السفينغولية الرئيسة والفرعية، فالسفينغوسين يُحفِّز
موت الخلية بشكل خاص في الخلايا اللمفاوية وخلايا سرطان الدم، ويثبِّط بعض الأهداف الإشارية الرئيسة، مثل
بروتين كيناز سي وبروتين كيناز بي. أما الفيتوسفينغوسين، فيؤدي العديد من استجابات الضغط، بما في ذلك الاستجابة للضغط الحراري في الخميرة[24].
إن جزيئات
السيراميد في
الخلايا البشرية، إضافة إلى الكائنات النموذجية (Model organisms)، قد دُرِست بشكل كبير جدًا مقارنة مع الدهون السفينغولية الأخرى. وعلى مستوى
الخلية، فإن
السيراميد يرتبط ارتباطًا وثيقًا بالاستماتة الخلوية (وهي نوع رئيس من موت الخلية المنظّم)، وشيخوخة الخلية (Cell senescence)، وتنظيم
دورة الخلية (Cell cycle regulation)، وهجرة الخلية (Cell migration)، والاستجابات
للهرمونات، وغيرها. تُنشِّط جزيئات
السيراميد، جزئيًّا على الأقل،
إنزيمَ فوسفاتاز السيرين/ ثريونين، ما يؤدي إلى إزالة
الفسفرة من جزيئات بروتينية أساسية تشارك في تنظيم
موت الخلية ونموها وشيخوختها، مثل بروتينات كيناز بي وبي سي إل 2 (Bcl2) ورتينوبلاستوما، والعديد من
البروتينات الأخرى.
إضافة إلى ذلك، فإن للجزيئات السفينغولية المفسفرة أدوارًا في بيولوجيا الخلية، فقد ظهر السفينغوسين 1-فوسفات بوصفه مرسالًا أوليًّا (First messenger)، إذ يرتبط بخمسة مستقبلات مقترنة ببروتين ج مؤديًا إلى تنظيم تكوّن الأوعية الدموية الجديدة (Angiogenesis)، وهجرة الخلية، ومقاومة الموت الخلوي، والاستجابات الالتهابية، في حين يشارك السيراميد 1-فوسفات في توجيه بعض الاستجابات الخلوية الالتهابية من خلال تنظيم مسار
الأيكوسانويد، وتنظيم
المستقبِلات على
الغشاء الخلوي أيضًا.
 أدوار الدهون السفينغولية المختلفة في الخلية
أدوار الدهون السفينغولية المختلفة في الخلية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
أما الدهون السفينغولية المرتبطة بالسكريات فلها أدوار أخرى، إذ يرتبط الغلوكوزيل سيراميد بمقاومة الدواء، وخصوصًا العلاج الكيميائي، ولكنه ليس واضحًا إذا ما كان لديه أهداف محددة أم أنه يخفّض بشكل أساسي مستويات
السيراميد. ومن ناحية أخرى، تقدّم
الدهون السفينغولية السكرية المختلفة الأخرى، التي توجد بشكل أساسي على الطبقة الخارجية
للغشاء البلازمي،
مستضداتٍ محددة على سطح
الخلايا، إضافة إلى أدوارها في الاستجابات المناعية وتعديل عمل
المستقبِلات على
الغشاء البلازمي. وتؤدي بعض
الدهون السفينغولية السكرية المحددة أيضًا وظائف بوصفها
مستقبِلات للسموم (Toxins)، مثل غانغليوسيد جي إم 1 (Ganglioside GM1) في حالة سم الكوليرا[25].
أدوارها في المرض
تؤدي الدهون السفينغولية أدوارًا متنوعة في العديد من الأمراض الوراثية والمكتسبة؛ ففي أمراض الاختزان في الجسميات الحالّة (Lysosomal storage diseases) تؤدي الاضطرابات في
استقلاب هذه الشحميات إلى تراكمها داخل
الليسوسومات، ما يسبب خللًا خلويًّا وتلفًا في الأنسجة. وإضافةً إلى ذلك، ترتبط الاضطرابات الوراثية غير الليسوسومية، بما في ذلك الاعتلالات العصبية الحسية واللاإرادية الوراثية، بالطفرات التي تؤثر في التخليق الحيوي للدهون السفينغولية أو نقلها أو تنظيمها، ما يؤكد أهمية هذه المركّبات في الحفاظ على السلامة العصبية. أما في الأمراض المكتسبة، فتسهم الاضطرابات في تنظيم
استقلاب الدهون السفينغولية في حدوث حالات مرضية مختلفة، مثل
السرطان، والأمراض التنكسية العصبية، والالتهابات. ومن ثم، فإن فهم الأدوار المعقدة للدهون السفينغولية في هذه الاضطرابات مهم لتطوير استراتيجيات علاجية مستهدفة تهدف إلى التخفيف من أعباء هذه الأمراض[26].
أمراض الاختزان في الجسميات الحالّة الموروثة
إن ارتباط الدهون السفينغولية بالمرض بدأ بالدراسات التي أُجريت على الاضطرابات الأيضية الموروثة (Inherited metabolic disorders)، ولا سيما مرض نيمان بيك (Niemann-Pick disease)، ومرض غوشيه (Gaucher disease)، ومرض تاي ساكس (Tay-Sachs disease). فمن خلال الدراسات البيوكيميائية الدقيقة، عُزِيَت هذه الأمراض إلى تراكم الشحميات السفينغولية (السفينغوميالين، السيريبروسيد/ غلوكوزيل سيراميد، والغانغليوسيد جي إم 2، على التوالي) في
الخلايا. وقد عَزَتْ الدراسات اللاحقة هذا التراكم إلى عيوب في
إنزيمات معينة مسؤولة عن تحلل هذه الشحميات السفينغولية، مثل
إنزيم سفينغومياليناز الحمضي (Acid sphingomyelinase) في مرض نيمان بيك، وإنزيم غلوكوزيل سيريبروسيداز (Glucosylcerebrosidase) في مرض غوشيه، وإنزيم هيكسوز أمينيداز أ (Hexosaminidase A) في مرض تاي ساكس. ثم تبيّن لاحقًا أن تراكم هذه الدهون يكمن في
الليسوسومات، وأن
الإنزيمات المسؤولة المختلّة هي
إنزيماتليسوسومية، ومن ثم أصبحت مجموعة الأمراض هذه معروفة بشكل جماعي باسم "أمراض تخزين الدهون السفينغولية" (Sphingolipidoses) وهي جزء من اضطرابات الاختزان في الجسميات الحالّة[27].
تشمل
أمراض اختزان الشحميّات السفينغولية الأخرى مرضَ فاربر (Farber’s disease، وهو نقص
إنزيم السيراميداز الحمضي (Acid ceramidase) وتراكم
السيراميد)، ومرض كرابي (Krabbe’s disease، وهو نقص
إنزيم غالاكتوسيريبروسيداز (Galactocerebrosidase) وتراكم غالاكتوزيل سيراميد)، وحَثَل المادة البيضاء المتبدل اللون (Metachromatic leukodystrophy، نقص
إنزيم السلفاتاز (Sulfatase) وتراكم السولفاتيد)، وداء العقدة المعمم (Generalized gangliosidosis، نقص
إنزيم بيتا غالاكتوسيداز (Beta-galactosidase) وتراكم الغانغليوسيدات). وتحدث الأشكال الحادة من هذه الأمراض في مرحلة الطفولة المبكرة، وينتج عنها في المقام الأول اضطرابات في
الجهاز العصبي المركزي، في حين يمكن اكتشاف أشكالٍ أكثر اعتدالًا من هذه الأمراض عند البالغين (خصوصًا في حالة مرض غوشيه)[28].
الاضطرابات الموروثة والخلقية غير الليسوسومية
مع الانتشار الواسع للفحوص الجينومية، ومع تحديد
الجينات التي تشفّر إنزيمات
استقلاب الدهون السفينغولية، عُزِيَ سبب العديد من الأمراض الوراثية البشرية إلى طفرات أحادية المنشأ في
الجينات المتعلقة باستقلاب الدهون السفينغولية، ومن هذه الأمراض اعتلال الأعصاب الحسي الذاتي الوراثي (Hereditary sensory autonomous neuropathy, HSAN) من النوع الأول الذي يحدث بسبب
طفرات في وحدة SPTLC2 من
إنزيم سيرين بالميتويل ترانسفيراز، وهذا هو السبب الأشيع لهذا المرض. وقد ثبت أن
طفرات أخرى في الجين ذاته تؤدي إلى مرض
التصلب الجانبي الضموري (Amyotrophic lateral sclerosis, ALS)، في حين تعتبر الاختلالات في
إنزيم غلوكوسيريبروسيداز (GBA1) السبب الأشيع للأشكال الوراثية لمرض باركنسون (Parkinson’s disease)[29].
ومن إنزيمات
استقلاب الدهون السفينغولية الأخرى التي يؤدي اعتلالها إلى أمراض وراثية
إنزيم السيراميداز القلوي 3 (Alkaline ceramidase 3, Acer3)، وإنزيم سفينغوسين 1-فوسفات لياز (Sphingosine 1-phosphate lyase)، إذ وُجد أن هناك اضطرابًا تنكسيًّا عصبيًّا وراثيًّا سببه
طفرات في
الإنزيم الأول، في حين تؤدي الطفرات في
الإنزيم الثاني إلى متلازمة نقص اللياز (Lyase-deficiency syndrome). وإضافة إلى ذلك، وُجدِت أيضًا طفرات مسبِّبة للأمراض في
إنزيمات سيراميد سينثاز 1، 2، و3، وإنزيم ديس1، وبعض
الإنزيمات المحددة لإنتاج
الدهون السفينغولية السكرية (Gb3، Gb4، GM2، GM3)، ومعظم هذه
الطفرات تؤدي إلى ظهور مبكر للاضطرابات التنكسيّة العصبيّة الشديدة[30].
دور الدهون السفينغولية في الأمراض المكتسبة
توصلت مجموعة كبيرة من الأبحاث إلى أن تورُّط الشحميات السفينغولية واختلال وظائف
إنزيماتها يعدّان أساسًا لعدد كبير من الاضطرابات والأمراض، فعلى سبيل المثال، قدمت دراسات مختلفة أدلةً على دور الدهون السفينغولية وإنزيماتها، ولا سيما
إنزيم السفينغومياليناز المتعادل (Neutral sphingomyelinase)، في مرض
الزهايمر (Alzheimer’s disease)[31]. وأجريت مجموعة أكبر من الأبحاث لمعرفة دور الشحميّات السفينغولية وإنزيمات استقلابها في مرض
السرطان، وذلك من خلال تنظيم العديد من السمات المميزة
للسرطان، مثل مقاومة موت الخلايا، وتولّد الأوعية، والانبثاث (Metastasis)، وتنظيم
عمليات الأيض، وهجرة الخلايا، والالتهابات.
كما ربطت الأبحاث بين جزيئات
السيراميد وعدة أمراض، مثل الاضطرابات الأيضية (Metabolic disorders)، والإصابة بضرر الإسكيمية وإعادة التروية {{ضرر الإسكيمية وإعادة التروية: تلف يحصل في بعض الأنسجة عند عودة إمداد الدم (إعادة التروية) بعد فترة من الحرمان (إسكيمية أو نقص التروية)، ما يؤدي إلى تفاقم موت الخلايا بسبب الالتهاب والإجهاد التأكسدي.}} (Ischemia reperfusion injury)، والتنكُّس الدهني (Steatosis)، وتليُّف الكبد (Fibrosis)، في حين يعتبر السفينغوسين 1-فوسفات ومستقبلاته أهدافًا علاجيةً في مرض التصلب المتعدد (Multiple sclerosis) والتهاب القولون التقرُّحي (Ulcerative colitis)[32]. أما بعض
الدهون السفينغولية السكرية والغانغليوسيدات المحدَّدة، فإنها تسهم في التسبُّب في المرض من خلال وظيفتها بوصفها مستقبلاتٍ للسموم أو
مستضداتٍ ذاتية في بعض أمراض المناعة الذاتية. ويؤدي الغانغليوسيد جي إم 1 وظيفته بوصفه مستقبلًا لسم
الكوليرا (Cholera toxin)، ما يسمح بإدخال السم إلى
الخلايا. وكذلك، يرتبط سم
الشيغيلا الزحارية (Shiga toxin) بالدهن السفينغولي السكري جي بي 3 (Gb3)، ما يؤدي إلى امتصاص السم ومنع تخليق
البروتين داخل
الخلايا[33]. أما الغانغليوسيد جي دي 1 (GD1)، فإنه يعتبر، إلى جانب غانغليوسيدات أخرى،
مستضدًا ذاتيًّا يؤدي وظيفته بوصفه هدفًا رئيسًا في
متلازمة غيلان باريه (Guillain-Barré syndrome)، وغيرها من الاعتلالات العصبية المحورية الحركية الحادة (Acute motor axonal neuropathies)[34].
دورها في التشخيص والعلاج
التشخيص
 فحص مؤشر السيراميد في مايو كلينِك
فحص مؤشر السيراميد في مايو كلينِك
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
أسهمت الدراسات الحديثة، في أوائل القرن الحادي والعشرين، في تخصيص أدوار لدهون سفينغولية محدَّدة ولمجموعات مختلفة من الدهون السفينغولية بوصفها
واسمات تشخيصية (Diagnostic biomarkers)[35]، فقد اعتمدت مختبرات مايو كلينِك (Mayo Clinic) مؤشرَ السيراميد (Ceramide index) لتقييم أخطار أمراض القلب والأوعية الدموية[36]. وفي مرض الزهايمر، تعتبر بعض الشحميّات السفينغولية
مؤشرات حيوية توجد في
السائل الدماغي الشوكي (Cerebrospinal fluid) للمرضى، كما ارتبطت الزيادة في
تركيزالسيراميد بالشيخوخة[37]. وقد اكتشف العلماء أن بعض
الدهون السفينغولية السكرية، التي تؤدي وظيفتها بوصفها
مستضدات محددة لفصائل الدم، مثل جي إم 2 (GM2) وجي دي 2 (GD2) وغيرهما، تؤدي وظيفتها أيضًا بوصفها مستضدات للورم ومستضدات للسرطان الجنيني. وترتبط مستويات إنزيم السفينغومياليناز الحمضي في الدم ارتباطًا وثيقًا بدرجة الإنتان (Sepsis) في حالات المرضى في وحدات العناية المركّزة. وقد عُرِّف العديد من الشحميّات السفينغولية، ولا سيّما
الدهون السفينغولية السكريّة، على أنه مستضدات للورم في العديد من أنواع
السرطان (مثل جي دي 2 في
الورم الدبقي، Glioma).
العلاج
أسفرت الدراسات السريرية والعلاجية في مجال الشحميّات السفينغولية عن أهداف علاجية جديدة متعددة، إذ تُستَخدم مقلِّدات
السفينغوسين، مثل فينغوليمود (Fingolimod) سريريًا في مرض التصلب المتعدد بآلية تتضمن فسفرة الجزيء الذي يثبط نشاط مستقبلات محددة للسفينغوسين 1-فوسفات[38]. وقد اكتُشفت مُعدِّلات لمستقبلات السفينغوسين 1-فوسفات مفيدة في مرض التهاب الأمعاء (Inflammatory bowel disease). وفي القرن الحادي والعشرين، تُقيَّم جزيئات
السيراميد قصيرة السلسلة، التي هي أكثر قابلية للذوبان من
السيراميدات ذات السلاسل الطويلة والطويلة جدًا، في التجارب السريرية في علاج
السرطان، وذلك باستخدام الحويصلات النانوية بوصفها وسيلة للتوصيل. كما أن هناك عدة دراسات تقوم على فحص إمكانية تخصيص
إنزيماتاستقلاب الشحميّات السفينغولية بوصفها أهدافًا علاجية خصوصًا في مرض
السرطان، وتشمل هذه الأبحاث
إنزيمات سفينغوسين كيناز، وغلوكوزيل سيراميد سينثاز، وسيراميد كيناز. ومن ناحية أخرى، اقتُرِح تثبيط تكوين
السيراميد عن طريق تثبيط بعض
الإنزيمات الرئيسة المكوّنة له بوصفه استراتيجية لتحسين الاضطرابات التنكسيّة العصبيّة (في حالة تثبيط السفينغومياليناز المتعادل)، وفي تنكس الكبد الدهني (تثبيط سيراميد سينثاز). وفي عشرينيات القرن الحادي والعشرين، استُخدِمت الخلايا التائية لمستقبلات المستضد الخيميري (Chimeric antigen receptor T cells) موجهة ضد غانغليوسيد جي دي 2 بوصفها خيارًا علاجيًّا في
الأورام الدبقية[39].
المراجع
Abed Rabbo, Muna et al. “Sphingolipid Lysosomal Storage Diseases: From Bench to Bedside.”
Lipids in Health and Disease. vol. 20, article no. 44 (2021).
Abou-Ghali, Majdouline & Johny Stiban. “Regulation of Ceramide Channel Formation and Disassembly: Insights on the Initiation of Apoptosis.”
Saudi Journal of Biological Sciences. vol. 22, no. 6 (2015). pp. 760-772.
Astudillo, Leonardo et al. “Human Genetic Disorders of Sphingolipid Biosynthesis.”
Journal of Inherited Metabolic Disease. vol. 38, no. 1 (2015). pp. 65-76.
Brinkmann, Volker et al. “Fingolimod (FTY720): Discovery and Development of an Oral Drug to Treat Multiple Sclerosis.”
Nature Reviews Drug Discovery. vol. 9, no. 11 (2010). pp. 883-897.
Carter, Herbert E. et al. “The Structure of Sphingosine.”
Jornal of Biological Chemistry. vol. 142, no. 1 (1942). pp. 449-450.
D’Angelo, Giovanni et al. “Glycosphingolipid Synthesis Requires FAPP2 Transfer of Glucosylceramide.”
Nature. vol. 449, no. 7158 (2007). pp. 62-67.
Dunn, Teresa M., Cynthia J. Tifft & Richard L. Proia. “A Perilous Path: The Inborn Errors of Sphingolipid Metabolism.”
Journal of Lipid Research. vol. 60, no. 3 (2019). pp. 475-483.
Feitz, Wouter J. C. et al. “The Shiga Toxin Receptor Globotriaosylceramide as Therapeutic Target in Shiga Toxin E. Coli Mediated HUS.”
Microorganisms. vol. 9, no. 10 (2021).
Hakomori, Sen-itiroh & Roger W. Jeanloz. “Glycolipids as Membrane Antigens.”
Blood and Tissue Antigens (1970). pp. 149-161.
Hammad, Samar M. & Maria F. Lopes-Virella. “Circulating Sphingolipids in Insulin Resistance, Diabetes and Associated Complications.”
International Journal of Molecular Sciences. vol. 24, no. 18, article no. 14015 (2023).
Hannun, Yusuf A. & Lina M. Obeid. “Sphingolipids and Their Metabolism in Physiology and Disease.”
Nature Reviews Molecular Cell Biology. vol. 19, no. 3 (2018). pp. 175-191.
Hannun, Yusuf A. & Lina M. Obeid. “Principles of Bioactive Lipid Signalling: Lessons from Sphingolipids.”
Nature Reviews Molecular Cell Biology. vol. 9, no. 2 (2008). pp. 139-150.
Hannun, Yusuf A. et al. “Sphingosine Inhibition of Protein Kinase C Activity and of Phorbol Dibutyrate Binding in Vitro and in Human Platelets.”
Journal of Biological Chemistry. vol. 261, no. 27 (1986). pp. 12604-12609.
Haughey, Norman J. et al. “Roles for Dysfunctional Sphingolipid Metabolism in Alzheimer’s Disease Neuropathogenesis.”
Biochimica et Biophysica Acta. vol. 1801, no. 8 (2010). pp. 878-886.
Hornemann, Thorsten. “Sphingoid Base Diversity.”
Atherosclerosis. vol. 401, article no. 119091 (2025).
Jamjoum, Rama et al. “Mysterious Sphingolipids: Metabolic Interrelationships at the Center of Pathophysiology.”
Frontiers in Physiology. vol. 14 (2023).
Kumagai, Keigo et al. “Structure, Functions and Regulation of CERT, a Lipid-Transfer Protein for the Delivery of Ceramide at the ER–Golgi Membrane Contact Sites.”
FEBS Letters. vol. 593, no. 17 (2019). pp. 2366-2377.
Lleixà, Cinta et al. “Autoantibody Screening in Guillain–Barré Syndrome.”
Journal of Neuroinflammation. vol. 18, article no. 251 (2021).
Lone, Museer A. et al. “1-Deoxysphingolipids.”
Biochimica et Biophysica Acta (BBA) - Molecular and Cell Biology of Lipids. vol. 1864, no. 4 (2019). pp. 512-521.
Stiban, Johnny (ed.).
Bioactive Ceramides in Health and Disease: Intertwined Roles of Enigmatic Lipids. Cham: Springer, 2019.
Ogretmen, Besim. “Sphingolipid Metabolism in Cancer Signalling and Therapy.”
Nature Reviews Cancer. vol. 18, no. 1 (2017). pp. 33-50.
Thudichum, J. L. W. A Treatise on the Chemical Constitution of the Brain: Based Throughout upon Original Researches. London: Baillière, Tindall & Cox, 1884.
Pokrovsky, Vadim S., Veronika I. Ivanova-Radkevich & Olga M. Kuznetsova. “Sphingolipid Metabolism in Tumor Cells.”
Biochemistry (Moscow). vol. 88, no. 7 (2023). pp. 847-866.
Prapa, Malvina et al. “GD2 CAR T Cells against Human Glioblastoma.”
Npj Precision Oncology. vol. 5, article no. 93 (2021).
Quinville, Brianna M. et al. “A Comprehensive Review: Sphingolipid Metabolism and Implications of Disruption in Sphingolipid Homeostasis.”
International Journal of Molecular Sciences. vol. 22, no. 11, article no. 5793 (2021).
Rabionet, Mariona et al. “1-O-Acylceramides are Natural Components of Human and Mouse Epidermis.”
Journal of Lipid Research. vol. 54, no. 12 (2013). pp. 3312-3321.
Raza, Yasharah, Jane Atallah & Chiara Luberto. “Advancements on the Multifaceted Roles of Sphingolipids in Hematological Malignancies.”
International Journal of Molecular Sciences. vol. 23, no. 21, article no. 12745 (2022).
Sandhoff, Roger, Heike Schulze & Konrad Sandhoff. “Ganglioside Metabolism in Health and Disease.”
Progress in Molecular Biology and Translational Science. vol. 156 (2018). pp. 1-62.
“Sphinx Riddle of the Sphinx.”
GreekMythology. at:
https://acr.ps/1L9F31z
“Test ID: Ceram.”
Mayo Clinic Laboratories. at:
https://acr.ps/1L9F2aG
Thomas, Mark P., Stephen J. Mills & Barry V. L. Potter. “The ‘Other’ Inositols and Their Phosphates: Synthesis, Biology and Medicine (with Recent Advances in Myo-Inositol Chemistry).”
Angewandte Chemie (International Edition in English). vol. 55, no. 5 (2015). pp 1614-1650.
Yan Chen et al. “Long Non-Coding RNAs-Sphingolipid Metabolism Nexus: Potential Targets for Cancer Treatment.”
Pharmacological Research. vol. 210, article no. 107539 (2024).
[1] وفقًا للأساطير اليونانية القديمة، فإن أبا الهول (وهي أنثى) قد طرحت لغزًا على المسافرين الذين أتوها حتى تسمح لهم بالمرور، ومن لم يستطع الإجابة عنه أكلته. وكان اللغز الذي سألته: "ما هو المخلوق الذي له صوت واحد ولكن له أربع أقدام في الصباح وقدمان بعد الظهر وثلاث أقدام في الليل؟"، فتمكن أوديب من الإجابة عن اللغز إجابةً صحيحة، فأجاب: "الإنسان"؛ فهو يحبو على أربع عندما يكون طفلًا، ويمشي على اثنتين عندما يصبح بالغًا، ويحتاج إلى عصا للمشي عندما يصبح كهلًا. يُنظر:
“Sphinx Riddle of the Sphinx,”
GreekMythology, accessed on 21/11/2024, at:
https://acr.ps/1L9F31z
[2] سمّى ثوديكوم المركب فرينوسين (Phrenosin)، وهي تسمية قديمة لم تَعُد مستخدمة.
[3] J. L. W. Thudichum, A Treatise on the Chemical Constitution of the Brain: Based Throughout upon Original Researches (London: Baillière, Tindall & Cox, 1884).
[4] Herbert E. Carter et al., “The Structure of Sphingosine,”
Jornal of Biological Chemistry, vol. 142, no. 1 (1942), pp. 449-450.
[5] Sen-itiroh Hakomori & Roger W. Jeanloz, “Glycolipids as Membrane Antigens,”
Blood and Tissue Antigens (1970), pp. 149-161.
[6] Yusuf A. Hannun et al., “Sphingosine Inhibition of Protein Kinase C Activity and of Phorbol Dibutyrate Binding in Vitro and in Human Platelets,”
Journal of Biological Chemistry, vol. 261, no. 27 (1986), pp. 12604-12609; Yusuf A. Hannun & Lina M. Obeid, “Principles of Bioactive Lipid Signalling: Lessons from Sphingolipids,”
Nature Reviews Molecular Cell Biology, vol. 9, no. 2 (2008), pp. 139-150.
[7] Thorsten Hornemann, “Sphingoid Base Diversity,”
Atherosclerosis, vol. 401, article no. 119091 (2025).
[8] Brianna M. Quinville et al., “A Comprehensive Review: Sphingolipid Metabolism and Implications of Disruption in Sphingolipid Homeostasis,”
International Journal of Molecular Sciences, vol. 22, no. 11, article no. 5793 (2021).
[9] Yusuf A. Hannun & Lina M. Obeid, “Sphingolipids and Their Metabolism in Physiology and Disease,”
Nature Reviews Molecular Cell Biology, vol. 19, no. 3 (2018), pp. 175-191.
[10] السَّيْلَلَة: هي إضافة حمض السياليك إنزيميًا إلى البروتينات أو الدهون السكرية، وهي تعديل أساسي للتواصل الخلوي والمناعة واستقرار البروتين.
[11] Mariona Rabionet et al., “1-O-Acylceramides are Natural Components of Human and Mouse Epidermis,”
Journal of Lipid Research, vol. 54, no. 12 (2013), pp. 3312-3321.
[12] Museer A. Lone et al., “1-Deoxysphingolipids,”
Biochimica et Biophysica Acta (BBA) - Molecular and Cell Biology of Lipids, vol. 1864, no. 4 (2019), pp. 512-521.
[13] Mark P. Thomas, Stephen J. Mills & Barry V. L. Potter, “The ‘Other’ Inositols and Their Phosphates: Synthesis, Biology and Medicine (with Recent Advances in Myo-Inositol Chemistry),”
Angewandte Chemie (International Edition in English), vol. 55, no. 5 (2015), pp 1614-1650.
[14] Giovanni D’Angelo et al., “Glycosphingolipid Synthesis Requires FAPP2 Transfer of Glucosylceramide,”
Nature, vol. 449, no. 7158 (2007), pp. 62-67.
[15] Hannun & Obeid, “Sphingolipids and Their Metabolism in Physiology and Disease.”
[16] Jamjoum et al.
[17] زمرة الدم المعروفة بـABO هي أنواع الدهون السفينغولية السكرية الموجودة على غشاء خلايا الدم الحمراء.
[18] D’Angelo et al.
[19] Jamjoum et al.
[20] Majdouline Abou-Ghali & Johnny Stiban, “Regulation of Ceramide Channel Formation and Disassembly: Insights on the Initiation of Apoptosis,”
Saudi Journal of Biological Sciences, vol. 22, no. 6 (2015), pp. 760-772.
[21] Vadim S. Pokrovsky, Veronika I. Ivanova-Radkevich & Olga M. Kuznetsova, “Sphingolipid Metabolism in Tumor Cells,”
Biochemistry (Moscow), vol. 88, no. 7 (2023), pp. 847-866.
[22] Yan Chen et al., “Long Non-Coding RNAs-Sphingolipid Metabolism Nexus: Potential Targets for Cancer Treatment,”
Pharmacological Research, vol. 210, article no. 107539 (2024).
[23] Keigo Kumagai et al., “Structure, Functions and Regulation of CERT, a Lipid-Transfer Protein for the Delivery of Ceramide at the ER–Golgi Membrane Contact Sites,”
FEBS Letters, vol. 593, no. 17 (2019), pp. 2366-2377.
[24] Yasharah Raza, Jane Atallah & Chiara Luberto, “Advancements on the Multifaceted Roles of Sphingolipids in Hematological Malignancies,”
International Journal of Molecular Sciences, vol. 23, no. 21, article no. 12745 (2022).
[25] Roger Sandhoff, Heike Schulze & Konrad Sandhoff, “Ganglioside Metabolism in Health and Disease,”
Progress in Molecular Biology and Translational Science, vol. 156 (2018), pp. 1-62.
[26] Muna Abed Rabbo et al., “Sphingolipid Lysosomal Storage Diseases: From Bench to Bedside,”
Lipids in Health and Disease, vol. 20, article no. 44 (2021).
[27] Ibid.
[28] Sandhoff, Schulze & Sandhoff.
[29] Teresa M. Dunn, Cynthia J. Tifft & Richard L. Proia, “A Perilous Path: The Inborn Errors of Sphingolipid Metabolism,”
Journal of Lipid Research, vol. 60, no. 3 (2019), pp. 475-483.
[30] Leonardo Astudillo et al., “Human Genetic Disorders of Sphingolipid Biosynthesis,”
Journal of Inherited Metabolic Disease, vol. 38, no. 1 (2015), pp. 65-76.
[31] Norman J. Haughey et al., “Roles for Dysfunctional Sphingolipid Metabolism in Alzheimer’s Disease Neuropathogenesis,”
Biochimica et Biophysica Acta, vol. 1801, no. 8 (2010), pp. 878-886.
[32] Besim Ogretmen, “Sphingolipid Metabolism in Cancer Signalling and Therapy,”
Nature Reviews Cancer, vol. 18, no. 1 (2017), pp. 33-50.
[33] Wouter J. C. Feitz et al., “The Shiga Toxin Receptor Globotriaosylceramide as Therapeutic Target in Shiga Toxin E. Coli Mediated HUS,”
Microorganisms, vol. 9, no. 10 (2021).
[34] Cinta Lleixà et al., “Autoantibody Screening in Guillain–Barré Syndrome,”
Journal of Neuroinflammation, vol. 18, article no. 251 (2021).
[35] Samar M. Hammad & Maria F. Lopes-Virella, “Circulating Sphingolipids in Insulin Resistance, Diabetes and Associated Complications,”
International Journal of Molecular Sciences, vol. 24, no. 18, article no. 14015 (2023); Faris Matanes, Waleed O. Twal & Samar M. Hammad, “Sphingolipids as Biomarkers of Disease,” in: Johnny Stiban (ed.),
Bioactive Ceramides in Health and Disease: Intertwined Roles of Enigmatic Lipids (Cham: Springer, 2019), pp. 109-138.
[36] “Test ID: Ceram,”
Mayo Clinic Laboratories, accessed on 16/7/2025, at:
https://acr.ps/1L9F2aG
[37] Hammad & Lopes-Virella.
[38] Volker Brinkmann et al., “Fingolimod (FTY720): Discovery and Development of an Oral Drug to Treat Multiple Sclerosis,”
Nature Reviews Drug Discovery, vol. 9, no. 11 (2010), pp. 883-897.
[39] Malvina Prapa et al., “GD2 CAR T Cells against Human Glioblastoma,”
Npj Precision Oncology, vol. 5, article no. 93 (2021).