تصلب الجلد (Scleroderma)، هو اضطراب مناعي ذاتي نادر نسبيًا، يتميز بزيادة إنتاج الكولاجين، ما يؤدي إلى تصلب الجلد وقد يمتد إلى الأعضاء الداخلية. يظهر المرض غالبًا بين سنّ الثلاثين والخمسين، ويصيب النساء أكثر بمعدلات أعلى من الرجال بنسبة تبلغ 4 إلى 1.
يُصنَّف تصلب الجلد عادةً إلى نوعين رئيسين: تصلب الجلد المحدود (Limited SSc)، وتصلب الجلد المنتشر (Diffuse SSc)، إذ يختلف كل منهما في شدة الأعراض ومدى تأثيره في الأعضاء الداخلية. وتتراوح المظاهر السريرية للمرض من ظاهرة رينو وتليف الجلد إلى اعتلال الأعضاء الداخلية، بما في ذلك الرئتان، والقلب، والكليتان، والجهاز الهضمي. وغالبًا ما تكون ظاهرة رينو أولى هذه المظاهر، إذ تظهر على اليدين أو الأصابع، ثم قد تتطور لاحقًا لتشمل أجهزة أخرى.
إن أسباب المرض غير معروفة على نحو دقيق، ويُعتقد أن التفاعل بين العوامل الوراثية والبيئية، مثل العدوى أو التعرض لموادّ كيميائية معينة، يساهم في تنشيط الجهاز المناعي، ما يؤدي إلى الالتهاب، والأضرار الوعائية، وتحفيز إنتاج الألياف الكولاجينية. وعلى الرغم من عدم وجود علاج شافٍ، فإن ثمة علاجًا يركز على تخفيف الأعراض، ومنع المضاعفات، وتحسين جودة الحياة، ويشمل مراقبة الأعضاء المتأثرة واستخدام الأدوية المناعية أو الداعمة بحسب الحاجة.
تعريف تصلب الجلد
تصلب الجلد هو اضطراب مناعي ذاتي نادر نسبيًا يصيب النسيج الضام، ويتميز بآلية مرضية معقدة وغير مفهومة بكاملها. يؤدي المرض إلى تصلب الجلد، وحدوث تغيّرات في الأوعية الدموية، وتكوّن أجسام مضادة. يمكن أن يصيب أي شخص، إلا أنه أكثر انتشارًا بين النساء مقارنةً بالرجال بنسبة مرتفعة، وغالبًا ما تبدأ الأعراض بالظهور بين عمرَي الـ30 والـ50 عامًا. وعلى الرغم من أن الآلية المرضية الدقيقة غير مفهومة بالكامل، فإن هناك تفاعلًا معقدًا بين العوامل الوراثية والبيئية يُؤدي دورًا محوريًا في حدوث المرض.
وصف الطبيب الإيطالي كارلو كورزيو (Carlo Curzio) أول حالة لتصلّب الجِلد في عام 1753، وأطلق الطبيب الإيطالي فانتونيتّي (Fantonetti) اسم تصلّب الجِلد على هذا المرض في عام 1836. وفي عام 1862، وصف الطبيب الفرنسي موريس رينو (Maurice Raynaud) الأعراض الثلاثية لِظاهرة رينو. تتراوح أعراض المرض بين البسيطة والشديدة، وتختلف بحسب انتشارها ومناطق الجسم المصابة. وعلى الرغم من عدم وجود علاج لتصلّب الجِلد، فإن العلاجات المتوفّرة يمكن أن تساعِد في التخفيف من تطور الأعراض إلى حدّ كبير، مثل تصلّب الجِلد، وظاهِرة رينو، وآلام المفاصل، وفشل القلب، والفشل الكلوي، وتليّف الرئتَين، ومشكلات الجهاز الهضمي[1].
الفيزيولوجيا المرضية
ينتمي تصلّب الجلد إلى أمراض المناعة الذاتية التي تتميّز باضطرابات وعائية، والتهابات، ومشكلات في المناعة، وتجلّط الدم. وفي هذا الاضطراب، تؤدي الاضطرابات المناعية الذاتية إلى تنشيط الخلايا الليفية وإفراط إنتاج الكولاجين والمكوّنات الأخرى للمصفوفة خارج الخلوية (The extracellular matrix - ECM)، ما يُسبّب تصلّب الأنسجة وتليف الأعضاء. إن السبب الدقيق وراء ذلك غير معروف، لكن يُعتقد أن العوامل الوراثية (مثل بعض أنماط الـHLA وجينات STAT4، وIRF5، وPTPN22، وغيرها) والعوامل البيئية (مثل الڤيروس المضخم للخلايا (Cytomegalovirus - CMV)، وڤيروس إبشتين-بار (Epstein-Barr Virus - EBV) والبارفوڤيروس-19 (Barvovirus 19)، أو التعرّض لغبار السيليكا والمذيبات العضوية والمواد الكيميائية) تُؤدي دورًا في حدوثه، وينتج من هذا التفاعل تضرّر الخلايا البطانية للأوعية الدموية، يُرافقه حدوث خلل في إفراز الموادّ المنظمة لتوتر الأوعية والتجلط والالتهاب، مع زيادة إنتاج موادّ مثل الإندوثيلين (Endothilin) وانخفاض إنتاج أكسيد النيتريك (Nitric Oxide) والبروستاسيكلين (Prostacyclin)، وزيادة التصاق الخلايا المناعية بالأوعية. تتجمع الخلايا الالتهابية (مثل الخلايا التائية المساعدة 2 (T-helper cells 2)، والخلايا البائية (B-cells)، والبالعات (Macrophages)) وتفرز سيتوكينات (Cytokines) وعوامل نمو تحفّز تكاثر الخلايا المبطنة والعضلية في الأوعية، وتُنشِّط الخلايا الليفية، ما يؤدي في النهاية إلى إعادة تشكيل الأوعية، وتليّف الأنسجة، وفقدان وظيفتها[2].
أنواع تصلب الجلد
لمرض تصلّب الجِلد أنواع عدة تختلف في شدّتها، فمنها: النوع المتموضع، والنوع الجهازي العام الذي يُمكن أن يكون شديدًا ومهدِّدًا لحياة المريض.
يظهر تصلّب الجِلد المتموضع (Localized Scleroderma) على هيئة بقع بيضاوية الشَّكل على الجِلد، أو خطوط أو شرائط على الذراعَين والساقَين والوَجه. أمّا تصلّب الجِلد الجهازي (Systemic sclerosis) فيندرج تحته نوعان من تصلّب الجِلد، هما: تصلب الجلد المحدود (Limited Systemic Sclerosis) الذي يؤثّر عادةً في الجِلد تحت الكوع والركبة، وقد يشمل الرقبة والوَجه؛ وتصلب الجلد المنتَشر أو الواسع (Diffuse Systemic Sclerosis) الذي يؤثّر في الجِلد فوق المرفقَين والركبتَين ويتضمّن الجذع[3].
أعراضه
تختلف مظاهر المرض السريرية بشكل كبير بين المرضى، إذ تشمل ظاهرة رينو، والمظاهر الجلدية، والمظاهر العضلية والهيكلية، والمظاهر الجهازية وغيرها.
[الصورة1)
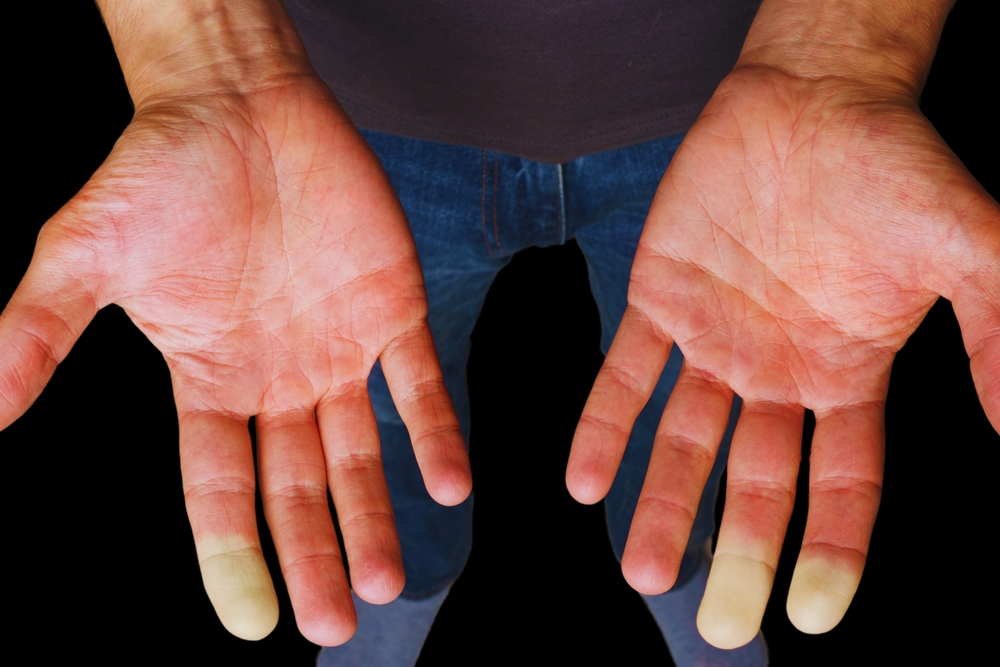 ظاهرة رينو: تغيرات في لون الأصابع
ظاهرة رينو: تغيرات في لون الأصابع
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
- ظاهرة رينو (Ryanoud’s phenomenon): ظاهرة من أولى المظاهر الشائعة لدى أكثر من 95 في المئة من مرضى تصلب الجلد ، وتتمثل في تشنجات وعائية تحدث نتيجة التعرض للبرد، مسببة تغيرات ثلاثية اللون في الأصابع (الصورة1)، وقد تشمل أيضًا الأذن، أو الأنف، أو اللسان. تبدأ هذه التغيرات بالبياض، متبوعًا بازرقاق الأطراف، ثم احمرار ناتج من تدفق الدم. في الحالات الثانوية مثل تصلب الجلد، قد تؤدي هذه الظاهرة إلى مضاعفات خطيرة، مثل تقرحات الأصابع، وفقدان الأنسجة، والغرغرينا الجافة التي قد تتطلب بترًا تلقائيًا، إضافة إلى العدوى الثانوية[4].
- المظاهر الجلدية: يُعدّ الجلد أكثر الأعضاء تأثرًا، وتختلف شدة الإصابة وتأثيرها بين المرضى. يشمل النوع المحدود الجلد القصيّ بعد المرفقين والركبتين، في حين يشمل النوع المنتشر الجلد الداني، ويصل أحيانًا إلى الجذع والوجه. تتميز المرحلة المبكرة بأصابع متورمة، والتهاب، وثخانة أو سماكة في الجلد، تليها مرحلة التليف التي تسبب تصلب الجلد والأوتار تحت الجلد، وتقليل حركة المفاصل الطرفية، مع فقدان الزوائد الجلدية والدهون تحت الجلد. قد تظهر تقرحات جلديّة بسبب التصلّب، فضلًا عن تغيّر في لون الجلد على شكل ملح وفلفل، إضافة إلى توسع الشعيرات الدموية، وترسّب الكالسيوم تحت الجلد[5].
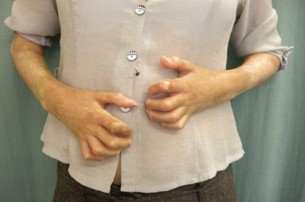 حالة متقدمة من مرض تصلب الجلد يظهر فيها تصلب الجلد وانحناء الأصابع
حالة متقدمة من مرض تصلب الجلد يظهر فيها تصلب الجلد وانحناء الأصابع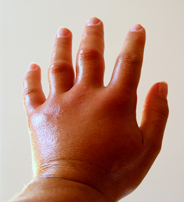 حالة مبكرة من مرض تصلّب الجلد
حالة مبكرة من مرض تصلّب الجلد
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
- المظاهر العضلية والهيكلية: تشيع الآلام المفصلية والعضلية بين مرضى تصلب الجلد، وقد يحدث التهاب مفصلي يشبه التهاب المفاصل الروماتويدي. في المراحل المتأخرة، قد تظهر تآكلات عظمية، وتقوسات في المفاصل، واحتكاكات في الأوتار نتيجة الضغط الذي يسببه تصلب الجلد، وضعف في العضلات نتيجة التليف أو الالتهاب، مع تأثير سلبي في الحركة والتغذية، كما أن ضعف العضلات مرتبط بسوء التشخيص[6].
- المظاهر الجهازية: تؤثر التصلّبات في أجهزة الجسم المختلفة، فيصاب الجهاز الهضمي بتغيرات تشمل تصلبًا حول الفم وجفافًا فيه، وصعوبات في البلع، وارتجاعًا مريئيًا، وبطئًا في تفريغ المعدة، إضافة إلى خللٍ حركي في المريء والأمعاء، واضطرابات في الأمعاء مثل الإسهال أو الإمساك. أما الجهاز التنفسي، فيصاب بأمراض الرئة الانسدادية، وتليف الرئة الذي يجعل أنسجة الرئة قاسية ويؤثر في فاعلية التنفس فيها، مسببًا ضيق التنفس وصعوبة في التوسع، وارتفاع ضغط الشريان الرئوي. وقد يؤدي تصلب الأنسجة في الرئة إلى فشل تنفسي تدريجي، وهو السبب الرئيس لوفاة المرضى. وفيما يخص القلب، قد تشمل الإصابة التهاب التامور، واعتلال عضلة القلب، واضطرابات النظم. أما الكلى، فتتمثل الأعراض الجهازية فيها في أزمة كلوية، تحدث نادرًا وتكون شديدة، وتظهر غالبًا في النوع المنتشر من تصلب الجلد، وقد تتسبب في ارتفاع حاد في ضغط الدم وفشل الكلوي[7].
- مظاهر أخرى: تشمل الإصابات الأخرى أمراض الغدة الدرقية، ومتلازمات التداخل مع أمراض المناعة الذاتية الأخرى، واضطرابات نفسية، مثل الاكتئاب خصوصًا مع التشوه الجسدي الذي يصيب المرضى. كما يظهر أحد الأنواع النادرة من تصلب الجلد بمظاهر داخلية جهازيّة فقط من دون سماكة جلدية (Systemic sclerosis sine scleroderma)، مع وجود ظاهرة رينو وشذوذ في شعيرات الأظافر والأجسام المضادة[8].
تشخيصه
يُشخَّص تصلب الجلد عبر التقييم السريري، ويُعدّ الكشف المبكر عن المرض، وتقييم مدى تأثيره، والمراقبة المستمرة للأعضاء الداخلية، أمورًا أساسية لإدارة فعّالة للمرض. تُقيَّم سماكة الجلد باستخدام درجة رودنان المعدلة (Modified Rodnan Skin Score)، إذ تُعطى درجات تتراوح بين 0 و3، مع مراقبة التغيرات مع الوقت لأهميتها التنبؤية. كما تُفحص الشعريات الظفرية، وهو إجراء يُسلط من خلاله مجهر ضوئي دقيق على الأوعية الدموية الدقيقة عند أطراف الأصابع لفحص تحت طية الظفر، إذ يُعدّ أداة مهمة للكشف المبكر لدى جميع المرضى الذين يعانون ظاهرةَ رينو ويُشتبه بإصابتهم بتصلب الجلد. كما يُجرى فحص سريري شامل يركز على عدة أجهزة للكشف عن أي إصابة للأعضاء الداخلية، مع ضرورة مراقبة ضغط الدم بانتظام، خصوصًا لدى مرضى تصلب الجلد الجهازيالمنتشر أو الذين يعانون ارتفاع ضغط الدم الجديد أو تفاقم ارتفاعه الحالي، إذ قد يشير ذلك إلى بداية أزمة الكلى الناتجة من تصلب الجلد[9].
تُؤدي الأجسام المضادة دورًا تشخيصيًا مهمًا، إذ تقدم مؤشرات على نمط المرض والتنبؤ بمساره، مثل: الأجسام المضادة للنواة (Anti-nuclear antibodies - ANA) التي تظهر إيجابية في أكثر من 90 في المئة من الحالات؛ والأجسام المضادة لمركز الكروموسوم (Anti-centromere)، التي ترتبط بتصلب الجلد المحدود، ويُعدّ وجودها مؤشرًا على زيادة خطر ارتفاع ضغط الشريان الرئوي وتقليل احتمالية الإصابة بأمراض الرئة. أما الأجسام المضادة لإنزيم التوبوأيزوميريز-1، أو ما يعرف بمضاد تصلب الجلد -70 (Anti Topoisomerase - I Anti–Scl-70)، فتشيع في حالات تصلب الجلد المنتشر، وترتبط بارتفاع خطر إصابة الجلد والأعضاء الداخلية، وأمراض الرئة والقلب. في المقابل، ترتبط الأجسام المضادة لبوليميريز الحمض النووي الريبوزي-3 (رنا) (Anti-RNA polymerase III) بتصلب الجلد المنتشر السريع، وأزمة الكلى، وانخفاض خطر أمراض الرئة. كما توجد أجسام مضادة أخرى يرتبط كل منها بأنماط مرضية محددة أو متلازمات تداخلية[10].
تُضاف إلى عملية التشخيص الفحوصُ المخبرية مثل تعداد الدم الكامل للكشف عن الأنيميا، وتقييم وظائف الكلى، ومراقبة البروتين في البول، وقد تُستخدم مؤشرات الالتهاب وارتفاع إنزيمات العضلات للكشف عن اعتلال عضلي التهابي. أما التقييم الإشعاعي، فيشمل الأشعة السينية للكشف عن التكلسات وتهتّك أطراف الأصابع البعيدة، والموجات فوق الصوتية للعضلات والمفاصل، وتخطيطًا كهربائيًا للعضلات عند الاشتباه في اعتلال عضلي، وأشعة مقطعية عالية الدقة لتقييم أمراض الرئة الخلالية. تستخدم اختبارات وظائف الرئة عند الاشتباه بارتفاع ضغط الشريان الرئوي، كما يُصور صدى القلب للتحقق من هذا الارتفاع، وقد يلزم إجراء قسطرة القلب اليمنى لتأكيد التشخيص. أما في حالة الاشتباه بتأثر المريء والجهاز الهضمي العلوي، يمكن استخدام التنظير العلوي، وقياس الضغط المريئي، ودراسات ابتلاع الباريم، ومسبار الحموضة على مدار 24 ساعة، إذ يظهر المريء المتوسع مع وجود هواء زائد في الأشعة المقطعية بوصفه علامةً مميزةً لخلل حركة المريء[11].
معايير تصنيفه
تعتمد المعايير الكلية الأميركية للروماتيزم في تصنيف تصلب الجلد على نظام نقاط، إذ يشير مجموع 9 نقاط أو أكثر إلى تشخيص تصلب الجلد. وحسب هذا المعيار، تُقيم النقاط كما يأتي:
- سماكة جلدية ثنائية الجانب تمتد إلى أقصى مفاصل الأصابع الطرفيّة: 9 نقاط.
- سماكة الجلد في الأصابع (تحتسب أعلى درجة فقط): بين المفاصل البعيدة والقريبة لفقرات الأصابع: 4 نقاط.
- أصابع متورمة (Puffy fingers): نقطتان.
- إصابات أطراف الأصابع (تحتسب أعلى درجة فقط): ندوب أطراف الأصابع: 3 نقاط؛ تقرحات أطراف الأصابع: نقطتان.
- توسع الشعيرات الدموية: نقطتان.
- تشوه شعيرات أظافر الأصابع (Abnormal nailfold capillaries): نقطتان.
- ظاهرة رينو: 3 نقاط.
- أمراض الرئة (الحد الأقصى للنقاط: 2): أمراض الرئة الخلالية: نقطتان؛ ارتفاع ضغط الشريان الرئوي: نقطتان.
- وجود الأجسام المضادة الخاصة بتصلب الجلد: 3 نقاط[12].
علاجه
يختلف العلاج حسب العضو المصاب، ومن المهم أن يكون علاج المرضى شاملًا، بحيث يتضمن توعية المريض وعائلته، والعلاج الدوائي، والتأهيل. ولا يوجد دواء يوقِف المرض أو يَشفيه تمامًا، أو يُعالِج كل أعراضه، ولكن هناك مجموعة من الأدوية التي يمكن أن توقِف تطوّره، خاصة إذا ابتدأ العلاج مبكرًا. وتنقسم الأدوية إلى مجموعات تشمل مثبطات المناعة، مثل ميثوتريكسات (Methotrexate)، والميكوفينولات موفيتيل (Mycophenolate mofetil)، وسيكلوفوسفاميد (Cyclophosphamide)، والأزاثيوبرين (Azathioprine)، وهيدروكسي كلوروكوين (Hydroxychloroquine)، والكورتيكوستيرويدات (Corticosteroids) التي تُستخدم بحذر لتجنب أزمة الكلى الناتجة من تصلب الجلد، وفي حالات محددة فقط[13].
يشمل العلاج علاج الأعراض مثل ظاهرة رينو التي تُعالج من خلال تدفئة الأطراف، وتجنب التدخين والتوتر، وتوسيع الأوعية الدموية بالدواء مثل حاصرات قنوات الكالسيوم. أما علاج الأعراض الجلدية، فتُستخدم فيه، إضافة إلى مثبطات المناعة، مراهم الترطيب، والستيرويدات الموضعية، والعلاجات الموضعية الأخرى. أما المفاصل والعضلات، فيُستخدَم لعلاجه مضادات الالتهاب اللاستيرويدية للأعراض الخفيفة، ومثبطات المناعة للحالات الالتهابية، والعلاج الطبيعي لمنع التقلصات.
أما الأمراض الرئوية المتوسطة والشديدة، مثل مرض الرئة الخلالي، فتعالج باستخدام أدوية، مثل السيكلوفوسفاميد، أو توسيليزوماب (Tocilizumab)، أو ميكوفينولات موفيتيل، وفي بعض الحالات يُستخدم ريتوكسيماب (Rituximab) أو بروستاسايكلين (Prostacyclin) حسب الشدة. وفي الحالات الشديدة، قد يُلجأ إلى زراعة الرئة أو إلى الأدوية المضادة للتليف مثل نينتيدانيب (Nintedanib).
أما الأعراض القلبية، فيشمل علاجها التعامل مع اضطرابات النظم القلبية بالأدوية أو أجهزة تنظيم ضربات القلب. ويُنصح بتعديل نمط الحياة والغذاء للمرضى الذين يعانون أعراضًا هضمية، إضافة إلى أدوية الحموضة والحركة المعوية، ومعالجة فرط نمو البكتيريا في الأمعاء بالمضادات الحيوية، وقد يُستخدم الليزر لحالات النزف. أما الأزمة الكلوية، فتُستخدم لعلاجها مثبطات إنزيم الإيس (ACE-inhibitors) مثل كابتوبريل (Captopril)، وهي العلاج الفعال الوحيد، وينصح بتجنب الستيرويدات العالية لخطورتها عند ظهور أول علامات المرض، مع الاستمرار في مراقبة وظيفة الكلى. يسعى العلماء لإيجاد أدوية فعّالة لمنع تشكّل الكولاجين داخل الأوعية الدموية، وفي بعض الحالات الحادة والشديدة التي لا تَستجيب للعلاج المتوفّر، قد تكون زراعة الخلايا الجذعية خيارًا أخيرًا[14].
يمكن أن تتحسّن الأشكال الموضعية من المرض وتختفي من تلقاء نفسها بمرور الوقت، أما الأشكال الجاهزيّة فتكون دائمة. ووفقًا لدراسة حديثة نُشرت في مجلة Arthritis Research & Therapy (أبحاث التهابات المفاصل وعلاجها)، فلا يزال المرضى المصابون بنوع تصلّب الجلد المنتشِر يعانون نسبة وفيات مبكرة عالية، إذ تبلغ فرص البقاء على قيد الحياة لخمس سنوات قادمة بعد التشخيص 80 في المئة، ويعد التشخيص المبكر عاملًا مهمًا في تحسين فرص النجاة [15].
المراجع
Adigun, Rotimi, Amandeep Goyal & Anis Hariz. “Systemic Sclerosis (Scleroderma).” in: StatPearls. Treasure Island, FL: StatPearls Publishing, 2026. at: https://acr.ps/1L9B9Vf
Hawk, Angela & John C. English. “Localized and Systemic Scleroderma.” Seminars in Cutaneous Medicine and Surgery. vol. 20, no. 1 (2001). pp. 27-37. doi: 10.1053/sder.2001.23093
Jaafar, Sara et al., “Clinical Characteristics, Visceral Involvement, and Mortality in At-Risk or Early Diffuse Systemic Sclerosis: A Longitudinal Analysis of an Observational Prospective Multicenter US Cohort.” Arthritis Research & Therapy. vol. 23, article no. 170 (2021). doi: 10.1186/s13075-021-02548-1
Kowalska-Kępczyńska, Agnieszka. “Systemic Scleroderma-Definition, Clinical Picture and Laboratory Diagnostics.” Journal of Clinical Medicine. vol. 11, issue 9, article no. 2299 (2022). doi: 10.3390/jcm11092299
Kucharz, Eugeniusz Józef & Magdalena Kopeć-Mędrek. “Systemic Sclerosis Sine Scleroderma.” Advances in Clinical and Experimental Medicine. vol. 26, no. 5 (2017). pp. 875-880. doi: 10.17219/acem/64334
Sambataro, Gianluca et al. “Progression and Prognosis of Interstitial Pneumonia with Autoimmune Features: A Longitudinal, Prospective, Multi-Centre Study.” Clinical and Experimental Rheumatology. vol. 41, no. 5 (2023). pp. 1140-1148. doi: 10.55563/clinexprheumatol/lycdca
Van den Hoogen, Frank et al. “2013 Classification Criteria for Systemic Sclerosis: An American College of Rheumatology/European League against Rheumatism Collaborative Initiative.” Arthritis & Rheumatism. vol. 65, issue 11 (2013). 2737-2747. doi: 10.1002/art.38098
Zhao, Ming et al. “Clinical Treatment Options in Scleroderma: Recommendations and Comprehensive Review.” Clinical Reviews in Allergy & Immunology. vol. 62, no. 2 (2022). pp. 273-291. doi: 10.1007/s12016-020-08831-4
[1] Agnieszka Kowalska-Kępczyńska, “Systemic Scleroderma—Definition, Clinical Picture and Laboratory Diagnostics,” Journal of Clinical Medicine, vol. 11, issue 9, article no. 2299 (2022), doi: 10.3390/jcm11092299
[2] Ibid.
[3] Angela Hawk & John C. English, “Localized and Systemic Scleroderma,” Seminars in Cutaneous Medicine and Surgery, vol. 20, no. 1 (2001), pp. 27-37, doi: 10.1053/sder.2001.23093
[4] Ibid.
[5] Rotimi Adigun, Amandeep Goyal & Anis Hariz, “Systemic Sclerosis (Scleroderma),” in: StatPearls (Treasure Island, FL: StatPearls Publishing, 2026), accessed on 4/3/2026, at: https://acr.ps/1L9B9Vf
[6] Ibid.
[7] Gianluca Sambataro et al., “Progression and Prognosis of Interstitial Pneumonia with Autoimmune Features: A Longitudinal, Prospective, Multi-Centre Study,” Clinical and Experimental Rheumatology, vol. 41, no. 5 (2023), pp. 1140-1148, doi: 10.55563/clinexprheumatol/lycdca
[8] Adigun, Goyal & Hariz, op. cit.; Eugeniusz Józef Kucharz & Magdalena Kopeć-Mędrek, “Systemic Sclerosis Sine Scleroderma,” Advances in Clinical and Experimental Medicine, vol. 26, no. 5 (2017), pp. 875-880, doi: 10.17219/acem/64334
[9] Kucharz & Kopeć-Mędrek, op. cit.
[10] Ibid.; Adigun, Goyal & Hariz, op. cit.
[11] Kucharz & Kopeć-Mędrek, op. cit.
[12] Frank van den Hoogen et al., “2013 Classification Criteria for Systemic Sclerosis: An American College of Rheumatology/European League against Rheumatism Collaborative Initiative,” Arthritis & Rheumatism, vol. 65, issue 11 (2013), pp. 2737-2747, doi: 10.1002/art.38098
[13] Ming Zhao et al., “Clinical Treatment Options in Scleroderma: Recommendations and Comprehensive Review,” Clinical Reviews in Allergy & Immunology, vol. 62, no. 2 (2022), pp. 273-291, doi: 10.1007/s12016-020-08831-4
[14] Ibid.; Adigun, Goyal & Hariz, op. cit.
[15] Sara Jaafar et al., “Clinical Characteristics, Visceral Involvement, and Mortality in At-Risk or Early Diffuse Systemic Sclerosis: A Longitudinal Analysis of an Observational Prospective Multicenter US Cohort,” Arthritis Research & Therapy, vol. 23, article no. 170 (2021), doi: 10.1186/s13075-021-02548-1