الموجز
علم دراسة البروتيوم (علم البروتيوميات/ Proteomics) هو دراسة شاملة وواسعة النطاق لبروتيوم الكائنات الحية، الذي يُعرَّف بأنه مجموعة البروتينات الكاملة التي يُنتجها الجينوم أو الخلية أو النسيج.
صاغ هذا المصطلح العالم الأسترالي مارك ويلكنز (Marc Wilkins) في أوائل تسعينيات القرن العشرين، لتمييز الناتج الوظيفي الديناميكي للخلية (البروتينات) عن
الجينوم الثابت نسبيًا. يُوفّر علم البروتيوميات خريطة وظيفية للنشاط الخلوي، وهو ضروري لفَهْم الأساس الجزيئي للأمراض، إذ يُقدّم إضافات لا يُمكِن لعلم الجينوم وحده توفيرها.
وتشمل تطبيقات هذا العلم مجالات
الطب والزراعة والعلوم البيئية، وهو يعتمد على مجموعة من
التقنيات التحليلية المتقدّمة لفصل البروتينات وتحديدها وقياس كمّيتها، مثل تقنية
الرحلان الكهربائي ثنائي الأبعاد، التي تفصل البروتينات بناءً على نقطة تعادلها الكهربائي ووزنها الجزيئي، ما يُنشِئ خريطة مرئية لوفرة البروتينات. وللتعرّف الدقيق إلى البروتينات، تُستخدَم تقنيات
مطيافية الكتلة المختلفة، وغالبًا ما يكون ذلك بعد تجزئة العيّنة باستخدام
الكروماتوغرافيا السائلة عالية الأداء النانوية. علاوة على ذلك، تُستخدَم
مصفوفات البروتينات لتمكين التوصيف عالي الإنتاجية لإنتاج البروتين خلويًا، وهي قادرة على معالجة مئات العيّنات في وقت واحد.
أهميته
يقوم علم دراسة البروتيوم (Proteomics) على دراسة مجمل البروتينات في الخلية، الذي يُشار إليه باسم البروتيوم (Proteome)[1]. ظهر مصطلح البروتيوم لأول مرة على يد
مارك ويلكنز وزملائه عام 1994، ليشابه مصطلح الجينوم الذي ظهر قبله. يسهم علم البروتيوم في فَهْم علم الأحياء بشمولية كبيرة، نظرًا لأن البروتينات هي التي تضطلع بالوظائف الخلوية وتتحكّم فيها[2]؛ ففي الوقت الذي يُركّز علم الجينوم فيه على دراسة الخريطة الجينية الكاملة للخلية، أي المادة الوراثية التي تُشفَّر ومن خلالها تُنتَج البروتينات كافة، فإن علم البروتيوم يدرس ناتج الجينوم، الذي يتمثَّل في البروتينات التي تضطلع بالعمليات الخلوية كافة.
تتكوَّن البروتينات من تسلسُلِ
الأحماض الأمينية التي تُحدّدها الشيفرة الوراثية في الجينوم. ويُحدِّد تسلسُلُ الأحماض الأمينية بنيةَ البروتين ووظيفته مباشرةً. وفي حين أن الجينوم يتشابه في جميع خلايا كائنٍ حيٍّ واحد، فإن البروتيوم يختلف باختلاف أنواع الخلايا في هذا الكائن، وذلك لتأثّره بالعناصر البيئية والفيزيولوجية. تنشَأ هذه التعقيدات نتيجة آليات تنظيمية داخل الخلية، تشمل
التضفير البديل (Alternative splicing)، والتعديلات ما بعد الترجمة (Post-translational modifications)، والتفاعلات بين البروتينات. كذلك يمكن لجينوم واحد أن يُنتِج عددًا كبيرًا من الحالات البروتيومية المختلفة، ما يجعل البروتيوم أساسًا لفَهْم الأمراض من الناحية الجزيئية[3]. أصبح علم البروتيومات جزءًا أساسيًا من تطبيق
علم الأحياء الجزيئي والبحث الطبي، ولا سيما في دراسة الأمراض، مثل تحديد وظيفة
الجينات الكابحة للأورام {{الجينات الكابحة للأورام (Tumor suppressor genes): جينات تعمل لإبطاء نموّ الخلايا، ما يؤدّي إلى إبطاء الانقسام وتكثيف إصلاح تلف الحمض النووي، وبدْء موت الخلايا المبرمج (الاستماتة) لمنع تكاثُر الخلايا غير المنضبط وتطوّر السرطان، فعندما تحدث طفرة أو تعطيل تُفقَد هذه الوظائف الوقائية، ما يسمح للخلايا بالنمو بشكل خارج عن السيطرة وتكوين الأورام.}}، واكتشاف المؤشرات الحيوية للتشخيص والعلاج[4]. يكْمُن الهدف الأساسي لعلم البروتيوم في إنتاج خريطة شاملة للتعبير البروتيني والوظيفة البروتينية، ومكان وجود البروتينات، وتفاعُلاتها وارتباطاتها داخل نوعِ خلايا مُعيَّن، وهي أمور لا يمكن تحقيقها عبر علم الجينوم وحده. من المتوقّع أن يؤدي علم البروتيومات دورًا محوريًا في
الطب المشخصن (Personalized medicine)، وتطوير
الأدوية، وبيولوجيا الأنظمة الحيوية. ورغم التحديات، فإن تقنيات
قياس الطيف الكتلي (Mass spectrometry) والمعلوماتية الحيوية (Bioinformatics) جعلت تحليل البروتينات أكثر دقةً وفاعلية[5].
تنوع البروتينات وتخصّصها
تُعَدّ البروتينات المسؤول الأساسي عن الوظائف الخلوية، ويعكس البروتيوم تعقيدَ النظام البيولوجي للخلية[6]. تُعبِّر كل خلية عن مجموعة فريدة من البروتينات، ويتأثر ذلك بعمليات تنظيم
النسخ واستقرار
الحمض النووي الريبي المرسال (mRNA)، ومعدلات
الترجمة، ومسارات تحلّل البروتين وتحويرها كالفسفرة (إضافة مجموعات فوسفات/ Phosphorylation) والغلكزة (إضافة مجموعات سكرية/ Glycosylation) وغيرها. تؤدي تلك العمليات إلى ظهور أنماط بروتيومية مميّزة، حتى بين الخلايا المتطابقة وراثيًا، التي من المفترض أن تُنتِج بروتينات متماثلة[7]. علاوة على ذلك، غالبًا ما تُظهِر البروتينات وظائفَ متداخلة، ويمكن تعديل نشاطها من خلال تعديلات ما بعد الترجمة للحمض النووي، والتضفير البديل للحمض النووي المرسال، والتفاعلات مع جزيئات أخرى[8]. يتغيَّر بروتيوم الخلية باستمرار، ويتميّز بحركيته حسب الظروف التي تتعرّض لها الخلية والكائن الحيّ عمومًا.
شهد علم دراسة البروتيوم في الآونة الأخيرة تقدُّمًا كبيرًا في إمكانية رسم خريطة للتعبير البروتيني، نظرًا للتقدّم التقني في دراستها وتحليلها، فمن خلال هذه التقنيات تُفحَص التفاعلات بين البروتينات والإشارات التي تُمكِّن من معرفة مكان تموضع البروتين داخل الخلية، ومن ثم مِن الممكن أيضًا معرفة المؤشرات الحيوية الخاصة بمرض
السرطان من خلال هذه الخرائط[9].
التعديلات ما بعد ترجمة البروتينات
من أبرز التحدّيات والفرص للمعرفة في علم البروتيوم هو دراسة التعديلات ما بعد الترجمة، وهي تغييرات كيميائية تتشكّل على البروتينات بعد تصنيعها داخل الخلية. يمكن أن تؤثّر هذه التعديلات في بنية البروتين ونشاطه ومكان وجوده في الخلية واستقراره، ما يؤثّر في وظيفة البروتين، ومن ثم في وظيفة الخلية وحالتها[10]. مِن التعديلاتِ التي يمكن أن تخضع لها البروتينات عمليّاتُ الفسفرة أو الغلكزة، وذلك نتيجة تأثيراتٍ داخل الخلية أو خارجها[11]. وثمة أنواع أخرى مهمة من التعديل الكيميائي للبروتينات، مثل
الأَسْتَلَة (Acetylation) والوَبْكَنَة (Ubiquitination)[12]. تكمُن أهمية هذه العمليات في إمكانية وجود عدة أشكال متباينة للبروتين ذاته، تبعًا لحالته من الفسفرة أو التعديلات الأخرى. تؤدي الفسفرة مثلًا دورًا رئيسًا في التحكم بوظيفة البروتينات، خصوصًا
الإنزيمات، إذ ترتبط الاختلالات في تنظيم مختلف بروتينات
الكيناز (Kinases) والفوسفاتاز (Phosphatases) مع حركات التفاعلات في أمراضٍ مثل السرطان[13]. ونظرًا لديناميكية التعديلات البروتينية وأهميتها تشكيليًا ووظيفيًا، فقد تفرَّع علم البروتيوم إلى علمَي
البروتيوم المفسفر (Phosphoproteomics) والبروتيوم المُغَلْكَز (Glycoproteomics) وغيرهما.
دراسة البروتينات مقابل دراسة الجينات
تُعَدّ دراسات البروتيوميات مُكمّلةً وداعمةً لدراسات الجينوم، ففي حين أن الجينوميات تركّز على فكّ الشيفرة الكاملة للمادة الجينية للكائن الحيّ، الموجودة داخل الخلايا، فإن علم البروتيوم يدرس البروتينات[14]. وعلى عكس الجينوم الذي يتميّز بالاستقرار النسبي الذي يمكن زيادة كمّياته وكذلك كمّيات
الحمض النووي الريبي (RNA) بدقةٍ عالية، باستخدام تقنيات مثل
تفاعل البوليميراز المتسلسل (Polymerase chain reaction, PCR) ما يُسهّل دراستهما، فإن البروتيوم يُعَدّ ديناميكيًا وكثير التعديلات، خصوصًا ما بعد الترجمة. ولا توجد استراتيجية تضخيم عامّة للبروتينات تُمكِّن من تكثير كمّياتها، ومن ثم فإن تحليل البروتيوم يُعَدّ أكثر تعقيدًا وإشكاليةً من التحليل الجيني لانخفاض وفرته[15]. من هنا، كان الاعتماد على إثراء العيّنات بطرق مختلفة، كأساليب الترسيب البروتيني (protein precipitation) أو
تجزئة الخلايا {{تجزئة الخلايا (Cell fractionation): تقنية مخبرية لفتح الخلايا وفصل أجزائها الداخلية (العضيات، والأغشية، والبروتينات الذائبة) باستخدام خصائصها الفيزيائية المختلفة مثل الحجم والشكل والكثافة، وذلك بشكل أساسي من خلال الطرد المركزي التفاضلي أو الطرد المركزي بتدرّج الكثافة.}} لمكوّناتها من
العضيات (Organelles).
التقنيات وأدوات التحليل
إن طرق فصل البروتينات، وقياس الطيف الكتلي لها، وأدوات المعلوماتية الحيوية، وقواعد بيانات التسلسل، مَكَّنَت مُجتمِعةً من تحليل البروتينات وتوصيفها على نطاق واسع وبدقّة عالية[16].
الرحلان الكهربائي الهُلامي ثنائي الأبعاد
من بين تقنيات فصل البروتينات، يُعَدّ الرحلان الكهربائي الهلامي ثنائي الأبعاد (2D-PAGE) من أُولى التقنيات المستخدمة في تحليلات البروتيوميات، إذ تُفصَل البروتينات وفقًا لنقطة تعادلها الكهربائي ووزنها الجزيئي[17]، ما يُنتِج خريطةً هُلاميةً يمكن من خلالها رؤية كل بروتين بشكل منفصل (الشكل 1). ففي البُعْد الأول، تُوضَع جميع البروتينات في عينةٍ ما في وسطٍ هُلامي تتدرّج فيه الحموضة حسب
الرقم الهيدروجيني (pH)، ومن ثم ترحّل البروتينات أفقيًا عند تفعيل الكهرباء، إلى أن تتوقّف تمامًا عند تعادل شُحناتها. وفي البُعْد الثاني، يُوضَع الشريط الهُلامي الذي فُصِلت فيه البروتينات في البُعْد الأول فوق وسطٍ هُلامي آخر مُكوَّن من البولي أكريلاميد (polyacrylamide)، فترحل مرّة أخرى عموديًا إلى الأسفل حسب وزنها الجزيئي، على النحو الذي تظل فيه البروتينات الأكبر حجمًا في الأعلى، وتتحرّك البروتينات الأصغر حجمًا إلى الأسفل. بعدئذٍ، يُلوِّن الباحث البروتينات في الوسط الهُلامي من أجل التحليل (الشكل 1).
[الشكل 1]
 تحليل البروتينات باستخدام الرحلان الكهربائي الهلامي ثنائي الأبعاد
تحليل البروتينات باستخدام الرحلان الكهربائي الهلامي ثنائي الأبعاد
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل 2]
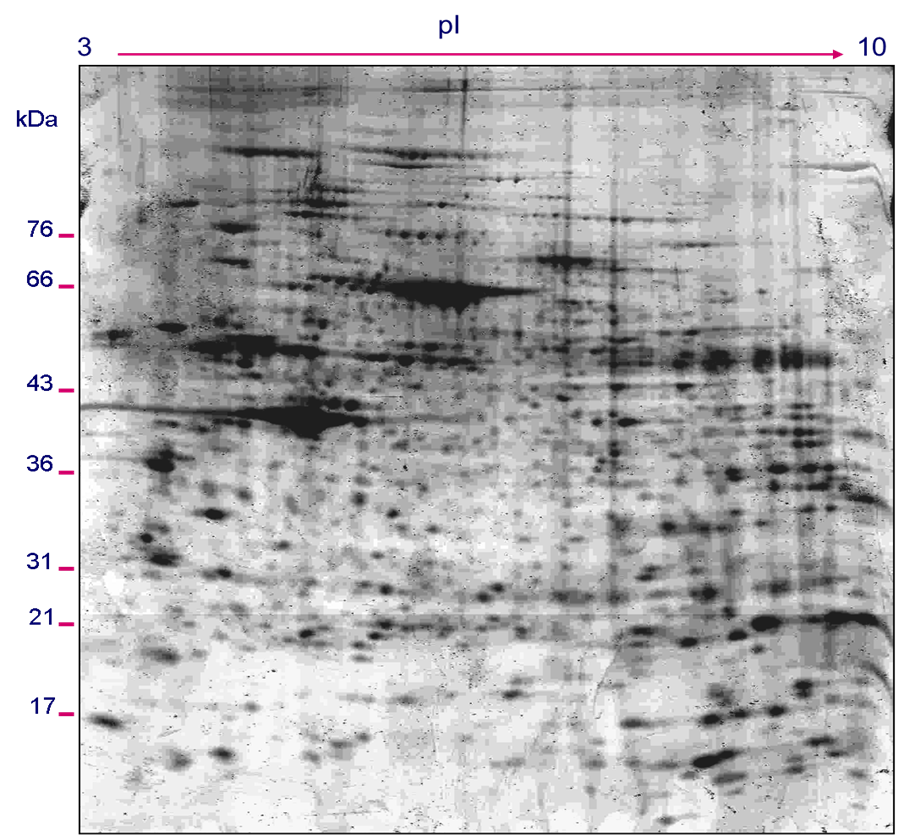 مثال حقيقي لإحدى نتائج تقنية الرحلان الكهربائي الهلامي ثنائي الأبعاد
مثال حقيقي لإحدى نتائج تقنية الرحلان الكهربائي الهلامي ثنائي الأبعاد
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تُتيح هذه التقنية للباحثين مقارنة وفرة البروتينات في ظروف بيولوجية مختلفة أو بعد المعالجات التجريبية[18]، إلا أنها ليست فعّالة نظرًا لكشفها عن البروتينات الموجودة بوفرة في العيّنات، وهي تُشكّل نسبة قليلة من بروتيوم الخلايا والعيّنات الحيوية. كذلك فإن هذه البروتينات ليست المهمّة وظيفيًا نسبيًا بالمقارنة بالبروتينات التي توجد بكميات أقلّ كعوامل النسخ (Transcription factors).
تُمثّل العلامات السوداء البروتينات بعد رحلانها حسب الشحنة أفقيًا، ومن ثم وزنها الذري عموديًا وتلوينها
قياس الطيف الكتلي
قياس الطيف الكتلي من أقوى الأدوات لتحليل تعديلات البروتينات، إذ يُتيح التعرّف إلى
الببتيدات {{الببتيدات (Peptides): هي سلاسلُ قصيرة من الأحماض الأمينية المرتبطة ببعضها، تُعَدّ أجزاءً أساسية للبروتينات.}} وقياس كميتها من خلال قياس نسبة كتلتها إلى شحنتها (m/z) بدقة، ما يُمكِّن الباحث من معرفة تسلسُل الأحماض الأمينية والحالة البنيوية للبروتين، من خلال مقارنتها بتسلسلات بروتينية معروفة مسبقًا[19]. من أكثر استخدامات قياس الطيف الكتلي تطوّرًا هو التسلسل المزدوج(Tandem MS/MS) ، الذي يُوفّر بيانات تفصيلية لتسلسل الببتيدات لغرض تحديد البروتينات الموجودة في عيّنة ما[20]. تتألّف هذه العملية من تحليل الببتيدات على مرحلتَيْن: في الأولى يُعزَل أيون الببتيدات بناءً على قياس نسبة الكتلة إلى الشحنة بوساطة الفاصل الأول (MS1)، ثم يُقَنَّن وتُحَلَّل الأجزاء الناتجة مرةً أخرى باستخدام فاصلٍ آخر (MS2)، لتحديد تسلسل الأحماض الأمينية في البروتين (الشكل 3).
الكروماتوغرافيا السائلة عالية الأداء النانوية
تُستخدَم
الكروماتوغرافيا السائلة عالية الأداء النانوية متناهية الصغر (nano-HPLC) غالبًا بالتكامل مع قياس الطيف الكتلي، وهي تقنية تُستخدَم لفصل الببتيدات والبروتينات أولًا قبل تحليلها. تُتيح هذه التقنية تجزئة المزيج البروتيني المعقّد، بناءً على
كراهيته للماء (Hydrophobicity) أو شحنته أو ألفته (affinity)، ما يُحسّن من دقة تحديد البروتينات في المراحل التالية للتحليل[21].
تبدأ إحدى طرق التحليل البروتيومي باستخدام هذه التقنية بتبسيط العيّنة البروتيومية، بتكسير البروتينات إلى ببتيدات بوساطة إنزيم مكسّر للبروتينات (بروتياز)، ومن ثم فصلها عن طريق تقنية
الكروماتوغرافيا اعتمادًا على خصيصةٍ للببتيدات مثل كُرهِها للماء. وخلال عملية الفصل، تدخل الببتيدات تباعًا إلى جهاز قياس الطيف الكتلي لتتأيّن أولًا، ومن ثم تنطلق خلال الفاصل الأول لمقياس الكتلة (Mass analyzer 1, MS1)، فيقيس الكاشف (Detector) سرعتَها المعتمِدة على خصيصة الكتلة/ الشحنة، وتدخل الببتيدات أيضًا تباعًا إلى مُفتِّت الببتيدات، الذي يعمل بطريقة التفكّك الناتج من التصادم (Collision-induced dissociation, CID). من ثم، تنطلق لبنات الأحماض الأمينية و/أو الببتيدات الأصغر حجمًا خلال الفاصل الثاني لمقياس الكتلة (MS2)، وتُقاس سرعتُها المعتمِدةُ على الكتلة/ الشحنة بالكاشف. وأخيرًا، تُحلَّل القياسات وتُحوَّل البيانات إلى ترتيب تسلسل الأحماض الأمينية في الببتيدات التي تم التعرّف إليها، ومن ثم تُحدَّد هُوية البروتينات في العيّنة الأساسية (الشكل 3).
[الشكل 3]
 شرح مبسّط لعملية التحليل بوساطة الكروماتوغرافيا ثم جهاز قياس الطيف الكتلي ذي التسلسل المزدوج
شرح مبسّط لعملية التحليل بوساطة الكروماتوغرافيا ثم جهاز قياس الطيف الكتلي ذي التسلسل المزدوج
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
مصفوفات البروتينات
تُعرَف هذه التقنية أيضًا باسم مصفوفات البروتين الدقيقة (microarrays)، وهي تستند إلى مفهوم "الطُّعم" و"الفريسة"، إذ يُثبَّت أحدهما على سطح صلب، بينما يكون الآخر مذابًا في محلول ويضاف إلى الطُّعم ليلتقطه، فيُكتشَف الارتباط أو التفاعل بينهما، ما يؤكد وجود البروتين المطلوب في العينة. إذا كان جزيء البروتين هو المُثبَّت، فإن مصفوفة البروتين تُعرَف باسم مصفوفة بروتين الطّور العكسي (Reverse phase)[22]. يمكن تقسيم مصفوفات البروتين إلى
مصفوفات التعبير البروتيني {{مصفوفات التعبير البروتيني (Protein expression array): أداة عالية الإنتاجية، تُثبَّت فيها آلاف البروتينات (أو الأجسام المضادة) المعروفة على سطح صلب (زجاج/ غشاء) لقياسِ مستويات البروتين في وقت واحد، أو الكشف عن التفاعلات، أو تحديد نشاط البروتين في عيّنات معقّدة.}} أو
مصفوفات الوظيفة البروتينية {{مصفوفات الوظيفة البروتينية (Functional protein array): أداة عالية الإنتاجية، تعمل على تثبيت آلاف البروتينات النقية والنشطة على سطحٍ ما لدراسة وظائفها البيوكيميائية، وتفاعُلاتها (مع الحمض النووي الريبي منقوص الأكسجين، والحمض النووي الريبي، والبروتينات الأخرى، والجزيئات الصغيرة)، وأنشطتها الإنزيمية، وتعديلاتها ما بعد الترجمة بشكل متوازٍ.}} وفقًا للغاية المرجوّة منها (الشكل 4). تَستخدِم كثيرٌ من المصفوفات جزيئات ذات أنشطة محدّدة معروفة، مثل
الأجسام المضادة (antibodies) أو
الليكتينات {{الليكتينات (lectins): مجموعة متنوعة من البروتينات التي ترتبط بالكربوهيدرات، وتوجد في جميع الكائنات الحية تقريبًا، وتتركّز خصوصًا في النباتات مثل الحبوب والبقوليات. لها أدوارٌ في التعرّف الخلوي والمناعة، وتعمل أحيانًا كآليات دفاعية. بعض أنواع الليكتين سامّة، لكن معظمها غير سامّ.}} أو الحمض النووي. وتُستخدَم هذه المصفوفات بناءً على طبيعة الطُّعم كفحص التعبير البروتيني، كمصفوفتَي التحديد ذي الطور الأمامي المباشر أو غير المباشر لقياس التعبير البروتيني أو مصفوفة النشاط الإنزيمي، وتحديد المؤشرات الحيوية، وتحليل علامات/ غليكوزيلات سطح الخلية، والتشخيص السريري، وتحليل سلامة البيئة/ الغذاء. وتُستخدَم مصفوفات البروتين الوظيفية بشكل رئيس لفحص أنواع مختلفة من أنشطة البروتين، بما في ذلك ارتباطات البروتين بعضها ببعض، أو بالأحماض النووية معروفة التكوين، أو بالمركّبات الكيميائية كالأدوية، ولتحديد
ركائز الإنزيمات وأنماط
الاستجابات المناعية.
[الشكل 4]
 أنواع مصفوفات البروتين: مصفوفات التعبير البروتيني ومصفوفات الوظيفة البروتينية
أنواع مصفوفات البروتين: مصفوفات التعبير البروتيني ومصفوفات الوظيفة البروتينية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تتميّز هذه الأنواع من مصفوفات البروتين بعدد من المزايا، بما في ذلك: الإنتاجية العالية، واستخدام العيّنات بكميات قليلة نسبيًا، والمرونة العالية، والحساسية المرتفعة، وقراءة النتائج مباشرةً. تتميّز مصفوفات البروتين ذات الطور العكسي كذلك بوجود بروتيومات لعدة عيّنات مصفوفة أو مرقطة على السطح، مع إضافة جزيء الالتقاط المحدّد، ولا سيما الأجسام المضادة إليها. والغرض من ذلك هو تقييم
التعبير الجيني ومستويات التعبير الجيني لبروتينٍ مُعيَّنٍ في عيّنات متعددة في آنٍ واحد، التي قد تصل إلى العشرات أو المئات أو حتى أكثر. ومن مزايا هذا النوع من المصفوفات أيضًا إمكانية الإرسال المتعدد، إذ يمكن استخدام أجسام مضادة تستهدف بروتينات مختلفة في وقت واحد للكشف عنها. كذلك يمكن قياس الاختلاف في مستويات بروتينات في عيّنات متعددة، مثل الخلايا الطبيعية مقابل الخلايا السرطانية. تتميّز هذه التقنية أيضًا بحساسية عالية في الكشف عن البروتينات التي تتراوح كمّيتها بين
بيكوغرام (10-12 غرام/ Picogram) وأتوغرام (10-18 غرام/ Attogram)، علاوة على اتساق القياسات باستخدام هذه التقنية. عمومًا، فإن التحدي الأكبر الذي تواجهه مصفوفات البروتين هو العثور على طُعم -سواء أكان جسمًا مضادًّا أم حمضًا نوويًا أم غير ذلك- يتمتّع بالكشف عن فريسته بخصوصية وجوْدة وتفاعُلية عالية.
العلاقة مع قواعد بيانات التسلسل
تكْمُن أهمية المعلوماتية الحيوية في تفسير الكَمّ الهائل من البيانات الناتجة من تقنيات مطياف الكتلة وغيرها من الأساليب التحليلية، إذ تُحوِّل المعلوماتيةُ الحيويةُ هذه البيانات إلى مَعرفةٍ منظَّمةٍ يُمكِن تخزينها واسترجاعها عند الحاجة[23]. تُستخدم
الخوارزميات لمطابقة الأطياف الخام مع الأوزان الجزيئية المتوقعة للببتيدات في قواعد بيانات البروتين والجينوم. وتعمل هذه الأتمتة على تسريع عملية تحديد البروتينات، ما يُمكِّن الباحثين من فحص مجموعات بيانات ضخمة، وتصفية البروتينات ذات الأهمية العالية لإجراء تحليلات وظيفية متقدّمة[24].
العلاقة مع التطبيقات الصناعية والبيئية
علم الأغذية والزراعة
يُطبَّق علم البروتيوم في الزراعة وصناعة الأغذية بهدف زيادة تحمّل النبات للضغوط اللاحقة، مثل الملوحة أو الجفاف بعد تعرّضه المسبق لمؤثّرٍ معيَّن. في الزراعة، تُستخدَم التحليلات البروتيومية، بما في ذلك بروتيومات الأكسدة والاختزال التي تتابِع التعديلات ما بعد الترجمة للبروتينات مثل
الكربلة {{الكربلة (carbonylation): هي عملية كيميائية تضيف مجموعة كربونيل (C=O) إلى جزيء حيوي أو كيميائي. في الأنسجة الحية، تُشير إلى الضرر التأكسدي غير القابل للانعكاس، الذي يؤدي إلى إضافة الكربونيل إلى البروتينات. كذلك فإنها عملية صناعية تسهم في إنتاج مواد كيميائية قَيّمة، مثل الأحماض أو الإسترات أو الألديهيدات.}} و النتروزلة {{النتروزلة (nitrosylation): عملية بيولوجية حيوية قابلة للانعكاس، حيث ترتبط مجموعة أكسيد النيتريك (NO) بمجموعة الثيول الموجودة على السيستئين في البروتين، ما يُشكِّل مسارَ إشارات رئيسًا يتحكّم في وظائف خلوية مثل التعبير الجيني، وإصلاح الحمض النووي، والاستجابة المناعية. يُنظِّم هذا التعديل الأساسي نشاط البروتين، وموقعه، واستقراره، ما يؤثر في كثير من العمليات الفيزيولوجية.}}، لفكّ شفرة الآليات الجزيئية التي تُعيد من خلالها عواملُ التهيئةِ الكيميائيةِ (مثل
بيروكسيد الهيدروجين (H2O2) أو المتبرّعين بأكسيد النيتريك (NO)) برمجةَ البروتيوم النباتي، ما يؤدّي إلى تكيُّفٍ فعّالٍ مع الإجهاد، وتحسين قوة النبات، فضلًا عن الكشف عن المؤشرات الحيوية المحتملة لزيادة قوة
البذور في محاصيل مثل البرسيم الحجازي وبنجر السكر، ما يضمن إنتاجيةً أفضل. أما في صناعة الأغذية، فيمتد دور البروتيوميات إلى مرحلة ما بعد الحصاد، إذ تُظهر الأبحاث أن بعض المعالجات مثل التعريض المطوّل للأوزون في أثناء التخزين البارد لثمار الكيوي على سبيل المثال، يمكن أن تعمل كعامل تهيئة
مضاد للأكسدة، ما يجعل الثمار أكثر قدرةً على تحمُّل مراحل الشيخوخة والنضج اللاحقة[25].
البروتوميات البيئية
يُعَدّ علم البروتيوميات، خصوصًا بروتيوميات
الأكسدة والاختزال (Redox proteomics)، أداةً اختيارية، لكنها متنامية بسرعة في
علم السموم البيئية، إذ تُستخدَم لفَهْم تأثيرات المُلوِّثات على المستويَيْن الخلوي والجزيئي، ما يساعد في التعرّف إلى المشكلات الناجمة عن المُلوِّثات البيئية ومعالجتها. تكشف بروتيومياتُ الأكسدةِ والاختزالِ البروتيناتِ المؤكسدةَ وتُحلِّلها ما بعد الترجمة، مثل كربلة البروتينات وأكسدة بقايا
الثيول {{الثيول (thiol): مركّب عضوي يحتوي على مجموعة السلفهيدريل (–SH) الوظيفية، ما يجعله النظير الكبريتي للكحول (R-OH).}}، وهي بمنزلة بصمات جزيئية محدّدة تَدُلّ على الضرر الناجم عن المُلوِّثات. يُوفّر هذا النهج رؤًى أساسيةً بشأن آليات السمّية، وهي معلومات غالبًا ما تعجز الدراسات الوبائية التقليدية عن كشفها (ما يُعرف بـ"الصندوق الأسود"). من خلال ذلك، يتمكّن الباحثون من:
- تحديد البروتينات المستهدفة بدقّة، مثل إنزيمات
التحلل الغلايكولي (Glycolysis)، وبروتينات الصدمة الحرارية (HSPs)، وروبيسكو (Rubisco).
- فَهْم أنماط السمّية الخاصة بالأنسجة وبنوْعِ المُلوِّث، مثل أنماط الكربلة في
محار البحر المعرّض لمركّب
ثنائي كلورو ثنائي فينيل ثنائي كلورو إيثيلين {{ثنائي كلورو ثنائي فينيل ثنائي كلورو الإيثيلين (Dichlorodiphenyldichloroethylene, DDE): مُركّب كيميائي ناتج من تحلّل مبيد الحشرات المحظور DDT، وهو قابل للذوبان في الدهون، ومعروف بثباته الشديد وقدرته على التراكم في الأنسجة الدهنية والتضخّم عبر السلاسل الغذائية، ما يُشكّل تهديدات خَطِرة للحياة البرية والإنسان.}}.
- تسهيل اكتشاف مؤشّرات حيوية حسّاسة للكشف المبكّر عن الإجهاد وتقييم جوْدة البيئة في الكائنات المتأثرة، وخصوصًا الأنواع الرصديّة مثل بلح البحر الأزرق، والمحار، والخميرة.
وبالكشف عن هذه العواقب الجزيئية وتحديد المؤشرات الحيوية، تُسهِم البروتيوميات في مواجهة تحدّيات التلّوث من خلال دعم الاختبارات الأكثر واقعيةً باستخدام المستحضرات التجارية، والمساعدة في
مراقبة الأثر البيئي، وتمكين تطبيق برامج الاستزراع المائي والزراعة المستدامة[26].
التحديات المستقبلية
من فهرسة البروتيوميات الكاملة إلى رسم خرائط التفاعلات والتعديلات البروتينية المعقدة، يُغيِّر علم البروتيوميات قدرة الباحثين على دراسة علم الأحياء على المستوى الوظيفي، وقد توسَّع نطاقه ليشمل مجالات تتجاوز البحث الطبي الحيوي، مُقدِّمًا حلولًا حاسمة في الزراعة، وسلامة الأغذية، ومراقبة البيئة، ما جعله ركيزة أساسية في علوم الحياة الحديثة والابتكار الصناعي على حدّ سواء. أما التحديات المستقبلية، فتتمثّل في الكشف عن البروتينات ذات الوفرة المنخفضة، وارتفاع تكلفة التقنيات والبنية التحتية اللازمة للتحليل، فضلًا عن الحاجة إلى دمج هذا الفرع من العلوم مع مجالات "الأوميكس" (Omics) الأخرى، لتحقيق فهْمٍ شامل ومتكامل للأنظمة البيولوجية.
المراجع
Ahram, Mamoun & Emanuel F. Petricoin. “Proteomics Discovery of Disease Biomarkers.”
Biomarker Insights. vol. 3 (2008). pp. 325-333.
Ahram, Mamoun. “An Introduction into Proteomics and Its Clinical Applications.” Saudi Medical Journal. vol. 28, no. 4 (2007). pp. 499-507.
Braconi, Daniela, Giulia Bernardini & Annalisa Santucci. “Linking protein oxidation to environmental pollutants: Redox proteomic approaches.” Journal of Proteomics. vol. 74, no. 11 (2011). pp.2324-2337.
Caron, Cécile, Cyril Boyault & Saadi Khochbin. “Regulatory Cross-Talk between Lysine Acetylation and Ubiquitination: Role in the Control of Protein Stability.” Bioessays. vol. 27, no. 4 (2005). pp. 408-415.
Chen, Guang et al. “Research Progress in Protein Microarrays: Focusing on Cancer Research.” Proteomics Clinical Applications. vol. 17, no. 1 (2023). art. e2200036.
Hondermarck, Hubert. “Breast Cancer: When Proteomics Challenges Biological Complexity.” Molecular & Cellular Proteomics. vol. 2, no. 5 (2003). pp. 281-291.
Lacoursiere, Rachel E., Dania Hadi & Gary S. Shaw. “Acetylation, Phosphorylation, Ubiquitination (Oh My!): Following Post-Translational Modifications on the Ubiquitin Road.” Biomolecules. vol. 12, no. 3 (2022). art. 467.
Li, Siting et al. “Applications of Protein Microarrays in Biomarker Discovery for Autoimmune Diseases.” Frontiers in Immunology. vol. 12 (2021). art. 645632.
Li, Yanqing, Runfang Zhang & Hu Hei. “Advances in Post-Translational Modifications of Proteins and Cancer Immunotherapy.”
Frontiers in Immunology. vol. 14 (2023).
Liebler, Daniel C. “Proteomic Approaches to Characterize Protein Modifications: New Tools to Study the Effects of Environmental Exposures.” Environmental Health Perspectives. vol. 110, suppl. 1 (2002). pp. 3-9.
Naik, Bindu et al. “Genomics, Proteomics, and Metabolomics Approaches to Improve Abiotic Stress Tolerance in Tomato Plant.” International Journal of Molecular Sciences. vol. 24, no. 3 (2023). art. 3025.
Orchard, Sandra et al. “Current Status of Proteomic Standards Development.” Expert Review of Proteomics. vol. 1, no. 2 (2004). pp. 179-183.
Tanou, Georgia, Vasileios Fotopoulos & Athanassios Molassiotis. “Priming against Environmental Challenges and Proteomics in Plants: Update and Agricultural Perspectives.” Frontiers in Plant Science. vol. 3 (2012). art. 216.
Wilkins, M. R. (ed.). Proteome Research: Concepts, Technology and Application. Berlin: Springer, 2007.
Wilkins, Marc R. et al. “Progress with Proteome Projects: Why All Proteins Expressed by a Genome Should Be Identified and How to Do It.” Biotechnology and Genetic Engineering Reviews. vol. 13, no. 1 (1996). pp. 19-50.
[1] Daniel C. Liebler, “Proteomic Approaches to Characterize Protein Modifications: New Tools to Study the Effects of Environmental Exposures,” Environmental Health Perspectives, vol. 110, suppl. 1 (2002), pp. 3-9.
[2] Marc R. Wilkins et al., “Progress with Proteome Projects: Why All Proteins Expressed by a Genome Should Be Identified and How to Do It,” Biotechnology and Genetic Engineering Reviews, vol. 13, no. 1 (1996), pp. 19-50.
[3] Nicolle H. Packer, Andrew A. Gooley & Marc R. Wilkins, “One Gene, Many Proteins,” in: M. R. Wilkins (ed.), Proteome Research: Concepts, Technology and Application (Berlin: Springer, 2007), pp. 95-121.
[4] Hubert Hondermarck, “Breast Cancer: When Proteomics Challenges Biological Complexity,” Molecular & Cellular Proteomics, vol. 2, no. 5 (2003), pp. 281-291.
[5] Sandra Orchard et al., “Current Status of Proteomic Standards Development,” Expert Review of Proteomics, vol. 1, no. 2 (2004), pp. 179-183.
[6] Liebler.
[7] Orchard et al.
[8] Wilkins et al.
[9] Mamoun Ahram, “An Introduction into Proteomics and Its Clinical Applications,” Saudi Medical Journal, vol. 28, no. 4 (2007), pp. 499-507; Mamoun Ahram & Emanuel F. Petricoin, “Proteomics Discovery of Disease Biomarkers,”
Biomarker Insights, vol. 3 (2008), pp. 325-333.
[10] Liebler.
[11] Yanqing Li, Runfang Zhang & Hu Hei, “Advances in Post-Translational Modifications of Proteins and Cancer Immunotherapy,”
Frontiers in Immunology, vol. 14 (2023), 1229397.
[12] Cécile Caron, Cyril Boyault & Saadi Khochbin, “Regulatory Cross-Talk between Lysine Acetylation and Ubiquitination: Role in the Control of Protein Stability,” Bioessays, vol. 27, no. 4 (2005), pp. 408-415; Rachel E. Lacoursiere, Dania Hadi & Gary S. Shaw, “Acetylation, Phosphorylation, Ubiquitination (Oh My!): Following Post-Translational Modifications on the Ubiquitin Road,” Biomolecules, vol. 12, no. 3 (2022), art. 467.
[13] Ibid.
[14] Bindu Naik et al., “Genomics, Proteomics, and Metabolomics Approaches to Improve Abiotic Stress Tolerance in Tomato Plant,” International Journal of Molecular Sciences, vol. 24, no. 3 (2023), art. 3025.
[15] Liebler.
[16] Ibid.
[17] Ahram.
[18] Liebler.
[19] Orchard et al.
[20] Liebler.
[21] Ibid.
[22] Guang Chen et al., “Research Progress in Protein Microarrays: Focusing on Cancer Research,” Proteomics Clinical Applications, vol. 17, no. 1 (2023), art. e2200036; Siting Li et al., “Applications of Protein Microarrays in Biomarker Discovery for Autoimmune Diseases,” Frontiers in Immunology, vol. 12 (2021), art. 645632.
[23] Ahram; Ahram & Petricoin.
[24] Orchard et al.
[25] Georgia Tanou, Vasileios Fotopoulos & Athanassios Molassiotis, “Priming against Environmental Challenges and Proteomics in Plants: Update and Agricultural Perspectives,” Frontiers in Plant Science, vol. 3 (2012), art. 216.
[26] Daniela Braconi, Giulia Bernardini & Annalisa Santucci, “Linking protein oxidation to environmental pollutants: Redox proteomic approaches,” Journal of Proteomics, vol. 74, no. 11 (2011), pp.2324-2337.