تنخر العظم، المعروف أيضًا بالنخر اللاوعائي أو النخر الإقفاري، حالة تنكسية تنتج عن فقدان الإمداد الدموي للعظام، ما يؤدي إلى موت الخلايا العظمية وفقدان تكامل النسيج العظمي.
يمكن أن يصيب التنخّر أي عظم في الجسم، لكنه أكثر شيوعًا في مفصل الورك، متبوعًا بالركبة والكتف والكعب، ومن أسبابه العوامل الرضيّة، مثل كسور عنق الفخذ أو خلع الورك، والعوامل غير الرضيّة، مثل الاستخدام طويل المدى للستيرويدات، والإفراط في شرب الكحول، واضطرابات الدم مثل فقر الدم المنجلي، وأمراض المناعة الذاتية.
تُشخّص حالة تنخّر العظم بالاعتماد على الفحص السريري، والتصوير بالأشعة التقليدية، والتصوير بالرنين المغناطيسي الذي يكشف التغيرات المبكرة في نسيج العظم. أما الخيارات العلاجية فمنها غير الدوائية، والتي تهدف للسيطرة على الألم وتحسين الوظيفة، ومنها الدوائية التي قد تساعد في تعديل مسار المرض وتأخير تقدمه، إضافة إلى العلاج الجراحي للحفاظ على المفصل أو استبداله في الحالات المتقدمة.
تعريفه
تنخر العظم (Osteonecrosis)، المعروف أيضًا بالنخر اللاوعائي (Avascular necrosis) أو النخر العقيم (Aseptic necrosis) أو نخر العظم الإقفاري (Ischemic necrosis of bone)، هو حالة تنكسية تصيب العظام نتيجة موت الخلايا العظمية بسبب انقطاع إمداد الدم إلى المنطقة المصابة. يؤدي هذا الانقطاع في تدفق الدم إلى تدهور العظم، وفي الحالات الشديدة يمكن أن يحدث انهيار في العظم تحت الغضروف أو انهيار كامل للمفصل، ما قد يؤدي إلى هشاشة العظم (Osteoporosis) وظهور التهاب متقدم في المفصل المصاب (الشكل 1)[1].
[الشكل 1]
 - مفصل الطبيعي ومفصل مصاب بالنخر العظمي -1.svg) مفصل الطبيعي ومفصل مصاب بالنخر العظمي
مفصل الطبيعي ومفصل مصاب بالنخر العظمي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يُعدّ تنخر العظم أكثر شيوعًا في مفصل الورك، إذ يصيب غالبًا رأس عظمة الفخذ، ويصيب أيضًا مفاصل الركبة، والكتف، والكاحل، ونادرًا يظهر في عظام أصغر مثل الرسغ، خاصة العظم الهلالي (Lunate bone)، أو الفك. وعادةً ما يُشخَّص المرض لدى الأشخاص الذين تتراوح أعمارهم بين 30 و65 عامًا، ويُلاحظ أن الرجال أكثر عرضةً للإصابة بشكل عام، في حين تكون النساء أكثر عرضةً لتنخر العظم المرتبط بأمراض المناعة الذاتية مثل الذئبة الحمراء (Systemic Lupus Erythematosus, SLE).[2]
أسبابه وعوامل خطورته
يُعتقد على نطاق واسع أن السبب الرئيس لتنخر العظم هو تقليل إمداد الدم إلى العظم تحت الغضروفي، إلا أن هناك العديد من العوامل والنظريات التي تفسّر تطور هذا الخلل الوعائي، وقد صنّف الباحثون هذه العوامل إلى ست مجموعات رئيسة، تشمل:
- السميّة الخلوية المباشرة الناتجة من التعرض للعلاج الكيميائي أو الإشعاعي، والإصابات الحرارية، والتدخين.
- إصابات الأوعية الدموية خارج العظم، وخلع مفصل الورك، وكسور عنق الفخذ، والأضرار الناتجة من العمليات الجراحية، أو التشوّهات الخلقية في الشرايين.
- المشاكل الوريدية، مثل: الاختلالات الوريدية أو ركود الدم، والضغط داخل العظم بما في ذلك النزيف، و زيادة الضغط داخل جوف نخاع العظم، والتسلل الدهني للنخاع الناتج من الاستخدام طويل الأمد وبجرعات عالية من الستيرويدات القشرية (Corticosteroids)، إضافةً إلى تضخم الخلايا وحدوث ارتشاح (تَسَلُّل) في نِخاع العظم (Marrow infiltration) كما في مرض غوشيه (Gaucher disease)، وتورم نخاع العظم أو الكسور المهشمة.
- انسداد الأوعية الدموية داخل العظم، مثل اضطرابات التخثر كما في حالة الثرومبوفيليا (Thrombophilia) أو نقص التحلل الليفي، وأزمات فقر الدم المنجلي {{فقر الدم المنجلي: (Sickle Cell Anemia) اضطراب وراثي للدم يسبب تشوّه خلايا الدم الحمراء لتصبح هلالية الشكل، هذه الخلايا غير طبيعية وتعيق تدفق الدم، ما يؤدي إلى نقص الأكسجين، وألم متكرر، ومضاعفات وعائية، وفقر دم مزمن يحتاج إلى متابعة طبية دقيقة.}}.
- الطفرات الجينية النادرة مثل الطفرة في جين COL2A1 المسؤول عن إنتاج الكولاجين من النوع الثاني {{الكولاجين من النوع الثاني: (Type II Collagen) بروتين أساسي يُشكّل الغضاريف والمفاصل، ويوفّر الهيكل والدعم للخلايا الغضروفية، ويرتبط نقصه أو تحلله بأمراض المفاصل التنكسية مثل الفصال العظمي، كما يُؤدي دورًا مهمًا في الحفاظ على مرونة وقوة الغضروف.}}، وهي حالات مجهولة السبب لدى نسبة كبيرة من المرضى[3].
- الصدمات المتكررة، كما في الأعمال الصناعية، التي تؤدي إلى تطور التنخر العظمي تدريجيًا، وتشمل العوامل غير الرضّية (Non-traumatic factors) وهي أي شيء قد يؤثر في تدفق الدم إلى العظم، مثل التعرّض للإشعاع الذي يسبّب تغيّرات في نخاع العظم، وارتفاع الدهون في الدم الذي يسدّ الأوعية الصغيرة ويقلّل الإمداد الغذائي للعظم.
يؤدي التشريح الخاص لبعض العظام دورًا إضافيًا في زيادة خطر التنخر العظمي، فالعظام ذات القدرة المحدودة على التعويض الوعائي أو ذات الدورة الدموية العكسية، مثل عظام الرسغ، معرضة أكثر للنخر، كما يُعدّ التشريح الفريد لعظم الكعب (Talus) عاملًا مهمًا، إذ يشغل الغضروف المفصلي مساحةً كبيرةً من سطحه، ما يحد من تدفق الدم. كما يمكن لاستخدام الستيرويدات القشرية بجرعات عالية ولمدة طويلة أن يسبب التنخر العظمي نتيجة لتحفيز موت الخلايا العظمية (Apoptosis)، الذي يؤدي إلى اضطراب نظام القنوات الدقيقة في العظم. وتُضاف إلى هذه العوامل الإفراط في تناول الكحول، واضطرابات الدم، والأمراض المناعية مثل الذئبة الحمراء. ومع ذلك، يظل سبب انقطاع تدفق الدم غير معروف لدى حوالي 25 في المئة من الأشخاص المصابين بالتنخر العظمي، كما هو الحال في أمراض كينبوك (Kienböck’s disease) و مرض بريزر (Preiser’s disease)، إذ يكون السبب غالبًا مجهولًا[4].
أعراضه
عادةً ما تظهر حالات تنخر العظم غير الناجم عن صدمات بألم ميكانيكي متفاوت في شدته ووقت ظهوره، وغالبًا ما يصعب تحديد موضعه بدقة[5].
[الشكل 2] - تنخر العظم في الورك
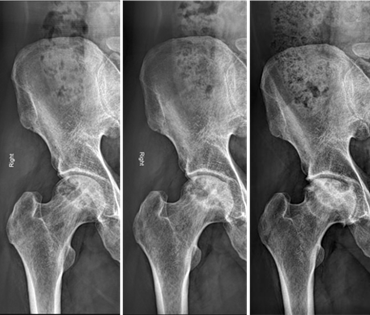 المصدر : https://acr.ps/1L9F2qN
المصدر : https://acr.ps/1L9F2qN
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
في حالة تنخر عظم في الورك، غالبًا ما تكون المراحل المبكرة من دون أعراض واضحة، ويُعدّ ألم الورك والفخذ من الأعراض الأكثر شيوعًا، ويشير عادةً إلى تقدم المرض إلى مراحل متأخرة. وقد تشمل الأعراض المصاحبة الألم المنتقل إلى الأرداف والفخذ، ويشكو معظم المرضى من الألم أثناء الراحة، إضافة إلى تيبّس وتغيّرات في طريقة المشي[6]. وفي بعض الحالات، يظهر الألم بصورة حادّة، خاصة أثناء الوقوف أو خلال الليل، وغالبًا ما يكون لدى المرضى تاريخ مرضي لهشاشة العظام أو انخفاض كثافة العظام من دون وجود إصابة حديثة. وعند إجراء الفحص السريري، يُلاحظ وجود ألم عند الضغط على اللقمة الفخذية الداخلية مع تراجع في مدى الحركة المفصلية[7] (الشكل 2).
غالبًا ما يكون تنخر العظم في الكتف، الذي يشمل الجزء العلوي من عظم العضد، مرتبطًا بالإصابة وتنخر العظم في مناطق أخرى من الجسم، إذ يتميز الألم بنبضه وانتشاره نحو المرفق، مع انخفاض في مدى الحركة النشطة للكتف[8].
غالبًا ما يرتبط تنخر عظم الكعب (Talus) بأمراض متعددة المفاصل والإصابات، إذ يشتكي المرضى من الألم وصعوبة المشي لفترة أطول ما هو متوقع بعد الحدث الصدمي[9].
أما تنخر العظم في العظام الصغيرة للمعصم، مثل العظم القمري (Lunate) وعظم الزورق (Scaphoid)، فيظهر غالبًا من دون تاريخ إصابة. وغالبًا ما يكون المرضى من العمال المهرة، ويشكون من ألم أحادي الجانب في الجهة الظهرية والشظوية للمعصم، مع انخفاض نطاق الحركة، وتورم المعصم، وضعف قوة القبضة[10].
تشخيصه
يشمل تشخيص التنخر العظمي استخدام مجموعة من الوسائل السريرية والشعاعية لتحديد وجود المرض ومرحلة تطوره، يبدأ التقييم عادةً بالفحص السريري المفصل والتاريخ المرضي، مع التركيز على عوامل الخطر المحتملة، مثل استخدام الستيرويدات، والأمراض المناعية، والصدمات السابقة، والإفراط في استهلاك الكحول. وغالبًا لا يكشف الفحص البدني وحده المرض في المراحل المبكرة، لذا يعتمد الأطباء على تقنيات التصوير لتأكيد التشخيص.
يُعدّ التصوير الشعاعي التقليدي (Conventional Radiography) الخطوة الأولى، ويشمل تصوير العظم من زاويتين متعامدتين على الأقل، إلا أن النتائج قد تبقى طبيعية في المراحل المبكرة للنخر. كما يُعدّ التصوير بالرنين المغناطيسي (Magnetic Resonance Imaging, MRI) الوسيلة الأكثر حساسية، إذ يمكنه كشف وذمة العظم والتغيّرات الدقيقة في نسيج العظم قبل ظهورها شعاعيًا. يظهر التنخر العظمي في التصوير بالرنين المغناطيسي (MRI) على صور T1 بوصفه منطقةً منخفضة الإشارة (Hypointense)، في حين يظهر على صور T2 بوصفه منطقةً مرتفعة الإشارة (Hyperintense)، مع ظهور خط مزدوج يميز النسيج المفرط الأوعية. وقد تُستخدم الأشعة المقطعية (Computed Tomography scan, CT Scan) لتقييم الانهيار تحت الغضروفي أو لتوضيح التفاصيل ثلاثية الأبعاد، لكنها أقل حساسية من الرنين المغناطيسي وتُعرض المريض للإشعاع. كما يُعدّ تصوير العظام بالنظائر المشعة (Bone Scintigraphy) أقل دقة ونادرًا ما يُستخدم[11].
لتحديد مرحلة المرض، تُستخدم تصنيفات مختلفة حسب العضو المصاب، وعادةً ما يُقيَّم نخر رأس عظم الفخذ (Hip Osteonecrosis) باستخدام أنظمة تصنيف تُحدِّد المراحل من البداية من دون تغيّرات شعاعية حتى الانهيار الكامل لرأس الفخذ وتضيّق مساحة المفصل. ومن هذه الأنظمة نظام فيكات (Ficat) وأريلِه (Arlet)، اللذان يعتمدان على الصور الشعاعية التقليدية (X-ray) والتغيّرات السريرية لتحديد النخر، ونظام ستاينبرغ (Steinberg) الذي يعتمد على الصور الشعاعية وأحيانًا الرنين المغناطيسي لتصنيف مراحل النخر بشكل أكثر تفصيلًا.
كما يُصنَّف نخر الركبة باستخدام تصنيف كوشينو {{تصنيف كوشينو: (Koshino Classification) نظام تصنيف يُستخدم لتقييم مراحل نخر عظمة اللوناتة (Kienböck disease) عبر الصور الشعاعية والرنين المغناطيسي، ويساعد الأطباء على تحديد مرحلة المرض، واختيار العلاج المناسب، ومتابعة تطور الحالة على مر الزمن.}} إلى أربع مراحل لتحديد مدى تطور المرض، بدءًا من تغيّرات شعاعية طفيفة حتى المرحلة التنكسية.[12] ويعتمد أيضًا نخر الكتف على تصنيف كروس {{تصنيف كروس: (Cruess classification) طريقة تصنيف طبي يُستخدم لتحديد مراحل نخر العظم اللاوعائي في الرسغ أو غيره من العظام، ويعتمد على التغيرات الشعاعية، والتجزؤ، والغضروف، ويُستخدم لتوجيه قرارات العلاج الجراحي أو المحافظة على الوظيفة العظمية.}} الذي يصنف إلى خمس مراحل. أما نخر عظم الكعبية (Talus Osteonecrosis) فيُصنَّف باستخدام مجموعة هوكينز (Hawkins Classification). وفي حالة نخر الزند أو داء كينبوك (Kienböck’s disease)، يُستخدم نظام ليشتمن (Lichtman classification) لتصنيفه. أما نخر العظم الزورقي أو داء بريزر (Preiser disease)، فيعتمد تصنيفه على نظام هربرت ولانزيت (Herbert and Lanzetta classification)[13].
علاج تنخر العظم
يهدف علاج تنخر العظم إلى تخفيف الألم، والحفاظ على وظيفة المفصل، وتأخير أو منع انهيار العظم، ويشمل ذلك علاجات غير دوائية، ودوائية، وجراحية حسب شدة المرض ومرحلة تقدم النخر.
العلاج غير الدوائي
يعتمد العلاج غير الدوائي على تقليل الحمل على المفصل المصاب وحماية العظم من الإجهاد المفرط، ففي حالات تنخر العظم في الورك، يُنصح المرضى بتعديل الأنشطة لتجنب الضغط الزائد على المفصل. أما في الركبة، وخصوصًا في حالة النخر العظمي التلقائي (Spontaneous Osteonecrosis of the Knee - SONK)، فيُوصى بحماية الركبة من الوزن الزائد، وممارسة العلاج الطبيعي لتقوية عضلة الفخذ الأمامية[14]. بالنسبة للكتف، يُعدّ تعديل الأنشطة لتجنب رفع الذراع فوق الرأس أو القيام بالأعمال اليدوية الثقيلة من أساسيات العلاج غير الجراحي. أما في حالات تنخر العظم الهلالي (Lunate Osteonecrosis) والعظم الزورقي (Preiser’s disease)، فيتضمن العلاج التثبيت والتحريك المحدود للمفصل، مع استخدام التثبيت الخارجي في بعض الحالات المبكرة لتقليل الضغط على العظم المصاب[15].
العلاج الدوائي
يُستخدم العلاج الدوائي لتخفيف الألم، وللحد من تقدّم النخر، وتأخير انهيار العظم، خصوصًا في المراحل المبكرة. ففي حالات نخر الورك، أظهرت بعض الدراسات فائدة البيسفوسفونات (Bisphosphonates) مثل الأليندرونات Alendronate))، سواء بوصفه علاجًا وحيدًا أو بالاشتراك مع أدوية أخرى. في المقابل للوقاية من انهيار رأس الفخذ وتأخير تقدم المرض، تساعد البيسفوسفونات على تقليل إعادة تشكيل العظم بعد النخر ومنع انهيار سطح المفصل، ما يقلل الحاجة إلى التدخل الجراحي. كما يوجد أيضًا أدوية مساعدة أخرى، مثل خافضات الدهون (Lipid-lowering agents)، ومضادات التخثر (Anticoagulants) التي تُستخدم أحيانًا للحد من تقدّم النخر، لكن فعاليتها محدودة نسبيًا[16].
العلاج الجراحي
يُعدّ العلاج الجراحي الخيار الأمثل في الحالات المتقدمة أو عند فشل التدخلات المحافظة. يشمل العلاج الجراحي في الورك، إزالة الضغط من العظم (Core Decompression) مع إمكانية استخدام ترقيع عظمي أو نخاع العظم، وجراحة قص العظم الدوراني (Rotational Osteotomy) لإبعاد الآفة عن سطح تحمُّل الوزن، وفي الحالات الأكثر تقدمًا أو مع انهيار كبير، يُستبدل الورك الكلي، في حين يُستعمل تثبيت المفصل (Arthrodesis) للشباب العاملين في أعمال شاقة[17].
في الركبة، يمكن استخدام إزالة الضغط من العظم أو نقل ترقيع عظمي للآفات الصغيرة، في حين تتطلب الآفات الأكبر استبدالًا جزئيًا أو كليًا للركبة، كما تُستخدم جراحة تصحيح محاذاة العظم (High Tibial Osteotomy) في حالات الخلل الهيكلي[18].
بالنسبة للكتف، يُوصى بإزالة الضغط من العظم في المراحل المبكرة، وإجراء إعادة تغطية رأس العضد أو نصف استبدال للكتف في المراحل المتوسطة، والاستبدال الكلي للكتف في المراحل المتقدمة. أما في عظم الكعبية (Talus)، فتُستخدم إعادة التثبيت التشريحي والتثبيت الجراحي بعد كسور عنق الكعبية للحدّ من خطر النخر[19].
أما في حالات تنخر العظم في العظم الهلالي (Lunate Osteonecrosis) وتنخر العظم في العظم الزورقي (Scaphoid Osteonecrosis)، فتهدف الجراحة المبكرة إلى إعادة التروية للعظم المصاب باستخدام ترقيع عظمي أو إجراءات لتقليل الضغط على العظم. أما في المراحل المتقدمة، فقد تتطلب العملية إصلاح انهيار العظم أو حتى إجراء تثبيت الرسغ أو استئصال الصف القريب للحفاظ على وظيفة المفصل وتقليل الألم[20].
المراجع
Agrawal, Kanhaiyalal, et al. “Nuclear Medicine Imaging in Osteonecrosis of Hip: Old and Current Concepts.” World Journal of Orthopedics. vol. 8, no. 10 (October 2017). pp. 747-753.
Allan, Christopher H., Atul Joshi & David M. Lichtman. Kienbock's Disease: Diagnosis and Treatment. Journal of the American Academy of Orthopaedic Surgeons. vol. 9, no. 2 (2001). pp. 128-136.
“Avascular Necrosis: When the Shoulder Humeral Head Suffers a Stroke.” Shoulder&Elbow. 19/9/2016. at: https://acr.ps/1L9F2gM
Franceschi, Francesco et al. Surgical Management of Osteonecrosis of The Humeral Head: A Systematic Review. Knee Surg Sports Traumatol Arthrosc. vol. 25, no. 10 (2017). pp. 3270-3278.
Jaheddin, Fadwa. “Osteonecrosis of the Lunate Bone.” Journal of Clinical Images and Medical Case Reports. vol. 5, no. 1 (2024).
Juréus, Jonas et al. “The Natural Course of Spontaneous Osteonecrosis of the Knee (SPONK): A 1- to 27-Year Follow-Up of 40 Patients.” Acta Orthopaedica. vol. 84, no. 4 (August 2013). pp. 410-414.
Karim, Abdul R. et al. “Osteonecrosis of the Knee: Review.” Annals of Translational Medicine. vol. 3, no. 1 (January 2015). pp. 1-11.
Lespasio, Michelle J, Nipun Sodhi & Michael A Mont. “Osteonecrosis of the Hip: A Primer.” The Permanente Journal. vol. 23, no. 1 (2019). pp.18-100.
Lin, James D. & Robert J. Strauch. “Preiser Disease.” Journal of Hand Surgery. vol. 38, no. 9 (September 2013). pp. 1833-1834.
Loppini, Mattia & Guido Grappiolo. “Osteonecrosis of the Femoral Head: Diagnosis and Management.” EFORT Open Reviews. vol. 3, no. 5 (2018). pp. 90-98.
Matthews, Alexander H. et al. “Avascular Necrosis.” in: StatPearls. Treasure Island, FL: StatPearls Publishing, 2025. at: https://acr.ps/1L9F2ci
Mohammad Taghi Niknejad. “Osteonecrosis of the femoral head - staging with follow-up x-rays.” Radiopaedia. at: https://acr.ps/1L9F2qN
Shah, Kalpit N et al. “Pathophysiology and Risk Factors for Osteonecrosis.” Curr Rev Musculoskelet Med. vol. 8, no. 3 (2015). pp. 201-209.
Sibilska, Aleksandra et al. “Spontaneous Osteonecrosis of The Knee: What Do We Know So Far? A Literature Review.” Int Orthop. vol. 44, no. 6 (2020). pp. 1063-1069.
Sultan, Assem A & Michael A Mont. “Core Decompression and Bone Grafting for Osteonecrosis of the Talus: A Critical Analysis of the Current Evidence.” Foot Ankle Clin. vol. 24, no. 1 (2019). pp. 107-112.
[1] Alexander H. Matthews et al., “Avascular Necrosis,” in: StatPearls (Treasure Island, FL: StatPearls Publishing, 2025), accessed on 2/2/2026, at: https://acr.ps/1L9F2ci; “Avascular Necrosis: When the Shoulder Humeral Head Suffers a Stroke,” Shoulder&Elbow, 19/9/2016, accessed on 2/2/2026, at: https://acr.ps/1L9F2gM
[2] Michelle J. Lespasio, Nipun Sodhi & Michael A. Mont, “Osteonecrosis of the Hip: A Primer,” The Permanente Journal, vol. 23, no. 1 (2019), pp.18-100.
[3] Kalpit N. Shah et al., “Pathophysiology and Risk Factors for Osteonecrosis,” Curr Rev Musculoskelet Med, vol. 8, no. 3 (2015), pp. 201-209; Matthews et al.
[4] Christopher H. Allan, Atul Joshi & David M. Lichtman, Kienbock's Disease: Diagnosis and Treatment, Journal of the American Academy of Orthopaedic Surgeons, vol. 9, no. 2 (2001), pp. 128-136.
[5] Lespasio, Sodhi & Mont.; Matthews et al.
[6] Lespasio, Sodhi & Mont.
[7] Aleksandra Sibilska et al., “Spontaneous Osteonecrosis of the Knee: What Do We Know So Far? A Literature Review,” Int Orthop, vol. 44, no. 6 (2020), pp. 1063-1069.
[8] Francesco Franceschi et al., Surgical Management of Osteonecrosis of the Humeral Head: A Systematic Review, Knee Surg Sports Traumatol Arthrosc, vol. 25, no. 10 (2017), pp. 3270-3278.
[9] Assem A Sultan & Michael A Mont, “Core Decompression and Bone Grafting for Osteonecrosis of the Talus: A Critical Analysis of the Current Evidence,” Foot Ankle Clin, vol. 24, no. 1 (2019), pp. 107-112.
[10] Allan, Joshi & Lichtman.
[11] Mohammad Taghi Niknejad, “Osteonecrosis of the femoral head - staging with follow-up x-rays,” Radiopaedia, accessed on 2/2/2026, at: https://acr.ps/1L9F2qN; Mattia Loppini & Guido Grappiolo, “Osteonecrosis of the Femoral Head: Diagnosis and Management,” EFORT Open Reviews, vol. 3, no. 5 (2018), pp. 90-98; Kanhaiyalal Agrawal et al., “Nuclear Medicine Imaging in Osteonecrosis of Hip: Old and Current Concepts,” World Journal of Orthopedics, vol. 8, no. 10 (October 2017), pp. 747-753.
[12] Allan, Joshi & Lichtman, op. cit.
[13] Shah et al., op. cit.; James D. Lin & Robert J. Strauch, “Preiser Disease,” Journal of Hand Surgery, vol. 38, no. 9 (September 2013), pp. 1833-1834.
[14] Abdul R. Karim et al., “Osteonecrosis of the Knee: Review,” Annals of Translational Medicine, vol. 3, no. 1 (January 2015), p. 6; Jonas Juréus et al., “The Natural Course of Spontaneous Osteonecrosis of the Knee (SPONK): A 1- to 27-Year Follow-Up of 40 Patients,” Acta Orthopaedica, vol. 84, no. 4 (August 2013), pp. 410-414.
[15] Fadwa Jaheddin, “Osteonecrosis of the Lunate Bone,” Journal of Clinical Images and Medical Case Reports, vol. 5, no. 1 (2024); Lin & Strauch.
[16] Matthews et al.
[17] Sultan & Mont; Lespasio, Sodhi & Mont.
[18] Karim et al.
[19] Franceschi et al., op. cit.; Sultan & Mont, op. cit.
[20] Allan, Joshi & Lichtman, op. cit.