سرطان القولون والمستقيم نوع من السرطانات يصيب القولون والمستقيم، ويُصنَّف وَفْقَ موقع الإصابة ومرحلة الانتشار. يُعَدّ هذا المرض من أكثر الأورام انتشارًا في العالم، إذ يحتل المركز الثالث من بين السرطانات عمومًا. تتمثل الإجراءات الوقائية التي تساعد في تقليل احتمالية الإصابة بسرطان القولون والمستقيم في إجراء فحوصات الكشف المبكر، والخضوع لإجراءات استباقية، مثل: العمليات الجراحية الموصى بها في حالات الخطر، واتّباع أنماط حياتية وغذائية صحية.
يحدث سرطان القولون والمستقيم بسبب طفرات جينية تُحفّز النمو غير الطبيعي لخلايا بطانة القولون أو المستقيم؛ ما يؤدي إلى تكوّن الأورام، ويصنف إلى خمس مراحل، تبدأ من المرحلة الصفرية وصولًا إلى المرحلة الرابعة، ويعتمد التصنيف على مدى تغلغل الورم، وانتشار الخلايا السرطانية إلى العقد اللمفاوية، ووجود نقائل سرطانية في الأعضاء البعيدة. قد لا تظهر أيّ أعراض على المرضى في بعض حالات، وفي حالات أخرى قد تظهر أعراض ناتجة من وجود الورم في جدار القولون أو الأعضاء المجاورة.
تعتمد الخطة العلاجية على مرحلة المرض عند التشخيص، والخصائص الجينية والبيولوجية للمرض، ونوع العلاج، والحالة العامة للمريض، وتشمل: الجراحة، والعلاج الكيميائي، والعلاج البيولوجي الموجه، والعلاج الشعاعي، والعلاج الجيني، والعلاجات التلطيفية. بعد انتهاء العلاج، يخضع المريض لبرنامج متابعة مكثّف للتأكد من استمرارية الشفاء واكتشاف أيّ انتكاسة أو عودة للمرض. وتقاس نسبة الشفاء بحساب نسبة المرضى الذين يتجاوزون خمسة أعوام بعد العلاج من دون وجود دلائل على وجود المرض في أي مكان من الجسم.
تعريف سرطان القولون والمستقيم
سرطان القولون والمستقيم (Colorectal cancer) نوعٌ من السرطانات يصيب
القولون أو
المستقيم، ويُصنَّف بناءً على موقع الإصابة، ومرحلة الانتشار، والعوامل الوراثية المرتبطة به. ووفقًا للمصادر الطبية الموثوقة، يُعدّ أول من وصف هذا الورم الطبيب العربي الأندلسي
ابن زهر (Ibn Zuhr ، 1162-1092) الذي مارس الطب خلال الحقبة العربية الإسلامية في الأندلس[1]. يُصنَّف سرطان القولون والمستقيم إلى خمس مراحل، تبدأ من المرحلة الصفرية وتنتهي بالمرحلة الرابعة.
الجهاز الهضمي السفلي
يتكون الجهاز الهضمي السفلي من
الأمعاء الدقيقة (Small intestine) والأمعاء الغليظة أو
القولون (Colon) والمستقيم (Rectum). يبدأ القولون من مكان اتصاله بالأمعاء الدقيقة، ويبلغ معدل طوله من 150 سنتيمترًا إلى 180 سنتيمترًا، وأجزاؤه هي:
الأعور (Cecum)، والصاعد (Ascending)، والمستعرض (Transverse)، والنازل (Descending)، والسيني (Sigmoid)، ويبلغ معدّل قطره 7 سنتيمترات في منطقة الأعور و2.5 سنتيمتر في منطقة القولون السيني (الشكل 1).
ينتهي القولون في مكان اتصاله بالمستقيم الذي يبلغ معدّل طوله من 12 سنتيمترًا إلى 15 سنتيمترًا، يتصل المستقيم في نهايته بفتحة الشرج (Anal canal)، وهي مكان خروج الفضلات أو
البراز (Stool)، وعضلتها أو العضلة
العاصرة الشرجية (Anal sphincter) التي تمكّن الإنسان من التحكّم بعملية الإخراج أو التغوّط[2].
وللقولون وظائف مهمة لجسم الإنسان، إذ يصله من الأمعاء الدقيقة ما يقارب لترًا ونصف لتر إلى لترين يوميًا من المواد الغذائية والسوائل والأملاح والفيتامينات وغيرها، فيمتص القولون معظمها تاركًا ما معدّله 128 غرامًا من البراز يوميًا. أما المستقيم فهو المكان الرئيس لتخزين الفضلات إلى حين التخلص منها، ومنه يبدأ الشعور بالرغبة في التخلّص من الفضلات ومن ثَمّ عملية التغوط.
يُعَدّ الجهاز الهضمي السفلي عرضة للعديد من الأمراض العضوية والوظيفية، لعل أكثرها خطورة على حياة الإنسان مرض سرطان القولون والمستقيم (Colorectal cancer).
[الشكل 1]
 القولون وأجزاؤه
القولون وأجزاؤه
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
انتشار سرطان القولون والمستقيم
يشكّل مرض سرطان القولون والمستقيم واحدًا من أكثر الأورام انتشارًا في العالم. تشير الإحصاءات العالمية إلى أنَّ سرطان القولون والمستقيم يحتل المركز الثالث من بين السرطانات عمومًا (10 في المئة من المجموع الكلي للسرطانات) من حيث الانتشار، إذ يسبقه
سرطان الرئة وسرطان الثدي، ويحتل المركز الثالث كذلك بوصفه مسبِّبًا للوفاة من بين السرطانات الأخرى. وفي العديد من دول المنطقة العربية وخصوصًا الشرقية منها مثل دول الخليج العربي، يحتل سرطان القولون والمستقيم المركز الأول في الذكور متبوعًا بسرطان الرئة، والمركز الثاني في الإناث مسبوقًا بسرطان الثدي.
تختلف نسبة انتشار مرض سرطان القولون والمستقيم من حيث الموقع الجغرافي والعرق اختلافًا كبيرًا، ففي الولايات المتحدة الأميركية مثلًا، يكون الأميركيون ذوو البشرة السوداء أكثر عرضة للإصابة من الأعراق الأخرى، وتبلغ هذه النسبة ما يقارب 4 حالات لكل 10 آلاف نسمة وإلى ما يزيد على 40 حالة لكل 100 ألف نسمة. ومن الملاحظات المسجّلة تاريخيًّا زيادة تلك النسبة كلّما ازداد المجتمع توجّهًا نحو حياة المدينة[3].
تزيد احتمالية إصابة الإنسان بسرطان القولون والمستقيم كلّما تقدّم في العمر، وتصبح هذه الزيادة أكثر حِدّة بعد سن الخمسين. كما أظهرت الدراسات الحديثة زيادةً مطّردة في نسبة الإصابة لدى صغار السن، وبزيادة سنوية تتراوح بين 1 و1.3 في المئة، ومن المتوقّع استمرار هذه الزيادة بنسبة تتجاوز 124 في المئة بحلول عام 2030 للفئة العمرية المتراوحة بين 20 و34 عامًا.
لقد كان لهذه النتائج أثرٌ في التوجّه نحو تحديد العمر المقترح لبدء عمليات التحرّي أو المسح للكشف المبكر (Screening programs) عن القولون والمستقيم وتقريبه إلى عمر الأربعين عامًا بدلًا من عمر الخمسين، إضافة إلى زيادة الاهتمام باحتمالية إصابة صغار العمر[4].
انخفضت معدّلات الوفاة الناتجة من سرطان القولون والمستقيم بما يقارب 50 في المئة عن ذروتها المسجّلة، ويُعزى ذلك إلى التشخيص المبكّر وتطوّر وسائل العلاج، إضافة إلى تقليل نسب الإصابة من خلال الإجراءات الاستباقية، مثل تشخيص
السلائل (Polyps) وإزالتها قبل تحوّلها إلى سرطان، وإلى عمليّات الاستئصال الاستباقية للقولون لدى مرضى الأمراض الوراثية والالتهابية المؤدّية إلى حدوث سرطان القولون والمستقيم.
عوامل خطر الإصابة بسرطان القولون والمستقيم
يؤدّي إلمام الطبيب وعامة الناس بالعوامل التي تزيد من احتمال الإصابة بسرطان القولون والمستقيم إلى زيادة كفاءة إجراءات تقليل الانتشار وارتفاع فرص الشفاء، ويتم ذلك من خلال اتخاذ الإجراءات الاستباقية لمنع وقوع الإصابة، خصوصًا إذا كانت تلك العوامل من النوع القابل للتعديل (Modifiable risk factors)، وكذلك زيادة الاهتمام بالأعراض الدالّة على وجود المرض؛ ما يؤدّي إلى التشخيص المبكر، إضافة إلى تحديد الفئة التي يجب زيادة الاهتمام بها في مجال التوعية وحملات التحرّي للكشف المبكر عن المرض. ومن أهم عوامل خطر الإصابة بسرطان القولون والمستقيم:
- العمر: تزيد احتمالية إصابة الإنسان بسرطان القولون والمستقيم كلما تقدّم في العمر، وخصوصًا بعد سن الخمسين، مع ضرورة التأكيد على أهمية الانتباه إلى إصابة صغار العمر أيضًا.
- السلائل الغُدّية[5] (Adenomatous polyps): من الجدير بالعلم أن الغالبية العظمى من حالات سرطان القولون والمستقيم تحدث نتيجة تطور السلائل. وتؤدّي وسائل التنظير الحديثة دورًا مهمًا في تشخيص هذه السلائل وإزالتها، ومن ثَمّ تقلل نسبة الإصابة بسرطان القولون والمستقيم (الشكل 2).
- التاريخ الشخصي والعائلي: يؤكد ذلك على دور العامل الوراثي في زيادة احتمالية الإصابة.
-
التهاب القولون التقرحي (Ulcerative colitis)، وخصوصًا
التهاب القولون الكامل (Pancolitis): إذ تزيد نسبة الإصابة بالسرطان بعد مرور عشرة أعوام على الإصابة بالتهاب القولون التقرحي، وبمعدل سنوي 1 في المئة تقريبًا. ويتطلب ذلك إجراءات استباقية، مثل: استئصال القولون والمستقيم، أو المتابعة بشكل مكثّف من خلال تنظير القولون والتدخل عند الحاجة. أما بالنسبة إلى الالتهاب من نوع
كرونز
(Crohn’s disease)، فخطورة تسببه بسرطان القولون والمستقيم قليلة بالمقارنة مع التهاب القولون الكامل. - داء السكّري: أظهرت العديد من الدراسات الحديثة زيادة ملحوظة للإصابة بسرطان القولون والمستقيم لدى مرضى داء السكري من النوع الثاني وغير المسيطر عليه، ويتميّزون بأنماط غذائية وحياتية معيّنة مثل الإكثار من تناول اللحوم الحمراء واللحوم المصنعة والمدخنة والدهون، والسمنة، والتدخين، وتناول الكحول، والخمول وقلة الحركة وعدم ممارسة الرياضة. كما بيّنت بعض تلك الدراسات التغيّرات الكيميائية والبيولوجية التي تسبّبها تلك الأنماط بوصفها مسببةً للسرطان، ما نقَلَ العلاقة بين تلك الأنماط وسرطان القولون والمستقيم إلى السببية (Cause effect relationship) وليس مجرد ترافق واقتران (Association).
- العلاج الشّعاعي السابق: إنّ تعرّض الجزء السفلي من البطن والحوض لعلاج شعاعي لسرطان آخر في السابق قد يزيد من احتمالية الإصابة بالسرطان وخصوصًا سرطان المستقيم.
-
النبيت الجرثومي المعوي (Gut microbiome): أظهرت بعض الدراسات الحديثة علاقة بين الإصابة بسرطان القولون والمستقيم وبين النبيت الجرثومي المعوي، وهي مجموعة الكائنات الدقيقة الموجودة والمستوطنة في القناة الهضمية، وتشمل أكثر من ألف نوع من البكتيريا، وتؤدّي دورًا مهمًا في عمل
الجهاز الهضمي، وتتعامل مع
البكتيريا الضارة، إضافة إلى دورها ضمن
الجهاز المناعي للجسم[6].
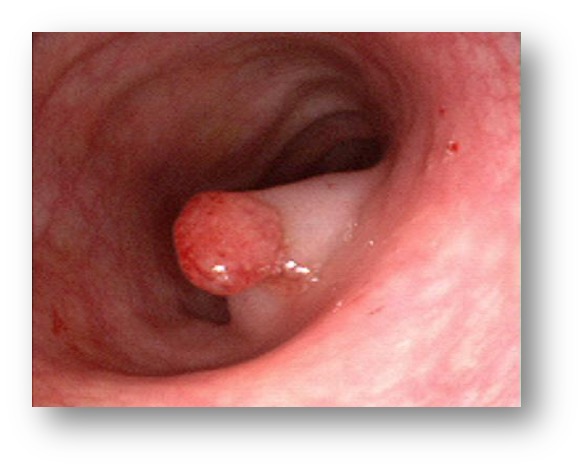 [الشكل 2] صورة داخلية للقولون مأخوذة بوساطة منظار القولون، تُظهر سليلة غدية
[الشكل 2] صورة داخلية للقولون مأخوذة بوساطة منظار القولون، تُظهر سليلة غدية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
آلية حدوث سرطان القولون والمستقيم
يحدث السرطان عمومًا، ومنه سرطان القولون والمستقيم، نتيجة
طفرات (Mutations) في التركيبة الجينية للمادة الوراثية للخلايا، أو نتيجة
التخلّق فوق الجيني (Epigenetic) في الأنماط الظاهرية الوراثية من دون وجود تغيير في تسلسل المادة الوراثية، ومن المعروف أنَّ حدوث التخلّق فوق الجيني يزداد بتقدم العمر (الشكل 3).
يتطلّب الانتقال من خلية غير سرطانية إلى خلية سرطانية حدوث عدد من هذه التغيرات، تؤدي إلى انتقال الخلية من المرحلة الطبيعية (Normal cell) إلى مرحلة خلل التنسج (Dysplasia) الظهاري (Epithelial)، أي الذي يحدث في الطبقة الظّهارية (Epithelial layer)، ثم يمر بمرحلة تكوين السليلة الغُدّية (Adenomatous polyp)، وتطوّر درجة التنسج من الخفيف (Mild) إلى المتوسط (Moderate) و من ثم الشديد (Sever)، ثُم مرحلة
السرطان اللابد أو الموضعي (Carcinoma in situ)، ثم السرطان (Carcinoma)، ثم النقيلة أو
الانبثاث (Metastasis).
يمكن أن تنتج هذه التغيرات من عوامل وراثية أو عوامل بيئية مكتسبة، ويمكن أن تحدث في العديد من المُوَرِّثات (Genes)، بعضها
مورّث كابت للورم (Tumor suppressor gene) مثل: APC، وSMAD4، وبعضها مورّث ورمي (Oncogene)، مثل: B-catenin، وCOX-2، وKRAS، وBRAF، وغيرها[7].
[الشكل 3]
 أنواع سرطان القولون والمستقيم من حيث الدور الوراثي
أنواع سرطان القولون والمستقيم من حيث الدور الوراثي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
الوراثة وأثرها في سرطان القولون والمستقيم
أظهرت الدراسات أنَّ نحو 20 في المئة من مرضى سرطان القولون والمستقيم لديهم تاريخ عائلي لهذا المرض، إلا أن الغالبية منهم لا يمتلكون نمطًا وراثيًا محدّدًا يتوافق مع أحد أنماط الوراثة المعروفة، مثل الاضطراب الصبغي الجسدي السائد (Autosomal dominant) أو المتنحّي (Autosomal recessive) أو المرتبط بالجين إكس (X-linked). في حين يعاني نحو 4 إلى 5 في المئة من هؤلاء المرضى من سرطان قولون المستقيم الموروث ويُسمّى سرطان القولون والمستقيم الوراثي غير السليلي (Hereditary nonpolyposis colorectal cancer, HNPCC)، ويعاني نحو 1 في المئة من
مرض متلازمة داء السلائل الورمي الغدي العائلي[8].
سرطان القولون والمستقيم الوراثي غير السليلي
يُطلق على سرطان القولون والمستقيم الوراثي غير السليلي أحيانًا
مرض لينش (Lynch syndrome) نسبةً إلى الطبيب الذي وصفه. ويمثل هذا المرض نحو 4 إلى 5 في المئة من حالات سرطان القولون والمستقيم.
يُتوارث هذا المرض عن طريق
الوراثة الجسدية السائدة (Autosomal dominant)؛ ما يعني أنّ 50 في المئة من أبناء الأم المصابة أو الأب المصاب سوف يحملون الخلل الجيني. ويحمل هذا الخلل قدرة على إحداث التأثير المرضي في الشخص الحامل للخلل الجيني (Penetrance) في حدود 75 إلى 80 في المئة.
وبما أنَّ الطفرة الجينية في هذا المرض تحدث في المورّثات المسؤولة عن ترميم وإصلاح المادة الوراثية (Mismatch repair genes) في حال حدوث عدم تطابقٍ خلال الانقسامات، فهذا يؤدّي إلى سهولة تقبّل خلايا الجسم لتكوين الطفرات المتلاحقة، ومن ثَمّ سهولة التحول من خلايا طبيعية إلى سرطانية وفي زمن أقل بكثير من
الأورام السرطانية المتفرقة (Sporadic cancers) .
يحتاج التحوّل من حالة السليلة الغُدّية إلى سرطان، في حالات السرطان المتفرق، إلى 15 عامًا تقريبًا، في حين تُختزل المدة في سرطان القولون والمستقيم الوراثي غير السليلي إلى حدود عامٍ واحد فقط. وبما أنَّ هذه الطفرة الجينية موجودة في جميع خلايا الجسم (القولون وغيره)، فإنَّ القابلية لتكوين سرطان لن تقتصر على القولون فقط، بل تشمل أعضاء أخرى.
نتيجة لذلك، إنَّ أهمية تشخيص هذا المرض تكمن في تأثيره المتوقَّع في نوع الفحوصات والعلاج والمتابعة للمريض، وكذلك البرنامج الأمثل للتحرّي عن المرض (Screening) لدى العائلة[9].
متلازمة داء السلائل الورمي الغُدّي العائلي
يُعد هذا المرض، واسمه بالإنكليزية (Familial adenomatous polyposis, FAP)، سببًا للإصابة بسرطان القولون والمستقيم بنسبة 1 في المئة. يُتوارث النوع الأشهر منه، وهو داء السلائل الغُدّية العائلي التقليدي (Classic FAP)، عن طريق الوراثة الجسدية السائدة (Autosomal dominant)؛ ما يعني أنّ 50 في المئة من أبناء الأم المصابة أو الأب المصاب سوف يحملون الخلل الجيني، ولكنَّ هذا المرض يحمل نفوذية شبه كاملة، أي أن 100 في المئة من حاملي هذه الطفرة سوف يعانون من الإصابة بسرطان القولون أو المستقيم. وفي المقابل هناك ما نسبته 25 إلى 30 في المئة من المرضى تتكون لديهم الطفرة المسببة للمرض من غير وراثة من أحد الوالدين، وتُعزى إلى عوامل خارجية. تقع الطفرة في هذا المرض في جين APC، وتتموضع هذه الطفرة على الذراع الطويل للكروموسوم الخامس ((5q21-q22 (الشكل 4).
يبدأ المصابون بهذا المرض في تكوين السلائل الغُدّية الحميدة (Adenomatous polyps) في العَقد الثاني من العمر، ويزداد عدد هذه السلائل وحجمها بمرور الوقت، وقد يصل عددها إلى المئات والآلاف، وبحلول نهاية العقد الرابع يعاني جميع المرضى تقريبًا من سرطان القولون. كما يتعرض هؤلاء المرضى لخطر الإصابة بأنواع أخرى من السرطانات، مثل:
سرطان المعدة وسرطان الأمعاء وسرطان البنكرياس وسرطان الغدة الدرقية والأورام الرباطية (Desmoid tumors)، وخصوصًا في منطقة البطن وغيرها بنسب متفاوتة، وكذلك التضخم الخلقي لظهارة الصبغ الشبكية Congenital retinal pigment epithelium hypertrophy, CHRPE)) وتشوهات الأسنان.
العلاج المتاح حاليًا لهذا المرض هو الاستئصال الكامل للقولون والمستقيم (Total proctocolectomy) وعمل المفاغرة اللفائفية الشرجية (Ileal pouch)، وهي جيب يُبنى من الأمعاء الدقيقة للمساعدة على تخزين البراز والإبقاء على الشرج، والبديل في حال عدم التمكّن من القيام بذلك هو تكوين فغرة (Stoma) دائمة من الأمعاء الدقيقة. تتوفر بعض الأدوية التي تساعد على التأثير في مسار تكوين السلائل وتطوّرها، ولكنها لا تكون بديلًا علاجيًا عن الجراحة.
هناك أنواع من داء السلائل الورمي الغدي أقل انتشارًا من داء السلائل الغُدّية العائلي التقليدي، ومن الأمثلة عليها[10]:
-
متلازمة داء السلائل الورمي الغُدّي العائلي المتنحي (Autosomal recessive familial adenomatous polyposis - ARFAP): يمتاز هذا المرض بأنَّ عدد الأبناء المصابين أقل لأن الوراثة متنحية، وعدد السلائل أقل، وكذلك حدّة المرض ونفاذيته.
-
متلازمة غاردنر (Gardner’s syndrome): يُتوارث عن طريق الوراثة الجسدية السائدة (Autosomal dominant)، ويزداد لدى هؤلاء المرضى خطرُ الإصابة بأورام العظام الحميدة وتكيسات الجلد الحميدة.
-
متلازمة توركوت (Turcot syndrome): ويزداد لدى هؤلاء المرضى خطر الإصابة بأورام الدماغ إضافة إلى سرطان القولون.
-
متلازمة السليلات اليفعي (Juvenile polyposis syndrome): وهو مرض نادر الحدوث، ينتج من طفرة تتموضع على موضع يختلف عن متلازمة داء السلائل الورمي الغدي العائلي، ويمتاز بظهور السلائل في سن مبكرة، وبعض أنواع أخرى في سن مبكرة جدًا.
 [الشكل 4] صورة بعد استئصال القولون لمريض مصاب بمتلازمة داء السلائل الورمي الغدي العائلي، تُظهر المئات من السلائل ذات الأحجام والأعمار المختلفة، إذ يُشير السهم إلى إحدى هذه السلائل بعد تحوّله إلى سرطان
[الشكل 4] صورة بعد استئصال القولون لمريض مصاب بمتلازمة داء السلائل الورمي الغدي العائلي، تُظهر المئات من السلائل ذات الأحجام والأعمار المختلفة، إذ يُشير السهم إلى إحدى هذه السلائل بعد تحوّله إلى سرطان
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
الأعراض الناتجة من سرطان القولون والمستقيم
يمكن تقسيم الأعراض الناتجة من سرطان القولون والمستقيم إلى خمسة أقسام رئيسة، فقد لا يكون هناك أعراض يلاحظها المريض، وهناك بعض الأعراض الناتجة من وجود الورم في جدار القولون وداخل تجويفه، والأعراض الناتجة من
ارتشاح الورم ونفاذه (Infiltration) في الأعضاء المجاورة، والأعراض الناتجة من النقيلة (Metastasis) أو الانبثاث أو هجرة الخلايا السرطانية إلى أعضاء بعيدة، وكذلك الأعراض العامة المصاحبة للأورام والناتجة منها[11] (24-26).
عدم وجود أعراض
يُكتَشَف المرض من خلال الفحوصات المسحية بوصفها جزءًا من إجراءات الكشف المبكّر عن سرطان القولون والمستقيم، سواء ضمن حملات عامة أو بشكل مخصص للمريض نظرًا إلى وجود عوامل خطر تزيد من احتمالية إصابته. وعلى الرغم من أن هذا النوع من التشخيص يشير في الغالب إلى أن المرض في مراحله المبكّرة، فإنه غالبًا ما يشكّل مفاجأة عندما يتبين أن المرض في مراحل متقدمة.
الأعراض الناتجة من وجود الورم في جدار القولون وداخل تجويفه
تتمثل أعراض وجود ورم في جدار القولون وداخل تجويفه في ما يأتي:
- تغير نمط التغوط وعادته، سواءً حدوث
الإمساك (Constipation) أو
الإسهال (Diarrhea) أو كليهما بالتناوب.
- تغيّر مواصفات البراز، سواءً من حيث القوام فيصبح أكثر صلابة أو أكثر رخاوةً أو كليهما بالتناوب، أو من حيث الشكل فيصغر قطر كتلة البراز أو يتفتّت إلى كتل صغيرة.
- وجود أعراض مصاحبة لعملية التبرز، مثل: الإلحاح الشديد (Urgency)، والحاجة للشد والدفع بقوة (Straining)، والشعور بعدم التفريغ الكامل للفضلات (Feeling of incomplete evacuation)، والشعور بالحاجة إلى الإخراج من دون نتيجة (التنسُّم، Tenesmus)، ووجود آلام في البطن والحوض خلال التبرز، وأحيانًا صعوبة في التحكم بالتبرّز (سلس البراز، Incontinence).
- وجود الدم وأحيانًا المخاط ضمن الفضلات. ومن المهم الإشارة إلى أن لون الدم لا يقتصر على اللون الأحمر الفاتح، فلربما كان غامقًا أو حتى أسود، ما قد يؤدي إلى تأخير في التشخيص.
- آلام البطن والشعور بالانتفاخ والضغط الداخلي في البطن وعدم الارتياح.
الأعراض الناتجة من ارتشاح الورم ونفاذه في الأعضاء المجاورة
تتفاوت هذه الأعراض حسب العضو المجاور المتأثر. ومن أبرز تلك الأعضاء المثانة البولية في حالات سرطان الجزء السفلي من القولون، إذ يعاني المريض من أعراض مشابهة للالتهابات البولية مثل كثرة التبول، والتقطيع، والحرقان، والألم، وربما النزف. وفي المراحل المتقدمة، قد يصاب المريض بخروج البراز والريح مع البول. كما يُعدّ المهبل من الأعضاء المتأثرة في حالات أورام المستقيم لدى الإناث، إذ تشكو المريضة من الإفرازات، وربما خروج البراز والريح من المهبل. من المهم التنبيه إلى أن هذه الأعراض قد تسبق في بعض الأحيان أعراض سرطان القولون والمستقيم، ما قد يؤدي إلى إرباك وتأخير في التشخيص.
هناك حالة خاصة من الانتشار أو الارتشاح، وهي الانتشار إلى داخل تجويف البطن إذ تلتصق الخلايا السرطانية بالغشاء المبطن لتجويف البطن أو الصفاق (Peritoneum)، ويعاني المريض في هذه الحالة من انتفاخ البطن الناتج من تجمع السوائل أو الاستسقاء البطني (Ascites)، وربما أدّى ذلك إلى الالتصاقات وانسداد الأمعاء (Adhesive intestinal obstruction).
الأعراض الناتجة من النقيلة أو الانبثاث (Metastasis)
ينجم عن ذلك انتقال الخلايا السرطانية إلى أعضاء بعيدة عبر الدم. ومن أكثر الأعضاء التي تستقبل الخلايا المهاجرة الكبدُ، والرئة، والدماغ، والعظام، والمبيض. وتعتمد الأعراض الناتجة من ذلك على الموقع المحدد للإصابة في العضو المستهدف ومدى انتشار الخلايا السرطانية فيه.
الأعراض العامة المصاحبة للأورام والناتجة منها
توجد أعراض عامة ترافق السرطانات بشكل عام، مثل: فقدان الشهية، وفقدان الوزن، وارتفاع درجة الحرارة، والتعرق. إضافة إلى ذلك، هناك أعراض ثانوية تنشأ نتيجة الأعراض الأساسية، وأهمها تلك التي تنتج من نزف الدم؛ ما يؤدي إلى فقر الدم (Anemia) الذي له أعراضه الخاصة، مثل: الشحوب، والدوخة أو الدوار، وضيق التنفس، وخفقان القلب خصوصًا بعد الإجهاد. قد تتداخل هذه الأعراض مع أعراض أمراض أخرى، ما يؤدي إلى تأخير في التشخيص. على سبيل المثال، قد يكون ضيق التنفس والخفقان ناتجَين من أمراض القلب أو الرئة، وقد يكون الدوار مرتبطًا بمشاكل في الجهاز العصبي، وهكذا.
الحالات الطارئة
قد يتسبب سرطان القولون والمستقيم في حدوث حالة طارئة تستدعي نقل المريض إلى قسم الطوارئ، وتتطلب تدخلات للإنعاش والإحياء(Resuscitation) ، وربما تدخلات جراحية عاجلة لإنقاذ الحياة وتصحيح المشكلة. ومن أبرز هذه الحالات انسداد القولون الكامل (Acute colonic obstruction)، وانثقاب القولون (Colonic perforation) ، وما يترتب عليه من التهاب في تجويف البطن وغشاء الصفاق (Peritonitis)، وفي حالات نادرة، النزف الحاد الشديد الذي يؤدي إلى الصدمة النزفية (Hemorrhagic shock). (الشكل 5، 6، 7).
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
سرطان قناة الشرج
لا بد من الإشارة إلى هذا النوع الخاص من السرطان، فقناة الشرج (Anal canal) عرضة لنوعين من السرطان، الأول في جزئها الأعلى الذي يُعدّ امتدادًا للمستقيم من حيث التكوين التشريحي وأصل التكوين، وبناء عليه يصيبه ما يصيب المستقيم من حيث نوع السرطان وعلاجه. أما الجزء الأسفل من قناة الشرج فيختلف من حيث أصل التكوين والخصائص التشريحية، ولذلك فإن السرطان الذي يصيبه من نوع سرطان الخلايا الحرشفية (Squamous cell carcinoma)، وكثيرًا ما تسبقه الإصابة بفيروس الورم الحليمي البشري (Human papilloma virus) على شكل
ثآليل (Warts)، ويعدّ الانتقال الجنسي أحد أسباب الإصابة بهذا الفيروس.
يعاني المصابون بهذا النوع من السرطان من ألم وحكة في منطقة الشرج والإحساس بوجود كتلة، والصعوبة في التغوط إضافة إلى النزف والإفرازات الشرجية[12].
 [الشكل 8] سرطان الجزء الأسفل من قناة الشرج
[الشكل 8] سرطان الجزء الأسفل من قناة الشرج
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
التشخيص والفحوصات الطبية
تنقسم الفحوصات الطبية المستخدمة في تشخيص سرطان القولون والمستقيم إلى أربعة محاور رئيسة، تشمل: تشخيص الورم وتحديد نوعه النسيجي، وتنظير القولون الكلّي، وتقييم مرحلة المرض، وتقييم الحالة العامة للمريض ومدى قدرته على تحمل الإجراءات العلاجية اللازمة[13].
تشخيص الورم وتحديد نوعه النسيجي (Pathological diagnosis)
تنتمي الغالبية العظمى من سرطانات القولون إلى النوع الغدّي (Adenocarcinoma)، ولكن في حالات نادرة قد يكون من نوع آخر؛ ما يتطلّب خطة علاجية مختلفة. لذلك، من الضروري إجراء تشخيص دقيق وإثبات نوع الورم نسيجيًا قبل البدء بالعلاج، إذ لا يجوز اتخاذ قرار العلاج بناءً على الشبهة أو المظهر السريري فقط، باستثناء الحالات الطارئة التي تستدعي التدخل الفوري لإنقاذ حياة المريض.
يُعد تنظير القولون (Colonoscopy) الوسيلة الأكثر فاعلية لتشخيص سرطان القولون، إذ يُتيح أخذ عيّنات للفحص النسيجي .(Histopathological examination) ويتم تنظير القولون عادة تحت
التنويم الواعي (Conscious sedation)، وذلك من خلال إدخال أنبوب مرن عبر فتحة الشرج وصولًا إلى القولون، مع إمكانية الولوج إلى الجزء النهائي من الأمعاء الدقيقة (الشكل 9).
يحتوي طرف الأنبوب على مصدر إضاءة وكاميرا تنقل الصور إلى شاشة حاسوبية، ما يسمح للطبيب بمراقبة الأنسجة الداخلية بدقة. كما يحتوي الأنبوب أيضًا على قناة داخلية تتيح إدخال
مسبار (Probe) لأخذ عيّنات من أيِّ منطقة يُشتبه في إصابتها، كما يمكن استخدامه لأغراض علاجية، مثل استئصال السلائل ووقف نزف القولون عبر حقن مواد قابضة، والكي بطرق مختلفة، أو إجراء الربط، ويمكن وضع دعامات في حالة انسداد القولون للحفاظ على مجرى لمرور الفضلات، إضافة إلى أن الفحوصات الجينية التي تُجرى على العيّنة قد توفر معلومات إضافية من شأنها أن تؤثر في الخطة العلاجية (الشكل 10).
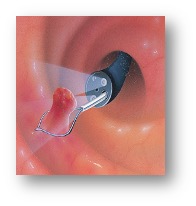 [الشكل 10] استئصال السلائل (Polypectomy) وبعض السرطانات في المرحلة الصفرية عن طريق منظار القولون قبل تطورها إلى مرحلة السرطان الكامل
[الشكل 10] استئصال السلائل (Polypectomy) وبعض السرطانات في المرحلة الصفرية عن طريق منظار القولون قبل تطورها إلى مرحلة السرطان الكامل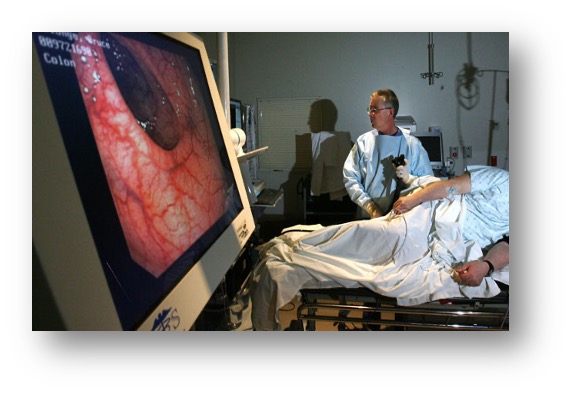 [الشكل 9] تنظير القولون
[الشكل 9] تنظير القولون
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يُعَدّ تصوير القولون الشعاعي الملون، الذي كان شائعًا في الماضي، من الفحوصات التي تُسهم في التشخيص لكنها لا توفر تأكيدًا نسيجيًا يُعتمد عليه لتوجيه العلاج. يُجرى هذا الفحص من خلال
حقنة الباريوم الشرجية للمغايرة المزدوجة (Double contrast barium enema)، إذ تُحقن مادة ملونة عبر قناة الشرج. وعلى الرغم من أن هذا الفحص قد يساعد في التشخيص الشعاعي، فإنه لا يوفر دقّة قاطعة ولا يتيح إمكانية الحصول على عينات نسيجية للفحص المجهري.
يوفّر تنظير القولون الافتراضي عبر التصوير المقطعي المحوسب (CT Colonography Virtual colonoscopy) تصويرًا للقولون من دون الحاجة إلى إدخال منظار عبر الشرج. ومع ذلك، لا يتيح هذا الفحص إمكانية الحصول على عيّنات نسيجية أو إجراء تدخلات علاجية كما في حالة تنظير القولون التقليدي.
أما فحص البراز للكشف عن
الدم الخفي (Occult blood) فهو فحص رخيص وسهل الإجراء، يكشف عن وجود دم في البراز غير مرئي بالعين المجردة، لكنه لا يتمتع بحساسية (Sensitivity) وخصوصية (Specificity) عالية، إذ يشير فقط إلى وجود دم في البراز، ولا يعني بالضرورة أن هذا الدم ناتج من السرطان. وفي الوقت نفسه، لا يعني عدم وجود دم أن المريض خالٍ من السرطان، فقد يكون هناك سرطان من دون أن يظهر دم خفي في الفحص.
بالنسبة إلى المستضد السرطاني المضغي (Carcinoembryonic antigen, CEA)، فهو فحص دم يُعد مؤشرًا ورميًا على وجود المرض (Tumor marker/ Indicator)، ويُستخدم بشكل رئيس لمتابعة تطور المرض بعد العلاج. إذا عاد المستوى إلى طبيعته، فهذا يُعَدّ دليلًا على نجاح العلاج، أما إذا ارتفع مستواه أثناء المتابعة، فقد يشير إلى تكرار المرض أو عودته (Tumor recurrence).
تنظير القولون الكلّي (Total colonoscopy)
في بعض الحالات يمكن الوصول للتشخيص وأخذ عيّنات بإجراءات أقل من التقييم الكامل وذلك عن طريق تنظير المستقيم (Proctoscopy)، أو التنظير السيني (Sigmoidoscopy) في حالات سرطان المستقيم أو أسفل القولون. ولكن حتى في مثل هذه الحالات لا بد من التنظير الكامل للقولون لاحتمالية وجود أورام أخرى متزامنة (Synchronous tumors) أو سلائل أو
التهاب القولون التقرحي أو غير ذلك.
تقييم مرحلة السرطان (Cancer stage assessment)
يهدف هذا التقييم إلى إجراء تحليل سريري وشعاعي للورم قبل بدء العلاج، نظرًا إلى تأثيره المباشر في الخطة العلاجية. ويختلف هذا التقييم عن تحديد مرحلة المرض نسيجيًا بعد الاستئصال، إذ تُفحص جميع الأنسجة المستأصلة.
تشمل الفحوصات المتاحة
التصوير المقطعي المحوسب ((Computed tomography, CT، ويُجرى غالبًا لمناطق الصدر والبطن والحوض، وأحيانًا لمناطق أخرى، إضافة إلى
التصوير بالرنين المغناطيسي (Magnetic resonance imaging)، خصوصًا الحوض في حالات سرطانات المستقيم، كما يستخدم التصوير المقطعي البوزيتروني (Positron emission tomography, PET)، وأحيانًا
التصوير النووي (Nuclear medicine imaging)، إلى جانب
التصوير بالأمواج فوق الصوتية (Ultrasound imaging)، ويمكن إضافة فحوصات أخرى حسب الحاجة.
صُنِّفَ سرطان القولون والمستقيم إلى خمس مراحل، تبدأ من المرحلة الصفرية (0) وصولًا إلى المرحلة الرابعة (IV)، إذ تزداد خطورة المرض تدريجيًا مع الانتقال من المرحلة الصفرية إلى المرحلة الرابعة. يعتمد هذا التصنيف على ثلاث خصائص رئيسة: مدى تغلغل الورم في جدار القولون والأعضاء المجاورة، وانتشار الخلايا السرطانية إلى
العقد اللمفاوية (Lymph nodes)، ووجود نقائل سرطانية في الأعضاء البعيدة. ولكل من هذه الخصائص درجات فرعية تحدد مدى تقدّم المرض.
في المرحلة الصفرية، يقتصر وجود الخلايا السرطانية على الغشاء المخاطي المبطن للقولون (Mucosa)، وفي المرحلة الأولى، تبدأ الخلايا باختراق جدار القولون، وفي المرحلة الثانية تخترق الخلايا الجدار بالكامل (Invasion)، وفي الثالثة تصل الخلايا إلى العقد اللمفاوية، وفي المرحلة الرابعة تنتشر إلى الأعضاء البعيدة (Metastasis).
يمكن تحديد المرحلة الأولية للمرض (المرحلة السريرية أو الشعاعية) قبل بدء العلاج أو الجراحة، وذلك بالاعتماد على الفحوصات السريرية والتصوير الشعاعي. أما المرحلة النهائية للمرض، فتُحدد بناءً على الفحص النسيجي المخبري بعد الاستئصال التام إنْ أُجْرِي. يساعد تصنيف المرض بهاتين الطريقتين في اختيار الخطة العلاجية المناسبة، كما يُستخدم للتنبّؤ بمآل المرض واحتمالات الشفاء أو متوسط العمر المتوقع للمريض.
تقييم الحالة العامة للمريض
نظرًا إلى أن الخطة العلاجية لمرضى سرطان القولون والمستقيم تتضمن الكثير من الإجراءات ذات التأثير الكبير على أعضاء جسم المريض المختلفة، فلا بد من تقييم حالة تلك الأعضاء، مثل:
قيمة خضاب الدم (Hemoglobin value)، ووظائف
القلب والرئة والكبد والكلى والدماغ قبل البدء بالعلاج، واتخاذ ما يلزم من الإجراءات الاستباقية لتحسين حالة تلك الأعضاء في حالة وجود اعتلالات، وتقليل احتمالية حصول مضاعفات لها.
الخطة العلاجية
يتميّز علاج مرضى سرطان القولون والمستقيم بالتفرد والتكيف مع كل حالة على حدة (Individualization)، إذ تُحدد الخطة العلاجية وفقًا لخصائص المرض الفردية، بما في ذلك موقع الورم، ومرحلته، والمواصفات النسيجية والجينية، والعمر البيولوجي للمريض، والأمراض المصاحبة، إضافةً إلى الإمكانات العلاجية المتاحة وعوامل أخرى.
تُبنى الخطة العلاجية على مزيج من الخيارات المتاحة التي قد تشمل الجراحة، والعلاج الكيميائي، والعلاج البيولوجي (الموجّه أو المستهدف)، والعلاج الشعاعي، والعلاج الجيني، إلى جانب العلاجات التلطيفية المختلفة، وذلك بما يتناسب مع حالة كل مريض لتحقيق أفضل النتائج العلاجية[14].
الجراحة
تُعَد الجراحة الطريقة الوحيدة للوصول إلى حالة الشفاء التام للمريض باستثناء حالات قليلة من سرطانات أسفل المستقيم. ومع ذلك، في العديد من الحالات تُعد الجراحة جزءًا من خطة علاجية متكاملة وتشمل وسائل علاجية أخرى.
يعتمد الإجراء الجراحي على عوامل متعددة، ومن أهمها موقع السرطان ومرحلته، والحالة العامة للمريض عند إجراء العملية وغيرها من العوامل. قد يتضمن العلاج الجراحي استئصال جزء من القولون، مثل: استئصال الجزء الأيمن (Right hemicolectomy)، أو استئصال الجزء الأيسر (Left hemicolectomy)، أو الجزء المستعرض (Transverse colectomy)، أو استئصال الجزء السيني (Sigmoid colectomy)، أو استئصال كامل القولون (Total colectomy)، وفي بعض حالات سرطان المستقيم، قد يُستأصل الجزء الأمامي (Anterior resection)، إذ يُستأصل المستقيم مع الحفاظ على قناة الشرج وعضلاتها، مع إجراء مفاغرة بين القولون والشرج .(Colo-anal anastomosis) أما في الحالات الأكثر تقدّمًا، فقد يتطلب الأمر استئصالًا بطنيًا عجانيًا (Abdominoperineal resection)، إذ يُستأصل المستقيم مع قناة الشرج.
 [الشكل 11] صورة تظهر فغرة من الأمعاء الدقيقة في جدار البطن
[الشكل 11] صورة تظهر فغرة من الأمعاء الدقيقة في جدار البطن
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
ويمكن إجراء الجراحة إما في مرحلة واحدة وإما على عدة مراحل (Staged). كما يمكن أن تتم الجراحة بالطريقة التقليدية عبر فتح البطن، أو من خلال
المنظار الجراحي (Laparoscopic)، أو باستخدام جهاز الروبوت (Robotic).
يمكن إجراء الجراحة إما في بداية العلاج (Upfront therapy)، وإمّا بعد تلقّي علاجات أخرى مثل العلاج الكيماوي أو الإشعاعي بوصفه علاجًا مبدئيًا مساعدًا (Neoadjuvant therapy). كما يمكن إجراء الجراحة أيضًا للمصابين بانتشار المرض إلى الكبد أو الرئتين أو الدماغ. وتهدف الجراحة إلى الشفاء التام (Curative therapy)، أو قد تكون تلطيفية (Palliative therapy) لتحسين جودة حياة المريض.
في بعض الحالات، قد يكون من الضروري إجراء فغرة (Stoma) (الشكل 11 ،12) وهي فتحة جانبية في جدار البطن لتصريف الفضلات بدلًا من فتحة الشرج. قد تكون الفغرة من الأمعاء الدقيقة (فغر اللفائفي) (Ileostomy) أو من الأمعاء الغليظة (Colostomy)، ويمكن أن تكون مؤقتة (Temporary) أو دائمة.(Permanent)
لا يُلجَأ إلى هذه الفغرات إلا في حالات الضرورة، نظرًا إلى أنها قد تؤثر بشكل كبير في نوعية حياة المريض ومن حوله. تشمل التأثيرات غير المرغوبة للفغرات: التأثيرات النفسية، ورعاية الفغرة من حيث تفريغ الفضلات، والتعامل مع الرائحة والنظافة الشخصية، إضافة إلى التهاب الجلد المحيط بالفغرة وتحسسه. كما تشمل المضاعفات المتعلقة بإنشاء الفتحة
نقص التروية (إقفار، (Ischemia، وتدلي المعي (Prolapse)، وحدوث فتق بجانب الفغر (Parastomal hernia)، إضافة إلى مضاعفات نقص السوائل والأملاح والعناصر الغذائية، خصوصًا في حالات فغرة الأمعاء الدقيقة، نتيجة فقدان كميات كبيرة من محتويات الأمعاء.
 [الشكل 12] مجموعة جهاز الفغرة: في اليسار صورة القاعدة، وفي اليمين صورة الكيس
[الشكل 12] مجموعة جهاز الفغرة: في اليسار صورة القاعدة، وفي اليمين صورة الكيس
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
العلاج الكيمائي (Chemotherapy)
العلاج الكيميائي هو استخدام أدوية لمعالجة الأورام السرطانية من خلال قدرتها على قتل الخلايا سريعة النمو في الجسم، بما في ذلك الخلايا السرطانية، إلا أنه قد يؤدّي أيضًا إلى قتل بعض الخلايا غير السرطانية التي تنمو بسرعة، مثل خلايا بطانة الجهاز الهضمي ونخاع العظم؛ ما يؤدي إلى أعراض جانبية تتراوح في شدّتها من طفيفة إلى شديدة.
يمكن استخدام العلاج الكيميائي بصفته علاجًا منفردًا أو علاجًا ضمن مجموعة من الأدوية. كما يمكن أن يُستخدَم علاجًا رئيسًا أو علاجًا مساعدًا بعد العمليات الجراحية (Adjuvant therapy) أو علاجًا مبدئيًا مساعدًا قبل الجراحة (Neoadjuvant therapy) لتقليص حجم السرطان وزيادة فرصة استئصاله بالكامل. إضافة إلى ذلك، يمكن استخدامه علاجًا تلطيفيًّا (Palliative therapy) لتقليص حجم الورم وتحسين الأعراض.
من أبرز الأعراض الجانبية للأدوية الكيميائية المستخدمة في علاج سرطان القولون والمستقيم: القيء، والغثيان، وفقدان الشهية، والحمّى، وتساقط الشعر، وتقرّحات الفم، وضعف المناعة، وزيادة القابلية للنزف، واعتلال الأعصاب خصوصًا في الأطراف، إضافة إلى أعراض أخرى.
العلاج الموجّه أو المستهدف (Targeted therapy)
تعالج هذه الأدوية السرطان من خلال التأثير في نمو الخلايا السرطانية وتكاثرها، وبالتحديد التأثير في جزيئات محدّدة لها علاقة بنمو تلك الخلايا، سواء كانت داخل الخلية أو على سطحها أو المحيطة بها مثل الأوعية الدموية؛ ما يقلل التأثير في الخلايا الطبيعية غير السرطانية، ومن ثَمّ التقليل من الآثار الجانبية.
يمكن أن تتكون هذه الأدوية من الأجسام المضادة أحادية النسيلة (Monoclonal antibodies) أو عقاقير ذات جزيئات صغيرة. ومن الأعراض الجانبية الشهيرة لهذه الأدوية المستخدمة في علاج سرطان القولون والمستقيم: الطفح الجلدي، واعتلالات وظيفة القلب والكبد والكلى، وارتفاع ضغط الدم وغيرها.
العلاج الشعاعي (Radiation therapy)
يتضمّن العلاج الشعاعي استخدام جرعات عالية من الإشعاع، مثل:
الأشعة السينية أو أشعة غاما أو الإلكترونات أو البروتونات لقتل الخلايا السرطانية أو تقليص حجمها.
يقتل العلاج الشعاعي الخلايا السرطانية عن طريق إتلاف الحمض النووي لها؛ ما يؤدّي إلى توقّفها عن الانقسام والنمو ومن ثَمّ موتها التدريجي. ومن المعروف أنّ العلاج الشعاعي يستغرق عدة أيام أو أسابيع لتحقيق تأثيره، كما يستمر تأثيره عدة أيام أو أسابيع بعد الانتهاء من العلاج.
يمكن استخدام العلاج الشعاعي بصفته علاجًا رئيسًا أو مساعدًا قبل العلاجات الأخرى أو أثناءَها أو بعدَها. كما يمكن استخدامه قبل الجراحة لتصغير حجم الورم؛ ما يسهّل استئصاله، أو بعد الجراحة لتنظيف منطقة العملية من الخلايا السرطانية وتقليل احتمالية عودة السرطان.
يُستخدَم هذا العلاج بشكل رئيس لعلاج أورام المستقيم، وخصوصًا الجزء السفلي منه، وفي بعض الحالات الخاصة يمكن أن يكون العلاج الشعاعي هو العلاج الرئيس لأورام أسفل المستقيم.
من أبرز الأعراض الجانبية لهذا العلاج: التعب العام، وتحسس الجلد، والإسهال، إضافة إلى أعراض التهاب المثانة والتهاب الأمعاء الإشعاعي.
العلاج التلطيفي (Palliative therapy)
يُلجَأ إلى هذا العلاج بعد استنفاد جميع وسائل الشفاء، أما مجالاته وأساليبه فمتعددة وتهدف إلى مساعدة المريض من الناحية النفسية وتخفيف الألم والتخلّص من الفضلات وغير ذلك.
متابعة ما بعد العلاج
بعد الانتهاء من العلاج، يخضع المريض لبرنامج متابعة مكثّف بهدف التأكّد من استمرارية الشفاء واكتشاف أي عودة أو انتكاسة للمرض (Tumor recurrence) في وقت مبكّر، سواء كانت الانتكاسة موضعية(Local recurrence) أو نقيلة (Metastasis)، ما يزيد من فرص نجاح العلاج. كما تُتابَع تأثيرات العلاج على جسم المريض واحتمالية الإصابة بسرطان جديد. تضع كلّ مؤسسة علاجية سياسة متابعة مرنة تتناسب مع حالة المريض. بشكل عام، يُنصح المريض بمراجعة دورية كل ثلاثة أشهر خلال العام الأوّل، وكل ثلاثة إلى ستة أشهر خلال العامَين التالِيَيْن، ثم كل ستة أشهر حتى العام الخامس.
خلال الزيارة، تُؤخذ سيرة مرضية كاملة، ويُجرى فحص سريري شامل، إضافة إلى فحوصات الدم الدورية. يُنصح أيضًا بإجراء تنظير للقولون بعد عام من العلاج، ثم كل ثلاثة أعوامٍ إلى خمسة. كما يخضع المريض لتصوير طبقي محوري للصدر والبطن والحوض كل ثلاثة أشهر إلى ستة أشهر خلال العام الأول، ثم سنويًا بعد ذلك. بالنسبة إلى مرضى سرطان المستقيم، فإنه يُجرى تصوير بالرنين المغناطيسي للحوض. قد يُعدَّل هذا البرنامج بناءً على تطورات الحالة الطبية أو المعطيات الجديدة.[15]
مآل المرض
عادة ما تُقاس نسبة الشفاء لمرضى سرطان القولون والمستقيم بحساب نسبة المرضى الذين يتجاوزون خمسة أعوام بعد العلاج من دون وجود دلائل على وجود المرض في أي مكان من الجسم. وتعتمد هذه النسبة على عوامل عديدة، أهمها: مرحلة المرض عند التشخيص، ووجود عوامل أخرى تتحكّم بمآل المرض، مثل: الخصائص الجينية والبيولوجية للمرض، ونوع العلاج، والحالة العامة للمريض وغيرها.
بناءً على ذلك، يمكن التنبّؤ بشفاء نحو 100 في المئة من مرضى المرحلة الصفرية، و90 في المئة من مرضى المرحلة الأولى، و70 إلى 80 في المئة من مرضى المرحلة الثانية، و30 إلى 50 في المئة من مرضى المرحلة الثالثة، وأقل من 20 في المئة من مرضى المرحلة الرابعة[16].
التثقيف والتوعية بسرطان القولون والمستقيم
اعتمدت منظمة الصحة العالمية شعارًا ذا لون أزرق للدّلالة على سرطان القولون والمستقيم، واعتمدت كذلك شهرًا خاصًّا للتثقيف والتعريف به، كما اختير الشهر الثالث من كل عام للتثقيف والتوعية به، فتكثر في هذا الشهر نشاطات الجمعيات العلمية والمستشفيات ووسائل الإعلام لهذه الغاية (الشكل 13).
[الشكل 13]
.svg) صورة تُظهر شعار مرض سرطان القولون والمستقيم بلونه الأزرق، وأخرى تُظهر إحدى النشرات الإعلانية للتوعية بسرطان القولون والمستقيم في الشهر الثالث من كل عام.
صورة تُظهر شعار مرض سرطان القولون والمستقيم بلونه الأزرق، وأخرى تُظهر إحدى النشرات الإعلانية للتوعية بسرطان القولون والمستقيم في الشهر الثالث من كل عام.
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
الإجراءات الوقائية
تتمثّل الإجراءات الوقائية التي تساعد في تقليل احتمالية الإصابة بسرطان القولون والمستقيم في التصدّي لعوامل الخطر من خلال عدة تدابير، ومن أبرزها: إجراء فحوصات التحرّي والكشف المبكر، مثل تنظير القولون، ابتداءً من سن الخمسين عامًا. أما في حال كان الشخص من ضمن الفئات عالية الخطر، فيُنصح بمواصلة المتابعة الطبيّة مع أطباء الاختصاص، مع تبكير فحوصات التحري إلى سن الأربعين أو أقل، حسب نوع الخطر. كما قد يتطلب الأمر الخضوع لإجراءات استباقية، مثل العمليات الجراحية الموصى بها في حالات الخطر، بناءً على نصائح الأطباء المختصين. ويُنصح أيضًا باتّباع أنماط حياتية وغذائية صحيّة تشمل زيادة تناول الألياف مثل تلك الموجودة في الخضار والفواكه والحبوب الكاملة، وتقليل تناول اللحوم الحمراء والدهون، إضافة إلى الإقلاع عن التدخين والكحول، وممارسة الرياضة بانتظام، والحفاظ على وزن صحي، والسيطرة على مرض السكري.
على الرغم من وجود بعض الأدلة التي تشير إلى أن أدوية مثل
الأسبرين (Aspirin) والسيليكوكسيب (Celecoxib) قد تقلل من خطر الإصابة بسرطان القولون، فإنّ الموازنة بين الفوائد والأعراض الجانبية لا تُوصي باستخدام هذه الأدوية لأغراض الوقاية. ومن المهم التعاطي بجدّيّة مع الأعراض التي قد تشير إلى الإصابة. وعلى الرغم من أن هذا لا يمنع الإصابة، فإنّه يُسهم في التشخيص المبكّر الذي ينعكس بشكل إيجابي على فرص الشفاء[17].
المراجع
Aarons, Cary B., Skandan Shanmugan & Joshua IS Bleier. “Management of Malignant Colon Polyps: Current Status and Controversies.”
World Journal of Gastroenterology. vol. 20, no. 43 (2014). pp. 16178-16183.
American Joint Committee on Cancer.
AJCC Cancer Staging Manual. Frederick L. Green et al. (eds.). 6th ed. New York: Springer, 2002.
Arya, Supreeta et al. “Imaging and Management of Rectal Cancer.”
Seminars in Ultrasound, CT and MRI. vol. 41, no. 2 (2020).
Azar, Henry A., Michael R. McVaugh & Joseph Shatzmiller. “Ibn Zuhr (Avenzoar)s Description of Verrucous Malignancy of the Colon.”
Canadian Bulletin of Medical History. vol. 19, no. 2 (2002). pp. 431-440.
Baidoun, Firas
et al. “Colorectal Cancer Epidemiology: Recent Trends and Impact on Outcomes.”
Current Drug Targets. vol. 22, no. 9 (2021). pp. 998-1009.
Benson, Al. B. et al. “Rectal Cancer, Version 2.2018, NCCN Clinical Practice Guidelines in Oncology.”
Journal of the National Comprehensive Cancer Network. vol. 16, no. 7 (2018). pp. 874-901.
________. Benson et al., “NCCN Guidelines Insights: Rectal Cancer, Version 6.2020,”
Journal of the National Comprehensive Cancer Network, vol. 18, no. 7 (2020).
Brosens, Lodewijk A. A. et al. “Risk of Colorectal Cancer in Juvenile Polyposis.”
Gut. vol. 56, no. 7 (2007), pp. 965-967.
Corman, Marvin L. (ed.).
Corman’s Colon and Rectal Surgery. 6th ed. Philadelphia: Wolters Kluwer, 2015.
Costas-Chavarri, Ainhoa et al. “Treatment of Patients with Early-Stage Colorectal Cancer: ASCO Resource-Stratified Guideline.”
Journal of Global Oncology. vol. 5 (2019).
Dekker, Evelien et al. “Update on the World Health Organization Criteria for Diagnosis of Serrated Polyposis Syndrome.”
Gastroenterology. vol. 158, no. 6 (2020). pp. 1520-1523.
DʼSouza, Nigel et al. “Definition of the Rectum: An International, Expert-based Delphi Consensus.”
Annals of Surgery. vol. 270, no. 6 (2019). pp. 955-959.
Gurjar, Shashank V. & Oliver M. Jones. “Physiology: Evacuation, Pelvic Floor and Continence Mechanisms.”
Surgery. vol. 29, no. 8 (2011), pp. 358-361.
Karamanou, Marianna et al. “Avenzoar's (1091-1162) Clinical Description of Cancer.”
JBUON. vol. 20, no. 4 (2015). pp. 1171-1174.
KhattabAhmed & Dulabh K. Monga. "Turcot Syndrome." [Updated 26 June 2023]
StatPearls [Internet] (January 2025). accessed on 21/5/2025, at:
https://acr.ps/1L9F38x
Ladabaum, Uri et al. “Strategies for Colorectal Cancer Screening.”
Gastroenterology. vol. 158, no. 2 (2020). pp. 418-432.
Laura et al. “Genetic Predisposition to Colorectal Cancer: Syndromes, Genes, Classification of Genetic Variants and Implications for Precision Medicine.” The
Journal of Pathology. vol. 247, no. 5 (2019). pp. 574-588.
Malki, Ahmed et al. “Molecular Mechanisms of Colon Cancer Progression and Metastasis: Recent Insights and Advancements.”
International Journal of Molecular Sciences. vol. 22, no. 1 (2020).
Song, Mingyang. “Global Epidemiology and Prevention of Colorectal Cancer,”
The Lancet Gastroenterology & Hepatology. vol. 7, no. 7 (2022). pp. 588-590.
Murphy, Caitlin C. & Timothy A. Zaki. “Changing Epidemiology of Colorectal Cancer - Birth Cohort Effects and Emerging Risk Factors.”
Nature Reviews Gastroenterology & Hepatology. vol. 21 (2024). pp. 25-34.
Murray, Christopher J. L. et al. “Global Burden of 87 Risk Factors in 204 Countries and Territories, 1990–2019: A systematic Analysis for the Global Burden of Disease Study 2019.”
Lancet. vol. 396, no. 10258 (2020). pp. 1223-1249.
Papamichael D. et al. “Treatment of Colorectal Cancer in Older Patients: International Society of Geriatric Oncology (SIOG) Consensus Recommendations 2013.”
Annals of Oncology. vol. 26, no. 3 (2015). pp. 463-476.
Peterse, Elisabeth F. P. et al. “The Impact of the Rising Colorectal Cancer Incidence in Young Adults on the Optimal Age to Start Screening: Microsimulation Analysis I to Inform the American Cancer Society Colorectal Cancer Screening Guideline.”
Cancer. vol. 124, no. 14 (2018). pp. 2964-2973.
Rose, C. et al. “The Characterization of Feces and Urine: A review of the Literature to Inform Advanced Treatment Technology.”
Critical Reviews in Environmental Science and Technology. vol. 45, no. 17 (2015). pp. 1827-1879.
Roshandel, Gholamreza, Fatemeh Ghasemi-Kebria & Reza Malekzadeh. “Colorectal Cancer: Epidemiology, Risk Factors, and Prevention.”
Cancers. vol. 16, no. 8 (2024).
Sawicki, Tomasz et al. “A Review of Colorectal Cancer in Terms of Epidemiology, Risk Factors, Development, Symptoms and Diagnosis.”
Cancers. vol. 13, no. 9 (2021).
Siegel, Rebecca L., Kimberly D. Miller & Ahmedin Jemal. “Cancer Statistics, 2020.”
CA: A Cancer Journal for Clinicians. vol. 70, no. 1 (2020). pp. 7-30.
Siegel,
Rebecca L.,Angela N. Giaquinto & Ahmedin Jemal.“Cancer statistics, 2024.”
CA: A Cancer Journal for Clinicians. vol. 74, no. 1 (2024). pp. 12-49.
Silviera, Matthew & Rebecca L. Hoffman. “Rectal Cancer Staging.”
Seminars in Colon and Rectal Surgery. vol. 30, no. 2 (2019). pp. 53-57.
Sinicrope, Frank A. “Lynch Syndrome-Associated Colorectal Cancer.”
The New England Journal of Medicine. vol. 379, no. 8 (2018). pp. 764-773.
________. “Increasing Incidence of Early-Onset Colorectal Cancer.”
The New England Journal of Medicine. vol. 386, no. 16 (2022). pp. 1547-1558.
Sung, Hyuna et al. “Colorectal Cancer Incidence Trends in Younger Versus Older Adults: An Analysis of Population-based Cancer Registry Data.”
The Lancet Oncology. vol. 26,
no. 1. pp. 51-63 (2025).
Sylla, Patricia, Andreas M. Kaiser & Daniel Popowich.
The SAGES Manual of Colorectal Surgery. Cham: Springer International Publishing 2020.
“Symptoms of Colorectal Cancer.”
CDC. 12/6/2024. accessed on 20/5/2025, at:
https://acr.ps/1L9F34u
Valle, Valle, Laura. “Update on Genetic Predisposition to Colorectal Cancer and Polyposis.”
Molecular Aspects of Medicine. vol. 69 (2019). pp. 10-26.
Yan, Lei, Jia Shi & Jiazuo Zhu. “Cellular and Molecular Events in Colorectal Cancer: Biological Mechanisms, Cell Death Pathways, Drug Resistance and Signaling Network Interactions.”
Discover Oncology. vol. 15, no. 1 (2024).
Yeo, Charles J. (ed.).
Shackelford's Surgery of the Alimentary Tract. vol. 2. 8th ed. Philadelphia, PA : Elsevier, 2019.
Zetner, Diana Bregner & Marie Luise Bisgaard. “Familial Colorectal Cancer Type X.”
Current Genomics. vol. 18, no. 4 (2017). pp. 341-359.
[1] Henry A. Azar, Michael R. McVaugh, Joseph Shatzmiller, “Ibn Zuhr (Avenzoar)s Description of Verrucous Malignancy of the Colon,”
Canadian Bulletin of Medical History. vol. 19, no. 2 (2002), pp. 431-440. Marianna Karamanou et al., “Avenzoar's (1091-1162) Clinical Description of Cancer,”
JBUON, vol. 20, no. 4 (2015), pp. 1171-1174.
[2] Nigel DʼSouza et al., “Definition of the Rectum: An International, Expert-based Delphi Consensus,”
Annals of Surgery, vol. 270, no. 6 (2019), pp. 955-959; C. Rose et al., “The Characterization of Feces and Urine: A review of the Literature to Inform Advanced Treatment Technology,”
Critical Reviews in Environmental Science and Technology, vol. 45, no. 17 (2015), pp. 1827-1879; Ana Garza & Robert W. Beart Jr., “Anatomy and Embryology of the Anus, Rectum, and Colon,” in: Marvin L. Corman (ed.),
Corman’s Colon and Rectal Surgery, 6th ed. (Philadelphia: Wolters Kluwer, 2015); Shashank V. Gurjar & Oliver M. Jones, “Physiology: Evacuation, Pelvic Floor and Continence Mechanisms,”
Surgery, vol. 29, no. 8 (2011), pp. 358-361.
[3] Rebecca L. Siegel, Kimberly D. Miller & Ahmedin Jemal, “Cancer Statistics, 2020,”
CA: A Cancer Journal for Clinicians, vol. 70, no. 1, pp. 7-30.; Firas Baidoun
et al., “Colorectal Cancer Epidemiology: Recent Trends and Impact on Outcomes,”
Current Drug Targets, vol. 22, no. 9 (2021), pp. 998-1009; Hyuna Sung et al., “Colorectal Cancer Incidence Trends in Younger Versus Older Adults: An Analysis of Population-based Cancer Registry Data,”
The Lancet Oncology, vol. 26,
no. 1, pp. 51-63 (2025); Christopher J. L. Murray et al. “Global Burden of 87 Risk Factors in 204 Countries and Territories, 1990–2019: A systematic Analysis for the Global Burden of Disease Study 2019,”
TheLancet, vol. 396, no. 10258 (2020), pp. 1223-1249;
Rebecca L. Siegel,Angela N. Giaquinto & Ahmedin Jemal, “Cancer statistics, 2024,”
CA: A Cancer Journal for Clinicians, vol. 74, no. 1 (2024), pp. 12-49.
[4] Frank A. Sinicrope, “Increasing Incidence of Early-Onset Colorectal Cancer,”
The New England Journal of Medicine, vol. 386, no. 16 (2022), pp. 1547-1558; Caitlin C. Murphy & Timothy A. Zaki, “Changing Epidemiology of Colorectal Cancer - Birth Cohort Effects and Emerging Risk Factors,”
Nature Reviews Gastroenterology & Hepatology, vol. 21 (2024), pp. 25-34.
[5] السلائل الغدية: وهي نمو غير طبيعي (أورام حميدة عادة) ينشأ من الغشاء المخاطي للقولون أو أجزاء أخرى من الجهاز الهضمي، وتُعد من الأنواع الشائعة للسلائل التي قد تتحول لاحقًا إلى سرطان القولون إذا لم تُزَل.
[6] Murphy & Zaki; Gholamreza Roshandel, Fatemeh Ghasemi-Kebria & Reza Malekzadeh, “Colorectal Cancer: Epidemiology, Risk Factors, and Prevention,”
Cancers, vol. 16, no. 8 (2024); Ahmed Malki et al., “Molecular Mechanisms of Colon Cancer Progression and Metastasis: Recent Insights and Advancements,”
International Journal of Molecular Sciences, vol. 22, no. 1 (2020); Lei Yan, Jia Shi & Jiazuo Zhu, “Cellular and Molecular Events in Colorectal Cancer: Biological Mechanisms, Cell Death Pathways, Drug Resistance and Signaling Network Interactions,”
Discover Oncology, vol. 15, no. 1 (2024).
[7] Yan, Shi & Zhu.
[8] Laura Valle et al., “Genetic Predisposition to Colorectal Cancer: Syndromes, Genes, Classification of Genetic Variants and Implications for Precision Medicine,”
The Journal of Pathology, vol. 247, no. 5 (2019). pp. 574-588; Frank A. Sinicrope, “Lynch Syndrome-Associated Colorectal Cancer,”
The New England Journal of Medicine, vol. 379, no. 8 (2018), pp. 764-773; Ahmed Khattab & Dulabh K. Monga, “Turcot Syndrome,” [Updated 26 June 2023] StatPearls [Internet] (January 2025), accessed on 21/5/2025, at:
https://acr.ps/1L9F38x ; Diana Bregner Zetner & Marie Luise Bisgaard, “Familial Colorectal Cancer Type X,”
Current Genomics, vol. 18, no. 4 (2017), pp. 341-359; Laura Valle, “Update on Genetic Predisposition to Colorectal Cancer and Polyposis,”
Molecular Aspects of Medicine, vol. 69 (2019). pp.10-26; Evelien Dekker et al., “Update on the World Health Organization Criteria for Diagnosis of Serrated Polyposis Syndrome,”
Gastroenterology, vol. 158, no. 6 (2020), pp. 1520-1523; Lodewijk A. A. Brosens et al., “Risk of Colorectal Cancer in Juvenile Polyposis,”
Gut, vol. 56, no. 7 (2007), pp. 965-967.
[9] Sinicrope; Khattab & Monga; Zetner & Bisgaard.
[10] Khattab & Monga; Valle; Dekker et al.; Brosens et al.
[11] Tomasz Sawicki et al., “A Review of Colorectal Cancer in Terms of Epidemiology, Risk Factors, Development, Symptoms and Diagnosis,”
Cancers, vol. 13, no. 9 (2021); “Symptoms of Colorectal Cancer,”
CDC, 12/6/2024, accessed on 20/5/2025, at:
https://acr.ps/1L9F34u ; Corman.
[12] Beatrice Pessia et al, “Squamous cell anal cancer: Management and therapeutic options,”
Annals of Medicine and Surgery, vol. 55 (2020), pp. 36-46.
[13] Corman; Al. B. Benson et al., “NCCN Guidelines Insights: Rectal Cancer, Version 6.2020,”
Journal of the National Comprehensive Cancer Network, vol. 18, no. 7 (2020); Al. B. Benson et al., “Rectal Cancer, Version 2.2018, NCCN Clinical Practice Guidelines in Oncology,”
Journal of the National Comprehensive Cancer Network, vol. 16, no. 7 (2018), pp. 874-901; American Joint Committee on Cancer,
AJCC Cancer Staging Manual, Frederick L. Green et al. (eds.), 6th ed. (New York: Springer, 2002); Papamichael D. et al., “Treatment of Colorectal Cancer in Older Patients: International Society of Geriatric Oncology (SIOG) Consensus Recommendations 2013,”
Annals of Oncology, vol. 26, no. 3 (2015), pp. 463-476; Emmanouil Pappou & Martin R. Weiser, “Principles of Rectal Cancer Management: Preoperative Staging, Neoadjuvant Treatment, Basic Principles of TME, and Adjuvant Treatment,” in: Patricia Sylla, Andreas M. Kaiser & Daniel Popowich,
The SAGES Manual of Colorectal Surgery (Cham: Springer International Publishing 2020), p. 331-351; Matthew Silviera & Rebecca L. Hoffman, “Rectal Cancer Staging,”
Seminars in Colon and Rectal Surgery, vol. 30, no. 2 (2019), pp. 53-57; Supreeta Arya et al., “Imaging and Management of Rectal Cancer,”
Seminars in Ultrasound, CT and MRI, vol. 41, no. 2 (2020).
[14] Arya; Cary B. Aarons, Skandan Shanmugan & Joshua IS. Bleier, “Management of Malignant Colon Polyps: Current Status and Controversies,”
World Journal of Gastroenterology, vol. 20, no. 43 (2014), pp. 16178-16183; Hisami Ando & Tadahiro Takada, “Basic Principles of the Operative Treatment of Colorectal Cancer,” in: Charles J. Yeo (ed.),
Shackelford's Surgery of the Alimentary Tract, vol. 2, 8th ed. (Philadelphia, PA : Elsevier, 2019), pp. 1981-1991; Ainhoa Costas-Chavarri et al., “Treatment of Patients with Early-Stage Colorectal Cancer: ASCO Resource-Stratified Guideline,”
Journal of Global Oncology, vol. 5 (2019).
[15] Arya et al.; Aarons, Shanmugan & Bleier; Ando & Takada; Costas-Chavarri et al.
[16] Corman; Benson et al.; Pappou & Weiser; Silviera & Hoffman; Arya et al.
[17] Uri Ladabaum et al., “Strategies for Colorectal Cancer Screening,”
Gastroenterology, vol. 158, no. 2 (2020), pp. 418-432; Roshandel, Ghasemi-Kebria & Malekzadeh; Elisabeth F. P. Peterse et al., “The Impact of the Rising Colorectal Cancer Incidence in Young Adults on the Optimal Age to Start Screening: Microsimulation Analysis I to Inform the American Cancer Society Colorectal Cancer Screening Guideline,”
Cancer, vol. 124, no. 14 (2018), pp. 2964-2973; Mingyang Song, “Global Epidemiology and Prevention of Colorectal Cancer,”
The Lancet Gastroenterology & Hepatology, vol. 7, no. 7 (2022), pp. 588-590.