أورام الأعصاب (Nerve tumors) هي أورام تنشأ في الحبل الشوكي، أو الأعصاب الطرفيّة، وتبدأ من الخلايا المحيطة بالأعصاب غالبًا، مما يسبّب خللًا في وظيفتها، ويؤدي إلى صداع، وآلام، وأعراض عصبية مختلفة. وتُقسم هذه الأورام إلى ثلاثة أنواع رئيسة: الورم الليفي العصبي، وورم شفان، وسرطان غمد العصب الطرفي. يبدأ تشخيص هذه الأورام بالفحص السريري، لكنه يؤكَّد باستخدام تقنيات التصوير، مثل: الرنين المغناطيسي (MRI)، والتصوير المقطعي (CT)، بالإضافة إلى فحوص مُتقدّمة، مثل: التصوير المقطعي بالإصدار البوزيتروني (PET)، وأخذ خزعات نسيجية لتحديد طبيعة الورم وإمكانات علاجه. في الغالب، لا تتطلب أورام الأعصاب الحميدة التي لا تسبّب أعراضًا علاجًا، وإنما تراقَب مراقبةً دورية، أما الأورام المصحوبة بأعراض أو تلك ذات الطبيعة السرطانية أو ما قبل السرطانية، فتُعالج بالاستئصال الجراحي غالبًا، وقد يتبع ذلك العلاج الإشعاعي حسب الحالة. ما تزال هذه الأورام محلَّ بحث طبّي مستمر، بهدف تطوير طرق العلاج، وتحسين فرص الوقاية منها في المستقبل.
تعريف أورام الأعصاب
أورام الأعصاب هي نموٌّ غير طبيعي في خلايا الجهاز العصبي (Nervous system)، وقد تكون حميدة أو خبيثة، وتنشأ من مكونات مختلفة للجهاز العصبي، مثل: الخلايا العصبية، أو الخلايا الدبقية، أو أغشية الدماغ والنخاع الشوكي، وقد تصيب الدماغ، أو الحبل الشوكي، أو الأعصاب الطرفية. تختلف أعراضها وخطورتها حسب نوع الورم وموقعه.
الجهاز العصبيّ
[الشكل 1]
 الجهاز العصبي
الجهاز العصبي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يعمل الجهاز العصبيّ (Nervous system) بالتعاون مع جهاز الغدد الصمّاء (Endocrine system) لتنظيم عمل الأجهزة الحيويّة المختلفة، ويُقسم الجهاز العصبيّ إلى قسمين: الجهاز العصبيّ المركزي (Central nervous system, CNS) الذي يعالج المعلومات ويرسل الأوامر، ويضمّ الدماغ (Brain)، والحبل الشوكي (Spinal cord)، والجهاز العصبيّ الطرفي (Peripheral nervous system, PNS) الذي ينقل الإشارات بين الجهاز العصبي المركزي وبقية الجسم، ويتكوّن من العقد العصبيّة (Ganglia)، والأعصاب الطرفيّة (Peripheral nerves)، والأعصاب القحفيّة (Cranial nerves)، باستثناء العصب الشمّي (العصب القحفي الأول، Olfactory nerve)، والعصب البصري (العصب القحفيّ الثاني، Optic nerve epithelia) اللذين يعدّان جزءًا من الجهاز العصبي المركزيّ. يعمل الجهاز العصبيّ الطرفي بوصفه امتدادًا طبيعيًّا للجهاز العصبيّ المركزي، ويُقسَم عمليًّا إلى قسمين رئيسين، هما: الجهاز العصبي الحسي (Sensory nervous system) الذي ينقل الإحساس، والجهاز العصبي الحركي الذي يتحكّم بالعضلات، ويُقسَم إلى قسمين، هما: الجهاز العصبي الجسماني (Somatic nervous system)، الذي يتحكّم الإنسان به تحكُّمًا واعيًا، والجهاز العصبي اللاإرادي ( Autonomic nervous system)، الذي يُدير العمليّات الحيويّة التي لا يتحكّم فيها الإنسان، مثل: نبض القلب، وعمليات التنفّس والهضم[1] (الشكل 1). ويعمل الجهاز العصبيّ اللاإرادي عبر ثلاثة مكوّنات فَرعيّة، هي: الجهاز العصبيّ الوديّ/ السمبثاويّ (Sympathetic nervous system)، والجهاز العصبيّ اللاودّي (parasympathetic Nervous system)، والجهاز العصبي المعوي (Enteric nervous system). تُغطّى معظم الأعصاب في الجهاز العصبي المركزي، والجهاز العصبي الطرفي بطبقةِ غلاف خارجيّة من مادة الميالين (Myelin) الدهنيّة وتسمّى غمد الميالين (Meylin sheath)، تُفرِزها خلايا مُختصّة تُعرف بالخلايا قليلة التغصُّن أو التشعّب (Oligodendrocytes) الموجودة في الجهاز العصبي المركزي، وخلايا أخرى تسمّى خلايا شفان (Schwann cells) موجودة في الجهاز العصبي الطرفي. وعلى الرّغم من أن الأعصاب ذاتها لا تُصاب بالسرطان، فإنّ الطبقات المحيطة بها قد تنمو نموًّا خارجًا عن السيطرة، مُسبِّبة ما يُعرَف بورم عصبيّ (Nerve tumor)، أو ورم الغمد العصبيّ (Nerve sheath tumor)[2].
أنواعها
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تُصيب أورام الأعصاب على نُدرتها الحبل الشوكيّ، والجهاز العصبيّ الطرفيّ. وتُقسَم حسب الأصل النسيجيّ للورم إلى ثلاثة أنواع رئيسة، منها اثنان حميدان، وورمٌ خبيث نادر كما في (الشكل 2).
الورم الليفيّ العصبي
يعد الورم الليفيّ العصبيّ (Neurofibroma) ورمًا حميدًا ينمو في أنواع مختلطة من الخلايا، كخلايا شفان (Schwann cells)، والخلايا المحيطة بالعصب (Perineural cells)، والخلايا الأروميّة الليفيّة (Fibroblasts)، كما تحوي الأورام الليفيّة العصبيّة خلايا بدنيّة (Mast cells)، أو تفرّعات محوريّة عصبيّة (Axonal processes)، وأنسجة خارج خلويّة كولاجينيّة (Collagenous extracellular matrix). تكون الأورام الليفيّة العصبيّة عادة جزءًا من مرض التورّم الليفيّ العصبيّ (Neurofibromatosis) الذي قد يظهر بسبب طفرة جينيّة، وفي بعض الأحيان لا يوجد سبب واضح لظهوره، كما لا تظهر على المرضى أيّ أعراض إذا كان حجم الورم صغيرًا، أمّا إذا كانت الأورام كبيرة ومعقّدة، فإنها تُسبّب آلامًا أو خدرًا في مكان الورم، أو على امتداد العصب المتورّم، وقد تتسبّب بأعراض داخليّة كفقدان الفعاليّة العصبيّة الحركيّة أو غيرها.
يوجد نوعان رئيسان لمرض الأورام الليفيّة العصبيّة، أوّلهما التورُّم الليفي العصبي من النوع الأول (Neurofibromatosis type 1)، أو مرض فون ريكلينغهاوزن (Von recklinghausen disease)، والتورم الليفيّ العصبيّ من النوع الثاني (Neurofibromatosis type 2).
[الشكل 3]
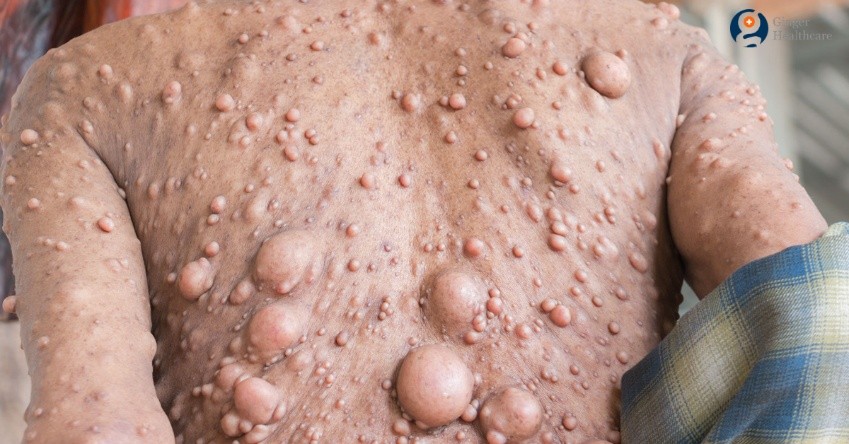 ورم ليفي عصبي من النوع الأول
ورم ليفي عصبي من النوع الأول
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يحدث التورّم الليفي العصبي من النوع الأول نتيجة طَفْرة وراثية جسدية سائدة (Autosomal dominant) في جين (NF1)، وهو جين مُثبّط للأورام ( Tumor suppressor gene)، تؤدي هذه الطفرة إلى فقدان وظيفة الجين، ما يُسهم في تكوّن الأورام الليفية العصبية (الشكل 3)، وعند الاشتباه بالإصابة بهذا المرض، قد تظهر على المرضى مجموعة من الأعراض الجلديّة وغير الجلديّة، منها: بقع القهوة المُبيَّضة (Café au lait spots)، والأورام الليفيّة العصبية (Neurofibromas)، ونمش في منطقة الإبط أو إرب الفخذ (Axillary or groin freckling)، وأورام دبقيّة بصريّة (Optic glioma)، وعقيدات ليش (Lisch nodules) في قَزَحيّة العين، وخلل في تنسّج العظمة الوتدية (Sphenoid bone dysplasia)[3].
في المقابل، يحدث الورم الليفيّ العصبيّ من النوع الثاني (Neurofibromatosis type 2) فينتج من طَفْرة في جين (NF2) تؤدي إلى تعطيله، ما يمنع إنتاج بروتين الميرلين(Merlin) المثبّط للأورام في الغشاء الخلوي. يُميّز هذا النوع غالبًا ظهورُ ورم شفاني دهليزي (Vestibular schwannoma) في إحدى الأذنين أو كلتيهما، ويُعدّ وجود الورم في الجانبين علامة تشخيصية مُميّزة لهذا المرض، وقد يعاني المرضى من أورام سحائية (Meningioma)، وأورام شفانيّة أخرى، إضافة إلى تغيُّرات في عدسة العين لدى الأطفال مثل عتامات عدسية تحت الكبسولة الخلفية (Juvenile posterior subcapsular lenticular opacities)، أو
الساد القشري ((Cortical cataract.
تتنوّع أشكال الورم الليفي العصبي، فقد يكون موضعيًا في منطقة واحدة، أو منتشرًا بعدد كبير من الأورام متفاوتة الحجم، أو ظاهرًا ظهورًا ضفيريًّا (Plexiform) معقّدًا يمتدّ في الجلد والأعضاء العميقة، وقد يسبّب أعراضًا عصبية. وعلى الرغم من أنّ هذه الأورام تكون حميدة غالبًا، فإنّ تحوُّلها إلى أورام خبيثة نادرُ الحدوث[4].
الورم الشفاني
ينمو الورم الشفاني (Schwannoma) كما يوحي اسمه في خلايا شفان (Schwann cells)، وهي خلايا تحيط بالعصب لحمايته وتوفير الدعامة له. وعندما تنمو هذه الخلايا أكثر من اللازم، ينشأ ما يُعرف بالورم الشفاني، أو ورم غمد الليف العصبيّ (Neurilemmoma)، وهو أكثر أورام الأعصاب الطرفيّة الحميدة انتشارًا، إلّا أنّ نسبةً ضئيلة منه قد تتطوّر إلى ورم سرطانيّ خبيث، ويُصنّفه بعض العلماء نوعًا من الأورام الليفيّة العصبيّة.
في العديد من الحالات، لا تظهر أعراض واضحة لدى مرضى الورم الشفاني، لكنّ بعضهم قد يعاني من ألم، أو ضعف عضلي، أو تنميل وخدر في المنطقة المصابة، وتميل هذه الأورام إلى أن تكون منفردة وبطيئة النمو، وغالبًا ما تظهر على شكل كتلة موضعية واحدة، ومع ذلك، وفي حالات نادرة، قد يتطور المرض إلى شكل أعقَد يُعرف بالتورّم الشفاني (Schwannomatosis)، وقد تنمو الأورام الشفانيّة أحيانًا بالقرب من جذع الدماغ (Brain stem) مُسبِّبة ما يُعرَف بورم العصب السمعي (Acoustic neuroma)، أو الورم الشفاني الدهليزيّ (Vestibular schwannoma) الذي يؤدي إلى مشاكلَ في التوازن والسَّمْع، ويُعدّ ظهور هذا الورم في كلتا الأذنين علامة مُميّزة لمرض الورم الليفي العصبي من النوع الثاني (Neurofibromatosis type 2). يمكن أن تصل هذه الأورام إلى أحجام كبيرة، وإذا لم تُعالج، قد تضغط على الأعصاب المجاورة، وحتى على جذع الدماغ نفسه، ما قد يُعطّل وظائفه الحيوية[5].
يُصنَّف الورم الشفاني إلى ثلاثة أنواع رئيسة تتضمّن: الورم الشفاني الجنبي (Pleural schwannoma)، وهو نوع شديد النُّدرة ينمو من دون وجود كبسولة نسيجيّة تحيط به، ما يجعله عرضة للتحوّل إلى ورم خبيث، والورم الشفاني الخلويّ (Cellular schwannoma)، الذي يُعد من الأنواع قليلة الشيوع، ويتميّز بكثافة خلوية مرتفعة مقارنة بالأنواع الأخرى، وسرطان غمد العصب الميلانيني (Malignant melanotic nerve sheath tumor)، وهو ورم عدواني يصيب أعصاب الجهاز العصبي الذاتي، سواء أكانت العصبية الشوكية أم الحشويّة[6].
ورم سرطان غمد الأعصاب الطرفيّة
[الشكل 4]
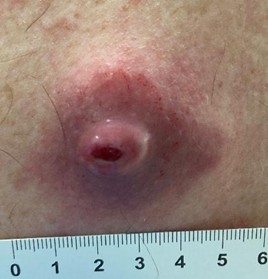 سرطان غمد الأعصاب الطرفيّة
سرطان غمد الأعصاب الطرفيّة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يعد ورم سرطان غمد الأعصاب الطرفيّة (Malignant peripheral nerve sheath tumor, MPNST) نوعًا من
سرطان الأنسجة الرخوة (Soft tissue sarcoma) وهو نوع نادر وسريع النُّموّ، وقد يظهر في أي جزء من الجسم، إلا أنه غالبًا ما يصيب الساقين أو الذراعين أو منطقة الحوض، ويتميز هذا الورم بمقاومته الشديدة للعلاج الكيميائي، ويُلاحظ بصورة أكبر لدى الشباب ومُتوسِّطي العمر، خاصةً لدى مرضى التورّم الليفي العصبي من النوع الأول، إذ إنّ احتمالية الإصابة به تتراوح بين 8 إلى 13 في المئة خلال حياة المريض. يبدأ الورم عادة من دون أعراض واضحة، ولكنّه ينمو بسرعة، ومع الوقت يبدأ المريض بالشعور بـألمٍ وضعف عضليَّينِ وظهور كتلة تحت الجلد، وقد تُصاحبه أعراض عصبية مثل التنميل، والخدران، والدُّوار، وغيرها[7](الشكل4).
تشخيص أورام الأعصاب
يعدّ التشخيص المبكر لأورام الأعصاب ضروريًّا لزيادة فرص نجاح العلاج، ولا سيما في حالات سرطان غمد الأعصاب الطرفية الذي يتطلّب علاجًا مُكثّفًا، إذ تزداد احتمالات الشفاء كلما بدأ التدخُّل العلاجي في وقت أبكر. يعتمد تشخيص هذه الأورام على الفحص السريري، إلى جانب التصوير بالرنين المغناطيسي (Magnetic resonance imaging, MRI)، وفي الحالات التي يصعب فيها التمييز بين الورم الليفي العصبي وسرطان غمد الأعصاب الطرفية، يمكن استخدام التصوير المقطعي بالإصدار البوزيتروني (Positron emission tomography, PET) لتعزيز دقّة التشخيص
[8].
ويستفيد الأطباء في تشخيص هذه الأورام من تقنيات أخرى، مثل: التصوير المقطعي المحوسب (Computerized tomography scan, CT scan)، أو
دراسات توصيل الأعصاب {{دراسات توصيل الأعصاب (Nerve conduction studies): قنية تشخيصيّة فسيولوجيّة كهربائيّة، تستخدم لقياس سرعة التوصيل الكهربائيّة وسعة الكمون في ألياف الأعصاب الحسيّة والحركيّة وتفيد في تشخيص الاعتلالات المحيطيّة العصبيّة أو انحشار الأعصاب واضطرابات الوصلات العصبيّة العضليّة. كما تساعد في تشخيص أمراض مثل متلازمة النفق الرسغي (Carpal Tunnel Syndrome) واعتلال السكري العصبي واعتلالات الأعصاب المناعيّة المزمنة}}، أو
التخطيط الكهربائي العضليّ (Electromyography)، وقد يلجأ الأطباء إلى أخذ خزعة (Biopsy) من الأنسجة أو الأعصاب، لفحصها مجهريًّا سواء أكان ذلك لتأكيد وجود الورم، أم لتحديد نوعه بدقة بهدف اختيار العلاج الأنسب
[9].
علاجه أورام الأعصاب
يعتمد علاج أورام الأعصاب على عواملَ عدة، من بينها نوعُ الورم، وشدّته، وموقعه، بالإضافة إلى الحالة الصحية العامة للمريض، واحتمالية تحوُّل الورم إلى صورته الخبيثة. وفي كثير من الحالات عامةً، لا تتطلب الأورام الليفية العصبية أو الأورام الشفانية علاجًا مباشرًا، خاصة إذا كانت صغيرة الحجم، ولا تُسبّب أعراضًا، بل يكتفي الأطباء بـالمُراقبة الدورية، والتصوير المُنتظَم لمتابعة تطوُّر الورم، أما في الحالات الأخرى، فيلجأ الأطباء إلى مجموعة من الخِيارات العلاجية للتعامل مع أورام الأعصاب، بحسب طبيعة الحالة، ومن الأمثلة عليها
[10]:
- الاستئصال الجراحيّ (Surgical resection): يُعد الاستئصال الجراحي من الوسائل الأساسية لعلاج الأورام العصبية المُسبّبة للأعراض، خاصة في حالات
الألم الجذريّ (Radicular pain) الشديد الذي ينتشر على طول الجلد حسب مسار العصب المصاب، كما تُستخدَم الجراحة في استئصال الأورام سريعة النمو أو السرطانية، وتحظى الأورام الليفيّة العصبيّة الضفيريّة (Plexiform neurofibromas) باهتمام خاصّ، نظرًا إلى احتمال تحوُّلها إلى أورام خبيثة، لذلك؛ يُعالَج كل مريض وفق خطّة علاجية فردية تشمل الاستئصال الجراحي غالبًا، ومع ذلك، تتوفّر أدوية حديثة للأطفال الذين يصعب إجراء الجراحة لهم؛ لتقليل حجم الورم، أو السيطرة على نموّه.
- العلاج الإشعاعي (Radiotherapy): إما بوصفه خِيارًا منفردًا، وإما بوصفه علاجًا تكميليًّا بعد استئصال الأورام الخبيثة، وتعد
تقنية العلاج الإشعاعي التجسيمي الموجه للجسم (Stereotactic body radiotherapy, SBRT) فاعلة بصورة خاصّة في استهداف الأورام الحميدة التي تنمو بالقرب من الدماغ أو الحبل الشوكي أو الأعصاب الطرفية، إذ توفّر دقّةً عالية في توجيه الأشعة مع تقليل الأضرار للأنسجة السليمة.
- العلاج الكيميائي (Chemotherapy): لا يعدّ العلاج الكيميائيّ ناجعًا في سرطان غمد الأعصاب الطرفية، إلّا أنّه يستخدم في الحالات التي يتعذّر فيها التدخل الجراحي، أو لدى المرضى الذين يعانون من أورام خبيثة عنيفة أو نقيلية.
- العلاج التأهيلي (Rehabilitation): يحتاج المرضى الذين تتأثّر لديهم الوظائف العصبيّة أو الحركية إلى علاج تأهيليّ؛ لإعادة تنشيط الأعصاب، والعضلات المتأثرة، وتقويتها لاستعادة وظيفتها، أو تحسين أدائها إلى أقرب مستوى طبيعي.
مآلاته المرضيّة
تُعدّ أورام الأعصاب الحميدة ذات مآلٍ جيد، ولا تُشكّل خطرًا على حياة المريض، أما سرطان غمد الأعصاب الطرفية، فيُعدّ حالة خطيرة تتطلّب علاجًا عاجلًا؛ نظرًا إلى سرعة نموّه، وقدرته على إتلاف الأنسجة المحيطة به، وغالبًا ما يخضع مرضى الورم الليفي العصبي للمتابعة الطبية المُستمرّة مدى الحياة من دون ظهور مضاعفات، خاصة إن كانت الأورام من النوع البسيط، لكن النوع الضفيريّ بالتحديد قد يتحوّل إلى ورم خبيث، مما يرفع من خطر تدهوُر الحالة
[11].
في المقابل، تعدّ أورام شفان أورامًا حميدة، وبطيئة النمو، ونادرًا ما ترجع بعد استئصالها، وتشير الأبحاث إلى أنّ معدل البقاء على قيد الحياة مدة عشرة أعوام لدى المصابين بها يقترب من 100 في المئة[12].
أما سرطان غمد الأعصاب الطرفيّة، فإن المآلَ عادة ما يكون سيئًا، إذ يتميّز هذا الورم بسرعة عودته بعد الاستئصال، وقد ينبَثُّ (Metastasis) إلى أماكنَ أخرى من الجسد. تتراوح نسبة النجاة لخمس سنوات بين 35 و50 في المئة في الحالات العفوية، وتنخفض إلى نسبة تتراوح بين 20 و30 في المئة عند وجود الورم ضمن النوع الأول من الورم الليفي العصبي[13]، وتتأثر احتمالات الشفاء في خمسةِ عواملَ رئيسة:
- ارتباطه بالورم الليفيّ العصبيّ من النوع الأول: يزداد خطر الوفاة عندما يكون السرطان جزءًا من متلازمة الورم الليفي العصبي.
- حجم الورم: ترتفع نِسَب الوفاة بين المرضى إذا تجاوز حجم الورم 5 سنتيمترات وقت اكتشافه.
- المستوى النسيجيّ المرتفع (High-stage histology): يُحدّد هذا المعيار مدى التلقائيّة والعشوائيّة في نمو الخلايا، وكلما ازداد مستوى الخلايا النسيجي، ازدادت درجة الاضطراب في بنية الخلايا السرطانية، وارتفعت قدرتها على النمو والانقسام العشوائي، ما يجعل الورم أكثر عدوانية.
- خلايا سرطانيّة على حوافِّ الاستئصال الجراحي: إذا لم يُزَل الورم إزالةً كاملة بسبب تشابُه الخلايا السرطانية مع السليمة على الأطراف، فإن خطر عودة الورم يزداد.
- الاستجابة للعلاج الكيميائيّ: يعد سرطان غمد الأعصاب الطرفيّة سرطانًا مُقاوِمًا للعلاج الكيميائي، إلّا أن نتائج العلاج به متفاوتة بين المرضى، ولكن تعرُّض المريض إلى علاج كيميائي، واستجابته استجابة ضعيفة، مؤشران على عنف السرطان وشدّته وسوء مآله[14].
المراجع
Behzad, Barzin & Saeed Dianat. “Magnetic Resonance Imaging of Nerve Tumors.”
Semin Musculoskelet Radiol. Vol. 26, no. 02 (2022), pp. 172–81.
Cai, Zhenyu, Xiaodong Tang, Haijie Liang, Rongli Yang, Taiqiang Yan, and Wei Guo. “Prognosis and Risk Factors for Malignant Peripheral Nerve Sheath Tumor: A Systematic Review and Meta-Analysis.”
World Journal of Surgical Oncology. vol. 18, no. 1 (2020).
Chengazi, Harris U., and Alok A. Bhatt. “Pathology of the Carotid Space.”
Insights into Imaging, vol. 10, no. 1 (2019).
Chowdhury, Ajmain et al. “Surgical Management of Craniospinal Axis Malignant Peripheral Nerve Sheath Tumors: A Single-Institution Experience and Literature Review.”
World Journal of Surgical Oncology. vol. 21, no. 1 (2023).
Donaldson, Elsa K. et al. “Malignant Peripheral Nerve Sheath Tumors of the Brachial Plexus: A Single-Center Experience on Diagnosis, Management, and Outcomes.”
Annals of Plastic Surgery. vol. 90, no. 4 (2023).
Evans, D. Gareth R., Susan M. Huson & Jillian M. Birch. “Malignant Peripheral Nerve Sheath Tumours in Inherited Disease.”
Clinical Sarcoma Research. vol. 2, no. 1 (2012).
Fisher, Michael J. et al. “Management of Neurofibromatosis Type 1–Associated Plexiform Neurofibromas.”.
Neuro-Oncology. vol. 24, no. 11 (2022), pp. 1827–1844.
Giannini, Caterina & Alberto Righi, “Peripheral Nerve Tumors.”
Handbook of Clinical Neurology. vol. 201 (2024), pp. 251-71.
Gui, Chloe et al. “Current State of Spinal Nerve Sheath Tumor Management and Future Advances.”
Neuro-Oncology Advances. vol. 6, suppl. 3 (2024), pp. iii83–iii93.
Hernández-Martín, A., and A. Duat-Rodríguez. “Neurofibromatosis Tipo 1: Más Que Manchas Café Con Leche, Efélides y Neurofibromas. Parte I. Actualización Sobre Los Criterios Dermatológicos Diagnósticos de La Enfermedad.”
Actas Dermo-Sifiliográficas. vol. 107, no. 6 (2016), pp. 454–464.
Le, Cuong, Aby Thomas & Forshing Lui, “Neurofibromatosis,” in:
StatPearls (Treasure Island, FL: StatPearls Publishing, 2025), accessed on 13/8/2025, at:
https://acr.ps/1L9F2VH
Messersmith, Lynn & Kevin Krauland, “Neurofibroma,” in:
StatPearls (Treasure Island, FL: StatPearls Publishing, 2025), accessed on 13/8/2025, at:
https://acr.ps/1L9F33f
Patestas, Maria Antoniou & Leslie P. Gartner.
A Textbook of Neuroanatomy. 2nd ed. Hoboken, NJ: Wiley Blackwell, 2016.
Porter, D. E. et al. “Survival in Malignant Peripheral Nerve Sheath Tumours: A Comparison between Sporadic and Neurofibromatosis Type 1–Associated Tumours.”
Sarcoma (2009): 756395.
“Schwannoma - NCI,”, National Cancer Institute, 30\07\2020, accessed on 4\2\2026, at:
https://acr.ps/1L9F2z3
Sheikh, Muhammad Mubbashir & Orlando De Jesus, “Vestibular Schwannoma,” in:
StatPearls (Treasure Island, FL: StatPearls Publishing, 2025), accessed on 13/8/2025, at:
https://acr.ps/1L9F2u3
Woehrer, A. et al. “Relative Survival of Patients with Non-Malignant Central Nervous System Tumours.”
British Journal of Cancer. Vol. 110, no. 2 (2014), pp. 286–296.
Zhou, Hai-Ying et al. “Peripheral Nerve Tumors of the Hand: Clinical Features, Diagnosis, and Treatment.”
World Journal of Clinical Cases. vol. 8, no. 21 (2020), pp. 5086–5098.
[1] Maria Antoniou Patestas & Leslie P. Gartner,
A Textbook of Neuroanatomy, 2nd ed. (Hoboken, New Jersey: Wiley Blackwell, 2016), pp. 3-9.
[2] Harris U Chengazi & Alok A. Bhatt, “Pathology of the Carotid Space,”
Insights into Imaging, vol. 10, no. 1 (2019).
[3] Lynn Messersmith & Kevin Krauland, “Neurofibroma,” in:
StatPearls (Treasure Island, FL: StatPearls Publishing, 2025), accessed on 13/8/2025, at:
https://acr.ps/1L9F33f; Cuong Le, Aby Thomas & Forshing Lui, “Neurofibromatosis,” in:
StatPearls (Treasure Island, FL: StatPearls Publishing, 2025), accessed on 13/8/2025, at:
https://acr.ps/1L9F2VH
[4] A Hernández-Martín and A Duat-Rodríguez, “Neurofibromatosis Tipo 1: Más Que Manchas Café Con Leche, Efélides y Neurofibromas. Parte I. Actualización Sobre Los Criterios Dermatológicos Diagnósticos de La Enfermedad,”
Actas Dermo-Sifiliográficas, vol. 107, no. 6 (2016), pp. 454-464.
[5] Muhammad Mubbashir Sheikh & Orlando De Jesus, “Vestibular Schwannoma,” in:
StatPearls (Treasure
[6]sland, FL: StatPearls Publishing, 2025), accessed on 13/8/2025, at:
https://acr.ps/1L9F2u3
Hai-Ying Zhou et al., “Peripheral Nerve Tumors of the Hand: Clinical Features, Diagnosis, and Treatment,”
World Journal of Clinical Cases, vol. 8, no. 21 (2020), pp. 5086–5098.
[7] D. Gareth R. Evans, Susan M Huson & Jillian M Birch, “Malignant Peripheral Nerve Sheath Tumours in Inherited Disease,”
Clinical Sarcoma Research, vol. 2, no. 1 (2012).
[8]Barzin Behzad & Saeed Dianat , “Magnetic Resonance Imaging of Nerve Tumors,”
Semin Musculoskelet Radiol, vol. 26, no. 02 (2022), pp. 172–81.
[9] Caterina Giannini & Alberto Righi, “Peripheral Nerve Tumors,”
Handbook of Clinical Neurology. vol. 201 (2024), pp. 251-71.
[10] Elsa K Donaldson et al., “Malignant Peripheral Nerve Sheath Tumors of the Brachial Plexus: A Single-Center Experience on Diagnosis, Management, and Outcomes,”
Annals of Plastic Surgery 90, no. 4 (2023); Michael J Fisher et al., “Management of Neurofibromatosis Type 1-Associated Plexiform Neurofibromas,”
Neuro-Oncology 24, no. 11 (November 1, 2022), pp. 1827–44; Ajmain Chowdhury et al., “Surgical Management of Craniospinal Axis Malignant Peripheral Nerve Sheath Tumors: A Single-Institution Experience and Literature Review,”
World Journal of Surgical Oncology, vol. 21, no. 1 (2023), p 338.
[11] “Schwannoma - NCI,”, National Cancer Institute, 30\07\2020, accessed on 4\2\2026, at: https://acr.ps/1L9F2z3; Zhenyu Cai et al., “Prognosis and Risk Factors for Malignant Peripheral Nerve Sheath Tumor: A Systematic Review and Meta-Analysis,”
World Journal of Surgical Oncology, vol. 18, no. 1 (2020), p. 257.
[12] A Woehrer et al., “Relative Survival of Patients with Non-Malignant Central Nervous System Tumours: A Descriptive Study by the Austrian Brain Tumour Registry,”
British Journal of Cancer, vol. 110, no. 2 (2014), pp. 286–96.
[13] D E Porter et al., “Survival in Malignant Peripheral Nerve Sheath Tumours: A Comparison between Sporadic and Neurofibromatosis Type 1-Associated Tumours,”
Sarcoma, 7\04\2009, accessed on 4\02\2026. at: https://acr.ps/1L9F2oF.
[14]Chloe Gui et al., “Current State of Spinal Nerve Sheath Tumor Management and Future Advances,”
Neuro-Oncology Advances, vol. 6, no. supl. 3 (2024), pp. iii83-iii93.