النواتج الطبيعية (Natural products) هي مواد ينتجها الكائن الحي، وتنتمي إلى عائلة كبيرة من المركّبات الكيميائية المتنوّعة التي تمتاز بمجموعة واسعة من الأنشطة البيولوجية التي لها استخدامات طبية متعددة، خصوصًا في الطب البشري والطب البيطري والزراعة، إذ تُعدّ مصدر إلهام لصناعة
الأدوية. تُقسّم النواتج الطبيعية إلى فئتين رئيسَتين؛ المُسْتَقْلَبات الأوّلية وهي جزيئات عضوية لها وظائف ضرورية لبقاء الكائن الحي الذي يُنتجها، والمُسْتَقْلَبات الثانوية التي تُعتبر غير ضرورية للبقاء، ولكنها تزيد من القدرة التنافسية للكائن الحي داخل بيئته. يمكن تصنيف النواتج الطبيعية وفقًا لوظائفها البيولوجية أو مساراتها الحيوية أو مصادرها. تتنوع مصادر النواتج الطبيعية؛ إذ يمكن استخلاصها من الخلايا والأنسجة وإفرازات الكائنات الحية الدقيقة والنباتات والحيوانات. غالبًا ما تكون النواتج الطبيعية على شكل مخاليط معقّدة للغاية، ويجب فصلها وتنقيتها، ومن الطرق المستخدمة في فصل تلك النواتج
التقطيرُ وتقنيات
الكروماتوغرافيا المختلفة والمذيبات الكلاسيكية وغيرها.
تصنيفات النواتج الطبيعية
تُعرّف المنتجات الطبيعية أو النواتج الطبيعية بأنها المواد التي تُنتجها الحياة، وتشمل المواد الحيوية، مثل: الخشب، والحرير، وغيرها من المواد الطبيعية. أما التعريف الأكثر تحديدًا للمنتج الطبيعي فهو أيُّ مركّب عضوي يُصنّعه كائنٌ حي. تعودُ أصول علم
الكيمياء العضوية (Organic chemistry) إلى دراسة النواتج الطبيعية، وقد أدّى إلى ظهور مجالات
الكيمياء العضوية الصناعية {{الكيمياء العضوية الصناعية: فرع من فروع الكيمياء، يركز على إنتاج المركبات الكيميائية العضوية على نطاق واسع في المصانع. تختلف عن الكيمياء العضوية الأساسية التي تركز على دراسة المركبات العضوية في المختبر. وتستخدم هذه الصناعة عمليات كيميائية معقدة لتحويل المواد الخام الأولية، مثل النفط، إلى منتجات نهائية لها قيمة اقتصادية وعملية في الحياة اليومية.}}، إذ يُحضِّر العلماء مركّبات عضوية في المختبرات بتقنيات مختلفة اعتمادًا على
المجموعات الوظيفية (Functional groups) الموجودة في هذه النواتج. وفي الكيمياء العضوية شبه الصناعية يُعدّل العلماء المواد الطبيعية الموجودة بهدف تحسين أنشطتها أو تغييرها[1].
تمتاز النواتج الطبيعية بتنوّعٍ هيكليٍ عالٍ وأنشطة دوائية أو بيولوجية فريدة من نوعها، ويُعتبر التنوع الهيكلي للمنتجات الطبيعية، خصوصًا مع تعدّد المجموعات الوظيفية في الجزيء الواحد، تحدِّيًا أمام الكيميائيين العضويّين الصناعيّين داخل المختبر. للنواتج الطبيعية استخدامات متعدّدة، إذ تُستخدم في الطب الحديث، واستُخدمت سابقًا في الطب التقليدي (الشعبي) لعلاج العديد من الأمراض[2].
وفي القرن الواحد والعشرين، غالبًا ما تُستخدم النواتج الطبيعية نقاطَ انطلاق لاكتشاف
الأدوية، يأتي بعدها تعديلات صناعية للمساعدة في تقليل الآثار الجانبية (Side effects) وزيادة
التوافر الحيوي {{التوافر البيولوجي (Bioavailability): مصطلح في علم الأدوية يُشير إلى النسبة المئوية للدواء الذي يصل إلى مجرى الدم ويصبح متاحًا للجسم ليعمل ببساطة، وهو مقياس لمدى فاعلية امتصاص الدواء من مصدره الأولي (مثل قرص الدواء) ووصوله إلى موقع تأثيره.}} للدواء. في الواقع، تُعتبر النواتج الطبيعية مصدر إلهام لما يقاربُ نصف الأدوية التي تعتمدُها
إدارة الغذاء والدواء الأميركية {{إدارة الغذاء والدواء الأميركية: وكالة تابعة للحكومة الفيدرالية في الولايات المتحدة الأميركية، ومسؤولة عن حماية الصحة العامة من خلال تنظيم الإشراف على سلامة الأغذية، ومنتجات التبغ، والمكملات الغذائية، والعقاقير الطبية الموصوفة وغير الموصوفة، واللقاحات، والمنتجات البيولوجية، وعمليات نقل الدم، والأجهزة الطبية، والأجهزة التي تصدر الإشعاع، والمنتجات البيطرية.}} (FDA). بالإضافة إلى الطب، تُستخدم النواتج الطبيعية ومشتقاتها بشكل شائع بصفتها مُضافات غذائية على شكل توابل وأعشاب، وعوامل مضادة
للبكتيريا، ومضادات الأكسدة لحفظ الطعام. كما أن النواتج العضوية الطبيعية تدخل في كل جانب من جوانب حياة البشر تقريبًا، مثل الملابس التي يرتدونها، والنواتج البلاستيكية والمطاطية، ومنتجات الصحة والجمال، وحتى الطاقة التي تشغّل السيارات والمصانع.
يمكن تصنيف النواتج الطبيعية وفقًا لوظائفها البيولوجية، أو مساراتها الحيوية، أو مصادرها.
فئات النواتج الطبيعية وفقًا لوظائفها البيولوجية
تُقسَم النواتج الطبيعية غالبًا إلى فئتين رئيستين وَفق وظائفها: المُسْتَقْلَبات الأولية (Primary metabolites) والمُسْتَقْلَبات الثانوية (Secondary metabolites). تُعتبر المستقلَبات الأولية جزيئات عضوية لها وظيفة ضرورية لبقاء الكائن الحي الذي ينتجها، فمن دونها يموت. ومن الأمثلة على المستقلَبات الأولية جزيئاتُ
الأحماض النووية (Nucleic acids)، والأحماض الأمينية (Amino acids) والسكّريات الأحادية {{السكريات الأحادية (Monosaccharides): المعروفة أيضًا باسم "السكريات البسيطة"، هي أبسط أنواع الكربوهيدرات، وتعدّ الوحدات الأساسية التي تتكون منها الكربوهيدرات المعقدة مثل السكريات الثنائية والسكريات المتعددة، ولا يمكن تحليل السكريات الأحادية إلى وحدات أبسط منها، ومن الأمثلة على السكريات الأحادية: الغلوكوز والفركتوز والغلاكتوز.}}، والأحماض الدهنية {{الأحماض الدهنية (Fatty acids): الوحدات الأساسية للدهون الثلاثية والدهون الفسفورية، تُعدّ مركبات عضوية تتكون من سلسلة طويلة من ذرات الكربون والهيدروجين، وفي أحد طرفيها مجموعة كربوكسيل. تؤدي الأحماض الدهنية أدوارًا مهمة في الجسم، مثل تخزين الطاقة، وبناء أغشية الخلايا، وتشكيل الهرمونات.}} اللازمة لتكوين الجزيئات الكبيرة (Macromolecules) الرئيسة، مثل:
الحمض النووي الريبي منقوص الأكسجين {{لحمض النووي الريبي منقوص الأكسجين: الجزيء الذي يحمل التعليمات الجينية اللازمة لنمو جميع الكائنات الحية المعروفة وتطورها وعملها وتكاثرها. ويحتوي على جميع المعلومات الوراثية التي تحدد خصائص الكائن الحي. ويتكون من شريط مزدوج من السلاسل التي تتكون من وحدات بنائية تسمى النيوكليوتيدات التي تتكون من مجموعة فوسفات وسكر ديوكسي ريبوز وقاعدة نيتروجينية.}}، (DNA)
والحمض النووي الريبي {{الحمض النووي الريبي: يشبه في تركيبه الـDNA ولكن مع بعض الاختلافات. ينقل التعليمات الجينية من الـDNA إلى الريبوسومات حيث تُصنَّع البروتينات في الخلية. وهو سلاسلُ تتكون من شريط واحد من الوحدات البنائية تسمى النيوكليوتيدات التي تتكون من سكر الريبوز وقواعد نيتروجينية.}} (RNA)، والبروتينات (Proteins)، والكربوهيدرات (Carbohydrates)، والدهون (Lipids)، وجميعها مسؤولة عن الحفاظ على الحياة. أما المستقلَبات الثانوية فتعتبر غير ضرورية للبقاء، ولكنها تزيد في القدرة التنافسية للكائن الحي داخل بيئته، وعادة ما تكون وظائفها خارجية، وتؤثر بشكل رئيس في الكائنات الحية الأخرى خارج الكائن المنتِج.
هناك اختلاف بين التعريف الكيميائي العضوي للنواتج الطبيعية (المستقلَبات الأولية والثانوية)، والتعريفات في مجالات
الكيمياء الطبية (Medicinal chemistry) وعلم العقاقير {{علم العقاقير (Pharmacognosy): علم يدرس الأدوية المشتقة من مصادر طبيعية، وهو علم متعدد التخصصات يجمع بين علم الأدوية وعلم النبات وعلم الكيمياء لتحديد الخصائص الطبية للنباتات والكائنات الدقيقة والحيوانات وتحليلها وفهمها.}} والطب من حيث دراستها واستخدامها، ففي هذه العلوم يشيع استخدام تعريف أكثر تحديدًا بأن النواتج الطبيعية هي المستقلبات الثانوية فقط، وذلك بسبب تعدّد وظائفها في البيئة المحيطة واستخداماتها في المجالات الطبية[3].
المستقلبات الأولية
هي المكونات الأساسية للمسارات الأيضية الأساسية المطلوبة للحياة، وترتبط بالوظائف الخلوية الأساسية، مثل استخدام المواد الأولية من أجل بناء الخلايا، وإنتاج الطاقة، والنمو، والتطور. تشمل المستقلبات الأولية اللبنات الأساسية اللازمة لتكوين الجزيئات الأربعة الكبيرة الرئيسة داخل الجسم: الكربوهيدرات والدهون والبروتينات والأحماض النووية[4].
[الشكل1]
 تكون البوليمرات من وحدات البناء الجزيئية
تكون البوليمرات من وحدات البناء الجزيئية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تُعتبر
الكربوهيدرات والبروتينات والأحماض النوويةمبلمرات (Polymers) كبيرة تُبنى من تكرار وحدات
المونومر (Monomer) الأصغر (الشكل 1). وحدات المونومر المستخدمة لبناء
الأحماض النووية هي
النيوكليوتيدات (Nucleotides)، في حين أن المونومرات المكوّنة
للبروتينات هي
الأحماض الأمينية، أمّا المونومرات المكوّنة
للكربوهيدرات فهي جزيئاتُ
السكّريات الأحادية. من الجدير ذكره أن
الدهون هي الجزيئات الكبيرة الوحيدة غير المكوّنة من عمليات بلمرة، وهي متعددة التكوينات الشكلية والوظيفية[5].
تشتمل المستقلبات الأولية التي تُساهم في إنتاج الطاقة على العديد من
الإنزيمات (Enzymes) التي تحطّم جزيئات الطعام، مثل
الكربوهيدرات والدهون، منتجة الطاقة الحيوية على شكل مركب
أدينوسين ثلاثي الفوسفات {{أدينوسين ثلاثي الفوسفات: جزيء عضوي يعدّ مخزنًا للطاقة الكيميائية الناتجة من تكسير الطعام مثل الغلوكوز في الخلايا الحية. ويُطلق هذه الطاقة عند الحاجة لدعم الأنشطة الخلوية، فتُكسر الرابطة النهائية لمجموعة الفوسفات من جزيء ATP وينتج من هذا التكسير كمية كبيرة من الطاقة، ويُحول الجزيء إلى أدينوسين ثنائي الفوسفات (ADP) ومجموعة فوسفات حرة.}} (ATP) الإنزيمات هي محفزات بيولوجية تُسرِّع معدل التفاعلات الكيميائية، وهي في غالب الأحيان جزيئات
بروتينية. كما يتكوّن الهيكل الأساسي للخلايا والكائنات الحية أيضًا من المستقلَبات الأولية، وتشمل هذه الهياكل
أغشية الخلايا (Cell membrane) المكوّنة من
الدهون الفسفورية (Phospholipids) والكولسترول {{الكولسترول (Cholesterol): مركب عضوي دهني ضروري للخلايا، ورغم أن ارتفاع مستوياته يُعد خطرًا على الصحة، فإنه يؤدي وظائف حيوية لا يمكن الاستغناء عنها في الجسم؛ فهو يساهم في بناء أغشية الخلايا، ومنه تصنع العديد من الهرمونات وبعض الڤيتامينات مثل ڤيتامين D، كما أنه جزء من العصارة الصفراوية.}} والبروتينات، وجدران الخلايا {{جدار الخلية (Cell wall): طبقة خارجية صلبة توجد في خلايا بعض الكائنات الحية، مثل النباتات، والفطريات، والطحالب، والبكتيريا. يعمل بوصفه طبقة حماية إضافية تقع خارج الغشاء الخلوي، وتُعد وظيفته الرئيسة توفير الدعم الهيكلي للخلية وحمايتها. ويتكون من السليلوز في الخلايا النباتية، ومن الكيتين في الفطريات، ومن الببتيدوغليكان في البكتيريا. ورغم صلابته فهو نفاذ لجميع المواد.}} التي تتكون من مركبات مختلفة كالببتيدوغليكان (Peptidoglycan)، والكيتين (Chitin) وغيرها، والهياكل الخلوية الداخلية التي تُصنّع من
البروتينات المختلفة. كما يتكوّن الحمضان النوويان الـ DNA والـ RNA، اللذان يخزّنان المعلومات الوراثية وينقلانها، من مستقلَباتٍ أولية أيضًا. وتشتمل المستقلبات الأولية كذلك على جزيئات تشارك في الإشارات الخلوية والاتصالات والنقل ومعظم العمليات الحيوية.
المستقلَبات الثانوية
بعكس المستقلَبات الأوّلية، يمكن للكائن الحي الاستغناء عن المستقلَبات الثانوية، فهي ليست مطلوبة لبقائه على قيد الحياة. إضافة إلى ذلك، فإن المستقلَبات الثانوية عادةً ما يكون لها توزيع ضيق في أنواع معينة من الكائنات الحية. على سبيل المثال، يُنتج نبات الباذنجان المميت (أتروبا بيلادونا،Atropa Belladonna) مركبات مُهلوسة سامة، مثل السكوبولامين وهو أحد قلويدات التروبان (يُنظَر: 1.2.1.2)، في حين أن الأنواع الباذنجانية الأخرى لا تمتلك هذه القدرة[6].
اكتُشفت مئات الآلاف من المستقلبات الثانوية، وتمتاز هذه المستقلَبات بمجموعة متنوعة من الوظائف. تشمل هذه المستقلَبات الثانوية
الفيرومونات {{الفيرمونات (Pheromones): مواد كيميائية تفرزها الكائنات الحية (الحيوانات، الحشرات، وحتى النباتات) في البيئة، وتؤثر في فيزيولوجيا أفراد آخرين من النوع نفسه أو في سلوكهم، على عكس الهرمونات التي تعمل داخل الجسم. وتعمل الفيرمونات خارج الجسم بوصفها وسيلة للاتصال بين الأفراد.}} التي تعمل بصفتها جزيئاتِ إشاراتٍ اجتماعية بين أفراد آخرين من النوع نفسه، وتشمل كذلك جزيئات الاتصال الأخرى التي تجتذب الكائنات الحية وتنشطها، والجزيئات التي تذيب العناصر الغذائية وتنقلها، والوسائل الدفاعية (المواد الطاردة، والسموم، وغيرها) التي تُستخدم ضد المنافسين والفرائس والحيوانات المفترسة[7]. تُعد وظائف العديد من المستقلَبات الثانوية الأخرى لغاية الثلث الأول من القرن الحادي والعشرين غير معروفة، إذ ترتكز إحدى الفرضيات على أن هذه الجزيئات تمنح ميزة تنافسيّة للكائن الحي الذي ينتجها؛ ولذلك يُنتج الكائن الحي عددًا قليلًا من المستقلَبات الثانوية اعتمادًا على ما يتعرّض له خلال حياته[8].
[الجدول1]
 أمثلة على الفئات الرئيسة للمستقلَبات الثانوية
أمثلة على الفئات الرئيسة للمستقلَبات الثانوية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تضمّ المُستقلَبات الثانوية مجموعة متنوعة من الهياكل، مثل: القلويدات (Alkaloids)، والفينيل بروبانويدات (Phenylpropanoids)، والبوليكيتيدات (Polyketides)، والتربينويدات (Terpenoids) (الجدول 1). القلويدات مستقلَبات ثانوية تحتوي على النيتروجين بصفته أحد مكوّنات تركيبها العضوي، ويمكن تقسيمها إلى العديد من الفئات الفرعية للمركبات. يعتبر النيكوتين، وهو المادة المسببة للإدمان في التبغ، مثالًا على القلويدات. أما مركّبات الفينيل بروبانويد، فهي عائلة متنوّعة من المركّبات العضوية التي يُصنّعها الحمضان الأمينيّان الفينيل ألانين (Phenylalanine) والتيروسين (Tyrosine)[9]. يُعتبر حمض السيناميك (Cinnamic acid) أحد جزيئات النكهة المتطايرة الموجودة في القرفة، وهو من عائلة الفينيل بروبانويد[10]. أما البوليكيتيدات، فتتكون من وحدات بناء الأسيتات (Acetate) والمالونات (Malonate) لتشكيل هياكل كبيرة ومعقّدة. يُعتبر الأفلاتوكسين (Aflatoxin) أحد النواتج الطبيعية متعددة الكيتيدات التي تُنتجها
الفطريات من جنس
الرشاشيات {{الرشاشيات: جنس شائع من الفطريات، يتضمن مئات الأنواع المختلفة التي توجد في كل البيئات تقريبًا، خاصة في التربة والنباتات المتحللة والغذاء والهواء. ورغم أن معظم أنواعها غير ضارة، فإن بعضها يمكن أن يُسبب أمراضًا للإنسان والحيوان.}} (Aspergillus). تنمو هذه الأنواع من العفن عادة على المحاصيل الغذائية المخزنة، مثل الذرة والفول السوداني، إذ تُدمّر الأفلاتوكسينات جزيئات الحمض النووي وتكون بمنزلة مادة مسرطنة[11]. أمّا التربينويدات، فهي فئة كبيرة أخرى من النواتج الطبيعية التي تُصَنَّع من وحدات مونومر مكونة من 5 كربونات تسمى آيزوبرين (الصورة 1). يُعَدّ المطاط الطبيعي مثالًا جيدًا على البنية القائمة على التربينويد الذي يتكون من وحدات آيزوبرين متعددة[12].
فئات النواتج الطبيعية وفقًا لأصلها الحيوي
تُصنَّف النواتج الطبيعية إلى أربع مجموعات مختلفة وفقًا لأصلها الحيوي، وهي: المُركبات شبه القلوية، والفينيل بروبانويد، والبوليكيتيدات، والتربينويدات. يوجد أكثر من 200000 مركّب معروف من النواتج الطبيعية ومُستَخلَص من النباتات، لا يَتَّسع المجال لذكرها كلها، وفي ما يأتي بعضٌ منها.
النواتج الطبيعية المحتوية على النيتروجين
يعود مصطلح قلوي (Alkali) إلى أصلٍ عربي، ويُعنى به الرماد المحتوي على كربونات البوتاسيوم[13]. أما المركّبات شبه القلوية أو القلويدات (Alkaloid)، فهي مركّبات حلقيّة (تحتوي على حلقة أو أكثر) غير متجانسة تحتوي على ذرة أو أكثر من النيتروجين (تكون في غالبيتها في هيئة نيتروجين ثلاثي)، تُصَنَّع هذه المركّبات بيولوجيًا من
الأحماض الأمينية. تُعد أغلب القلويدات موادّ صلبة غير قابلة للذوبان في الماء، ولكنّها تذوب في الإيثانول أو الكلوروفورم أو الإيثر[14]. من الجدير ذكره أنّ بعض هذه المُركّبات قابلة للذوبان في الماء، مثل النيكوتين. إن خصائص النواتج الطبيعية المحتوية على النيتروجين متعدّدة ووظائفها مهمة للنباتات، إذ تُشكّل موادّ واقية من هجوم الحيوانات والحشرات، وكذلك منظمات للنمو والأيض والتّكاثر. كما أظهرت هذه المركّبات تأثيرات بيولوجية قويّة على الكائنات الحيّة والبشر حتى باستخدام جرعات وتراكيز قليلة جدًا. فمثلًا، أثبتت الدراسات عن هذه النواتج احتواءها على العديد من الأنشطة الدوائية، فيمكن استعمال بعض المركبات
مضاداتٍ للسرطان {{مضادات السرطان: فئة من الأدوية تُستخدم لعلاج السرطان عن طريق استهداف الخلايا السرطانية وتدميرها، أو منع نموها وانتشارها. تختلف أنواع هذه المضادات في آليات عملها، وتُستخدم عادةً في العلاج الكيميائي، أو العلاج الموجه، أو العلاج المناعي.}}، واستعمال غيرها
مضادات للالتهابات {{مضادات الالتهابات: مجموعة من الأدوية تُستخدم لتقليل الالتهاب وتخفيف الأعراض المرتبطة به، مثل الألم والتورم والحمى، وتعمل عن طريق تثبيط إنزيمات أو مواد كيميائية في الجسم تُسبب الالتهاب. منها مضادات الالتهابات غير الستيرويدية مثل الأسبرين والإيبوبروفين، ومنها الكورتيكوستيرويدات مثل الديكساميثازون.}} أو
مضادات للملاريا {{مضادات الملاريا: فئة من الأدوية تُستخدم لعلاج الملاريا، وهو مرض طفيلي خطير تُسببه طفيليات من جنس المتصورة، تنتقل إلى الإنسان عن طريق لدغات إناث بعوض الأنوفيلة. تهدف هذه الأدوية إلى القضاء على الطفيلي في مراحل مختلفة من دورة حياته داخل جسم الإنسان، منها الكلوروكين والأرتيميسينين.}}، وأخرى
مضادات للميكروبات {{مضادات الميكروبات: فئة واسعة من الأدوية التي تُستخدم لقتل الكائنات الحية الدقيقة (الميكروبات) أو تثبيط نموها، مثل البكتيريا، والفطريات، والڤيروسات، والطفيليات. تُعد هذه الأدوية حجر الزاوية في الطب الحديث، إذ أحدثت ثورة في علاج الأمراض المعدية منها المضادات الحيوية بمختلف أنواعها.}} ومضادات ارتفاع ضغط الدم {{مضادات ارتفاع ضغط الدم: فئة من الأدوية تُستخدم لعلاج ارتفاع ضغط الدم الذي يزيد من خطر الإصابة بأمراض القلب والسكتات الدماغية. تعمل هذه الأدوية بآليات مختلفة للمساعدة في خفض ضغط الدم إلى مستوياته الطبيعية؛ فمنها ما يعمل على إدرار البول (مدرات البول)، ومنها ما يثبط عمل مستقبلات بيتا، ومنها مثبطات الإنزيم المحول للأنجيوتنسين.}} ومضادات السكري {{مضادات السكري: فئة من الأدوية تُستخدم لعلاج ارتفاع مستويات السكر (الغلوكوز) في الدم، وتعمل بآليات مختلفة للمساعدة في تنظيم سكر الدم، وتُستخدم عادةً لعلاج السكري من النوع الثاني، ومنها ما يقلل إنتاج الغلوكوز المنتج في الكبد مثل الميتفورمين، ومنها ما يحفر البنكرياس على إفراز الإنسولين مثل السلفونيل يوريا، ومنها ما يمنع الكلى من إعادة امتصاص الغلوكوز مثل داباغليفلوزين.}}، وأيضًا
مضادات للأكسدة {{مضادات الأكسدة: مركبات كيميائية موجودة في الأطعمة، وخاصةً في الفواكه والخضروات، وظيفتها الأساسية حماية خلايا الجسم من التلف الذي تُسببه جزيئات غير مستقرة تُسمى الجذور الحرة.}}[15].
تُعَدّ مجموعة النواتج الطبيعية المحتوية على النيتروجين واحدة من أكبر مجموعات النواتج الطبيعية عددًا بوجود أكثر من 20000 مركّب معروف من المركبات شبه القلوية، وبسبب عددها الكبير وتنوّعها الهيكلي، فإنه من الصعب تقديم ملخص شامل لجميع أنواع المركبات شبه القلوية المختلفة والإحاطة بها[16]، وفي ما يأتي عرضٌ لبعض فئاتها.
- قلويدات البيورين (Purine alkaloids): هي مركّبات نيتروجينية مشتقة من استقلاب النيوكليوسيد (Nucleoside metabolism). تصنع الخلية هيكل البيورين باستخدام عدة جزيئات صغيرة كالفورمات (Formate)، بالإضافة إلى
الأحماض الأمينية الآتية: الأسبارتات (L-aspartate)، والغلوتامين (L-glutamine)، والغلايسين (Glycine).
[الشكل2]
/_أحد قلويدات البيورين (الكافيين).jpg) أحد قلويدات البيورين (الكافيين)
أحد قلويدات البيورين (الكافيين)
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يُعد
الكافيين {{الكافيين: مادة كيميائية تُعرف باسم القلوي، توجد بشكل طبيعي في أكثر من 60 نوعًا من النباتات، أشهرها حبوب البن، وأوراق الشاي، وحبوب الكاكاو. يُعد منبهًا طبيعيًا للجهاز العصبي المركزي، ويعمل عن طريق حجب مستقبلات مادة الأدينوسين في الدماغ.}} (Caffeine)(الشكل 2) الأكثر وفرة من بين قلويدات البيورين، ويوجد في بعض البذور مثل القهوة والكاكاو[17].
وفي القرن العاشر الميلادي خُمِّرت بذور القهوة المحمّصة في شبه الجزيرة العربية لإعداد مشروب القهوة، وسرعان ما انتشرت إلى باقي دول العالم. أما بذور شجرة الكاكاو (التي تنحدر من حوض الأمازون، ووزُرِعت في أميركا الوسطى)، فتُستخدم لإنتاج مشروبات ومأكولات مختلفة كالشوكولاتة. يُصنّف
الكافيين على أنه منبّه مركزي وينتشر على نطاق واسع في المشروبات مثل القهوة والشاي والمشروبات الغازية، إضافة إلى استخدامه في أدوية البرد والمسكّنات، وتستعمله النباتات أيضًا باعتباره وسيلةَ دفاع ضِدّ الحيوانات العاشبة[18]. يؤثّر التركيز العالي للكافيين في نمو الجذور، إذ يُثبّط نمو شتلات البنّ عند زراعتها في محاليل مائية ذات تراكيز مختلفة من
الكافيين بسبب منعه لنمو الجذور[19]. في جسم الإنسان، يعمل
الكافيين بوساطة تثبيط إنزيمات فسفودايستيراز بالإضافة إلى انسداد مستقبلات الأدينوسين (Adenosine receptors)؛ ما يؤدي إلى إطلاق
الناقلات العصبية[20]. من الجدير ذكره أن هذه الآلية ليست حكرًا على
الكافيين فقط، بل هي الطريقة السائدة لكيفية عمل قلويدات البيورين الأخرى بشكل عام. أشارت بعض الدراسات أيضًا إلى أنّ شاربي القهوة، بسبب احتوائها على تركيز أعلى من
الكافيين مقارنة بالمشروبات الأخرى، يُظهرون انخفاضًا ملموسًا لخطر الإصابة
بمرض باركنسون (الشلل الرُّعاش)[21].
[الشكل3]
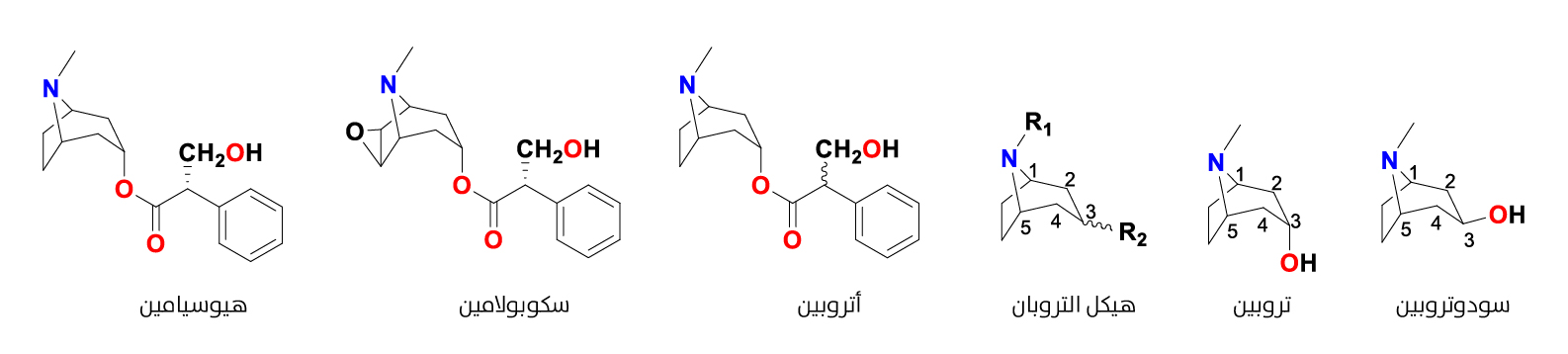 بعض قلويدات التروبان
بعض قلويدات التروبان
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
- قلويدات التروبان: يمكن تعريف قلويدات التروبان (الشكل 3) أنها جميع الجزيئات التي تمتلك نظام حلقة تروبان، وتوجد هذه المجموعة بشكل رئيسٍ في عائلة النباتات الباذنجانية (Solanaceae) والكوكيات (Erythroxylaceae) وغيرها. وتُستخدم في علاج الغثيان والقيء ودوار الحركة وكذلك تقلّصات العضلات. تتكون قلويدات التروبان (Tropane alkaloids) باستخدام
الأحماض الأمينية أورنيثين و/ أو الأرجينين. قلويد التروبان مركب ثنائي الحلقات؛ إذ فيه حلقة مكوَّنة من سبع ذرات وتُشكِّلُ حلقةً أخرى مع جسر من ذرة النيتروجين بين C-1 وC-5، وتكون ذرة النيتروجين متصلة بمجموعة ميثيل. العديد من قلويدات التروبان هي إسترات الكحول تروبين (المركب الوسيط لتخليق السكوبولامين) أو السودوتروبين (المركب الوسيط لتخليق الكاليستيغين الحيوي)[22].
يُعتبر الأتروبين مزيجًا راسيميًا من المتصاوغات الفراغية اليمينية واليسارية (R, S) لمركب الهيوسيامين. بسبب ثباته مقارنة مع المتصاوغ الفراغي (S) لمركّب الهيوسيامين، فإن الأتروبين يُستخدم لعلاج التشنجات، ويُستخدم ترياقًا ضد التسمم بالمبيدات الحشرية العضوية الفسفورية، ويُستخدم أيضًا قبل العمليات الجراحية لتقليل إفراز اللعاب وإفراز
الجهاز التنفسي. كذلك يعتبر الهيوسيامين والسكوبولامين من الأمثلة الأكثر انتشارًا من قلويدات التروبان، وهي إسترات للكحول الأميني تروبين وسكوبين مع حمض التروبيك المشتق من الحمض الأميني فينيل ألانين.
[الشكل4]
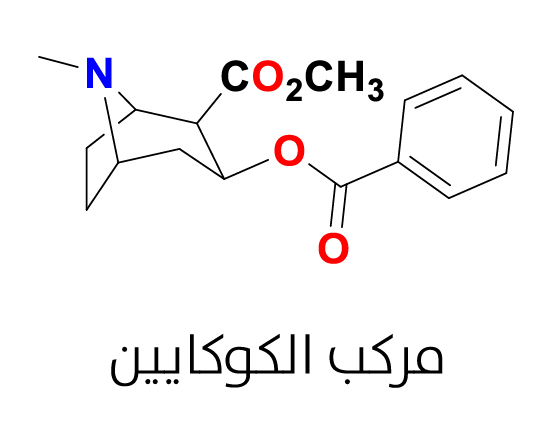 مركب الكوكايين
مركب الكوكايين
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
- الكوكايين: تعود التقارير الأولى لاستخدام الكوكايين (Cocaine) (الشكل 4) إلى 3000 عام قبل الميلاد في الإكوادور. إذ إن نبات الكوكا (Erythroxylon coca) قد نشأ على المنحدر الشرقي لجبال الأنديز الإكوادورية أو البيروفيّة، وزرعته شعوب الإنكا. يُعتبر نبات الكوكا من أكثر النباتات التي تحتوي على كميّات كبيرة من الكوكايين في أوراقها، إذ تصل نسبته إلى 1 في المئة تقريبًا. تعود البداية إلى اعتياد سكّان أميركا الجنوبية فترة طويلة على مضغ أوراق هذا النبات بسبب تأثيراتها المنشّطة، إذ تجلب الأوراق إحساسًا واضحًا بالرفاهية العقلية والجسدية، ولديها تأثير على زيادة القدرة على التحمّل[23].
يُعتبَر الكوكايين منبّهًا مركزيًا شديد الإدمان يمنع إعادة امتصاص
الناقلات العصبية؛
الدوبامين والنورأدرينالين، في نقاط الاتصال العصبي، كما أنه يثبّط عمل الإنزيم أكسيداز أحادي الأمين (Monoamine oxidase)، وهو الإنزيم الذي يحلّل النواقل العصبية؛
الدوبامين والأدرينالين والنورأدرينالين.
[الشكل5]
 الصيغة البنائية للنورتروبان وأحد مركبات الكاليستيغينات
الصيغة البنائية للنورتروبان وأحد مركبات الكاليستيغينات
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل6]
 أحد قلويدات البيروليزيدين
أحد قلويدات البيروليزيدين
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل7]
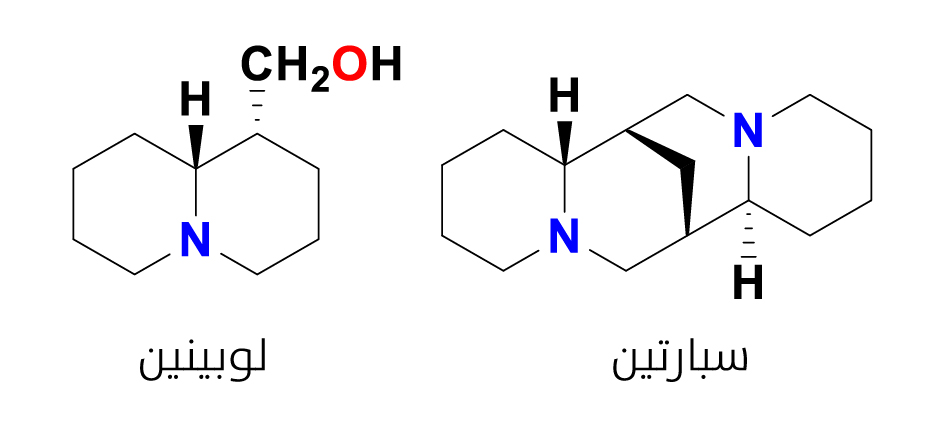 بعض قلويدات الكينوليزيدين
بعض قلويدات الكينوليزيدين
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تُعتبر الكاليستيغينات من مثبطات الغليكوسيداز (Glycosidase)، وبسبب تشابهها الهيكلي مع السكّريات، فإنها تتنافس مع السكّريات للربط في الموقع النشط للغليكوسيداز. لذلك، إنّ أحد التطبيقات الطبية الممكنة لهذه المجموعة من النواتج الأيضية الثانوية هو منع حدوث ذروة الغلوكوز بعد الأكل لمرضى
السكّري من النوع الثاني[26].
- قلويدات البيروليزيدين: تنتشر قلويدات البيروليزيدين (Pyrrolizidine alkaloids) بشكل رئيسٍ في عدة فصائل نباتية، مثل: النجمية والحمحمية والبقولية وغيرها. يُعتبر العديد من قلويدات البيروليزيدين مسببًا
للسرطان، إضافة إلى أنه يمكن أن يؤدّي إلى
تليّف الكبد {{تليّف الكبد: حالة مرضية خطيرة، ومزمنة، تحدث عندما يُستبدل النسيج السليم في الكبد بنسيج ندبي غير وظيفي. يؤدي هذا التليف إلى تلف دائم في الكبد، فيعيق قدرته على أداء وظائفه الحيوية، مثل تنقية الدم من السموم، وإنتاج البروتينات، والمساعدة في الهضم. وقد يحدث التليّف بسبب إصابة الكبد بڤيروسات التهاب الكبد أو إدمان الكحول أو بسبب تراكم الدهون في الكبد.}} وفشله في نهاية المطاف[27]. يتكوّن هيكل قلويدات البيروليزيدين من هيدروكسي ميثيل البيروليزيدين (قاعدة نيسين)، الذي يُؤَسْتَر في الغالب بأحماض ألِفاتية متفرّعة أحادية الكربوكسيل أو ثنائيّة الكربوكسيل (أحماض نيسيك) ومنها قلويد السينيسيونين (الشكل 6).
- قلويدات الكينوليزيدين: يمكن الحصول على قلويدات الكينوليزيدين (Quinolizidine alkaloids) (الشكل 7) من مختلف الحيوانات والنباتات البحرية والبرية. وتحتوي قلويدات الكينوليزيدين على مضادّات
للسرطان والبكتيريا والالتهابات والفيروسات وتُستخدم أيضًا لعلاج نقص سكّر الدم. تُصنَّع قلويدات الكينوليزيدين حيويًا من استقلاب الحمض الأميني لايسين. ويُعتبر اللوبينين من المركّبات ثنائية الحلقات البسيطة، ولكنّ معظم المركّبات الأخرى من هذه المجموعة ثلاثية الحلقات أو رباعية الحلقات مثل قلويد سبارتين[28].
- قلويدات مشتقة من التيروسين: يُعتبر الحمض الأميني التيروسين (Tyrosine) مركّبًا وسيطًا يُستعمل لتكوين العديد من القلويدات[29]، منها:
- قلويدات بنزيل آيزوكينولين (Isoquinoline alkaloids)
هي مركّبات مشتقة من جزيئين من التيروسين. يمكن أن يخضع المركّب الوسيط الريتيكولين (S)-reticuline في بنائه الحيوي لعمليات إعادة ترتيب جُزيئِي وتعديلات مختلفة لإنتاج الفئات الهيكلية المختلفة للبنزيل آيزوكينولين.
تنتشر قلويدات إبيكاك (Ipecac) في
نباتات ثنائية الفلقة {{نباتات ثنائية الفلقة: أو ما يُعرف بـ"Dicot"، هي واحدة من مجموعتين رئيسيتين تُصنف إليهما النباتات المزهرة. تتميز هذه النباتات بخصائص فريدة؛ فبذور هذه النباتات تحتوي على ورقتين جنينيتين تُسمى "فلقات"، وتُعتبر هذه الخاصية السببَ في تسميتها. تعمل هذه الفلقات بوصفها غذاء للجنين حتى يُصبح قادرًا على أداء عملية التمثيل الضوئي.}} مثل فصيلة الفويّة (التي تضم نبات البن). تُعتبر جذور نبات عرق الذهب مصدرًا لقلويد السيفالين (Cephaline) الذي يُستخدم للتخلّص من البلغم والأميبا {{الأميبا: كائن حي وحيد الخلية، ينتمي إلى مجموعة من الكائنات تُسمى الأوليات. تُعرف الأميبا بشكلها المتغير وقدرتها على الحركة عن طريق تكوين امتدادات مؤقتة من جسمها تُسمى الأقدام الكاذبة، وتتغذى على البكتيريا والطحالب، وتتكاثر عن طريق الانشطار.}} (Amoeba). ينتشر نبات عرق الذهب في الغابات المطيرة في أميركا الجنوبية، إذ كان يُستخدم تقليديًا في الطب الشعبي البرازيلي. تتكون قلويدات إبيكاك من الحمض الأميني تيروسين وسيكولوغانين أحادي التربين (Monoterpene secologanin)، ومن ثَمّ تسمى قلويدات شبه تربين آيزوكينولين (Terpenoid-isoquinoline).
- قلويدات النرجسية (alkaloids Amaryllidaceae)
تنتشر عائلة النرجسيات في المناطق الاستوائية والمعتدلة الدافئة، واستُخدِمت نباتات هذه العائلة قديمًا في طب الأعشاب التقليدي. تُظهر القلويدات المستخلصة من النرجسيات أنشطة بيولوجية متنوعة، مثل:
مضاد الأورام {{مضاد الأورام: من العلاجات الكيميائية التي تستخدم لعلاج الأورام السرطانية، تعمل هذه العلاجات على وقف نمو الخلايا السرطانية أو إبطائه، أو منع انتشارها في الجسم، ومنها العوامل المؤلكلة ومضادات الأيض ومضادات الأنابيب الدقيقة.}} ومضاد الفيروسات ومضاد الفطريات ومضاد الملاريا وتُستخدم أيضًا مسكّنًا للآلام. تتكون قلويدات النرجسية من جزيء ألدهيد بروتوكاتيكويك (Protocatechuic aldehyde) وجزيء التيروسين الذي ينتج من جزيء الفينيل ألانين. ومن الأمثلة على قلويدات هذه المجموعة الليكورين والنوربلادين، ويعتبر النوربلادين الوسيط المركزي لمسار التخليق الحيوي للقلويدات النرجسية[30](الشكل8).
[الشكل8]
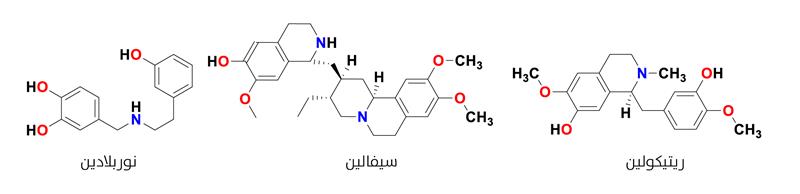 بعض القلويدات المشتقة من التيروسين
بعض القلويدات المشتقة من التيروسين
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل9]
 أحد القلويدات المشتقة من التيروسين
أحد القلويدات المشتقة من التيروسين
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل10]
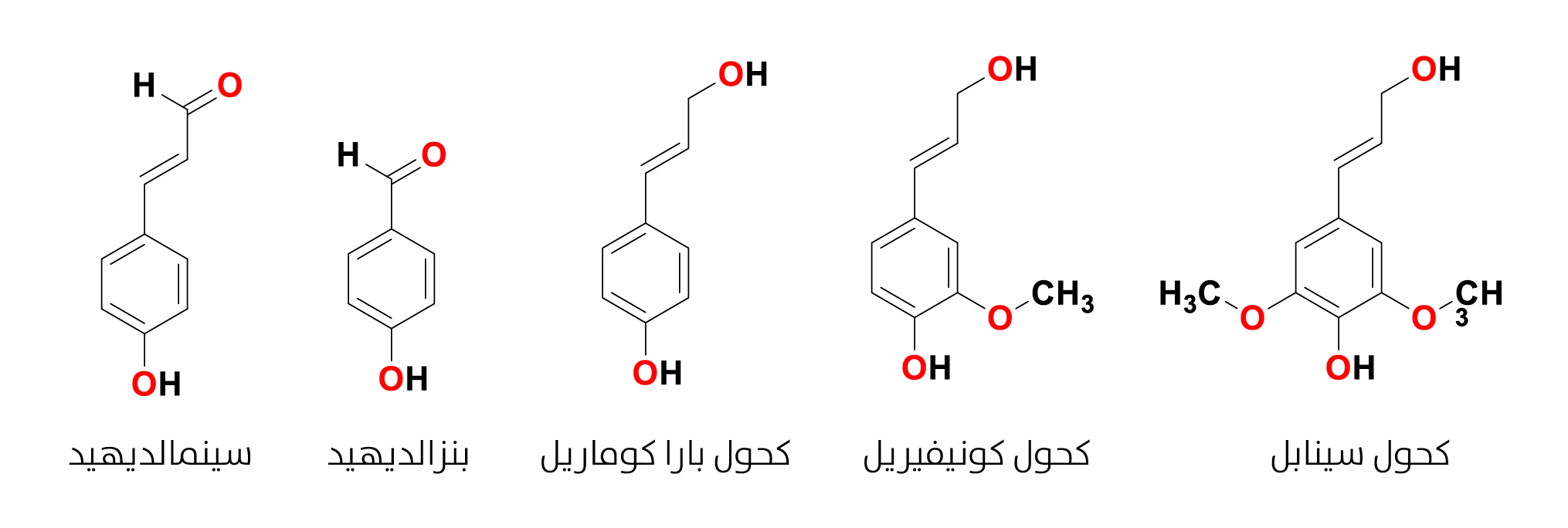 بعض النواتج الطبيعية المشتقة من مسار الشيكيمات والفينيل بروبانويد
بعض النواتج الطبيعية المشتقة من مسار الشيكيمات والفينيل بروبانويد
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
النواتج الطبيعية المشتقّة من مسار الشيكيمات والفينيل بروبانويد
يُخَلَّق جزيء الشيكيمات حيويًا من إريثروز 4-فوسفات (D-erythrose-4-phosphate) وفسفوإينول بيروفات (Phosphoenolpyruvate). يحدث مسار الشيكيمات فقط في النباتات والكائنات الحية الدقيقة، لذلك فإن
الأحماض الأمينية؛ الفينيل ألانين والتيروسين والتربتوفان، ضرورية للحيوانات ويجب تناولها مع الطعام[32]. يُعتبر الفينيل ألانين والتيروسين في
نباتات ذات الفلقة من المركّبات وسيطة لتخليق الفينيل بروبانويد (Phenylpropanoid). تشتمل هذه الفئة على مشتقات حمض السيناميك والفينيل بروبين والكومارين وغيرها (الشكل 10)، إذ تشترك جميعها في الهيكل الأساسي C6 -C3. تُعتبر مركّبات الفينيل بروبانويد مجموعة واسعة من المركّبات العطرية ومتنوعة هيكليًا، وغالبًا ما تحتوي على مجموعة هيدروكسيل أو أكثر، وتؤدّي دورًا مهمًا في تفاعل النباتات مع الكائنات الحية الأخرى[33]. يوفّر مسار الشيكيمات (Shikimate pathway) في النباتات مركّبات مشتقة من حمض البنزويك (Benzoic acid) والفينيل بروبانويد، ومنها:
- اللغنان واللغنين
اللغنان (Lignan) واللغنين (Lignin) مجموعة من النواتج الطبيعية الثانوية ذات الوزن الجزيئي القليل نسبيًا التي تتكون في الأجزاء المختلفة للنباتات. تُشتق هذه المركبات من تأكسد وحدتين أو أكثر من وحدات الفينيل بروبانويد. يطلق اسم المونولغنول على كل كحول هيروكسي سيناميك، مثل كحول كوماريل (p-coumaryl alcohol) أو كحول كونيفيريل (Coniferyl alcohol) أو كحول سينابل (Sinapyl alcohol). يتكون اللغنان من اتحاد جزءَين من كحول كوماريل، في حين يُعتبر اللغنين مبلمرًا من أيٍّ من جزيئات المونولغنول.
- الفينيل بروبينات والبنزينويدات
مركّبات الفينيل بروبين (Phenylpropenes) مشتقة من حمض السيناميك (حمض القرفة)، وتشترك في الخطوات الأولى من تصنيع اللغنين واللغنان الحيويَّيْن. ينتج من تقصير السلسلة الجانبية لحمض السيناميك ما مقداره ذرّتا كربون إلى مركّبات ذات هيكل C6-C1 تُسمى البنزينويدات (Benzenoids). تُشكل البنزينويدات رائحة مميزة للعديد من الأزهار، ومثال على ذلك الميثيل بنزوات، وهو أحد مكونات الرائحة الرئيسة لزهور النباتات التبغية. يعتبر البنزألدهيد وكحول البنزيل وأسيتات البنزيل وميثيل الساليسيلات من البنزنويدات الأخرى التي تساهم بشكل كبير في روائح الأزهار.
البوليكيتيدات
تُبنى البوليكيتيدات (Polyketides) (الشكل 11) مثل ما تُبنى
الأحماض الدهنية باستخدام وحدات كربونية مشتقة من أسيتيل مرافق الإنزيم أ (Acetyl-CoA) ومالونيل مرافق الإنزيم أ (Malonyl-CoA). وبعكس
الأحماض الدهنية، تحتفظ البوليكيتيدات بجميع ذرات الأكسجين الخاصة بالمركّبات المصنعة لها أو معظمها[34]. خلال عملية تكوين البوليكيتيد بيولوجيًا، تتشكل سلاسل بوليكيتون متعاقبة الترتيب لذرات الأُكسجين القادرة على التفاعل، التي غالبًا ما ترتبط أجزاؤها في مناطق مختلفة لينتج منها المركّبات الحلقية العطرية. تُعَدّ الفينولات من أكثر البوليكيتيدات انتشارًا مثلها مثل الفينيل بروبانويد، ولكن يمكن تمييز المجموعتين بنمط توزيع ذرات الأُكسجين على الحلقة. ففي حين أن البوليكيتيدات تحتوي عادة على ذرات الأكسجين مرتبطة بذرات الكربون واحدة بعد الأخرى، فإن الفينولات المشتقة من مسار الفينيل بروبانويد تحتوي على ذرة أكسجين على ذرات كربون متجاورة
[35](Ortho).
- البوليكيتيدات المشتقة من وحدات الأسيتات: تنتشر النفثوكينونات (Naphthodianthrones) ذات الأصل البوليكيتيدي في عدد قليل من العائلات ذات الصلة التصنيفية من رتبة القرنفليات، ومنها على سبيل المثال الدروسريات )Droseraceae( (الشكل 11). تتكون هذه المركّبات من ست وحدات أسيتات، وتُفقَد ذرة كربون واحدة في مسار تكوينها الحيوي؛ ما ينتج منه سلسلة من إحدى عشرة ذرة كربون، مكوِّنة حلقتين سداسيَّتين.
- البوليكيتيدات مع هيكل الفينيل بروبانويد: يمكن اتحاد المركّبات المشتقة من مسار الشيكيمات والفينيل بروبانويد (Phenyl propanoid) مع وحدة إلى ثلاث وحدات أسيتات مشتقة من مالونيل مرافق الإنزيم أ لإنتاج بوليكيتيدات بصيغ بنائية مختلفة في النبات. تُعتبر مركّبات الفلاڤونويدات (Flavonoids) (الشكل 11) أكبر مجموعة من هذه المركّبات مع أكثر من 6000 مركب جرى فصله والتعرف إليه[36].
[الشكل11]
 بعض البوليكيتيدات المشتقة من الأسيتات والفينيل بروبانويد والتربينويدات والقلويدات البوليكيتيدية
بعض البوليكيتيدات المشتقة من الأسيتات والفينيل بروبانويد والتربينويدات والقلويدات البوليكيتيدية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
- البوليكيتيدات مع وحدات بناء من التربينويدات: تُصنّف مركّبات هذه المجموعة بأنها تذوب في
الدهون بسبب احتوائها على هيكل التربينويد (Terpenoid)، وغالبًا ما تُنتَج أو تُخَزَّن في الغدد الخاصة أو الترخوم الغدية (Glandular trichomes) في النباتات والطحالب {{الطحالب: مجموعة متنوعة من الكائنات الحية التي تُعتبر جزءًا من النظم البيئية المائية، تُصنف ضمن مملكة الطلائعيات، وعلى عكس النباتات، لا تمتلك الطحالب جذورًا، أو سيقانًا، أو أوراقًا حقيقية، إلا أنها تشارك النباتات في أنها ذاتية التغذية. وتتباين أحجامها بوضوح، فمنها وحيدة الخلية ومنها الطحالب العملاقة. وتتكاثر الطحالب جنسيًا ولا جنسيًا.}} (Algae) وغيرها. يعتبر الكانابينويد (Cannabinoid) من أشهر مركّبات هذه المجموعة ويُصنّع بيولوجيًا من جزيء هكسانويل مرافق الإنزيم أ (Hexanoyl-CoA) وثلاثة جزيئات مالونيل مرافق الإنزيم أ وتربين جيرانيل بيروفوسفات. ينتشر الكانابينويد في القنّب الهندي الذي ينتمي إلى الفصيلة القنّبيّة (Cannabaceae). تُراكم نباتات القنّب (Cannabis sativa) صمغًا في الترخومات الغدية بكمية أكبر في النورات الأنثوية. يحتوي الصمغ الغدي على أكثر من ستّين مادة قنّب، ومنها على سبيل المثال رباعي هيدرو كانابينول (δ9-Tetrahydrocannabinol (THC)) (الشكل 11)، وكان يُستخدم قديمًا دواءً نفسيًّا، وحظر استخدامه في ما بعد في معظم أنحاء العالم.
- القلويدات البوليكيتيدية: قد تكون المركّبات الأكثر شهرة في هذه المجموعة هي قلويدات البيبيريدين (Piperidine) (الشكل 11) المستخلصة من الشوكران السام (Conium maculatum)، واستُخدِمت لإعدام الفيلسوف اليوناني سقراط.
عادة تُكوَّن قلويدات البيبيريدين من الحمض الأميني لايسين، أما السلسلة الكربونية لقلويدات البيبيريدين في الشوكران فإنها تتكون من أربع وحدات أسيتات[37].
التربينات
تُسمّى التربينات (Terpenes) أيضًا "آيزوبرينويدات" (Isoprenoids)، وتُعد أكبر مجموعة من النواتج الطبيعية في النباتات، وتضمّ أكثر من 40000 صيغة مختلفة[38]. التربينات مشتقة من وحدات الآيزوبرين (Isoprene) المكوّنة من خمس ذرات كربون، ووفقًا لعدد جزيئات الآيزوبرين المدمجة، يمكن تصنيفها إلى هيميتربين (C5)، وأحادي تربين (C10)، وسيسكيتربين (C15)، وثنائي تربين (C20)، وثلاثي تربين (C30)، ورباعي تربين (C40)، ومتعدد تربين مثل المطاط (الشكل 12)[39].
[الشكل12]
 بعض التربينات المشتقة من وحدات الآيزوبرين
بعض التربينات المشتقة من وحدات الآيزوبرين
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
- هيمي تربين: يعتبر الآيزوبرين أكثر هيمي تربين (Hemiterpene) وفرة من النباتات، وهو مركّب متطاير بسبب وزنه الجزيئي القليل نسبيًا. يُنتَج الآيزوبرين وينبعث على نطاق واسع جدًا في النباتات، لا سيّما أشجار الحور. ينبعث الآيزوبرين في الغلاف الجوي كي يحمي الأوراق من درجات الحرارة العالية للبقاء على قيد الحياة فترات قصيرة، إضافة إلى أنه يزيد من قدرة تحمّل النبات لأنواع الأوزون.
- التربينات الأحادية: تتكون التربينات الأحادية (Monoterpenes) من اتحاد جزيء ثنائي ميثيل أليل بيروفوسفات (Dimethylallyldiphosphate (DMAPP)) وجزيء آيزوبنتنيل بيروفوسفات (Isopentyl diphosphate (IPP))، إذ يُربطان في معظم الحالات من الرأس إلى الذيل، لينتج من ذلك المركّب الوسيط جيرانيل بيروفوسفات (Geranyl diphosphate (GPP)). يمكن ارتباط ذرات جزيء الجيرانيل بيروفوسفات بعدة طرق لإنتاج هياكل أحادية الحلقات وثنائية الحلقات وثلاثية الحلقات، وقد تخضع لتفاعلات أخرى لإنتاج أكثر من 1000 صيغة أحادي تربين مختلفة[40].
- السيسكيتربينات: تحتوي السيسكيتربينات (Sesquiterpenes) على ثلاث وحدات آيزوبرين، وتتشكل عن طريق ارتباط جزيء ثنائي ميثيل أليل بيروفوسفات مع جزيئَي آيزوبنتنيل بيروفوسفات. يعتبر جزيء فارنيسيل بيروفوسفاتFarnesyldiphosphate (FPP)) ) مركّبًا وسيطًا، وقد يتشكّل بطرق مختلفة لإنتاج مركّبات أحادية الحلقات أو ثنائية الحلقات أو ثلاثية الحلقات.
- التربينات الثنائية: تتكون التربينات الثنائية (Diterpenes) من جزيء ثنائي ميثيل أليل بيروفوسفات، وثلاثة جزيئات آيزوبنتنيل بيروفوسفات التي ينتج عنها مستقلَب (الناتج الوسطي Metabolite;) جيرانيل جيرانيل بيروفوسفات (Geranyl geranyl diphosphate (GGPP)). ترتبط ذرات الناتج الوسطي جيرانيل جيرانيل بيروفوسفات بطرق مختلفة لتكوّن العديد من الهياكل الحلقية المختلفة.
- التربينات الثلاثية: تتكون التربينات الثلاثية (Triterpene) من اتّحاد جزيئَي فارنيسيل بيروفوسفات من خلال ارتباط الذيل بالذيل لتكوين جزيء السكوالين (Squalene). من خلال تدوير مستقلب 2،3-أوكسيدوسكوالين (2,3-oxidosqualene) وإعادة الترتيب الجزيئِي وتحوّلات الميثيل ينتج هياكل لمركبات مختلفة، معظمها حلقات رباعية أو خماسية. يُعتبر
الكوليسترول الذي يتكون من 27 ذرة كربون من الأمثلة على هذه المركبات الحلقية بعد فقدان ثلاث مجموعات ميثيل. على عكس الحيوانات، يُعتبر
الكوليسترول هو الستيرول الرئيس، إذ تُضاف مجموعة ميثيل أو إيثيل في العديد من الستيرولات النباتية (Phytosterols) على كربون رقم 24 من السلسلة الجانبية، مثل ستغماستيرول (Stigmasterol). تشكّل الستيرولات النباتية مكوّنات
الأغشية الحيوية في النباتات وتؤثر في نفاذيتها، وتمنع امتصاص
الكوليسترول في الحيوانات. وبسبب أنها أقل قطبية من
الكوليسترول، فهي تندمج بسهولة أكبر في المذيلات التي تشارك في هضم
الدهون.
- التربينات الرباعية: تتكون التربينات الرباعية (Tetraterpenes) من اتحاد جزيئَي جيرانيل جيرانيل بيروفوسفات من خلال ارتباط الذيل بالذيل. تشكّل التربينات الرباعية مجموعة واحدة فقط من المركّبات وهي الكاروتينات. تتميز الكاروتينات باللون الأصفر والبرتقالي والأحمر بسب احتوائها على روابط ثنائية بنظام مترافق (نظام للذرات المرتبطة تساهميًا بتبادل فردي وزوجي). يتم تشكيل أحد طرفي سلسلة التربينات الرباعية أو كليهما لترتبط بحلقة سداسية كما يحدث في مركّب البيتا كاروتين (β -carotene).
- التربينات العديدة (Polyterpenes): جزيئات كبيرة تتكون من العديد من وحدات الآيزوبرين، ويعدّ المطاط الطبيعي من أكثر مركبات هذه المجموعة انتشارًا[41].
مصادر النواتج الطبيعية
يُمكن استخلاص النواتج الطبيعية من الخلايا والأنسجة وإفرازات
الكائنات الحية الدقيقة (Microorganisms) والنباتات والحيوانات[42]. يعتمد التنوع الكيميائي في الطبيعة على
التنوع البيولوجي، لذلك يأخذ الباحثون حول العالم عيّنات من مختلف مصادرها لتحليلها وتقييم آثارها البيولوجية للتوصية باستخدامات طبية مناسبة. يمكن استخدام هذه الجزيئات النشطة بيولوجيًا (Bioactive molecules) في اكتشاف
الأدوية وتطويرها بشكل مباشر كما هي، أو يمكن تعديلها صناعيًا لتعزيز الخصائص البيولوجية أو تقليل الآثار الجانبية[43]. ومن الأمثلة على المصادر البيولوجية للنواتج الطبيعية:
الكائنات بدائية النواة
بدائيات النوى {{بدائيات النوى (Prokaryotes): كائنات حية وحيدة الخلية، تُعد من أقدم أشكال الحياة على الأرض، تُعرف بـبدائية النواة لأنها لا تحتوي على نواة حقيقية أو أي عضيات أخرى محاطة بغشاء (مثل الميتوكوندريا أو الشبكة الإندوبلازمية) وهي بسيطة في التركيب، ولها جدار خلوي، وتكون أضغر حجمًا من الخلايا حقيقية النواة.}} هي
كائنات وحيدة الخلية تفتقر إلى نواة محاطة بغشاء (كاريون) أو
ميتوكوندريا (Mitochondria) أو أية عضية (Organelle) أخرى محاطة بغشاء داخل الخلية. يمكن تقسيم بدائيات النوى إلى نوعين؛
العتائق {{العتائق (Archaea): كائنات حية وحيدة الخلية تُشبه البكتيريا في مظهرها، ولكنها تختلف عنها بشكل كبير على المستوى الجيني والكيميائي الحيوي. تُعتبر العتائق من أقدم أشكال الحياة على الأرض، وهي فرع رئيس في شجرة الحياة منفصل تمامًا عن البكتيريا وحقيقيات النوى، تعيش في بيئة ذات ظروف قاسية مثل البحر الميت، وتؤدي دورًا مهمًا في النظم البيئية، وتسهم في إنتاج الغازات الدفيئة مثل الميثان.}} والبكتيريا (Bacteria). في
بدائيات النوى، توجد جميع المكوّنات القابلة للذوبان في الماء داخل الخلايا (البروتينات والحمض النووي والمستقلَبات) معًا في
السيتوبلازم (Cytoplasm) المحاط
بغشاء الخلية، وليس في حجيرات خلوية متخصصة منفصلة كما في
حقيقيات النوى {{حقيقيات النوى (Eukaryotes): مجموعة واسعة من الكائنات الحية التي تتميز بخلايا تحتوي على نواة حقيقية وعضيات أخرى، مثل: الميتوكوندريا والبلاستيدات الخضراء وأجسام غولجي. تُعتبر حقيقيات النواة أكثر تعقيدًا وتطورًا من بدائيات النواة، وتتكاثر عن طريق الانقسام المتساوي أو الانقسام المنصف.}}.
[الشكل13]
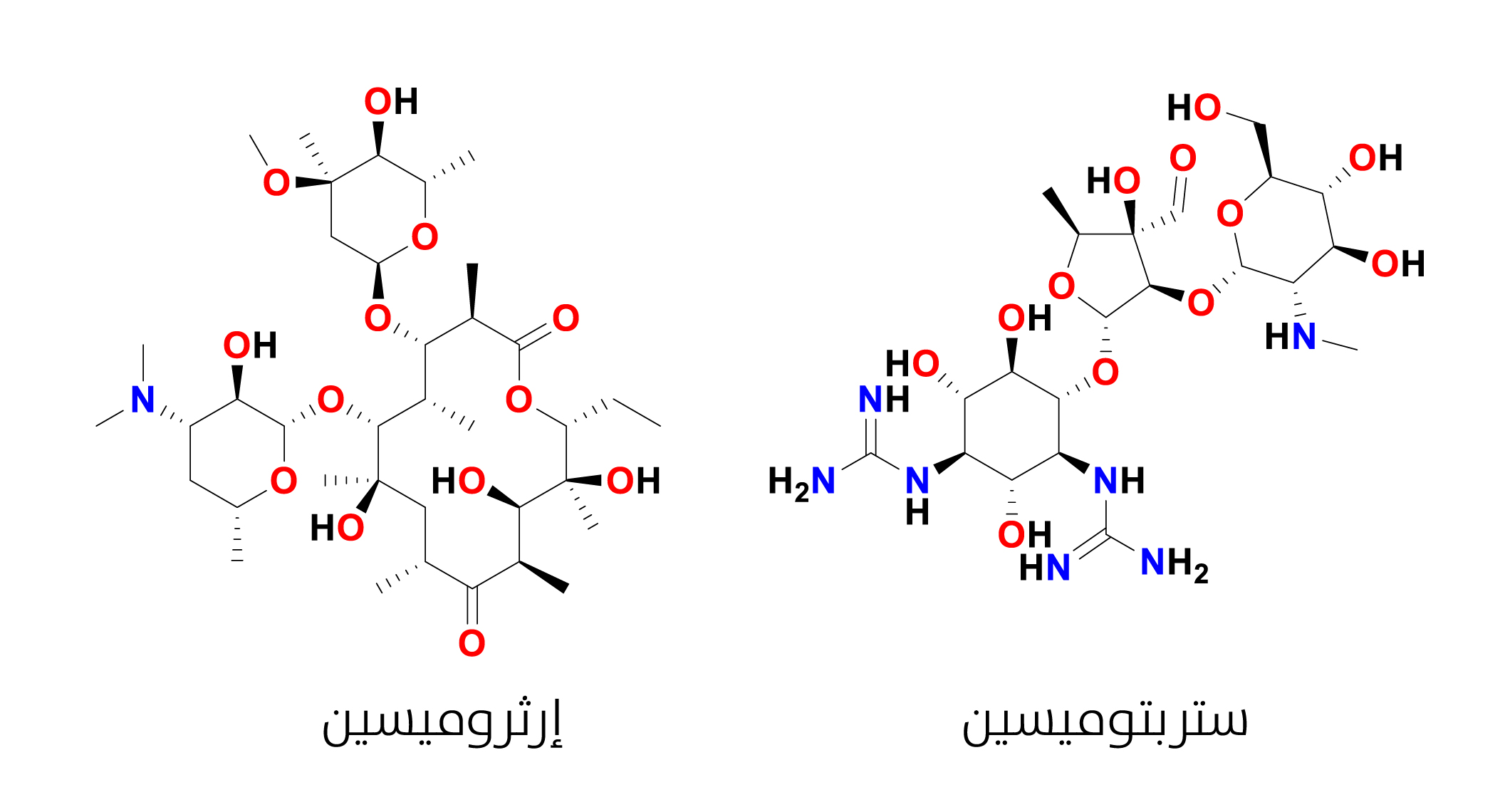 بعض النواتج الطبيعية البكتيرية
بعض النواتج الطبيعية البكتيرية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
بالنسبة إلى
البكتيريا، وهي الكائنات الحية الأولى في تاريخ الكرة الأرضية، فلها عدد من الأشكال، بدءًا من الأشكال الكروية إلى الأشكال العصوية واللولبية. يبلغ طول الخلية البكتيرية عادةً بضعة ميكرومترات. كانت
البكتيريا من أوائل أشكال الحياة التي ظهرت على الأرض، وهي موجودة في معظم بيئاتها. فتسكن
البكتيريا التربة والمياه والينابيع الساخنة الحمضية والنفايات المشعة والأجزاء العميقة من القشرة الأرضية، مثلما تسكن في داخل
الجهاز الهضمي للحيوانات ومن ضمنها الإنسان. تُعتبر
البكتيريا مصدرًا بارزًا للمنتجات الطبيعية، ومن الأمثلة على النواتج الطبيعية البكتيرية مركبات الإيريثروميسين (Erythromycin) والستريبتوميسين (Streptomycin) (الشكل13) المستخدمة
مضاداتٍ حيوية (Antibiotics)، ولها تأثير كبير على المجتمعات البشرية بسبب قدرتها على إنقاذ الحياة.
أما
العتائق فإنّها على العكس من اسمها تطورت بعد
البكتيريا، فقد اكتُشِفَت في عام 1977. وقد اكتشفها الباحثان كارل ووز (Carl Woese) وجورج إي فوكس (George E. Fox) وعدّاها فرعًا منفصلًا من
الكائنات بدائية النواة القديمة استنادًا إلى التسلسل الجيني[44]. يُذكر أن العديد من
العتائق تكيّفت مع الحياة في البيئات القاسية مثل المناطق القطبية، والينابيع الساخنة، والينابيع الحمضية، والينابيع القلوية، والبحيرات المالحة والبحر الميت بين فلسطين والأردن، والضغط العالي لمياه المحيطات العميقة.
على سبيل المثال، يعدّ بيروكوكوس فوريوسوس (Pyrococcus furiosus) نوعًا من
العتائق المحبّة للظروف القاسية، إذ يمكن تصنيفه على أنه محبّ للحرارة المرتفعة؛ لأنه يتكاثر بشكل أفضل في ظروف ذات درجات حرارة مرتفعة للغاية[45]. في عام 2014، عزل فريق بحث الدكتور كينغ دونغ (Qing Dong) إنزيم بيتا غالاكتوسيداز (β-galactosidase) من هذا النوع من
العتائق الذي يمتاز بثباته على درجة حرارة عالية ويمكنه تفكيك اللاكتوز (سكر ثنائي السكاريد موجود في الحليب)[46].
الكائنات حقيقية النواة
تشتمل
الكائنات حقيقية النواة على ثلاث ممالك رئيسة:
الفطريات (Fungi)، والنباتات (Plantae)، والحيوانات (Animalia). أما في التصنيفات القديمة، فكان هناك مملكة رابعة وهي
الطلائعيات {{الطلائعيات (Protista): مجموعة متنوعة من الكائنات الحية حقيقية النواة، أي أن خلاياها تحتوي على نواة محاطة بغشاء. تُعتبر الطلائعيات مملكة منفصلة في التصنيف البيولوجي، فكائناتها لا تصنف على أنها حيوانات، أو نباتات، أو فطريات. ومعظم الطلائعيات كائنات حية وحيدة الخلية، لكن بعضها يتكون من عدة خلايا، ويعيش معظمها في بيئة مائية أو داخل أجسام الكائنات الحية الأخرى.}} مصنفةً مملكة منفصلة، وفيها كائنات بسيطة لا تُعتبر
فطريات أو نباتًا أو حيوانًا. إلا أنها، ومع تطور طرق التسلسل الجيني، أظهرت تنوّعًا جينيًا وبيئيًا كبيرًا للغاية في جميع البيئات. إن تنوعها الهائل يفوق تنوع جميع
حقيقيات النوى الأخرى.
الفطريات
[الشكل14]
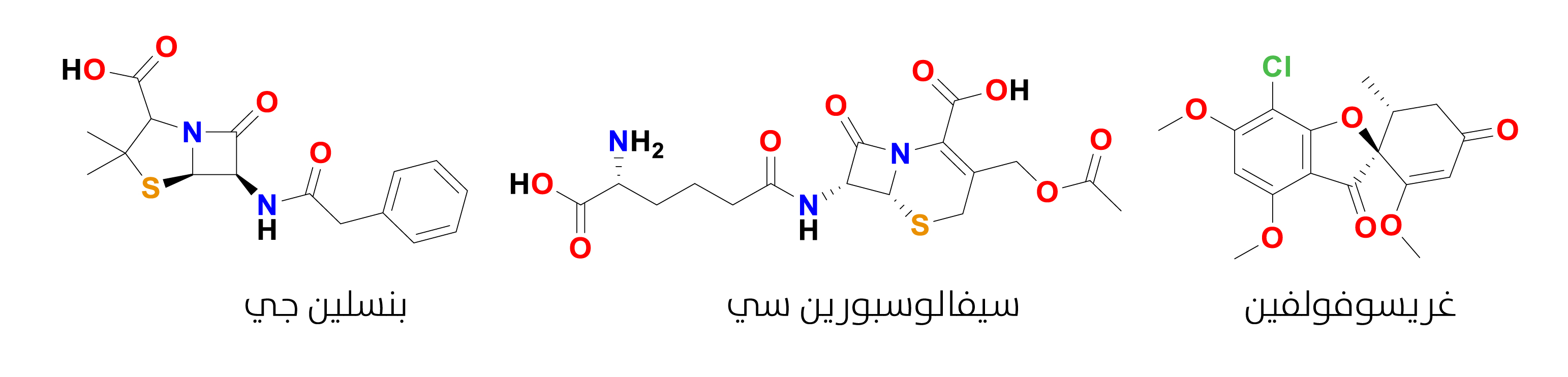 بعض النواتج الطبيعية الفطرية
بعض النواتج الطبيعية الفطرية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تُعتبر
الفطرياتكائنات غيريّة التغذية (Heterotrophs)،
حقيقية النواة، إما وحيدة الخلية أو متعددة الخلايا، وهي في المقام الأول كائنات محلّلة في البيئة. وتمتاز هذه الكائنات الحية بأنها لا تستطيع إنتاج طعامها بنفسها. وتشمل الكائنات وحيدة الخلية مثل الخميرة والعفن، والكائنات متعددة الخلايا التي لها أجسام مثمرة مثل
الفطر. تُنتج
الفطريات عددًا لا يُحصى من النواتج الطبيعية الثانوية، بعضها شديد السميّة، وبعضها له فائدة كبيرة في التطبيقات الطبية[47]. على سبيل المثال، استُخلِص العديد من
الأدوية المضادة للعدوى من
الفطريات بما في ذلك
البنسلين {{البنسلين: أول مضاد حيوي مُكتشَف، ويُعتبر أحد أهم الاكتشافات في تاريخ الطب. يمنع بناء جدران الخلايا البكتيرية، ويُستخدم لعلاج مجموعة واسعة من الالتهابات البكتيرية، وقد أنقذ حياة الملايين منذ أن اكتشفه العالم ألكسندر فلمنغ عام 1928.}} (المفصول من Penicillium chrysogenum) والسيفالوسبورين (المفصول من Cephalosporium acremonium) اللذان يُستخدمان بصفتِهما أدوية
مضادة للبكتيريا، والغريسيوفولفين (المفصول من Penicillium griseofulvum) ويستخدم
مضادًا للفطريات (الشكل 14). المستقلَب الفطري الآخر المفيد طبيًا هو اللوفاستاتين (المفصول من Aspergillus terreus)، الذي أصبح رائدًا في سلسلة من الأدوية المستخدمة لخفض مستويات
الكوليسترول في الدم.
أدّى اكتشاف
البنسلين بالصدفة وفاعليته البيولوجية إلى إجراء أبحاث واسعة النطاق على
الكائنات الحية الدقيقة الأخرى التي قد تُنتج منتجات طبيعية مضادة للعدوى. لذلك جُمِعت عيّنات التربة والمياه من جميع أنحاء العالم؛ ما أدّى إلى اكتشاف الستربتوميسين (المشتق من بكتيريا Streptomyces griseus)، وإدراك أن
البكتيريا، وليس
الفطريات فقط، تمثل مصدرًا مهمًا للمنتجات الطبيعية
المضادة للبكتيريا[48].
النباتات
[الشكل15]
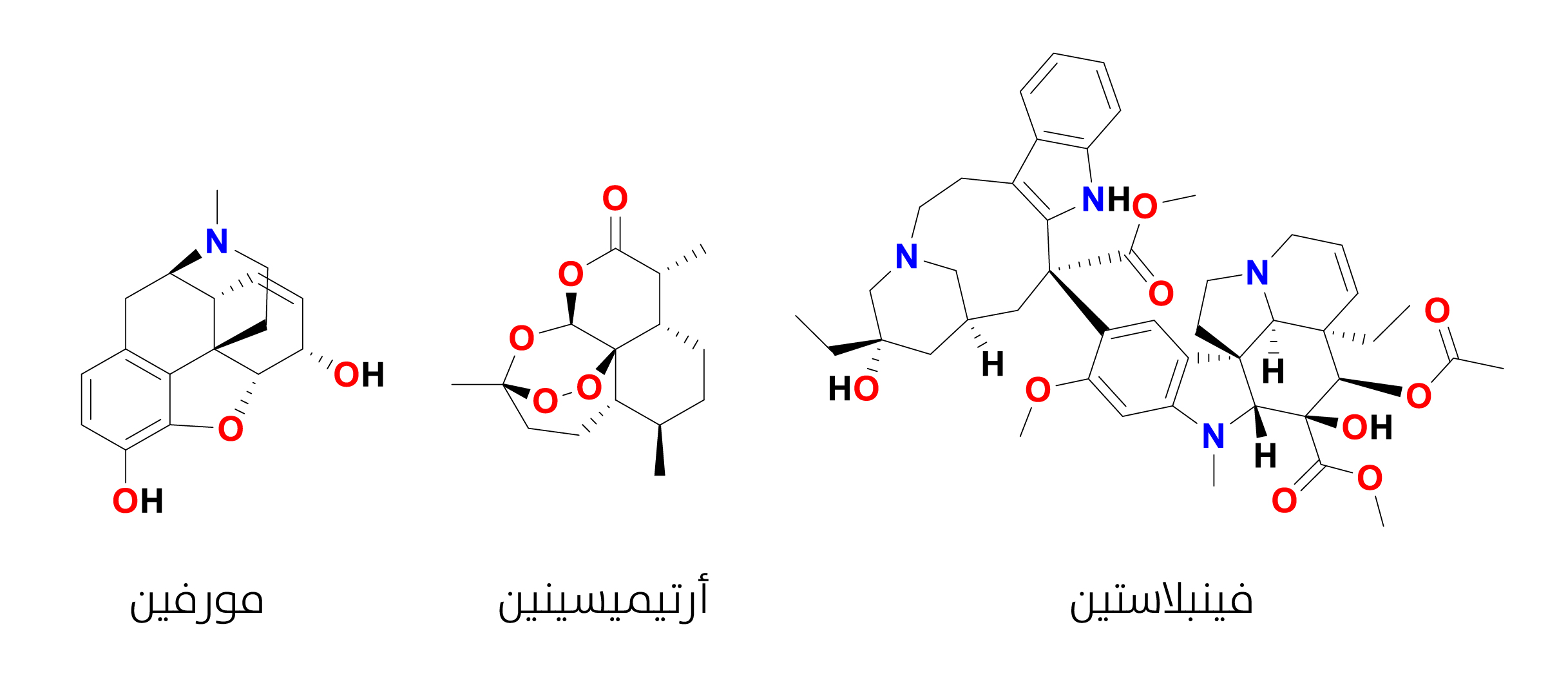 بعض النواتج الطبيعية النباتية
بعض النواتج الطبيعية النباتية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تُعتبر الكائنات المصنَّفة في المملكة النباتية
كائنات حقيقية النواة متعدّدة الخلايا
ذاتية التغذية (Autotrophs)؛ فهي قادرة على إنتاج طعامها بنفسها بوساطة
عملية البناء الضوئي (Photosynthesis) باستخدام الطاقة الضوئية من الشمس لتحويل ثاني أكسيد الكربون والماء إلى سكّريات بسيطة. يُعتبر الأكسجين منتجًا ثانويًا لهذه العملية، ومن ثمّ تُعتبر النباتات مصدرًا رئيسًا للأكسجين على الكوكب. بالإضافة إلى إنتاجها الأكسجين واستخدامها مصدرًا للغذاء، تُعتبر النباتات أيضًا مصدرًا رئيسًا للمستقلَبات الثانوية المعقّدة والمتنوعة هيكليًا. على الرغم من أن عدد النباتات التي دُرِست على نطاق واسع صغيرٌ نسبيًا، فقد حُدِّدت العديد من النواتج الطبيعية النشطة دوائيًا واستُخدمت في العلاجات الطبيّة. تشمل الأمثلة المركّبات
المضادة للسرطان مثل الفينبلاستين (Vinblastin) المفصول من نبات الكتارنتوس الوردي (Catharanthus roseus)، ومركب الأرتيميزينين
المضاد للملاريا المفصول من نبات الشيح الحولي (Artemisia annua)، والمخدّرات المسكّنة مثل
المورفين {{المورفين: مسكن ألم قوي ينتمي إلى فئة من الأدوية تُسمى الأفيونات، يُستخرج بشكل طبيعي من نبتة الخشخاش الأفيوني، ويُعتبر أحد أقوى المسكنات المتاحة لعلاج الآلام الحادة والمزمنة. يعمل من خلال ارتباطه بمستقبلات أفيونية موجودة في الجهاز العصبي المركزي، فيمنع إشارات الألم من الوصول إلى الدماغ.}} المفصول من الخشخاش المنوم (Papaver somniferum) (الشكل 15).
الحيوانات
هي كائنات حيّة متعددة
الخلايا حقيقية النواة تنتمي إلى المملكة الحيوانية وتُعتبر
كائنات غيرية التغذية. تُمثّل الحيوانات أيضًا مصدرًا للمنتجات الطبيعية النشطة بيولوجيًا. على وجه الخصوص، جذبت الحيوانات السامة مثل الثعابين والعناكب والعقارب واليرقات والنحل والدبابير والنمل والضفادع الكثير من الاهتمام؛ وذلك لأن مكونات السم (الببتيدات والإنزيمات والنيوكليوتيدات والدهون وغيرها) غالبًا ما يكون لها تفاعلات محدّدة جدًا مع هدف جزيئي كبير في الجسم. كما هو الحال مع رادعات التغذية النباتية، يُعزى هذا النشاط البيولوجي إلى الانتقاء الطبيعي، فالكائنات الحية القادرة على قتل فرائسها أو شلّها و/أو الدفاع عن نفسها ضد الحيوانات المفترسة تكون أكثر عرضة للبقاء والتكاثر. على سبيل المثال، الكلوروتوكسين ببتيد مكوّن من 36 حمضًا أمينيًا موجودًا في سم العقرب الأصفر (Leiurus quinquestriatus)، وهو يثبّط قنوات الكلوريد قليلة التوصيل.
هناك أيضًا سمّ الألفا-كوبراتوكسين (α-Cobratoxin) الذي يُعتبر سمًا عصبيًا من سموم بعض أجناس الكوبرا، بما في ذلك الكوبرا التايلاندية، والكوبرا الهندية الصينية الباصقة (Naja siamensis)، والكوبرا الصينية (Naja atra)، ويُعزى فتك سموم الكوبرا إلى أنها تُصنّف من ضمن السموم القلبية والعصبية. تعيش الكوبرا التي تنتج السم في المناطق الاستوائية وشبه الاستوائية في أفريقيا وآسيا. السم الذي تنتجه هذه الثعابين خليط من
البروتينات والكربوهيدرات ومواد أخرى. يُستخدم السم فقط عندما يحتاجه الثعبان للبقاء على قيد الحياة؛ لأن إنتاجه يكلّف الكثير من الجهد. إذا لم يكن تسميم الجسم ضروريًا، فيمكن للكوبرا أن تعض من دون أن تفرز السم. في حال استخدمت الكوبرا سمها، فإنها تحاول في الغالب شلَّ حركة فريستها أو قتلها. يعمل ألفا-كوبراتوكسين بوصفه مضادًا لمستقبِلات الأسيتيل كولين النيكوتينية (Nicotinic acetylcholine receptors, nAChR) الذي يسبب الشلل عن طريق منع ربط
الأسيتيل كولين بالمستقبِل الخاص به. يسبب السم في البداية عرقلة انتقال
السيالات العصبية، وتظهر الأعراض الأوّلية للشلل بتدلّي الجفن وشلل العين الخارجي، والسبب في ذلك هو أن عضلات العين أكثر عرضة للتأثّر بالسم مقارنة بالعضلات الأخرى، بسبب عرقلة انتقال
السيالات العصبية. تؤدّي لدغة الكوبرا إلى شلل العضلات، وبسبب هذا الشلل قد تتطور مشاكل في
الجهاز التنفسي؛ ما قد يؤدي إلى الوفاة[49].
[الشكل16]
/_أحد النواتج الطبيعية الحيوانية (التيترودوتوكسين).jpg) أحد النواتج الطبيعية الحيوانية (التيترودوتوكسين)
أحد النواتج الطبيعية الحيوانية (التيترودوتوكسين)
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
ومن الأمثلة الأخرى على السموم الحيوانية سموم الحلزون، فهي مجموعة من الببتيدات النشطة بيولوجيًا. على الرغم من وجود أكثر من 800 نوع معروف من الحلزون يُنتج كلٌّ منها أكثر من 1000 ببتيد سام، فقد شُخِّص ودُرِس نحو 150 نوعًا من الببتيدات السامة من الناحية الهيكلية والوظيفية. تُمثّل ببتيدات سم الحلزون مصدرًا مثاليًا لاستخراج الأدوية المحتملة المرشّحة، إلا أنّ التطور في الاكتشاف في كثير من الأحيان يكون محدودًا لأسبابٍ منها أن الكميّة التي فُصِلت قليلة وطرق تشخيص النواتج قليلة الحساسية[50]. وهناك التيترودوتوكسين (Tetrodotoxin) (الشكل 16)، الذي يُعتبر سُمًّا عصبيًّا قويًا، وقد جرى التعرّف إليه في عدة أنواع من الأسماك مثل أسماك الينفوخ وأسماك النيص وغيرها، إضافة إلى وجوده في العديد من الحيوانات الأخرى، وكان البروفيسور يوشيزومي تهارا (Yoshizumi Tahara) هو من أطلق عليه هذا الاسم في عام 1909. يعد التيترودوتوكسين أحد أقوى السموم غير البروتينية المعروفة، وهو المسؤول عن العديد من حالات التسمم الناتجة من الأسماك. يُعتقد أن هذا السم أحد أقدم السموم الطبيعية المعروفة المسجّلة في الأدب الصيني والمصري، ويُعَدّ سُمًا مميتًا، كما أن استعمال كمية ضئيلة جدًا منه تسبّب الشلل[51].
الطلائعيات
[الشكل17]
 أحد النواتج الطبيعية الطلائعية
أحد النواتج الطبيعية الطلائعية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
من الأمثلة على الطلائعيات
اليوغلينا {{اليوغلينا: أحد الأمثلة على الطلائعيات، لها خصائص فريدة، إذ تجمع بين خصائص النباتات والحيوانات؛ فهي قادرة على الحركة باستخدام السوط، وتمتلك بقعة حساسة للضوء فتؤدي بعملية التمثيل الضوئي لاحتوائها على البلاستيدات الخضراء، ولكنها في معظم الوقت تكون في بيئة مظلمة، لذلك تكون غير ذاتية التغذية. أما تكاثرها فلاجنسي.}}، (Euglena) وتُعتَبر من الكائنات وحيدة الخلية، وتشمل نحو 200 نوع، وتعيش في مياه البرك والمستنقعات العذبة. تتحرك
اليوغلينا بوساطة السوط، ولديها
بلاستيدات خضراء {{البلاستيدات الخضراء: عضيات توجد في خلايا النباتات والطحالب، وظيفتها الرئيسة أداء عملية التمثيل الضوئي، إذ تُحوّل طاقة ضوء الشمس إلى طاقة كيميائية يستخدمها النبات في إنتاج الغلوكوز. توجد فيها أقراص مكدسة تُدعى الغرانا، تحتوي على الكلوروفيل الذي يمتص ضوء الشمس، وهذه الأقراص موجودة في سائل يُدعى الستروما، تحدث فيه التفاعلات التي تنتج الغلوكوز من ثاني أكسيد الكربون والماء.}} تؤدّي
عملية البناء الضوئي. من النواتج الطبيعية التي جرى التعرّف إليها في اليوغلينا الدموية (Euglena sanguinea) الكاروتينات مثل الدياتوكسانثين (Diatoxanthin) (الشكل 17) واللوتين (Lutein) والبيتا كاروتين (β-carotene)، وذلك يؤكد عل أهميتها بصفتها مصدرًا محتملًا لإنتاج المكمّلات الغذائية[52].
طرق فصل النواتج الطبيعية
توجد جميع المنتجات الطبيعية في هيئة مخاليط مع مركّبات أخرى من المصدر الطبيعي، وغالبًا ما تكون مخاليط معقّدة للغاية، ويجب فصل المنتج المعني وتنقيته منها بهدف توضيح التركيب الكيميائي، وعمل الاختبارات البيولوجية. تعتمد الكمية المفصولة على الطريقة المستخدمة، ولكنّها عادة ما تكون بنسب قليلة جدًا[53].
تُحَدَّد بنية المركّبات المستخلَصة باستخدام الطرق المطبّقة لتحديد التركيب الكيميائي لمنتج طبيعي، وهي عملية تتضمن مجموعة من الطرق الكيميائية والفيزيائية التي تُحدد وتُقاس من خلالها الخصائص الفيزيائية، مثل: نقطة الانصهار (Melting point)، ونقطة الغليان (Boiling point)، وتحديد الوزن الجزيئي، واستخدام تقنية الرنين المغناطيسي النووي (Nuclear magnetic resonance)، وفي بعض الأحيان تصوير البلورات الجزيئية الصغيرة. على سبيل المثال، حدّدت
دوروثي هودجكين (Dorothy Hodgkin) التركيب الكيميائي
للبنسلين، وهو العمل الذي حصلت بسببه لاحقًا على جائزة نوبل في الكيمياء عام 1964[54].
تبدأ عملية فصل النواتج الطبيعية من النباتات بتقطيع الأجزاء النباتية وطحنها في معظم الأحيان، ويتخلل عملية فصل النواتج الطبيعية من مصدرها الطبيعي العديد من المشكلات. تشمل هذه المشكلات استقرار المذيبات والنواتج المستخلصة واستقطابها، وتطاير المذيب المستخدم وسُمّيته ونقاءَه ولُزوجَتِه[55]. ومن الطرق المستخدمة لفصل النواتج الطبيعية[56]:
- التقطير
تُفصَل المواد المتطايرة، مثل
الزيوت الأساسية {{الزيوت الأساسية (Essential oils): مركبات عطرية مركزة تُستخلص من النباتات، تحمل رائحة النبات المميزة ونكهته وخصائصه العلاجية. لا تُعتبر الزيوت الأساسية زيوتًا بالمعنى الكيميائي، فهي لا تحتوي على دهون، بل هي مركبات متطايرة تتبخر بسهولة عند تعرضها للهواء، ويمكن استخلاصها بطرق عديدة منها التقطير بالبخار وبالضغط البارد. تستخدم هذه الزيوت في العلاجات ومنتجات التجميل والمنظفات.}}، من خلال عملية
التقطير (Distillation)، مع أن العمل في درجات حرارة مرتفعة يمكن أن يؤدي إلى تغيرات كيميائية في النواتج الطبيعية، لذلك أُدخِلت تحسينات على منهجية
التقطير، كعملية
التقطير بالبخار {{التقطير بالبخار (Steam distillation): عملية فصل كيميائية تُستخدم لاستخلاص الزيوت الأساسية من المواد النباتية. وتُعد هذه الطريقة الأشيع والأكثر فاعلية لاستخراج المركبات العطرية المتطايرة من النباتات.}}؛ تجنّبًا لاستخدام درجات حرارة عالية للحفاظ على النواتج الطبيعية كما هي.
- فصل المنتجات الطبيعية باستخدام التقنيات
الكروماتوغرافية
يمكن استخدام مجموعة واسعة من الطرق
الكروماتوغرافية (Chromatography) من أجل فصل النواتج الطبيعية وتنقيتها، ومن أكثرها استخدامًا
الكروماتوغرافيا العمودية (Column chromatography)
وكروماتوغرافيا الطبقة الرقيقة (Thin layer chromatography).
- فصل المنتجات الطبيعية باستخدام المذيبات الكلاسيكية
لا تزال معظم عمليات الفصل تستخدم طرق الفصل باستخدام المياه والمذيبات العضوية {{المذيبات العضوية: مركبات كيميائية تُستخدم لإذابة مواد أخرى (المذابات) لتكوين محاليل عضوية. وتسمى بالعضوية لأنها تحتوي على الكربون في تركيبها. وتتميز بقدرتها على إذابة المواد غير القطبية مثل الدهون والزيوت والشموع، على عكس الماء الذي يُعتبر مذيبًا قطبيًا، ويذيب المواد القطبية مثل الأملاح.}} (Organic solvents). تتضمن هذه العمليات النقع
والترشيح {{الترشيح: عملية فيزيائية تُستخدم لفصل المواد الصلبة غير الذائبة عن السوائل أو الغازات، باستخدام حاجز مسامي يُسمى المرشح. يعمل هذا المرشح عمل الشبكة، إذ يسمح بمرور السائل (الراشح) أو الغاز من خلاله، في حين يحتجز الجزيئات الصلبة الأكبر حجمًا.}} (Filtration) وجهاز السوكسلت (Soxhlet extractor) والاستخلاص الارتجاعي (Reflux extraction) وغيرها. وعندما يكون الغرض من النواتج الطبيعية هو استعمال دوائي أو علاجي، فإن المذيب الذي يُستخدم هو الماء، سواء بالطريقة الباردة، وهي عملية نقع الأجزاء النباتية بالماء من دون التسخين، أو الطريقة الساخنة، وهي عملية غلي الأجزاء النباتية بالماء في درجات حرارة مختلفة حسب طبيعة المادة المراد استخلاصها.
- استخراج بمساعدة الموجات فوق الصوتية
تُوضَع المادة بشكل عام في وعاء زجاجي، وتُنقَع في مذيب الاستخلاص، ثم تُوضَع في حمام بالموجات فوق الصوتية، إذ يُقلّل من وقت الاستخراج، ويعزّز من نسبة النواتج المستخلَصة. يمكن أيضًا استخدام الاستخراج بمساعدة الموجات فوق الصوتية مع مخاليط المذيبات غير القابلة للامتزاج، مثل الهكسان (hexane) مع الميثانول والماء. لكن هذه العملية تولّد حرارة، لذا فقد تؤدي إلى تكسير في بنية الجزئيات المراد فصلها.
- استخراج بمساعدة السوائل الأيونية
حظي استخدام السوائل الأيونية في فصل النواتج الطبيعية باهتمام متزايد. تستطيع السوائل الأيونية إذابة أنواع مختلفة من النواتج الطبيعية القطبية أو غير القطبية، ولها ضغط بخار منخفض، ولها قابلية احتراق منخفضة.
المراجع
Abegaz, Berhanu M., and Henok H. Kinfe. “Secondary Metabolites, Their Structural Diversity, Bioactivity, and Ecological Functions: An Overview.” Physical Sciences Reviews, vol. 4, no. 6 (2019).
“Alkaloids Derived from Phenylalanine and Tyrosine.” In Alkaloids, edited by Shinji Funayama and Geoffrey A. Cordell, 21–61. London: Academic Press, 2015.
Ascherio, Alberto et al. “Coffee Consumption, Gender, and Parkinson’s Disease Mortality in the Cancer Prevention Study II Cohort: The Modifying Effects of Estrogen.”
Am. J. Epidemiol. vol. 160, no. 10 (2004). pp. 977-984.
Ashihara, Hiroshi & Crozier Alan. “Caffeine: a well known but Little Mentioned Compound in Plant Science.”
Trends Plant Sci. vol. 6, no. 9 )2001(. pp. 407-413.
Bhambhani, S., K. R. Kondhare, and A. P. Giri. “Diversity in Chemical Structures and Biological Properties of Plant Alkaloids.” Molecules, vol. 26, no. 11 (2021).
Benowitz, Neal L. “Clinical Pharmacology of Caffeine.”
Annual Review Medicine. vol. 41 (1990). pp. 277-288.
Breitmaier, Eberhard. Terpenes: Flavors, Fragrances, Pharmaca, Pheromones. Weinheim: Wiley-VCH, 2006.
Bunsupa, Somnuk, Yamazaki Mami & Satio Kazuki. “Quinolizidine Alkaloid Biosynthesis: Recent Advances and Future Prospects.”
Front. Plant Sci. vol. 3 (2012).
Dewick, Paul M.
Medicinal Natural Products: A Biosynthetic Approach. 3rd ed. Chichester : Wiley, A John Wiley & Sons. 2009.
Dey, P., A. Kundu, A. Kumar, M. Gupta, B. M. Lee, T. Bhakta, S. Dash, and H. S. Kim. “Analysis of Alkaloids (Indole Alkaloids, Isoquinoline Alkaloids, Tropane Alkaloids).” In Recent Advances in Natural Products Analysis, edited by A. M. Giuffrè, S. F. Nabavi, and M. R. Silva,. Amsterdam: Elsevier, 2020.
Dong, Qing et al. “Characterization of an extremely thermostable but cold-adaptive β-galactosidase from the hyperthermophilic archaeon Pyrococcus furiosus for use as a recombinant aggregation for batch lactose degradation at high temperature.”
Journal Biosci Bioeng. vol. 117, no. 6 (2014). pp. 706-710.
Friedman, Jacob & George R. Waller. “Caffeine Hazards and Their Prevention in Germinating Seeds of Coffee (Coffea Arabica L.).” Journal of Chemical Ecology. vol. 9, no. 8 (1983). pp. 1099-1106.
Gershenzon, J., and N. Dudareva. “The Function of Terpene Natural Products in the Leaf of a Plant.” Nature Chemical Biology, vol. 3, no. 7 (2007): 408–414.
Harborne, Jeffrey Barry & Herbert Baxter.
The Handbook of Natural Flavonoids. New York: Wiley, 1999.
Hartmann,Thomas & Dietrich Ober. “Biosynthesis and Metabolism of Pyrrolizidine Alkaloids in Plants and Specialized Insect Herbivores.” in: Finian J. Leeper & John C. Vederas (eds.).
Biosynthesis: Aromatic Polyketides, Isoprenoids, Alkaloids. Berlin: Springer, 2000.
He, Maomao et al. “Biological and Pharmacological Activities of Amaryllidaceae Alkaloids.”
RSC Advances. vol. 5, no. 21 (2015).
Himaya, Sashini & Richard J. Lewis. “Venomics-accelerated Cone Snail Venom Peptide Discovery.” International Journal of Molecular Sciences. vol. 19, no. 3 (2018).
Hollingsworth, Robert G., John W. Armstrong & Earl Campbell. “Caffeine as a Repellent for Slugs and Snails.”
Nature. vol. 417 (2002).
Hwang, Deng-Fwu & Tamao Noguchi. “Tetrodotoxin poisoning.” Advances in Food and Nutrition Research. vol. 52 (2007). pp. 141-236.
Joachim Pietzsch, "Speed Read: An Eye for Structure,"
NobelPrize. 6/7/2025. at:
https://acr.ps/1L9F2Bm
Kohnen-Johannen, Kathrin Laura & Oliver Kayser. “Tropane Alkaloids: Chemistry, Pharmacology, Biosynthesis and Production.”
Molecules. vol. 24, no. 4 (2019).
Kottuparambil, Sreejith, Roshni Lilly Thankamony & Susana Agusti. “Euglena as a potential natural source of value-added metabolites.” Algal research. vol. 37 (2019). pp. 154-159.
Kumar, Thallampuranam et al. “Understanding the Structure, Function and Folding of Cobra Toxins.” Proceedings of the National Science Council republic of China, part (A). vol. 23, no. 1 (1999).
Kumar, P., D. K. Mahato, M. Kamle, T. K. Mohanta, and S. G. Kang. “Aflatoxins: A Global Concern for Food Safety, Human Health and Their Management.” Frontiers in Microbiology, vol. 7 (2017).
Leete, Edward. “The Biosynthesis of Coniine from Four Acetate Units.”
Journal of the American Chemical Society. vol. 85, no. 21 (1963). pp. 3523-3524.
Li, Bin et al. “Preparation of lactose-free pasteurized milk with a recombinant thermostable β-glucosidase from Pyrococcus furiosus.”
BMC Biotechnology. vol. 13, no. 1 (2013).
Lin, D., S. Jiang, A. Zhang, T. Wu, Y. Qian, and Q. Shao. “Structural Derivatization Strategies of Natural Phenols by Semi-Synthesis and Total-Synthesis.” Natural Products and Bioprospecting, vol. 12, no. 1 (2022).
Merriam-Webster.com Dictionary, s.v. “alkali,” accessed on 20\1\2026, at:
https://acr.ps/1L9F39Z
Nawrot-Chorabik, Katarzyna, Małgorzata Sułkowska, and Natalia Gumulak. “Secondary Metabolites Produced by Trees and Fungi: Achievements So Far and Challenges Remaining.” Forests, vol. 13, no. 8 (2022).
Nguyen, N. U., and B. D. Stamper. “A Template-Based Approach for Guiding and Refining the Development of Cinnamon-Based Phenylpropanoids as Drugs.” Molecules, vol. 25, no. 20 (2020).
Ninkuu, V., O. O. Aluko, J. Yan, H. Zeng, G. Liu, J. Zhao, H. Li, S. Chen, and F. D. Dakora. “Phenylpropanoids Metabolism: Recent Insight into Stress Tolerance and Plant Development Cues.” Frontiers in Plant Science, vol. 16 (2025).
O’Connor, Sara. E. & Justin J. Maresh. “Chemistry and Biology of Monoterpene Indole Alkaloid Biosynthesis.”
Natural Prod.uct Reports. vol. 23, no. 4 (2006). pp. 532-547.
Rensheng Xu, Yang Ye & Weimin Zhao (eds.).
Introduction to Natural Products Chemistry. Boca Raton: CRC press, 2011.
Springob, Karina & Toni M. Kutchan. “Introduction to the Different Classes of Natural Products.” in:
Anne E. O. &
Virginia L. (eds.).
Plant-derived Natural Products. New York, NY: Springer, 2009.
Sticher, Otto. “Natural product isolation.” Natural product reports. vol. 25, no. 3 (2008).
Tepfer, David et al. “A Plasmid of Rhizobium Meliloti 41 Encodes Catabolism of Two Compounds from Root Exudate of Calystegium Sepium.”
Journal Bacteriology. vol. 170, no. 3 (1988). pp.1153-1161.
Wink, M. “Plant Secondary Metabolites Modulate Insect Behavior-Steps Toward Addiction?.” Frontiers in Physiology, vol. 9 (2018).
Woese, Carl R. & George E. Fox. "Phylogenetic Structure of the Prokaryotic Domain: The Primary Kingdoms."
Proceedings of the National Academy of Sciences of the United States of America. vol. 74, no. 11 (1977).
Yan, Yumei, Xing Li, Chunhong Zhang, Lijuan Lv, Bing Gao, and Minhui Li. “Research Progress on Antibacterial Activities and Mechanisms of Natural Alkaloids: A Review.” Antibiotics, vol. 10, no. 3 (2021).
Zhang, Q. W., L. G. Lin, and W. C. Ye. “Techniques for Extraction and Isolation of Natural Products: A Comprehensive Review.” Chinese Medicine, vol. 13 (2018).
[1] Karena Springob & Toni M. Kutchan, “Introduction to the Different Classes of Natural Products,” in: Anne E. O. & Virginia L. (eds.),
Plant-derived Natural Products (New York: Springer, 2009), pp 3-50.
[2] Ibid.
[3] Paul M. Dewick,
Medicinal Natural Products: A Biosynthetic Approach, 3rd ed. (Chichester: Wiley, A John Wiley & Sons, 2009).
[4] Ibid.
[5] David L. Nelson and Michael M. Cox, Lehninger Principles of Biochemistry, 8th ed. (New York: W. H. Freeman, 2021).
[6] Kathrin Laura Kohnen-Johannsen & Oliver Kayser, “Tropane Alkaloids: Chemistry, Pharmacology, Biosynthesis and Production,”
Molecules, vol. 24, no. 4 (2019).
[7] M. Wink, “Plant Secondary Metabolites Modulate Insect Behavior-Steps Toward Addiction?,” Frontiers in Physiology, vol. 9 (2018), p. 364.
[8] Katarzyna Nawrot-Chorabik, Małgorzata Sułkowska, and Natalia Gumulak, “Secondary Metabolites Produced by Trees and Fungi: Achievements So Far and Challenges Remaining,” Forests, vol. 13, no. 8 (2022), p. 1338.
[9] Berhanu M. Abegaz and Henok H. Kinfe, “Secondary Metabolites, Their Structural Diversity, Bioactivity, and Ecological Functions: An Overview,” Physical Sciences Reviews, vol. 4, no. 6 (2019), p. 20180100
[10] N. U. Nguyen and B. D. Stamper, “A Template-Based Approach for Guiding and Refining the Development of Cinnamon-Based Phenylpropanoids as Drugs,” Molecules, vol. 25, no. 20 (2020), p. 4629.
[11] P. Kumar et al., “Aflatoxins: A Global Concern for Food Safety, Human Health and Their Management,” Frontiers in Microbiology, vol. 7 (2017), p. 2170.
[12] Nelson and Cox, “Lehninger Principles of Biochemistry.”
[13] Merriam-Webster.com Dictionary, s.v. “alkali,” accessed on 20\1\2026, at:
https://acr.ps/1L9F39Z .
[14] P. Dey et al., “Analysis of Alkaloids (Indole Alkaloids, Isoquinoline Alkaloids, Tropane Alkaloids),” in Recent Advances in Natural Products Analysis, ed. A. M. Giuffrè et al. (Amsterdam: Elsevier, 2020), pp. 505-567.
[15] Yumei Yan et al., “Research Progress on Antibacterial Activities and Mechanisms of Natural Alkaloids: A Review,” Antibiotics, vol. 10, no. 3 (2021), p. 318.
[16] S. Bhambhani, K. R. Kondhare, and A. P. Giri, “Diversity in Chemical Structures and Biological Properties of Plant Alkaloids,” Molecules, vol. 26, no. 11 (2021), p. 3374.
[17] Hiroshi Ashihara & Crozier Alan, “Caffeine: a well known but Little Mentioned Compound in Plant Science,”
Trends Plant Sci, vol. 6, no. 9 (2001), pp. 407-413.
[18] Robert G. Hollingsworth, John W. Armstrong & Earl Campbell, “Caffeine as a Repellent for Slugs and Snails,”
Nature, vol. 417 (2002).
[19] Jacob Friedman & George R. Waller, “Caffeine Hazards and Their Prevention in Germinating Seeds of Coffee (Coffea Arabica L.),”
Journal of Chemical Ecology, vol. 9, no. 8 (1983), pp. 1099-1106.
[20] Neal L. Benowitz, “Clinical Pharmacology of Caffeine,”
Annual Review Medicine, vol. 41 (1990), pp. 277-288.
[21] Alberto Ascherio et al., “Coffee Consumption, Gender, and Parkinson’s Disease Mortality in the Cancer Prevention Study II Cohort: The Modifying Effects of Estrogen,”
Am. J. Epidemiol, vol. 160, no. 10 (2004), pp. 977-984.
[22] Kohnen-Johannsen.
[23] Ibid.
[24] David Tepfer et al., “A Plasmid of Rhizobium Meliloti 41 Encodes Catabolism of Two Compounds from Root Exudate of Calystegium Sepium,”
Journal of Bacteriology, vol. 170, no. 3 (1988), pp.1153-1161.
[25] Kohnen-Johannsen.
[26] Dewick.
[27] Thomas Hartmann & Dietrich Ober, “Biosynthesis and Metabolism of Pyrrolizidine Alkaloids in Plants and Specialized Insect Herbivores,” in: Finian J. Leeper & John C. Vederas (eds.),
Biosynthesis: Aromatic Polyketides, Isoprenoids, Alkaloids (Berlin: Springer, 2000).
[28] Somnuk Bunsupa, Yamazaki Mami & Satio Kazuki, “Quinolizidine Alkaloid Biosynthesis: Recent Advances and Future Prospects,”
Front. Plant Sci, vol. 3 (2012).
[29] “Alkaloids Derived from Phenylalanine and Tyrosine,” in Alkaloids, ed. Shinji Funayama and Geoffrey A. Cordell (London: Academic Press, 2015), pp. 21–61.
[30] Maomao He et al., “Biological and Pharmacological Activities of Amaryllidaceae Alkaloids,”
RSC Advances, vol. 5, no. 21 (2015), pp.16562-16574.
[31] Sarah E. O’Connor & Justin J. M, “Chemistry and Biology of Monoterpene Indole Alkaloid Biosynthesis,”
Natural Product Reports, vol. 23, no. 4 (2006), pp. 532-547.
[32] Nelson and Cox, “Lehninger Principles of Biochemistry.”
[33] V. Ninkuu et al., “Phenylpropanoids Metabolism: Recent Insight into Stress Tolerance and Plant Development Cues,” Frontiers in Plant Science, vol. 16 (2025), at:
https://acr.ps/1L9F2Fw
[34] Nelson and Cox, “Lehninger Principles of Biochemistry.”
[35] D. Lin et al., “Structural Derivatization Strategies of Natural Phenols by Semi-Synthesis and Total-Synthesis,” Natural Products and Bioprospecting, vol. 12, no. 1 (2022), p. 8.
[36] Jeffrey Barry Harborne & Herbert Baxter,
The Handbook of Natural Flavonoids (New York: Wiley, 1999).
[37] Edward Leete, “The Biosynthesis of Coniine from Four Acetate Units,”
Journal of the American Chemical Society, vol. 85, no. 21 (1963), pp. 3523-3524.
[38] J. Gershenzon and N. Dudareva, “The Function of Terpene Natural Products in the Leaf of a Plant,” Nature Chemical Biology, vol. 3, no. 7 (2007), pp. 408–414.
[39] Eberhard Breitmaier, Terpenes: Flavors, Fragrances, Pharmaca, Pheromones (Weinheim: Wiley-VCH, 2006); Abegaz and Kinfe. “Secondary Metabolites, Their Structural Diversity, Bioactivity, and Ecological Functions: An Overview.”
[40] O’Connor.
[41] Ibid.
[42] Rensheng Xu, Yang Ye & Weimin Zhao (eds.),
Introduction to Natural Products Chemistry (Florida: CRC press, 2011).
[43] Dewick.
[44] Carl R. Woese & George E. Fox, "Phylogenetic Structure of the Prokaryotic Domain: The Primary Kingdoms,"
Proceedings of the National Academy of Sciences of the United States of America, vol. 74, no. 11 (1977), pp. 5088–5090.
[45] Bin Li et al., “Preparation of Lactose-free Pasteurized Milk with a Recombinant Thermostable β-Glucosidase from Pyrococcus Furiosus,”
BMC Biotechnology, vol. 13, no. 1 (2013).
[46] Qing Dong et al., “Characterization of an extremely thermostable but cold-adaptive β-galactosidase from the hyperthermophilic archaeon Pyrococcus furiosus for use as a recombinant aggregation for batch lactose degradation at high temperature,”
Journal Biosci Bioeng, vol. 117, no. 6 (2014), pp. 706-710.
[47] Dewick.
[48] Rensheng.
[49] Thallampuranam Kumar et al., “Understanding the Structure, Function and Folding of Cobra Toxins,” Proceedings of the National Science Council republic of China, part (A), vol. 23, no. 1 (1999).
[50] Sashini Himaya & Richard J. Lewis, “Venomics-accelerated Cone Snail Venom Peptide Discovery,” International Journal of Molecular Sciences, vol. 19, no. 3 (2018).
[51] Deng-Fwu Hwang & Tamao Noguchi, “Tetrodotoxin poisoning,” Advances in Food and Nutrition Research, vol. 52 (2007), pp. 141-236.
[52] Sreejith Kottuparambil, Roshni Lilly Thankamony & Susana Agusti, “Euglena as a potential natural source of value-added metabolites,” Algal research, vol. 37 (2019), pp. 154-159.
[53] Otto Sticher, “Natural product isolation,” Natural product reports, vol. 25, no. 3, pp. 517-554.
[54] Joachim Pietzsch, "Speed Read: An Eye for Structure,"
NobelPrize, 6/7/2025, accessed on 7/7/2025, at:
https://acr.ps/1L9F2Bm
[55] Sticher.
[56] Q. W. Zhang, L. G. Lin, and W. C. Ye, “Techniques for Extraction and Isolation of Natural Products: A Comprehensive Review,” Chinese Medicine, vol. 13 (2018), p. 20.