الميتوكوندريا (أو المتقدِّرة، Mitochondria)
عضيّة {{العضيّات: (Organelle) جسيمات خلوية متخصصة محاطة بغشاء (أو أكثر) تتواجد داخل الخلايا حقيقية النواة (Eukaryotic cells)، تؤدي وظائف متخصصة، مثل النواة (Nucleus) أو الميتوكوندريا (Mitochondria) أو البلاستيدات (Chloroplasts).}} موجودة داخل
الخلايا حقيقية النوى (Eukaryotic cells)، تؤدي أدوارًا محورية في العمليات البيولوجية فيها، فمن خلالها تُولَّد معظم
الطاقة الحيوية الضرورية لوظائف الخلية. يحيط بالميتوكوندريا غشاءان واقيان؛ يُعدّ الغشاء الخارجي حاجزًا منفِّذًا نفاذية جزئية (Semi-permeable)، بينما يُعَدُّ الغشاء الداخلي المكوّن من أسطح ملتوية جدًا تسمى
الأعراف (Cristae)، حزامًا ناقلًا فعّالًا لإنتاج الطاقة. إن المهمّة الأساسية للميتوكوندريا هي توليد الطاقة، ولذا تسمّى "محطات الطاقة في الخلية" (Energy powerhouses in the cell)، فهي مسؤولة عن تصنيع مركب
الأدينوسين ثلاثي الفوسفات {{أدينوسين ثلاثي الفوسفات (أو أدينوزين ثلاثي الفوسفات): (ATP)، نوكليوتيد (Nucleotide) عالي الطاقة، يعتبر المصدر الرئيسي للطاقة الحيوية في الخلية، إذ إن تكسيره يعطي الطاقة الكافية للقيام بالعمليات المختلفة. يتكون من جزيء أدينين (Adenine) مرتبط بسكر الريبوز (Ribose) المرتبط بثلاث مجموعات فوسفات.}} بكميات كبيرة. هذا المركّب هو العُملة الخلوية المسؤولة عن تغذية كل الأنشطة الخلوية الفيزيولوجية، بما فيها
تقلّصات العضلات، وحتى العمليات الإدراكية، وغيرها الكثير. يُشبه شكل الميتوكوندريا شكلَ حبة الفاصولياء، ولديها أيضًا أشكال أخرى؛ فهي تشكّل داخل الخليّة شبكات ديناميكية، تتكيف مع احتياجات الخلية من الطاقة. ومن خلال عمليات انشطار الميتوكوندريا واندماجها، يمكن الزيادة أو التقليل من عددها في الخلية؛ ما يسمح لها بضمان الجودة الديناميكية لتوفير الطاقة الأمثل حسب حاجة الخلية. إلى جانب دورها المركزي في إنتاج الطاقة، تحتوي الميتوكوندريا على
الحمض النووي والريبوسومات؛ ما يجعلها قادرة على إنتاج بعض
البروتينات المتخصصة. وكما تؤثر على حياة الخلايا، تتحكم الميتوكوندريا أيضًا ببعض عمليات
الموت الخلوي، مثل
المسار الداخلي للاستماتة (Intrinsic apoptosis).
شكلها
[الشكل 1]
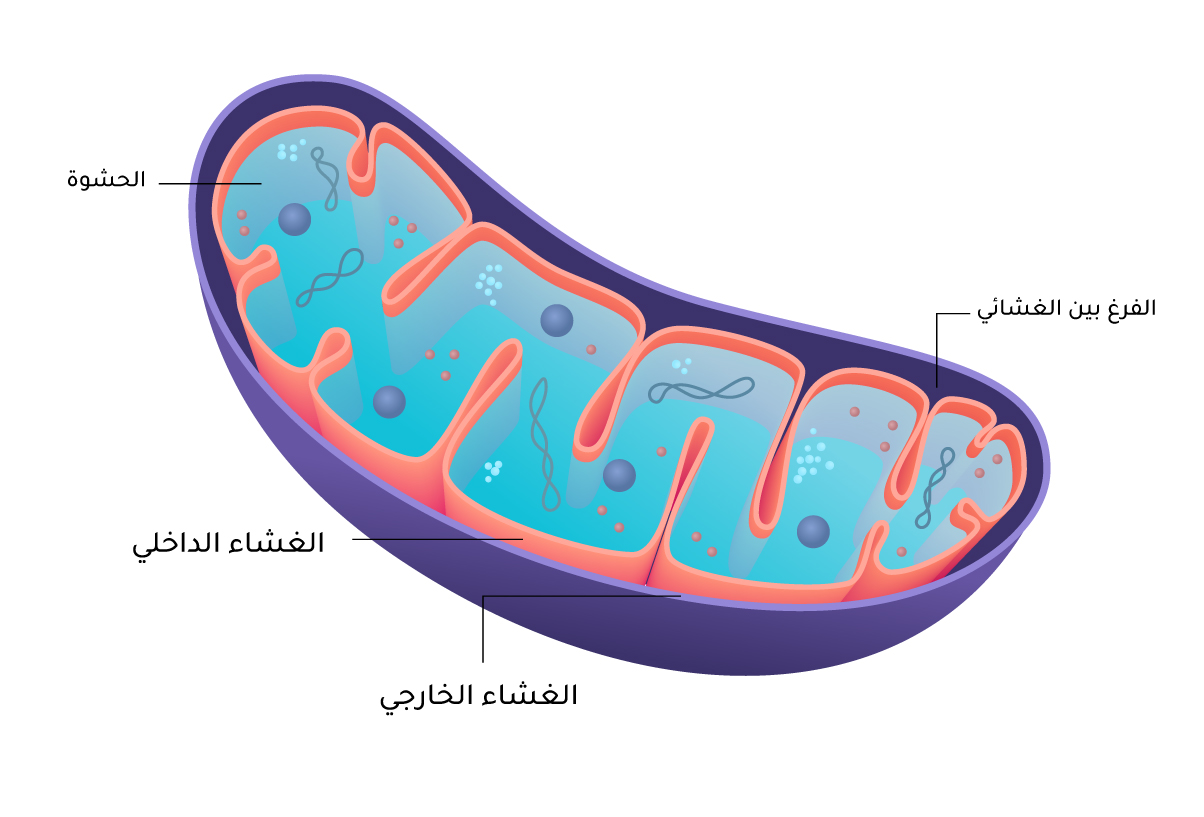 شكل الميتوكوندريا
شكل الميتوكوندريا
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
للميتوكوندريا تصميم هيكلي مميز يلائم أدوارها الحيوية المتمثلة بصورة أساسية في إنتاج الطاقة الخلوية. فهذه العضيّات لها غشاء مزدوج وطبيعة ديناميكية متغيرة تسمح لها بالتكيف مع متطلبات الطاقة الخلوية. يحيط بالميتوكوندريا غشاءان:
الغشاء الخارجي للميتوكوندريا (Mitochondrial outer membrane - MOM) والغشاء الداخلي للميتوكوندريا (Mitochondrial inner membrane - MIM). وبما أن هناك غشاءين، فإن داخل الميتوكوندريا ينقسم إلى منطقتين:
حشوة الميتوكوندريا (Mitochondrial matrix) وهي الجزء الداخلي، والحيّز بين الغشاءين (Inter membrane space) الذي يفصل الغشاء الخارجي عن الداخلي (الشكل 1). يُعَدّ الغشاء الخارجي منفّذًا للجزيئات والأيونات الصغيرة، إذ يحتوي على بروتينات تسمى
بورين (Porins) تشكّل قنوات في الغشاء الخارجي. من عائلة البورين، يوجَد البروتين الأساسي على الغشاء الخارجي لخلاياالثدييات يدعى
القناة الأيونية المعتمدة على فرق الجهد،
فيداك (Voltage-dependent anion channel - VDAC). تُسهّل عائلة البورين مرور الجزيئات صغيرة الحجم بين
السيتوبلازم {{السيتوبلازم (أو الوسط الخلوي): هو ما يوجد داخل الخلية باستثناء
النواة في الخلايا حقيقية النوى (Eukaryotic cells)، وكل ما يوجد داخل الخلية في الخلايا غير حقيقية النوى.}} والحيّز بين الغشاءين. يعمل الغشاء الخارجي حاجزًا وقائيًا، حيث يفصل محتويات الميتوكوندريا غير القادرة على المرور من خلال فيداك عن بقية الخلية؛ ولهذا أهمية بالغة، فإن مرّت بعض البروتينات من الحيّز بين الغشاءين للسيتوبلازم، فإن الخلية تبدأ عملية
الموت الخلوي المبرمج (استماتة الخلايا، Apoptosis).
في المقابل، إن الغشاء الداخلي غير نفّاذ لمعظم الأيونات والجزيئات، بسبب تركيبته الدهنية الفريدة، ونسبة البروتين إلى
الدهون العالية، ووجود بروتينات تنظم عمليات النقل من خلاله. تُعَد هذه النفاذية الانتقائية أمرًا حيويًا للحفاظ على
التدرّج الكهروكيميائي (Electrochemical gradient) الضروري لإنتاج الأدينوسين ثلاثي الفوسفات (ATP) أثناء عملية
الفسفرة التأكسدية (Oxidative phosphorylation). يُطوى الغشاء الداخلي للميتوكوندريا في نظام معقّد من الطيّات المعروفة بالأعراف (Cristae) التي توفر مساحة سطح واسعة للتفاعلات البيوكيميائية، خاصّة تلك المتعلقة بسلسلة نقل الإلكترونات (Electron transport chain). تعَدّ هذه الأعراف ضرورية لإنتاج الطاقة الحيوية؛ لأنها تحتوي على
المجمّعات البروتينية (Protein complexes) التي تؤدّي عملية
الفسفرة التأكسدية، فتسمح المساحة السطحية المتزايدة للأعراف بنقل
الإلكترونات بشكل أسرع وأكثر كفاءة. ولذلك، كلما كان هناك حاجة لمزيد من الطاقة، شُكِّلَت المزيد من الأعراف في الميتوكوندريا[1].
يفصل الغشاءُ الداخلي حشوةَ الميتوكوندريا (الجزء الداخلي منها) عن الحيّز بين الغشاءين. تحتوي الحشوة على جميع
الإنزيمات اللازمة لعمليات
الأكسدة وإنتاج الطاقة في
الخلية، باستثناء إنزيمات
التحلّل الغلايكولي (Glycolysis) الموجودة في السيتوبلازم، فجميع إنزيمات
أكسدة الدهون والأحماض الأمينية وكذلك إنزيمات
حلقة كربس (Citric acid cycle; Krebs’ cycle) موجودة في الحشوة، وفيها أيضًا
الحمض النووي للميتوكوندريا {{الحمض النووي للميتوكوندريا (mtDNA): هو حمض نووي دائري صغير يوجد في ميتوكوندريا الخلايا، منفصلًا عن الحمض النووي للنواة. يُشفّر الحمض النووي للميتوكوندريا 37 جينًا أساسيًا لإنتاج الطاقة من خلال الفسفرة التأكسدية، ويُورث حصريًا من الأم.}}، وهو دائري ويحتوي على
جينات تشفّر بعض وحدات بروتينات الميتوكوندريا، وجزيئات
الحمض النووي الريبي الناقل (tRNA)، والحمض النووي الريبي الريبوسومي (rRNA)[2].
تشبه الميتوكوندريا حبّة الفاصولياء، وفي كل كتب الأحياء تُرسم كذلك، مع العلم أن هذا ليس أمرًا ثابتًا. في الحقيقة، تشكّل الميتوكوندريا شبكات ديناميكية داخل الخلية، ويمكن لهذه العضيّات الاندماج معًا لتكوين أشكال أكبر وأكثر كفاءة عندما تحتاج الخلية إلى زيادة إنتاج الطاقة. ويمكن كذلك أن تخضع للانشطار، فتنقسم إلى وحدات أصغر، تلبية لمتطلبات الطاقة المتغيرة للخلية أو استجابة للإجهاد الخلوي (الشكل 2). إن عمليتي الاندماج والانشطار تراقبان جودة الميتوكوندريا، لأنهما تسمحان بعزل الميتوكوندريا التالفة والقضاء عليها، ما يضمن الصحة العامة للخلية. تمتد ديناميكيات الميتوكوندريا أيضًا إلى الحفاظ على الحمض النووي للميتوكوندريا، فأثناء الاندماج، يمكن استكمال الحمض النووي التالف بآخر سليم من الميتوكوندريا المجاورة، ما يحافظ على السلامة الوظيفية لهذه العضيّات[3].
[الشكل 2]
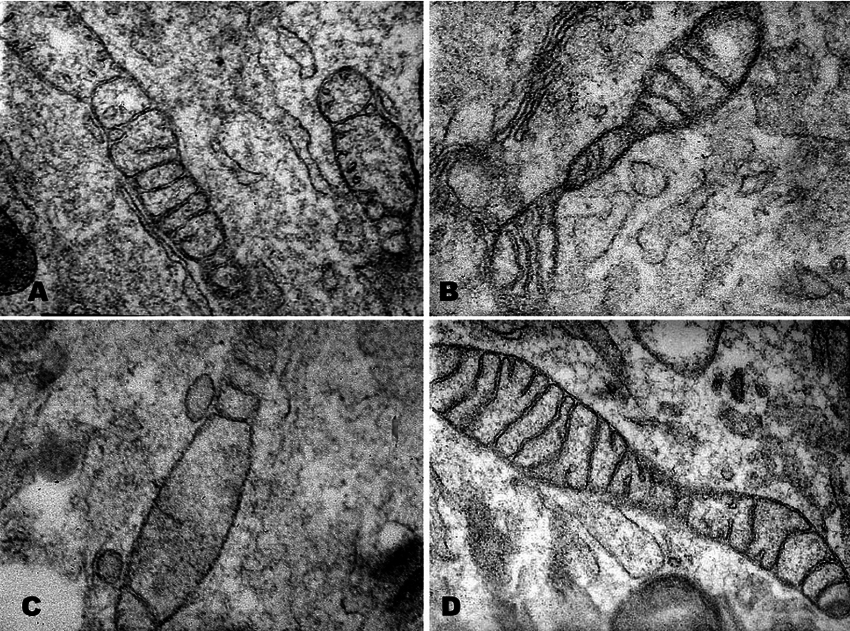 الأشكال المتعددة للميتوكوندريا
الأشكال المتعددة للميتوكوندريا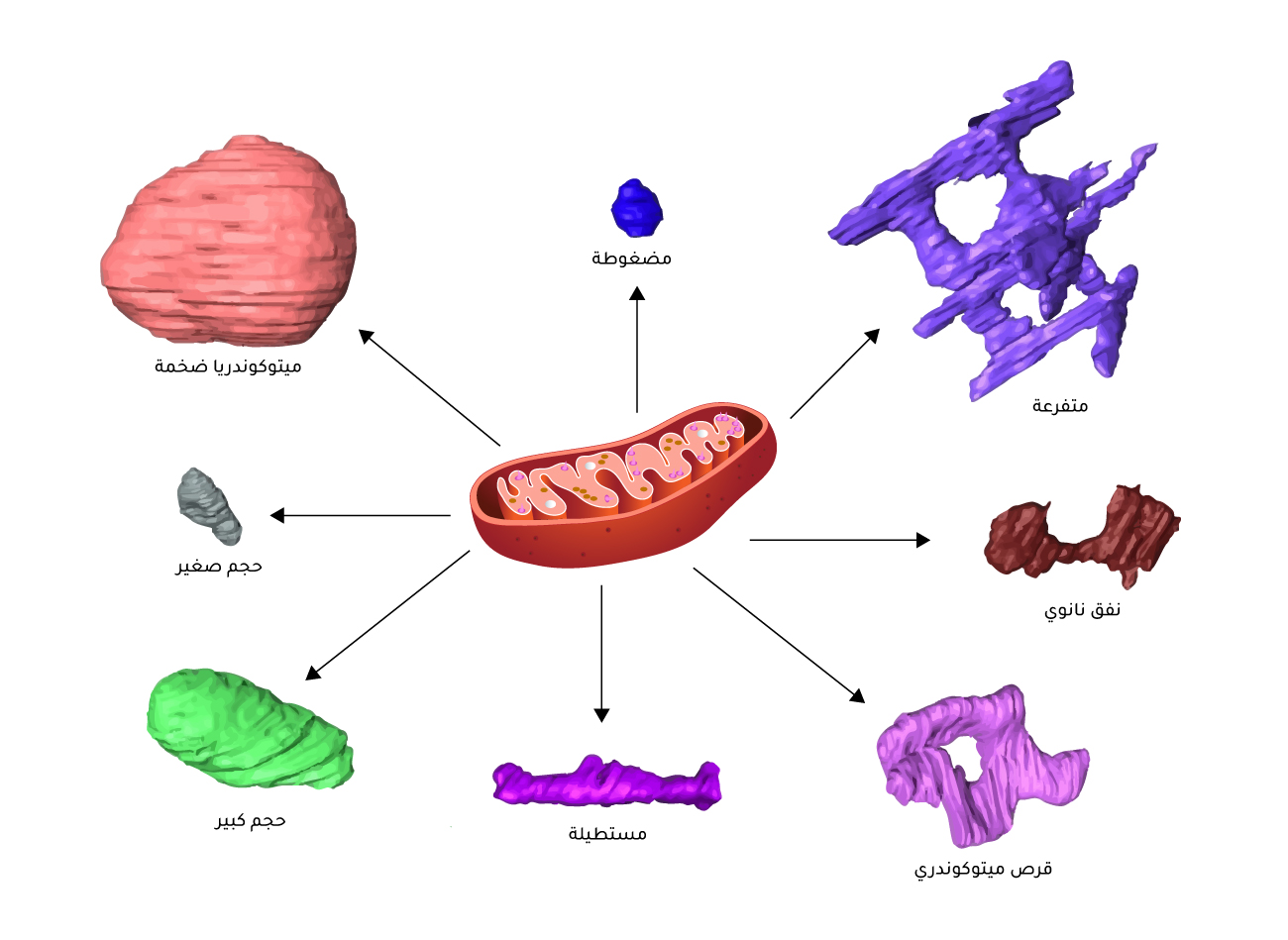 الأشكال المتعددة للميتوكوندريا
الأشكال المتعددة للميتوكوندريا
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
وظائفها
تشتهر الميتوكوندريا بوظيفتها الرئيسة، وهي توليد معظم الطاقة الخلوية في
الخلية حقيقية النواة. ومع ذلك، فإن الميتوكوندريا مهمة لعمليات فيزيولوجية متنوعة تمتد إلى ما هو أبعد من دورها الأساسي في إنتاج الـ ATP، العُملة الخلوية للطاقة. تؤدي الميتوكوندريا دورًا مركزيًا في عملية
التمثيل الغذائي الوسيط (Intermediary metabolism)، بما في ذلك تحلّل
الكربوهيدرات والأحماض الدهنية والبروتينات. وكذلك تؤدي دورًا في حلقة كربس، إذ تحوّل الميتوكوندريا الأحماض الدهنية، والأحماض الأمينية، ومركب
البيروفات (Pyruvate) الذي يُحصَل عليه من تحلل
الغلوكوز {{الغلوكوز: (C₆H₁₂O₆) سكر أحادي سداسي الكربون، وهو المصدر الرئيس للطاقة لمعظم الكائنات الحية. هو الناتج الرئيس لعملية
التمثيل الضوئي (Photosynthesis)، والركيزة الأساسية للتنفس الخلوي (Cellular respiration). يدور في الدم، على شكل سكر الدم، ويُخزن على شكل غلايكوجين (Glycogen) في الكبد والعضلات لدى الحيوانات أو على شكل نشا (Starch) في النباتات. يتحلل في الخلية لإنتاج طاقة بوساطة التحلل الغلايكول (Glycolysis) والفسفرة التأكسدي (Oxidative phosphorylation).}} في السيتوبلازم، إلى
أسيتيل مرافق الإنزيم أ (Acetyl-CoA)، المركب الأساسي لبداية حلقة كربس. تُصنِّع حلقة كربس مركّبات مختزلة (NADH وFADH2)، تزوّد
سلسلة نقل الإلكترونات بالإلكترونات؛ ما يؤدي إلى إنتاج الـ ATP. في هذه العملية، تُمَرَّر الإلكترونات من هذه الجزيئات عالية الطاقة إلى سلسلة من مجمّعات البروتين الموجودة في الغشاء الداخلي، ويؤدي مرورها إلى ضخ
البروتونات من الحشوة إلى الحيّز بين الغشاءين؛ ما يخلق
تدرّجًا كهروكيميائيًا (مصنوعًا من البروتونات) عبر الغشاء الداخلي. يُخزّن هذا التدرّج الطاقة التي يمكن استخدامها لتحفيز
مجمّع ATP سينثاز (ATP synthase complex) الذي يحفز اتحاد
الأدينوسين ثنائي الفوسفات (ADP) مع جزيء فوسفات غير عضوي مكونًا ATP. وهكذا، تزود الميتوكوندريا الخلايا بالطاقة الضرورية لعدد لا يحصى من العمليات البيوكيميائية[4].
للميتوكوندريا أيضًا العديد من الوظائف الأساسية الأخرى (الشكل 3). فهي تنظّم، على سبيل المثال، بالاشتراك مع الشبكة الإندوبلازمية، مستويات
الكالسيوم داخل الخلايا، وتعمل مخازنَ مؤقتة تعزل أيونات الكالسيوم الزائدة. تؤدّي هذه الوظيفة دورًا في العمليات الخلوية التي تعتمد على تنظيم مستويات الكالسيوم في الخلية، مثل:
انقباض العضلات، وإفراز الحويصلات، وعمليات موت الخلايا المبرمج. في بعض الخلايا المتخصصة، مثل تلك الموجودة في
قشرة الغدة الكظرية (Adrenal cortex) والغدد التناسلية (Gonads)، تحتوي الميتوكوندريا على الإنزيمات الضرورية لإنتاج
الهرمونات الستيرويدية (Steroid hormones)، مثل:
الكورتيزول (Cortisol) والألدوستيرون (Aldosterone)، والهرمونات الجنسية (Sex hormones)، مثل:
التستوستيرون (Testosterone) والبروجستيرون (Progesterone)، في عملية تُسمى
تكوين الستيرويد (Steroidogenesis). في
الأنسجة الدهنية البنية (Brown adipose tissue)، تحتوي الميتوكوندريا على بروتين فريد خاص يسمى
بروتين فك الارتباط 1 (UCP-1). يفصل هذا البروتين
الفسفرة التأكسدية عن إنتاج الـ ATP؛ ما يؤدي إلى تبديد الطاقة في هيئة حرارة بدلاً من تكوين الـ ATP. يعد إنتاج الحرارة، المعروف باسم
التوليد الحراري (Thermogenesis)، أمرًا ضروريًا للحفاظ على درجة حرارة الجسم[5].
[الشكل 3]
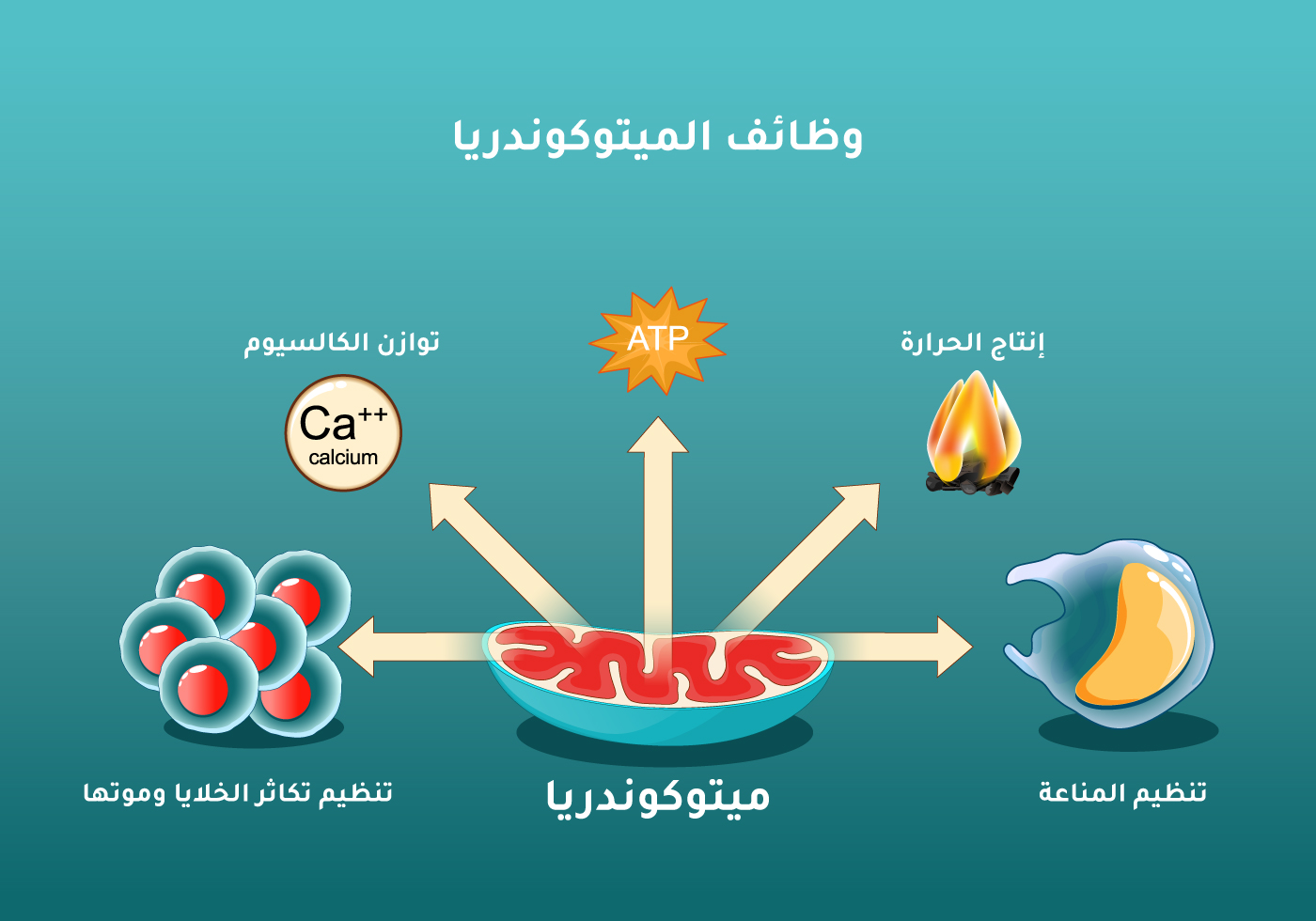 وظائف الميتوكوندريا المختلفة
وظائف الميتوكوندريا المختلفة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تُعدّ الميتوكوندريا
عضيّة مركزية في المسار الداخلي لموت الخلايا المبرمج أو الاستماتة الخلوية، فهي تطلق
بروتينات مؤازرة للاستماتة، مثل
السيتوكروم سي (Cytochrome c) وغيره من الحيّز بين الغشاءين إلى السيتوبلازم؛ ما يؤدي إلى سلسلة من الأحداث التي تؤدي إلى
موت الخلايا {{موت الخلايا: عملية بيولوجية حيوية ومستمرة تُزال فيها الخلايا التالفة أو المُصابة أو غير الضرورية، ما يُحافظ على توازن الأنسجة ونموها بشكل طبيعي. هناك العديد من المسارات المُنظّمة المؤدية للموت الخلوي، من أبرزها موت الخلايا المُبرمج، أو استماتة الخلايا (Apoptosis)، والنخر (Necrosis)، أي موت الخلايا غير المُتحكّم فيه، والالتهام الذاتي (Autophagy) أي التحلل الذاتي.}}. تُنظَّم هذه العملية بإحكام، وتؤدّي دورًا محوريًا في إزالة الخلايا التالفة أو غير المرغوب فيها من الجسم (الشكل 4).
[الشكل 4]
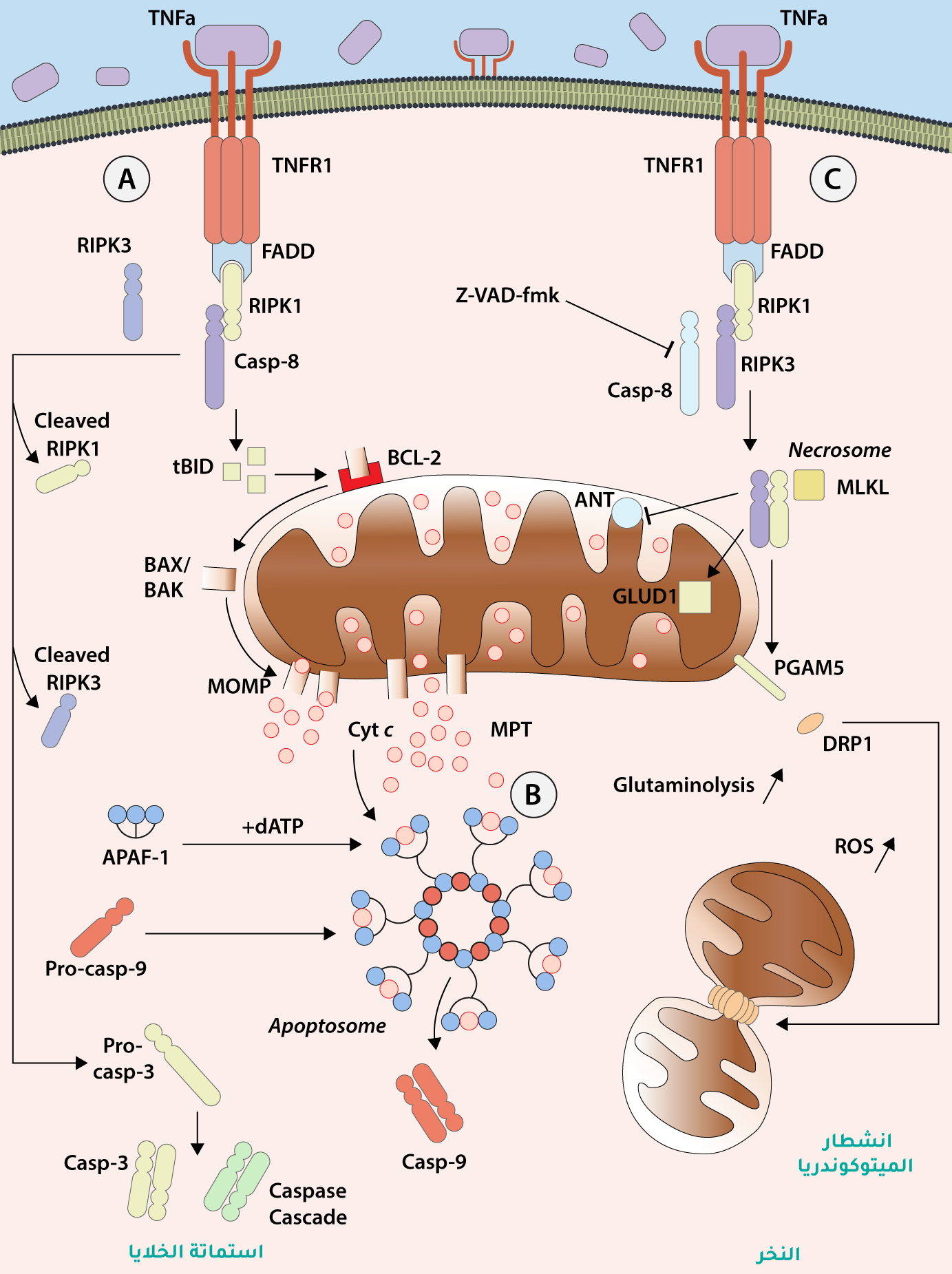 الميتوكوندريا والاستماتة الخلوية
الميتوكوندريا والاستماتة الخلوية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
أصلها
يرتبط أصل الميتوكوندريا في الخلايا حقيقية النوى بدراسة التطور وإعادة تشكيل مساره. يتفق العلماء على أن الميتوكوندريا والبلاستيدات الخضراء Chloroplasts)) نشأت من خلال ابتلاع
خلية بدائية النواة (أركيون، Archaeon) خليةً أخرى (بكتيريا، Bacterium)، ومن ثمَّ نشأتا معًا وتطوّرتا لتكوين الخلية حقيقية النواة[6]. إن ظهور الخلايا حقيقية النواة في مسار التطور كان نتيجةً لتحالف تكافلي بين خلية مضيفة
أركيونية وبكتريا ألفا-بروتيوباكتيريوم، وهي سلائف الميتوكوندريا كما تُعرَف الآن. بمرور الوقت، أنتجت هذه الشراكة خلية متكاملة ومعقدة تتمتع بقدرات جديدة، مثل غزارة إنتاج الطاقة؛ ما مهّد الطريق لظهور حياة متعددة الخلايا. تُعرف هذه النظرية بنظرية النشوء التعايشي الداخلي {{نظرية النشوء العشوائي التعايشي الداخلي: (Endosymbiotic theory) تقول نظرية التكافل الداخلي إن حقيقيات النوى تطورت من بدائيات النوى عبر علاقة تكافلية. ووفقًا لهذه النظرية، نشأت الميتوكوندريا والبلاستيدات الخضراء من خلايا بدائية نوى مستقلة ابتلعتها خلية أكبر، وأصبحت في النهاية عضيات دائمة متخصصة. ساهمت بانتشار هذه النظرية عالمة الأحياء الدقيقة لين مارغوليس في ستينيات القرن الماضي، وأحدثت ثورة في علم الأحياء التطوري بإثباتها أن الطفرات التطورية الكبرى يمكن أن تنتج عن التعاون والاندماجات التكافلية، وليس فقط عن طريق الطفرات التدريجية والتنافس.}}، وهي واحدة من عدة إصدارات مختلفة للفكرة نفسها[7] (الشكل 5).
[الشكل 5]
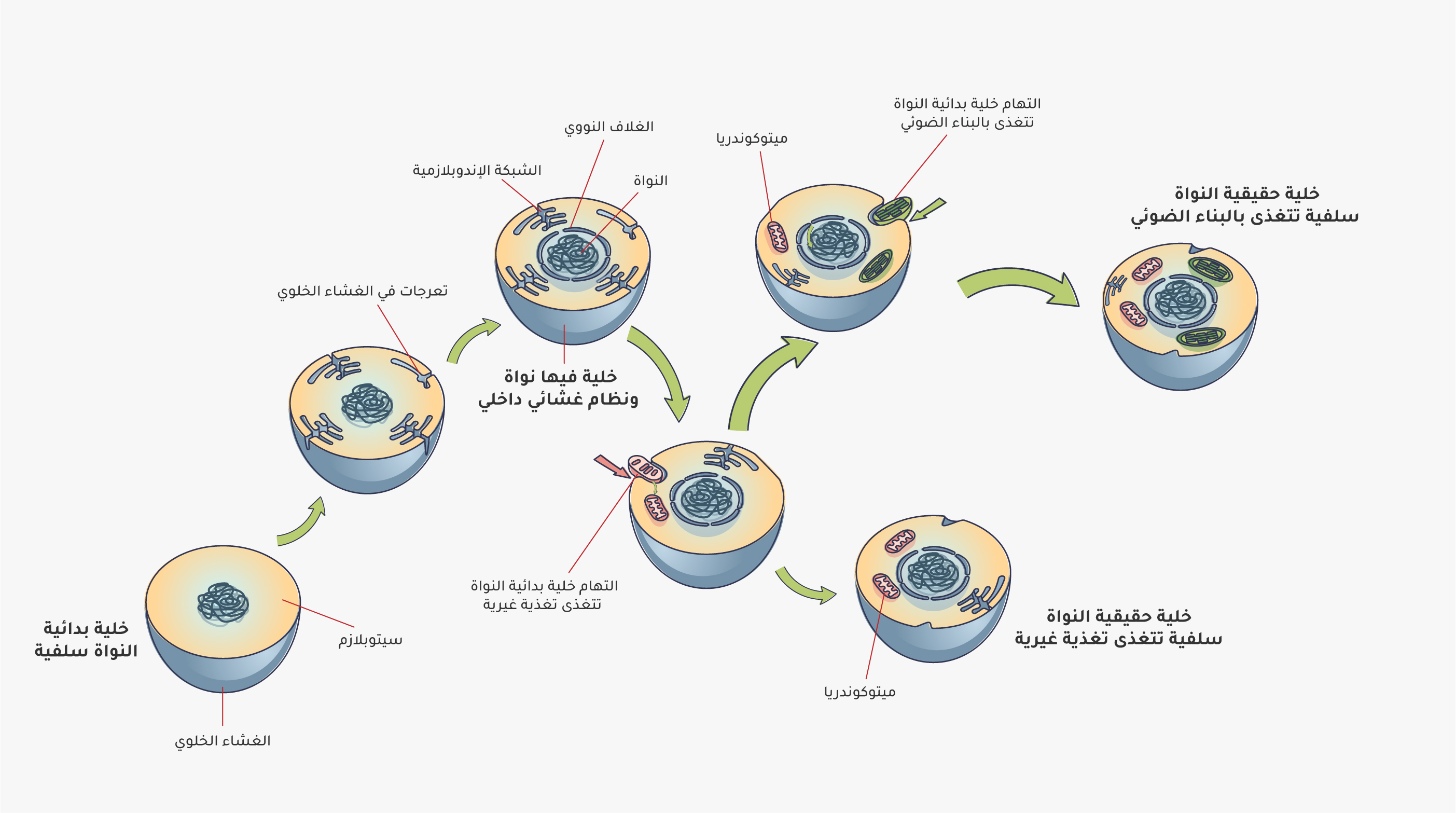 نظرية النشوء التعايشي
نظرية النشوء التعايشي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
غالبًا ما ترجع
نظرية النشوء التعايشي الداخلي، التي وجدت جذورها في أوائل القرن العشرين، إلى أعمال عالم النبات الروسي
كونستانتين ميرشكاوسكي (Konstantin Mereschkowski، 1855-1921). فقد أوجز، في عام 1905، لأول مرة، نظرية النشوء التكافلي الحيوي (Symbiogenesis)، وهو مصطلح مشتق من اليونانية، وشرح هذه النظرية بشكل أكبر في عام 1910. لم يكن ميرشكاوسكي أول من فكّر بالموضوع؛ فقد تأثرت أفكاره بالملاحظات السابقة لعالم النبات
أندرياس شيمبر (Andreas Franz Schimper، 1856-1901) الذي اقترح، في عام 1883، أن النباتات الخضراء ربما نشأت من اتحاد تكافلي بين كائنين حيين. جاءت أفكار شيمبر بناءً على ملاحظته أن البلاستيدات الخضراء في النباتات الخضراء تشبه إلى حد كبير
البكتيريا الخضراء المزرقة (Cyanobacteria). بعد ذلك، في عام 1918، نشر العالم الفرنسي
بول جول بورتييه (Paul Portier، 1866-1962) كتابًا افترض فيه أن الميتوكوندريا نشأت من عملية تكافلية. كذلك دعم
إيڤان والين (Ivan Wallin، 1883-1969) في العشرينيات من القرن العشرين النشوء التعايشي الداخلي للميتوكوندريا[8]. لم تكتسب هذه النظريات المبكرة اهتمامًا كبيرًا حتى منتصف القرن العشرين، عندما عُقِدت مقارنات مجهرية إلكترونية مفصّلة بين البكتيريا الخضراء المزرقة والبلاستيدات الخضراء، وأدّى اكتشاف الحمض النووي داخل البلاستيدات والميتوكوندريا إلى زيادة الاهتمام بالنشوء التعايشي الداخلي. يرتبط اسم العالمة الأميركية
لين مارغوليس (Lynn Margulis، 1938-2011) بنظرية النشوء التعايشي ارتباط
تشارلز داروين (Charles Darwin، 1809-1882) بنظرية التطور[9]، فهي التي قدّمت النظرية ودعّمتها بالأدلة في عام 1967[10]. تُعَدّ هذه النظرية التي تبحث في أصل الميتوكوندريا والبلاستيدات الخضراء مقبولة على نطاق واسع، فهي مدعومة بعدد من الأدلة المقنعة في نواحٍ متعددة، وفق ما يأتي:
- الحمض النووي: وجوده داخل الميتوكوندريا والبلاستيدات الخضراء من أحد أبرز الأدلة على ذلك، فكل من الحمض النووي للميتوكوندريا (mtDNA) والحمض النووي للبلاستيدات الخضراء (cpDNA)، هو
جينوم دائري صغير يحتوي على جينات، يشفّر بعض البروتينات الضرورية لوظائف هذه العضيّات. يشبه الحمض النووي في الميتوكوندريا، من حيث شكله وتوزيعه، إلى حد كبير ذلك الحمض النووي الموجود في البكتيريا، ويختلف كثيرًا عن الحمض النووي الموجود في أنوية
الخلايا حقيقية النوى. تكشف التحليلات المقارنة للمواد الوراثية من الميتوكوندريا والبلاستيدات الخضراء ومختلف
بدائيات النوى عن أوجه تشابه كبيرة؛ ما يدعم فكرة أن هذه العضيّات تشترك في أصل مشترك مع مجموعات محدّدة من البكتيريا.
- التشابه الهيكلي: شكليًّا، تشبه الميتوكوندريا والبلاستيدات الخضراء البكتيريا من حيث الحجم والبنية. يشترك وجود أكثر من غشاء في الميتوكوندريا والبلاستيدات الخضراء مع بعض أنواع البكتيريا، فهو تصميم أقرب إلى غلاف الخلية بدائية النواة، وبعيد كل البعد عن
أغشية الخلايا حقيقية النوى، كما أن التركيب الدهني لأغشية الميتوكوندريا أقرب كثيرًا إلى البكتيريا، خاصّة وجود دهن
الكارديوليبين (Cardiolipin) غير الموجود في حقيقيات النوى إلّا في الميتوكوندريا[11].
- التكاثر: تتكاثر الميتوكوندريا والبلاستيدات الخضراء بشكل مستقل عن الخلية، على غرار البكتيريا، وبالآليات نفسها من خلال
الانشطار الثنائي (Binary fission). يتماشى هذا مع نظرية أن هذه العضيّات كانت يومًا ما كائنات حية حرة، ولها آلياتها الخاصة للتكاثر.
- الريبوسومات: هي مصانع لإنتاج البروتينات داخل الميتوكوندريا والبلاستيدات الخضراء. في الخلايا حقيقية النواة، توجد الريبوسومات في شكلين:
الريبوسومات السيتوبلازمية والريبوسومات داخل العضيّات. تشبه الريبوسومات الموجودة في الميتوكوندريا والبلاستيدات الخضراء، من الناحية الهيكلية،
الريبوسومات بدائية النواة (النوع الموجود في البكتيريا) أكثر من الريبوسومات الموجودة في سيتوبلازم حقيقيات النوى. وعلى وجه التحديد، فهي تشبه الريبوسومات في البكتيريا
ألفا-بروتيوباكتيريوم، في حالة الميتوكوندريا، والريبوسومات في البكتيريا الخضراء المزرقة، في حالة البلاستيدات الخضراء. ومن ناحية الحجم، فإن هذه الريبوسومات أصغر من الريبوسومات الموجودة في السيتوبلازم، وتشبه إلى حد كبير حجم الريبوسومات الموجود في بدائيات النوى.
الحمض النووي فيها
يختلف الحمض النووي للميتوكوندريا عن نظيره في النواة. فهو مادة وراثية حلقيّة موجودة داخل حشوة الميتوكوندريا موروثة بشكل حصري من الأم، على عكس الحمض النووي الموجود في نواة الخلية الموروث من كلا الوالدين[12]. فالحمض النووي للميتوكوندريا ينتقل حصريًا من الأمهات إلى أبنائهن، من دون أي إسهام من المادة الوراثية للأب أثناء
الإخصاب[13]. يختلف هيكل الحمض النووي للميتوكوندريا عن الحمض النووي في النواة بأنه جزيء دائري يتكون من
الحمض النووي المزدوج (DNA double helix) (الشكل 6)، وهناك نسخ متعددة من الحمض النووي الحلقي الموجود في الميتوكوندريا. يحتوي هذا الجزيء على الجينات التي تشفّر بعض أجزاء البروتينات المعقدة الأساسية الضرورية لوظيفة الميتوكوندريا وإنتاج الطاقة، بالإضافة إلى جزيئات الحمض النووي الريبي الناقلة (tRNAs)، والريبوسومية (rRNAs) التي تسهم في بناء البروتينات داخل الميتوكوندريا. في الحمض النووي للميتوكوندريا في معظم الحيوانات (مع استثناءات قليلة) يوجد 37 جينًا؛ 13 منها يشفرون بروتينات، و22 يشفرون الحمض النووي الريبي الناقل، و2 يشفران الحمض النووي الريبي الريبوسومي ويبلغ متوسط طول جينوم الميتوكوندريا في الحيوانات حوالي 16,000 وحدة بنائية (زوج
نيوكليوتيدات)[14].
[الشكل 6]
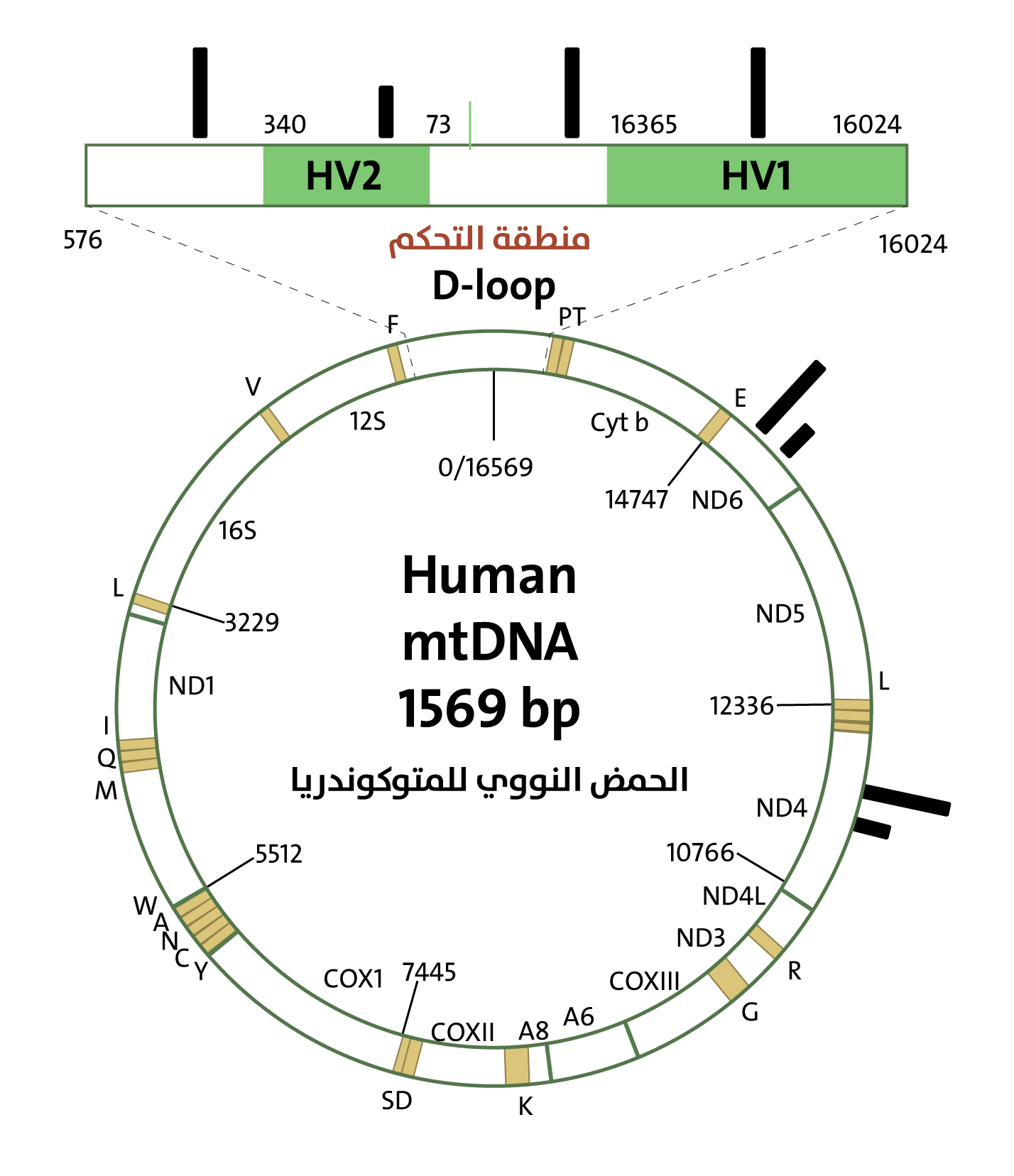 الحمض النووي للميتوكوندريا
الحمض النووي للميتوكوندريا
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تتمثل الوظيفة الأساسية لـلحمض النووي للميتوكوندريا في توفير تعليمات لتكوين أجزاء من البروتينات المشاركة في
الفسفرة التأكسدية، وهي عملية حاسمة يُنتَج فيها جزيء
الأدينوسين ثلاثي الفوسفات، وهو عُملة الطاقة الأساسية في الخلية. بالإضافة إلى ذلك، يؤدّي الحمض النووي للميتوكوندريا دورًا محوريًا في تنظيم وظيفتها، والتمثيل الغذائي، ومسارات الإشارات الخلوية المتعلقة بإنتاج الطاقة وبقاء الخلية. بالمقارنة مع الحمض النووي في النواة، فإن معدّل
الطفرات في الحمض النووي للميتوكوندريا أعلى؛ ويرجع ذلك جزئيًا إلى عدم وجود بروتينات
الهستون {{عائلة الهستون: (Histones) تتكون من بروتينات قلوية (شحنتها موجبة في الظروف الفيزيولوجية) يلتف حولها الحمض النووي (DNA) لتكوين النيوكليوزومات، ما يُمكّن من تنظيم الكروموسومات بكفاءة وتنظيم التعبير الجيني.}} على الحمض النووي في الميتوكوندريا، بالإضافة إلى محدودية آليات الإصلاح فيها، كما أن الميتوكوندريا تُعَدّ مركز التأكسد داخل الخلية، وبناء عليه، فإنها تنتج كميات من
مركبات الأكسجين التفاعلية (Reactive oxygen species) التي قد تؤدي إلى إحداث الضرر في الحمض النووي[15]. للحد من الطفرات والحفاظ على سلامة الحمض النووي للميتوكوندريا، طوّرت الميتوكوندريا آلية فريدة غير موجودة في النواة، بأن تكسّر الجينومات المتضررة بوتيرة عالية، وفي الوقت نفسه، مضاعفة الحمض النووي للميتوكوندريا السليم أو الذي أُصلِح. هذه الآلية ممكنة بسبب وجود نسخٍ متعددة من الحمض النووي للميتوكوندريا[16].
مع أن الحمض النووي للميتوكوندريا أساسي ومهم لوظائفها التأكسدية، فإن بعض الكائنات الحية تخلّت عنه بأن فُقدت الجينات المشفرة تمامًا أو نُقِلت إلى النواة. على سبيل المثال، تفتقر
الطلائعيات الطفيلية
كريبتوسبوريديوم (Cryptosporidium) إلى وجود الحمض النووي في الميتوكوندريا. في هذه
الطفيليات أحادية الخلية، وبسبب عدم وجود الحمض النووي في الميتوكوندريا، فإن نظام تصنيع الطاقة يختلف عن الكائنات الأخرى؛ ما يجعلها مقاومةً للعديد من العقاقير التي تثبّط عمل الميتوكوندريا، مثل
السيانيد وغيره[17]. هناك أدلة كافية على أن بعض جينات الميتوكوندريا يمكن دمجها في الحمض النووي في النواة من خلال
نقل الجينات (Gene transfer). لقد ثبت أن عددًا كبيرًا من البشر لديهم بعض الحمض النووي للميتوكوندريا مدرجًا في جينوماتهم النووية. تدعم هذه النتائج
نظرية التعايش الداخلي التي تقول إن حقيقيات النوى تطورت من تعايش داخلي، وتحولت إلى عضيّات أثناء نقل معظم حمضها النووي إلى النواة، إذ تقلّص جينوم الميتوكوندريا في هذه العملية.
تُستخدم تقنيات تحليل الحمض النووي للميتوكوندريا في
العلوم الجنائية والطب الشرعي، خاصة الحالات التي تكون فيها
الكروموسومات النووية معطوبةً أو غير متوفرة. وفي العديد من القضايا الجنائية في العالم، استُخدِم الحمض النووي للميتوكوندريا في حل الجرائم والربط بين الأفراد ومسرح الجريمة والاستقصاء التاريخي للحقائق[18]. يمتد مجال أبحاث الحمض النووي للميتوكوندريا إلى ما هو أبعد من تطبيقات الطب الشرعي، ويتعمق في مجالات التطور البشري، وعلم الوراثة السكانية، وأنماط الهجرة المعقدة للمجموعات البشرية القديمة. من خلال فحص طفرات الحمض النووي وتغيراته واختلافاته للميتوكوندريا، بالإمكان فحص التاريخ التطوري للبشرية، والكشف عن النسيج الجيني المعقد الذي يحدد
السلف المشترك الأخير {{السلف المشترك الأخير: (Last common ancestor) هو أحدث فرد تنحدر منه جميع الكائنات الحية في مجموعة ما. إنها نقطة زمنية افتراضية، غالبًا ما تُمثل بمجموعة من الكائنات الحية، تتفرع منها جميع سلالات مجموعة محددة من الأنواع أو الأصناف.}}. إضافة إلى ذلك، برزت دراسة أمراض الميتوكوندريا بوصفها مجالًا بالغ الأهمية ضمن أبحاث الميتوكوندريا؛ ما حفّز التقدم الكبير في فهم الخلل الوظيفي في الميتوكوندريا، ووضع استراتيجيات علاجية محتملة. ومن الجدير بالذكر أن
العلاج ببدائل الميتوكوندريا {{العلاج باستبدال الميتوكوندريا: (Mitochondrial replacement therapy - MRT) يسمى أيضًا التبرع بالميتوكوندريا، وهو تقنية متخصصة في التلقيح الصناعي (IVF) تمنع انتقال أمراض الحمض النووي للميتوكوندريا (mtDNA) للجنين عندما تكون الأم حاملة لها. تستخدم هذه التقنية مادة وراثية من ثلاثة أفراد: الأب (للحيوانات المنوية) والأم (للبويضات التي تُفرّغ من الميتوكوندريا) ومتبرعة (لإعطاء ميتوكوندريا سليمة). الهدف الرئيسي هو تمكين النساء المصابات بعيوب في الحمض النووي للميتوكوندريا من إنجاب أطفال أصحاء وراثيًا.}} برز بوصفه وسيلة واعدة لمنع انتقال أمراض الميتوكوندريا من الأم إلى الطفل؛ ما يوفر الأمل للعائلات التي تتصارع مع هذه الحالات الوراثية المنهكة[19]. يؤكد تطوير
التصوير بالرنين المغناطيسي والتدخلات المبتكرة الأخرى على التأثير التحويلي لأبحاث الحمض النووي للميتوكوندريا في الممارسة السريرية؛ ما يمهّد الطريق لعلاجات شخصية ومستهدفة لاضطرابات الميتوكوندريا.
لكن حتى في خضم هذه التطورات الرائدة، تلوح الاعتبارات الأخلاقية بشكل بارز في المناقشات المحيطة بأبحاث الحمض النووي للميتوكوندريا، خاصة فيما يتعلق باستخدام العلاج باستبدال الميتوكوندريا والتعديل الوراثي للأجنة للتخفيف من أمراض الميتوكوندريا. تسلّط المناقشات الأخلاقية التي تتناول سلامة التقنيات، والموافقة المستنيرة (Informed consent)، والعواقب الطويلة الأجل، الضوءَ على المعضلات الأخلاقية المتأصلة في التدخلات الجينية، ما يستلزم اتباع نهج متوازن، يعطي الأولوية للتقدم العلمي، مع الحفاظ على المعايير الأخلاقية والقيم المجتمعية[20].
انشطارها واندماجها
الميتوكوندريا عضيّات ديناميكية دائمة التحرك والتحوّل الشكلي، وفي الحقيقة نادرًا ما يشبه شكلها شكلَ حبة الفاصولياء التي غالبًا ما تصوّرها كذلك كتب علم الأحياء. فقد تندمج اثنتان أو أكثر من الميتوكوندريا معًا، وقد تنقسم إحداهما إلى عضيتين أو أكثر (الشكل 7). يعد اندماج الميتوكوندريا وانشطارها من العمليات الأساسية التي تنظم السلوك الديناميكي وتشكل الميتوكوندريا داخل الخلايا. تُعَدّ هذه الآليات المعقدة ضرورية للحفاظ على وظيفة الميتوكوندريا، والتوازن الخلوي {{الاستتباب الخلوي (التوازن الخلوي): هو العملية البيولوجية التي تحافظ بها الكائنات الحية على استقرارها الداخلي رغم التغيرات الخارجية. ويشمل آليات التغذية الراجعة التي تنظم درجة الحرارة، ودرجة الحموضة، وتوازن السوائل، ومستويات العناصر الغذائية. تُنسق الأنظمة الرئيسية في الجسم (مثل
الغدد الصماء والجهاز العصبي) استجاباتها للتغيرات التي قد تؤدي إلى المرض، ما يضمن وظائف خلوية مثالية}}، والاستجابة لمختلف الإشارات الفيزيولوجية والبيئية. يمثل انشطار الميتوكوندريا واندماجها عمليات منظمة بدقة تحكم مورفولوجيا الميتوكوندريا وتوزيعها ووظيفتها داخل الخلايا[21].
[الشكل 7]
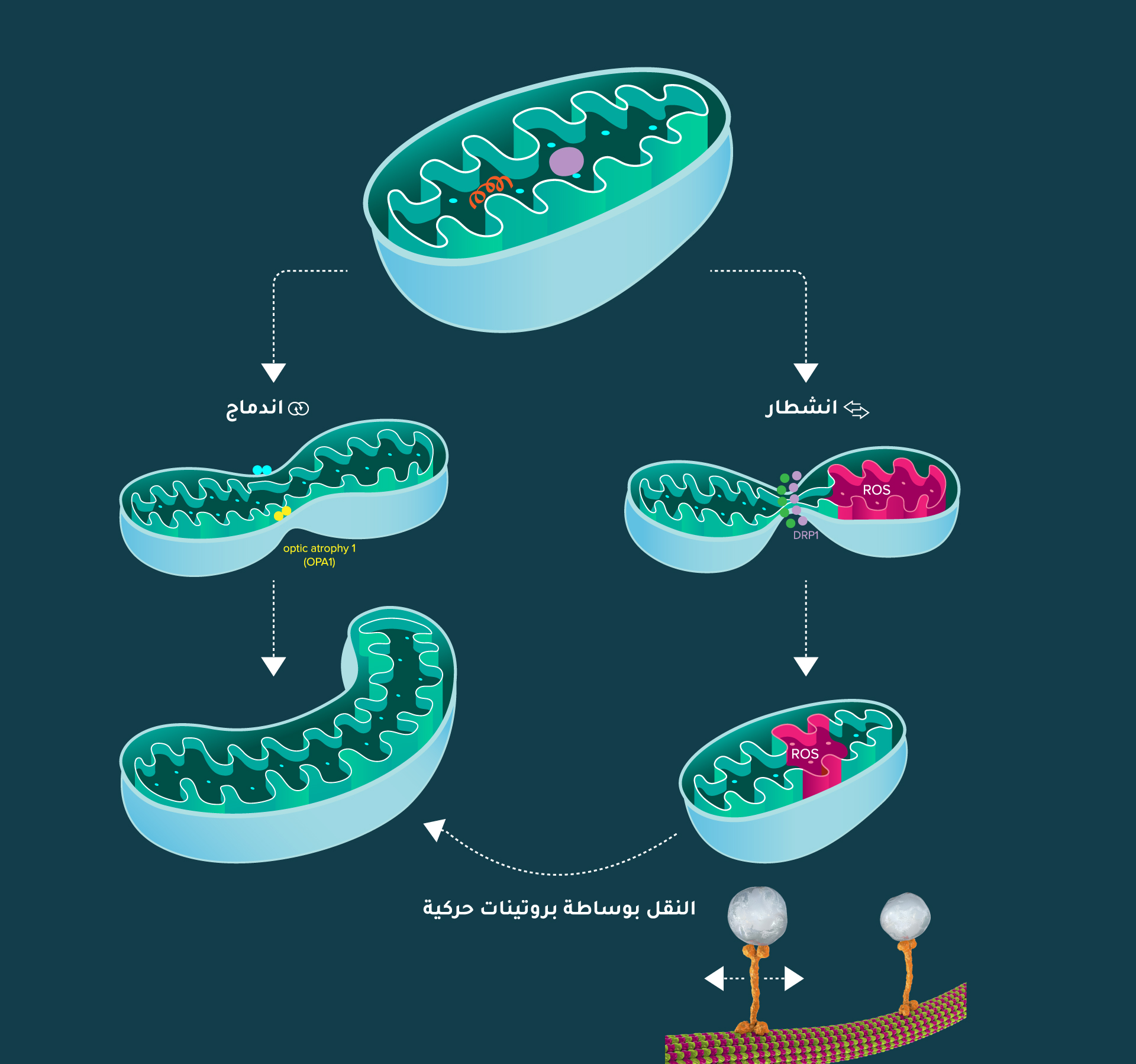 انشطار الميتوكوندريا واندماجها
انشطار الميتوكوندريا واندماجها
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
انشطارها
يشير انشطار الميتوكوندريا إلى العملية التي تنقسم فيها الميتوكوندريا إلى اثنتين أو أكثر من الميتوكوندريا الأصغر. تُنظَّم هذه العملية من خلال تفاعلات معقّدة بين البروتينات والعوامل التنظيمية التي تنسّق تقسيم أغشية الميتوكوندريا ومحتوياتها. يُعَدّ
البروتين المرتبط بالدينامين 1 (Dynamin-related protein 1 - Drp1) من بين العوامل الرئيسة في انشطار الميتوكوندريا، ويُحضَر إلى الغشاء الخارجي للميتوكوندريا؛ ليشكّل هياكل حلزونية تضيّق على الميتوكوندريا، وتقسمها في النهاية إلى أجزاء أصغر. يؤدّي انشطار الميتوكوندريا دورًا حيويًا في آليات مراقبة الجودة داخل الخلايا[22]؛ ما يسهّل إزالة الميتوكوندريا التالفة أو المختلة وظيفيًا من خلال عملية
الميتوفاجي {{الميتوفاجي: (Mitophagy) شكل متخصص من الالتهام الذاتي (Autophagy)، وهي عملية خلوية تقوم الخلايا بتكسير وإعادة تدوير مكوناتها الخاصة. في حالة الميتوفاجي، تستهدف الخلية الميتوكوندريا التالفة أو المختلة وظيفيًا على وجه التحديد استهداف وتزيلها. هذا الإزالة الانتقائية أمر بالغ الأهمية للحفاظ على الصحة الخلوية ومنع تراكم الميتوكوندريا الضارة التي يمكن أن تسهم في أمراض مختلفة.}}، وهي شكل انتقائي من
الالتهام الذاتي (Autophagy) يستهدف الميتوكوندريا.
اندماجها
على عكس الانشطار، يتضمن اندماج الميتوكوندريا دمج اثنتين أو أكثر منها لتكوين ميتوكوندريا واحدة أكبر حجمًا. وتخضع هذه العملية لمجموعة من بروتينات الاندماج التي تتوسط اندماج الأغشية الداخلية والخارجية للميتوكوندريا. تُسهِّل بروتينات الاندماج مثل
الميتوفوسين (Mfn1 وMfn2) وأوبا 1 (Opa1) ربط أغشية الميتوكوندريا وتقريبها ودمجها معًا؛ ما يؤدّي إلى تكوين شبكة من الميتوكوندريا المتّصلة. يعد اندماج الميتوكوندريا أمرًا بالغ الأهمية للحفاظ على وظيفتها، وتوزيع الحمض النووي فيها، وكفاءة
الاستقلاب الغذائي داخل الخلايا، كما أنه يُسهم في تبادل البروتينات والدهون والجزيئات الأخرى بين العديد من الميتوكوندريا، ما يضمن التجانس الوظيفي داخل شبكتها[23].
تنظيم العمليتين
يُنظَّم التوازن بين انشطار الميتوكوندريا واندماجها بإحكام من خلال مسارات إشارات مختلفة، بما في ذلك إشارات الكالسيوم، ومسارات
بروتين ماب كيناز (Mitogen activated protein kinase - MAPK)، وآليات استشعار حالة الطاقة مثل
بروتين كيناز المنشط بـالأدينوسين أحادي الفوسفات (AMP activated protein kinase - AMPK). إن خلل تنظيم ديناميكيات الميتوكوندريا، الذي يتميز بالانشطار المفرط أو ضعف الاندماج، متورط في مجموعة من الاختلالات الخلوية والحالات المرضية، بما في ذلك اضطرابات التمثيل الغذائي، والعمليات المرتبطة بالشيخوخة. يعد التفاعل الديناميكي بين انشطار الميتوكوندريا واندماجها أمرًا بالغ الأهمية للتكيف الخلوي مع الإجهاد وتقلبات الطلب على الطاقة وعمليات التمايز الخلوي. ارتبطت ديناميكيات الميتوكوندريا المختلة بأمراض مختلفة، كالسرطان، والأمراض الوراثية، وأمراض القلب، والأمراض التنكسيّة العصبية، وغيرها[24].
الأمراض الوراثية المرتبطة بها
تشمل أمراض الميتوكوندريا الموروثة، والمعروفة أيضًا باسم اضطرابات الميتوكوندريا أو أمراض الحمض النووي للميتوكوندريا، مجموعة متنوعة من الاضطرابات الوراثية التي تنشأ بسبب خلل في وظيفة الميتوكوندريا. قد تكون اضطرابات الميتوكوندريا ناجمة عن طفرات مكتسبة أو موروثة في الحمض النووي للميتوكوندريا، أو في الجينات النووية التي تشفّر لمكونات الميتوكوندريا، وقد تكون أيضًا نتيجة لخلل وظيفي مكتسب في الميتوكوندريا، بسبب الآثار الضارة للأدوية أو الالتهابات أو لأسباب بيئية أخرى[25].
بما أن الميتوكوندريا تورثها الأم، فإن أمراض الميتوكوندريا تُظهر نمطًا وراثيًا من جهة الأم (Maternal inheritance)، ومع ذلك، فإن الأساس الوراثي لهذه الأمراض متنوع. تُعَدّ الطفرات في الحمض النووي للميتوكوندريا ذات أهمية، خاصةً أنها يمكن أن تؤثر في نسخ متعددة من جينومات الميتوكوندريا داخل الخلية؛ ما يؤدّي إلى حالة تسمى
هيتيروبلازمي (Heteroplasmy)، حيث توجد ميتوكوندريا طبيعية ومختلة معًا في الخلية نفسها بنسب مختلفة. ويمكن أن تتسبب
طفراتالحمض النووي في النواة في الحصول على أمراض الميتوكوندريا من خلال التأثير على البروتينات المشاركة في بنيتها أو وظيفتها أو تنظيمها. قد تؤدي هذه الطفرات إلى ضعف التولّد الحيوي للميتوكوندريا، أو إنتاج الطاقة، أو ديناميكيات الميتوكوندريا (الانشطار والاندماج).[26]
سريريًّا، تتنوع أعراض أمراض الميتوكوندريا بشكل كبير، بدءًا من الأعراض الخفيفة إلى الاضطرابات الشديدة المتعددة الأنظمة التي تؤثر على أعضاء وأنسجة عديدة. تشمل المظاهر الشائعة:
ضعف العضلات (Myopathy)، وعدم تحمل التمارين الرياضية (Exercise intolerance)، واضطرابات القلب، وضعف البصر والسمع، واختلال وظائف
الجهاز الهضمي، واضطرابات الغدد الصماء، والأعراض العصبية؛ مثل: النوبات، والنوبات الشبيهة بالسكتة الدماغية، والضعف الإدراكي. يمكن أن يختلف عمر ظهور الأعراض وتطورها وشدتها بشكل كبير بين الأفراد المصابين بأمراض الميتوكوندريا؛ ما يؤدي غالبًا إلى تحديات تشخيصية وتعقيدات في إدارة المريض. تصنّف أمراض الميتوكوندريا إلى أنواع فرعية مختلفة بناءً على سماتها السريرية، والمسببات الوراثية، والأنسجة أو الأجهزة المصابة. تشمل هذه الأنواع الفرعية
متلازمة لي (Leigh syndrome) ومتلازمة ميلاس (MELAS syndrome) ومتلازمة بارث (Barth syndrome) واعتلال ليبر العصبي الوراثي البصري (LHON)، ومتلازمة كيرنز ساير (Kearns-Sayer syndrome)، وغيرها الكثير. قد يكون لكل نوع فرعي خصائص سريرية محددة، ومعايير تشخيصية، وأساليب إدارة مصممة لمواجهة التحديات الفريدة التي يفرضها المرض[27].
المراجع
Alberts, Bruce et al.
Molecular biology of the cell. 7th ed. New York: W. W. Norton & Company, 2022.
Alexeyev, Mikhail et al. “The Maintenance of Mitochondrial DNA Integrity--Critical Analysis and Update.”
Cold Spring Harb Perspect Biol. vol. 5, no. 5 (2013).
Boore, Jeffrey L. “Animal Mitochondrial Genomes.”
Nucleic Acids Research. vol. 27, no. 8 (1991). pp. 1767-1780.
Gorman, Gráinne S. et al. “Mitochondrial diseases.”
Nature Reviews Disease Primers. vol. 2 (2016).
Hardin, Jeff & Gregory Bertoni.
World of the cell. 9th ed. Boston: Pearson, [2016].
Henriquez, Fiona L. et al. “The unusual mitochondrial compartment of Cryptosporidium parvum.”
Trends Parasitol. vol. 21, no. 2 (2005). pp. 68-74.
Ladoukakis, Emmanuel D. & Eleftherios Zouros. “Evolution and Inheritance of Animal Mitochondrial DNA: Rules and Exceptions.”
Journal of Biological Research-Thessaloniki. vol. 24, no. 2 (2017).
Liu, Yasmine J. et al. “Mitochondrial fission and fusion: A dynamic role in aging and potential target for age-related disease.”
Mechanisms of Ageing and Development. vol. 186 (2020).
Mancuso, Michelangelo et al. “Mitochondrial DNA sequence variation and neurodegeneration.”
Human Genomics. vol. 3, no. 1 (2008). pp. 71-78.
Margulis, Lynn.
the life and legacy of a scientific rebel. Dorion Sagan (ed.). Vermont: Chelsea Green Publishing, 2012.
Martin, William F., Sriram Garg & Verena Zimborski. “Endosymbiotic theories for eukaryote origin.”
Philos Trans R Soc Lond B Biol Sci. vol. 370, no. 1678 (2015).
“Mitochondrial Disorders.”
National Institute of Neurological Disorders and Stroke. accessed on 2/10/2024, at:
https://acr.ps/1L9F2tY
Nelson, David L., Michael M. Cox & Aaron
A. Hoskins. Lehninger principles of biochemistry. 8th ed. Austin: Macmillan Learning, [2021].
Newson, Ainsley J., Stephen Wilkinson & Anthony Wrigley. “Ethical and legal issues in mitochondrial transfer.”
EMBO Mol Med. vol. 8, no. 6 (2016). pp. 589-591.
Rappocciolo, Emilia & Johnny Stiban. “Prokaryotic and Mitochondrial Lipids: A Survey of Evolutionary Origins.”
Adv Exp Med Biol. vol. 1159 (2019). pp. 5-31.
Ren, Lin et al. “Mitochondrial Dynamics: Fission and Fusion in Fate Determination of Mesenchymal Stem Cells.”
Front Cell Dev Biol. vol. 8 (2020).
Sagan, Lynn. “On the origin of mitosing cells.”
Journal of Theoretical Biology. vol. 14, no. 3 (1967). pp. 225-274.
Serasinghe, Madhavika N. & Jerry E. Chipuk. “Mitochondrial Fission in Human Diseases.”
Handb Exp Pharmacol. vol. 240 (2017). pp. 159-188.
Sharma, Hitika et al. “Development of mitochondrial replacement therapy: A review.”
Heliyon. vol. 6, no. 9 (2020).
Syndercombe Court, Denise. “Mitochondrial DNA in forensic use.”
Emerg Top Life Sci. vol. 5, no. 3 (2021). pp. 415-426.
Van der Giezen, Mark, Jorge Tovar & C. Graham Clark. “Mitochondrion-derived organelles in protists and fungi.”
Int Rev Cytol. vol. 244 (2005). pp. 175-225.
Wei, Wei et al. “Nuclear-embedded mitochondrial DNA sequences in 66,083 human genomes.”
Nature. vol. 611 (2022). pp. 105-114.
[1] David L. Nelson, Michael M. Cox & Aaron A. Hoskins,
Lehninger Principles of Biochemistry, 8th ed. (Austin: Macmillan Learning, [2021]).
[2] Ibid.
[3] Yasmine J. Liu et al., “Mitochondrial Fission and Fusion: A Dynamic Role in Aging and Potential Target for Age-related Disease,”
Mechanisms of Ageing and Development, vol. 186 (2020).
[4] Nelson, Cox & Hoskins op. cit.
[5] Jeff Hardin & Gregory Bertoni,
World of the cell, 9th ed. (Boston: Pearson, [2016]).
[6] Mark Van der Giezen, Jorge Tovar & C. Graham Clark, “Mitochondrion-derived Organelles in Protists and Fungi,”
Int Rev Cytol, vol. 244 (2005), pp. 175-225.
[7] Hardin & Bertoni,
op. cit.
[8] William F. Martin, Sriram Garg & Verena Zimborski, “Endosymbiotic Theories for Eukaryote Origin,”
Philos Trans R Soc Lond B Biol Sci, vol. 370, no. 1678 (2015).
[9] Lynn Margulis,
The Life and Legacy of a Scientific Rebel, Dorion Sagan (ed.) (Vermont: Chelsea Green Publishing, 2012).
[10] Lynn Sagan, “On the Origin of Mitosing Cells,”
Journal of Theoretical Biology, vol. 14, no. 3 (1967), pp. 225-274.
[11] Emilia Rappocciolo & Johnny Stiban, “Prokaryotic and Mitochondrial Lipids: A Survey of Evolutionary Origins,”
Adv Exp Med Biol, vol. 1159 (2019), pp. 5-31.
[12] Bruce Alberts et al.,
Molecular biology of the cell, 7th ed. (New York: W. W. Norton & Company, 2022).
[13] Emmanuel D. Ladoukakis & Eleftherios Zouros, “Evolution and Inheritance of Animal Mitochondrial DNA: Rules and Exceptions,”
Journal of Biological Research-Thessaloniki, vol. 24, no. 2 (2017).
[14] Jeffrey L. Boore, “Animal Mitochondrial Genomes,”
Nucleic Acids Research, vol. 27, no. 8 (1991), pp. 1767-1780.
[15] Wei Wei et al., “Nuclear-Embedded Mitochondrial DNA Sequences in 66,083 Human Genomes,”
Nature, vol. 611 (2022), pp. 105-114.
[16] Mikhail Alexeyev et al., “The Maintenance of Mitochondrial DNA Integrity--Critical Analysis and Update,”
Cold Spring Harb Perspect Biol, vol. 5, no. 5 (2013).
[17] Fiona L. Henriquez et al., “The Unusual Mitochondrial Compartment of Cryptosporidium Parvum,”
Trends Parasitol, vol. 21, no. 2 (2005). pp. 68-74.
[18] Denise Syndercombe Court, “Mitochondrial DNA in Forensic Use,”
Emerg Top Life Sci, vol. 5, no. 3 (2021). pp. 415-426.
[19] Hitika Sharma et al., “Development of Mitochondrial Replacement Therapy: A Review,”
Heliyon, vol. 6, no. 9 (2020).
[20] Ainsley J. Newson, Stephen Wilkinson & Anthony Wrigley, “Ethical and legal issues in mitochondrial transfer,”
EMBO Mol Med, vol. 8, no. 6 (2016), pp. 589-591.
[21] Lin Ren et al., “Mitochondrial Dynamics: Fission and Fusion in Fate Determination of Mesenchymal Stem Cells,”
Front Cell Dev Biol, vol. 8 (2020).
[22] Liu et al op. cit.
[23] Ibid.
[24] Madhavika N. Serasinghe & Jerry E. Chipuk, “Mitochondrial Fission in Human Diseases,”
Handb Exp Pharmacol, vol. 240 (2017). pp. 159-188.
[25] Michelangelo Mancuso et al., “Mitochondrial DNA Sequence Variation and Neurodegeneration,”
Human Genomics, vol. 3, no. 1 (2008), pp. 71-78.
[26] Gráinne S. Gorman et al., “Mitochondrial Diseases,”
Nature Reviews Disease Primers, vol. 2 (2016).
[27] “Mitochondrial Disorders,”
National Institute of Neurological Disorders and Stroke, accessed on 2/10/2024, at:
https://acr.ps/1L9F2tY