الدهون (وتدعى أيضًا الليبيدات، Lipids) فئة واسعة ومتنوعة هيكليًا من الجزيئات العضوية البيولوجية الكبيرة، تتميز بخصيصة
كره الماء (hydrophobicity)، فإن أي جزيء عضوي قليل الذوبان في الماء يصنّف تحت هذه الفئة. تنبع عدم قدرة الدهون على الذوبان في الماء، وقابليتها للذوبان في
المذيبات غير القطبية، مثل
الكلوروفورم أو
الإيثر، من وجود كثير من سلاسل
الهيدروكربون غير القطبية في بنيتها.
تُعد الدهون أساسية في أشكال الحياة المعروفة جميعها، إذ تؤدي ثلاثة أدوار بيولوجية رئيسة؛ فهي تعمل بوصفها المكون الأساسي للأغشية الخلوية جميعها، ما يوفر حاجزًا انتقائيًا يُعرّف الحياة ويُقسّمها؛ وهي الشكل الأكثر تركيزًا وكفاءة لتخزين الطاقة في الجسم، إذ يخزن الجسم الدهون ويكدسها لتشكل احتياطي وقود طويل الأمد؛ ثم إن كثيرًا من الجزيئات الدهنية تعمل بوصفها جزيئات إشارات حيوية، وهرمونات تُنظم مجموعة واسعة من العمليات الفيزيولوجية، من
الالتهاب والمناعة إلى
الأيض والتكاثر وموت الخلية.
أمّا كيميائيًا، فتتكون الدهون أساسًا من
الكربون والهيدروجين والأكسجين، وتصنف إلى ثماني فئات رئيسة، بحسب
نظام اتحاد استراتيجيات المستقلبات الدهنية ومساراتها الدولي (LIPID MAPS)، تشمل: الأسيلات الدهنية (مثل
الأحماض الدهنية)، والدهون الغليسرولية (مثل
الدهون الثلاثية)، والدهون الفسفورية (المكون الرئيس للأغشية)، والدهون السفينغولية (المهمة في
الإشارات الخلوية)، والستيرولات (مثل
الكوليسترول والهرمونات الجنسية)، والبرينولات (مثل بعض
الفيتامينات)، والدهون السكارية، ومتعددات الكيتيد. وتكمن أهمية هذا التنوع البنيوي في تنوع الوظائف التي تؤديها، بدءًا من العزل الحراري والحماية الميكانيكية للأعضاء، وصولًا إلى تسهيل هضم الدهون الغذائية عبر
الأحماض الصفراوية.
يخضع استقلاب الدهون في الجسم لعمليات دقيقة تشمل العمليات الهدمية (تحلل الدهون لتوليد الطاقة)؛ والبنائية (تصنيع الدهون للتخزين). ونظرًا لطبيعتها الكارهة للماء، تُنقل الدهون في مجرى الدم محاطة بالبروتينات، فتشكل
البروتينات الدهنية، مثل
الكيلوميكرونات، والبروتين الدهني منخفض الكثافة (LDL أو "الكوليسترول الضار") والبروتين الدهني عالي الكثافة (HDL أو "الكوليسترول النافع")، التي تؤدي أدوارًا حيوية في نقل الكوليسترول والدهون الأخرى. يرتبط اختلال توازن الدهون بعدد من الأمراض الخطرة، إذ يعد ارتفاع مستوى البروتين الدهني منخفض الكثافة، عاملًا خطرًا رئيسًا لتصلب الشرايين وأمراض القلب والأوعية الدموية، كذلك ترتبط
السمنة المفرطة والمتلازمة الأيضية بشكل وثيق باضطرابات
استقلاب الدهون. وتوصي الإرشادات الغذائية الحديثة بالحد من
الدهون المشبعة والمتحولة مع زيادة تناول
الدهون غير المشبعة، مثل تلك الموجودة في زيت الزيتون والأسماك الدهنية، لدورها في تعزيز صحة القلب والحد من الالتهابات.
التعريف
الدهن هو أي جزيء غير قابل للذوبان في الماء، وقابل للذوبان في المذيبات العضوية {{المذيبات العضوية: هي سوائل تحتوي على الكربون، مثل الإيثانول والإيثير والأسيتون وغيرها، قادرة على إذابة مواد عضوية أخرى (كارهة للماء)، تُستخدم على نطاق واسع في العمليات الصناعية والمختبرات لأداء عمليات الاستخلاص الكيميائية.}}. عادةً ما تشير الدهون البيولوجية إلى مجموعة واسعة من الجزيئات الطبيعية، التي تشمل
الأحماض الدهنية (Fatty acids)، والشموع، والأيكوسانويدات (Eicosanoids)، والدهون الأحادية (الغليسيريدات الأحادية، Monoglycerides)، والدهون الثنائية (الغليسيريدات الثنائية، Diglycerides)، والدهون الثلاثية (الغليسيريدات الثلاثية، Triglycerides)، والدهون الفسفورية (Phospholipids)، والدهون السفينغولية (Sphingolipids)، والستيرولات (Sterols)، والتربينات (Terpenes)، والبرينولات (Prenols)، والفيتامينات القابلة للذوبان في الدهون (مثل
فيتامينات أ،
د،
هـ،
ك)[1]. وعلى عكس المجموعات الرئيسة الأخرى من الجزيئات البيولوجية (الأحماض النووية، والبروتينات، والكربوهيدرات (السكريات))، فإن الدهون لا تتكون من
تفاعلات بلمرة (Polymerization reactions) بصورة عامة، بل يمكن تعريف الدهون بصورة أدق بأنها جزيئات كارهة للماء أو
أمفيباثية {{الأمفيباثية: مصطلح يصف جزيئًا يمتلك مناطق محبة للماء وأخرى كارهة لها، وهي سمة أساسية للفوسفوليبيدات، تُمكّنها من تكوين أغشية خلوية.}}، تنشأ كليًا أو جزئيًا من تفاعلات تكثيف (Condensation reactions) لثيوإسترات (Thioesters) قائمة على
الكربانيون (Carbanion)، و/ أو تفاعلات تكثيف وحدات آيزوبرين (Isoprene) قائمة على الكربوكاتيون (Carbocation) (الشكل1)[2]. تشمل الوظائف البيولوجية الرئيسة للدهون، دورها المحوري في تخزين الطاقة، وكونها مكونات هيكلية أساسية لأغشية الخلايا، وعملها المهم في نقل الإشارات الخلوية.
[الشكل1]
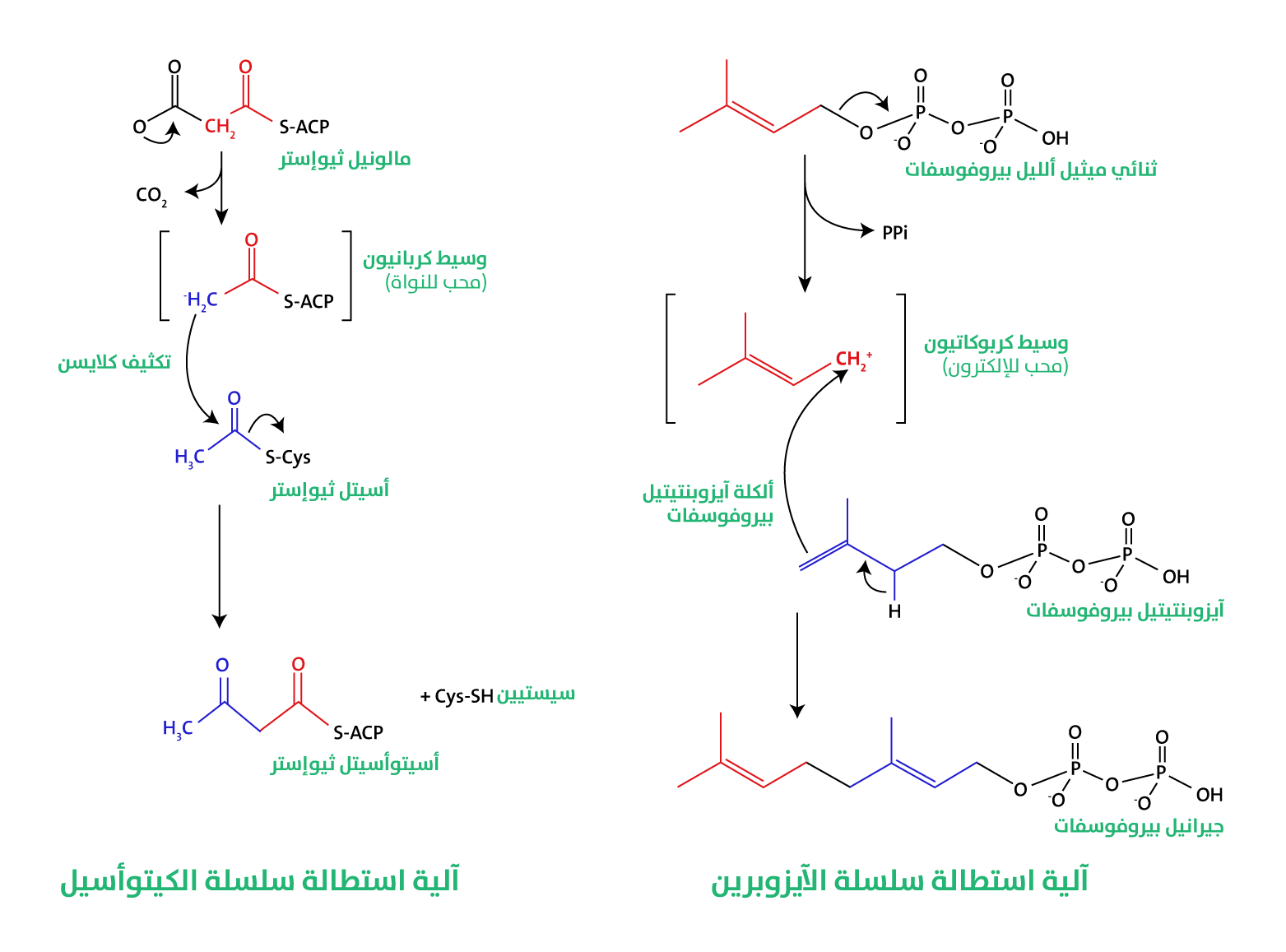 تكون الدهون عن طريق تفاعلات تكثيف تعتمد على الكربانيون أو على الكربوكاتيون
تكون الدهون عن طريق تفاعلات تكثيف تعتمد على الكربانيون أو على الكربوكاتيون
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
الخلفية التاريخية
يُعدّ تاريخ البحث العلمي في الدهون واحدًا من الأمور التي استغرق فهمها وقتًا طويلًا، ووضحت تدريجيًا، مدفوعة بالتقدم التكنولوجي في تقنيات
الكيمياء الحيوية التحليلية، ما زاد من الفهم المتزايد لدورها المحوري في علوم
الأحياء كافة. كان الناس يستخدمون الدهون في حياتهم العملية بشكل يومي، من دون أي فهم لطبيعتها الكيميائية، وقد بدأ الانتقال من التطبيق العملي للدهون إلى الفهم الكيميائي الحقيقي في أواخر القرن الثامن عشر، ويُنسب العمل الأساسي عالميًا إلى الكيميائي الفرنسي
ميشيل أوجين شيڤرول (Michel Eugène Chevreul، 1786-1889)، فمن خلال سلسلة من التحاليل الكيميائية الدقيقة للدهون الحيوانية، أثبت
شيڤرول أن الدهون ليست مواد بسيطة مفردة، بل تتكون من
الغليسرول (Glycerol) وأحماض دهنية محددة[3]. أثبت عمله الرائد
أبحاث كيميائية حول الدهون الحيوانية (Recherches chimiques sur les corps gras d'origine animale) عام 1823، الطبيعة الحقيقية لتفاعل
التصبن (Saponification)، موضحًا أنه عملية كيميائية يستبدل فيها أيونٌ قلويٌ جزيءَ
الغليسرول في
تفاعل إزاحة (Displacement reaction)، لتكوين ملح
الحمض الدهني (Fatty acid) أو
الصابون[4]. وفي سياق هذا العمل، حدد وأطلق أسماء على
أحماض دهنية محددة، مثل
حمض الستياريك (من الكلمة اليونانية للشحم، "ستيار" στέαρ)؛ وحمض الأوليك (من الكلمة اللاتينية oleum التي تعني زيت). وبعد دراسة
حصوات المرارة البشرية، اكتشف جزيئًا سمّاه "كوليسترينCholestérine "، وهو ما يعرف الآن بالكوليسترول (Cholesterol). واكتشف الكيميائي والسياسي الفرنسي
مارسيلين بيرثيلو (Marcellin Berthelot، 1827-1907) في عام 1859
المجموعة الوظيفية الكحولية (الهيدروكسيل) الموجودة على كربون رقم 3 فاقترح تسمية هذا المركب بالكوليسترول (المركبات العضوية التي تنتهي بـ"-ول" في معظمها تنتمي للكحوليات).
مهدت أعمال
شيڤرول الطريق لمجال كيمياء الدهون[5]، وكان العمل الضخم للعالم البيوكيميائي الألماني
يوهان لودڤيغ ثوديكوم (Johann Ludwig Thudichum، 1829-1901)، الذي نُشر عام 1884 بحثًا بعنوان
رسالة في التركيب الكيميائي للدماغ (A Treatise on the Chemical Constitution of the Brain) إنجازًا بارزًا في
الكيمياء التحليلية، إذ تمكن من خلال فحص دقيق لأدمغة البشر والحيوانات، أن يعزل ويصف كثيرًا من المركبات المعقدة، بما في ذلك
السفينغوميالين (Sphingomyelin)، والدهون السكرية (Glycolipids)، والسيفالينات (وهي ما تسمى الآن
الدهون الفسفورية)[6]. أما المصطلح الحديث نسبيًا "ليبيد، Lipide" (وهو مصطلح فرنسي مشتق من الكلمة اليونانية λίπος، أي "دهن")، فقد قدّمه رسميًا عالم الصيدلة الفرنسي
غابرييل برتران (Gabriel Bertrand، 1867-1962) عام 1923[7]، واعتمدته
جمعية الكيمياء الحيوية (Société de Chimie Biologique) رسميًا بعد ذلك بوقت قصير. حُوِّلت الكلمة لاحقًا إلى اللفظ الإنكليزي "ليبِد Lipid"، وهو المصطلح المستخدم اليوم في الأوساط العلمية[8].
شهد القرن العشرين سلسلة من الاكتشافات المحورية، التي تجاوزت التركيب العام إلى البنية الجزيئية الدقيقة، والمسارات الأيضية المختلفة للدهون، كان من أبرزها تعيين البنية الحلقية المندمجة المعقدة للستيرولات (Sterols)، مثل الكوليسترول. وقد أسهم عالما الكيمياء الألمانيان،
هاينريش أوتو ڤيلاند (Heinrich Otto Wieland، 1877-1957) الحائز على جائزة نوبل في الكيمياء عام 1927؛ وأدولف أوتو راينهولد ڤينداوس (Adolf Otto Reinhold Windaus، 1876-1959) الحائز على جائزة نوبل في الكيمياء عام 1928 في إثباتها. مُنح ڤيلاند جائزته لأبحاثه في تكوين الأحماض الصفراوية (bile acids)[9]، وكان عمله خطوة أولى حاسمة، لأن الأحماض الصفراوية مشتقة من الكوليسترول، ثم مُنح ڤينداوس جائزته في العام التالي "للخدمات التي قدمها من خلال بحثه في تكوين
الستيرولات وعلاقتها بالفيتامينات"[10]، وقد أدى عملهما المشترك، وعمل كثير من الباحثين الآخرين في النهاية، على تحديد التركيب الصحيح لنواة الستيرولات {{نواة الستيرولات: (Sterol nucleus) بنية هيدروكربونية صلبة مكونة من أربع حلقات مدمجة، ثلاث منها سداسية وواحدة خماسية. وهي موجودة في الستيرولات جميعها، مثل الكوليسترول.}} رباعي الحلقات، وهو إنجاز جوهري[11].
لم يكن اللغز الكبير التالي هو تركيب الدهن، بل كيفية تصنيعه في الجسم، وقد واجه هذا التحدي الألمانيان
كونراد إميل بلوخ (Konrad Emil Bloch، 1912-2000)، وفيودور لينين (Feodor Lynen، 1876-1959)، اللذان مُنحا جائزة نوبل في الفيزيولوجيا أو الطب عام 1964، لعملهما الرائد في الاصطناع الحيوي للكوليسترول والأحماض الدهنية[12]، فقد استطاعا رسم المسار الأيضي المعقد لاصطناع الكوليسترول بدقة، باستعمال
النظائر المشعة (Radioisotopes) المتاحة حديثًا في وقتهما كمتتبعات الأثر (tracers). هذا المسار المكون من 36 خطوة، يتحول فيه جزيء
الأسيتات (acetate) المكون البسيط والمؤلف من ذرتي
كربون، إلى بنية الكوليسترول المعقدة المكونة من 27 كربونًا[13]. كشف هذا الإنجاز الضخم عن غموض عملية أيضية رئيسة، مهدت الطريق لتطوير
علم الأدوية الحديث.
في الوقت نفسه، كان فهم
الأغشية الخلوية يشهد ثورة خاصة به، إذ اكتشف عالم النبات السويسري
كارل نيغلي (Carl Wilhelm von Nägeli، 1817-1891)
غشاء الخلية (Cell membrane) عام 1855، وبرهن
إرنست أوڤرتون (Ernest Overton، 1865-1933) في عام 1895، أن المواد القابلة للذوبان في الدهون تخترق
الخلايا بسهولة أكبر، وأن هناك مقاومة عالية لمرور التيار الكهربائي عبر الغشاء، وبناء عليه، استنتج أن الغشاء الخلوي يتكون من الدهون[14]. في عام 1925، استخرج العالمان الهولنديان إيڤيرت غورتر (Evert Gorter، 1881-1954)؛ وفرانسوا غريندل (François Grendel، 1897-1969)، الدهون من أغشية خلايا الدم الحمراء، ولحظا أنها تغطي مساحة ضعف مساحة سطح خلايا الدم الحمراء، واستنتجا أن الغشاء يتكون من طبقة ثنائية من الدهون (Bilayer). وعلى الرغم من صحة استنتاجاتهما، فإن بعض البيانات التجريبية كانت خاطئة، مثل سوء تقدير مساحة الطبقة الأحادية الدهنية وضغطها، وعدم القدرة على استخلاص الدهون بشكل كامل، كذلك أخفقا في وصف وظيفة الغشاء، وافترضا افتراضات خاطئة، مثل افتراض أن الأغشية الخلوية تتكون في معظمها من الدهون من دون اعتبار للبروتينات. ومع ذلك، وبشكل عام، أصبح هذا التصور لبنية الطبقة الثنائية الدهنية هو الافتراض الأساسي لكل تحسين لاحق في نماذج الغشاء[15]، فقد وصف "نموذج الشطيرة" (sandwich model) المبكر، الذي اقترحه العالمان الإنكليزيان هيو داڤسون (Hugh Davson، 1909-1996) وجيمس دانييلي (James Danielli، 1911-1984) عام 1935، طبقة ثنائية دهنية ثابتة مغلفة بطبقة رقيقة من بروتينات الغشاء[16]. في الخمسينيات من القرن العشرين، استطاع العلماء التأكيد على وجود الأغشية البلازمية باستعمال
المجهر الإلكتروني (Electron microscopy)، إذ استخدم
ديفيد روبرتسون (David Robertson) صبغة المعادن الثقيلة على الأغشية البلازمية، ولحظ وجود نمط ثلاثي الطبقات، يبدو أنه يتوافق مع
نموذج دافسون-دانييلي، واقترح أن الأغشية تتكون من طبقتين دهنيتين، مغطاة على كلا السطحين بطبقات رقيقة من البروتينات[17]. استُبدل هذا النموذج عام 1972 بالنموذج الفسيفسائي المائع (Fluid mosaic model)، الذي اقترحه
سيمور سينغر (Seymour J. Singer، 1924-2017) وغارث نيكولسون (Garth L. Nicolson، 1943-)، وأسس هذا النموذج الجديد الطبقة الدهنية الثنائية، ليس بنية صلبة، بل مصفوفة ديناميكية سائلة تُدمج فيها بروتينات الغشاء وتستطيع الانتشار داخلها، وهو مفهوم لا يزال حجر الزاوية في
علم الخلية وعلم الخلية البنيوي (الشكل2)[18].
[الشكل 2]
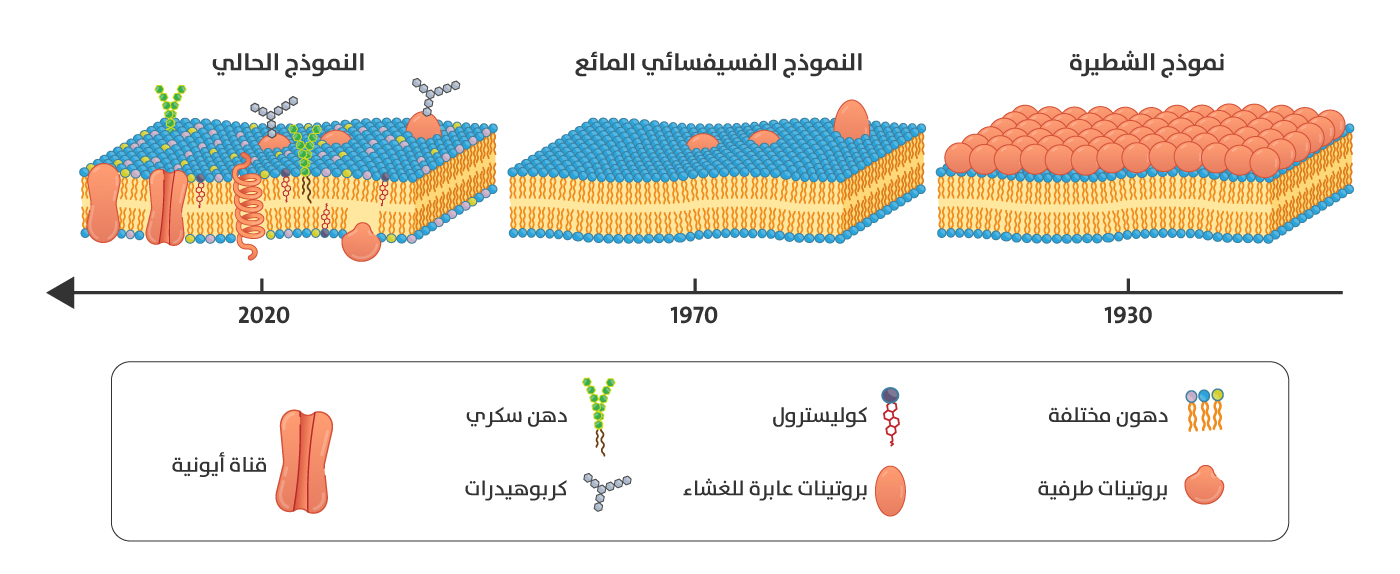 التطور التاريخي في نماذج الغشاء الخلوي، من نموذج الشطيرة لداڤسون ودانيللي إلى النموذج المعتمد حاليًا
التطور التاريخي في نماذج الغشاء الخلوي، من نموذج الشطيرة لداڤسون ودانيللي إلى النموذج المعتمد حاليًا
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
شهد منتصف القرن العشرين ظهور أزمة صحية عامة، وهو انتشار وباء
أمراض القلب والأوعية الدموية في الدول الغربية، وقد وفّر هذا التحدي الطبي الزخم لعصر جديد من الدراسات الوبائية واسعة النطاق، فكانت دراسة فرامنغهام للقلب (Framingham heart study)[19]، التي أُطلقت عام 1948 في فرامنغهام في ولاية ماساتشوستس الأميركية، دراسةً رائدة طويلة الأمد، حددت بشكل قاطع أن ارتفاع ضغط الدم وارتفاع نسبة الكوليسترول في الدم، هي عوامل خطرة رئيسة لأمراض القلب[20]، وقد سار هذا العمل بالتوازي مع الدراسات المؤثرة التي أجراها عالم وظائف الأعضاء
أنسيل كيز (Ancel Keys، 1904-2004). أشارت أعمال كيز، بما في ذلك "دراسته حول سبع دول" التي بدأت عام 1958[21]، إلى وجود صلة قوية بين تناول الدهون في الغذاء، ولا سيما الدهون المشبعة (Saturated fats)، ومستويات الكوليسترول في الدم، ما أدى إلى ظهور "فرضية العلاقة بين النظام الغذائي وصحة القلب"[22]، إلا أن هذه الفرضية كانت مثيرة للجدل منذ البداية، فقد تعرض رسمه البياني الشهير لعام 1953، الذي أظهر ارتباطًا قويًا بين استهلاك الدهون ومعدلات الوفيات بأمراض القلب، لانتقادات لاحتمالية "انتقاء" بيانات من ست دول فقط[23]. كذلك جادل النقاد بأن نماذج كيز، بما في ذلك معادلاته التنبؤية لمستوى الكوليسترول في الدم، لم تُفرّق بين الدهون المشبعة الطبيعية والدهون المتحولة {{الدهون المتحولة: (Trans fats) هي دهون تنتج صناعيًا بسبب الهدرجة غير المكتملة للدهون غير المشبعة، وتحتوي على أحماض دهنية غير مشبعة، ذات ذرات هيدروجين على الطرفين المتقابليين من رابطة الكربون المزدوجة، ما يعطي شكل المركب شكلًا غير منحنٍ.}} الصناعية، وهو تمييز جوهري لم يُفهم تمامًا في ذلك الوقت، وأسهم في تبني الجمهور الخاطئ للأنظمة الغذائية منخفضة الدهون[24]، ولم يأتِ الإثبات النهائي القاطع لهذه الفرضية من هذه الدراسات الرصدية، بل من فئة جديدة من الأدوية. في عام 1973، كان عالم
الكيمياء الحيوية الياباني
أكيرا إندو (Akira Endo، 1933-2024) رائدًا في البحث عن مركب لخفض الكوليسترول، مُفترضًا وجود مُثبط طبيعي لتخليق الكوليسترول في الكائنات الدقيقة[25]. وقد أدى فحصه الشامل لآلاف الأنواع الفطرية إلى اكتشاف
الميڤاستاتين (Mevastatin) (المعروف أيضًا باسم كومباكتين)، وهو أول ستاتين على الإطلاق، معزول من فطر
البنسيليوم سيترينوم (Penicillium citrinum)[26]. كان هذا الاكتشاف نقطة تحول، فرغم أن
الميڤاستاتين لم يُطرح نفسه في الأسواق بسبب آثاره الجانبية، فإنه ألهم شركات الأدوية في العالم، بما في ذلك
شركة ميرك (Merck)، لتطوير ستاتينات أخرى مثل لوڤاستاتين وسيمڤاستاتين. قدمت التجارب السريرية التي أُجريت في تسعينيات القرن الماضي باستخدام هذه الأدوية، أدلةً سببية دامغة عجزت عقودٌ من الدراسات الوبائية عن إثباتها، ما حوّل "فرضية الدهون" إلى حجر الزاوية في
طب القلب الوقائي[27].
وفي ثمانينيات القرن العشرين، زادت أبحاث الدهون، وتوصل الحقل لإنجازين محوريين حازا على جائزة نوبل في الفيزيولوجيا أو الطب، مُنحت الجائزة الأولى عام 1982 لكل من سوني كارل بيغستروم (Sune Karl Begström)، وبينغت صمويلسون (Bengt Samuelsson)، وجون ڤين (John R. Vane)، تكريمًا لاكتشافاتهم المتعلقة بدهون البروستاغلاندين (Prostaglandin) والمواد النشطة بيولوجيًا ذات الصلة، وهي نظام من الإشارات النسيجية الموضعية، يتكون من الأحماض الدهنية غير المشبعة، مثل
حمض الأراكيدونيك (Arachidonic acid). واستكمالًا لنتائج سابقة كانت في الثلاثينيات للعالمين أولف فون أويلر (Ulf von Euler) وغولدبلات (Goldblatt)، اللذين وجدا بشكل مستقل أن ثمة مواد في الحويصلات المنوية والسائل المنوي، تحفز انقباض
الرحم، وسمى فون أويلر المواد خطأً
بروستاغلاندين، لاعتقاده أنها تفرز من
غدة البروستاتا (Prostate gland)[28]، وعزل بيغستروم وحدد بنية عدد من البروستاغلاندينات، ووجد أن أصلها الأحماض الدهنية غير المشبعة (Unsaturated fatty acids). ثم رسم
صمويلسون خريطة مفصلة لعملية أيضها، محددًا المركبات الرئيسة مثل
الثرومبوكسانات (Thromboxanes) واللوكوترينات (Leukotrienes). وأسهم ڤين باكتشافه للبروستاسيكلين (Prostacyclin)، والأهم من ذلك، بإثباته أن الأدوية المضادة للالتهابات مثل
الأسبرين، تعمل عن طريق منع تكوين البروستاغلاندين والثرموبوكسان[29]. أحدث التقدم الكبير الثاني، الذي منح مايكل براون (Michael S. Brown)، وجوزيف غولدستين (Joseph L. Goldstein) جائزة نوبل عام 1985، ثورةً في فهم استقلاب الكوليسترول، من خلال اكتشافهما
لمستقبلات البروتين الدهني منخفض الكثافة (LDL receptor)، ووجدا أن
الخلايا تستخدم هذه المستقبلات السطحية، للتوسط في امتصاص
البروتين الدهني منخفض الكثافة (LDL)، الناقل الرئيس للكوليسترول في الدم. والأهم من ذلك، أثبتا أن
مرض فرط كوليسترول الدم العائلي الوراثي (Familial hypercholesterolemia)، ينتج من نقص في مستقبلات البروتين الدهني منخفض الكثافة، وأن حلقة التغذية الراجعة الطبيعية (إذ يثبط امتصاص الكوليسترول تكوين كل من الكوليسترول ومستقبلات البروتين الدهني منخفض الكثافة) تُنظم مستويات الكوليسترول في الدم[30]. وقد وفّر عملهما إطارًا جديدًا لفهم
تصلب الشرايين وعلاجها.
ركّزت ثورةٌ أحدث في علم بيولوجيا الدهون على وظائف الإشارة للدهون السفينغولية (Sphingolipids)، التي كان يُعتقد سابقًا أنها مجرد مكونات هيكلية لأغشية الخلايا، ومؤسسا هذا المجال، المعروف باسم بيولوجيا
الدهون السفينغولية (Sphingolipid biology)، هما العالمان العربيان
يوسف حنون (Yusuf Awni Hannun، 1955-) الفلسطيني الأصل، وزوجته الراحلة اللبنانية الأصل
لينا عبيد (Lina Marie Obeid، 1955-2019). أنشأ حنون المجال في السبعينيات والثمانينيات من القرن العشرين، وعمل مع زوجته لعقود، وكان لهما دور أساسي في إثبات أن مستقلَبات الدهون السفينغولية، مثل
السيراميد (Ceramide) والسفينغوسين 1-فوسفات (Sphingosine 1-phosphate)، ليست خاملة، بل تعمل بوصفها رسلًا ثانوية فعالة، تُنظّم العمليات الحيوية في الخلايا. وقد أثبتت أبحاثهما أن السيراميد وسيط رئيس في
استماتة الخلايا (الموت الخلوي المبرمج، Apoptosis)[31] وتوقف دورة الخلية (Cell cycle arrest)[32]، ما وفر إطارًا جديدًا لفهم آليات
السرطان وأمراض أخرى[33]. وقد نقلت إسهاماتهما الدهون السفينغولية من مجالٍ خفي في
الكيمياء الحيوية، إلى عوامل محورية في نقل الإشارات الخلوية، ما أوجد مجالًا دراسيًا جديدًا وحيويًا، لا يزال يُقدّم إسهامات أساسية في دراسة مسببات الأمراض وتوفير أهداف علاجية جديدة.
وقد اتسم أواخر القرن العشرين وأوائل القرن الحادي والعشرين بظهور علم
الليبِدوميكس، وهو فرع متخصص من علم
الأيض، يستند بفضل التطورات الثورية في قياس
الطيف الكتلي (Mass spectrometry)، إلى تحليل واسع النطاق وعالي الإنتاجية للمجموعة الكاملة من الدهون (الليبيدوم، Lipidome) في
الخلية أو
النسيج أو الكائن الحي[34]. ويتجاوز هذا النهج دراسة الجزيئات المفردة، إلى فهم الشبكة الكاملة لمسارات أيض الدهون وأدوارها المعقدة في الصحة والمرض[35].
يرتبط تاريخ دراسات الدهون ارتباطًا وثيقًا بالإسهامات الجليلة للحائزين على جوائز نوبل، فقد مهدت أبحاثهم الطريق لإنجازات طبية وصيدلانية كبرى، إذ حوّلت أعمالهم الدهون من مجرد مخازن طاقة إلى جزيئات معقدة ذات أدوار حيوية في البنية والاستقلاب والإشارات، ما يُظهر كيف يمكن للاكتشافات التأسيسية أن تُحدث تقدمًا ثوريًا في الوقاية من الأمراض وعلاجها (الجدول 1).
[الجدول 1]
جوائز نوبل للإسهامات العلمية في علم الدهون
الفائز/ون |
السنة |
الحقل |
وصف الإسهام |
|---|
هاينريش أوتو ڤيلاند | 1927 | الكيمياء | اكتشاف تركيب الأحماض الصفراوية، خطوة حاسمة في فهم الهيكل الأساسي للستيرولات. |
أدولف ڤينداوس | 1928 | الكيمياء | اكتشاف تركيب الستيرولات، بما في ذلك الكوليسترول، وعلاقتها بالفيتامينات. |
كونراد بلوخ وفيودور لونين | 1964 | الفيزيولوجيا أو الطب | اكتشاف المسار الحيوي الكامل للكوليسترول من الأسيتات، المكون من 36 خطوة. |
سوني كارل بيغستروم، وبينغت صمويلسون، وجون ڤين | 1982
| الفيزيولوجيا أو الطب | اكتشاف البروستاغلاندينات والمواد ذات الصلة. |
مايكل براون وجوزيف غولدستين | 1985 | الفيزيولوجيا أو الطب | اكتشاف مستقبل البروتين الدهني منخفض الكثافة (LDL receptor)، وكيفية تنظيم الخلايا للكوليسترول في الدم والأساس الجيني لفرط كوليسترول الدم العائلي الوراثي. |
التركيب والخصائص الكيميائية
تتكون الدهون بصورة أساسية من ذرات الكربون والهيدروجين والأكسجين، وتتضمن بعض الفئات المعينة منها عناصر أخرى، فعلى سبيل المثال، تحتوي
الدهون الفسفورية على عنصر الفوسفور، في حين تحتوي الدهون السفينغولية على النيتروجين. تتمثل سمة الجزيئات الدهنية المميزة جميعها في كرهها للماء (Hydrophobicity)، التي تنجم عن وجود أجزاء كبيرة من بنيتها، تتكون من روابط كربون - هيدروجين غير القطبية، مثل سلاسل
الهيدروكربون الطويلة أو الحلقات المندمجة[36]. تجعل هذه الخصيصة الدهون غير قابلة للامتزاج بالماء، في حين تذوب بسهولة في المذيبات العضوية غير القطبية، كالأسيتون والإيثر والكلوروفورم.
ومع أن الدهون تشترك في كرهها للماء، فإن بعض الفئات منها، ولا سيما تلك الموجودة في الأغشية، لديها خصيصة مميزة، وهي الأمفيباثية، وهي احتواء الجزيء على طرف كاره للماء (Hydrophobic) وآخر محب للماء (Hydrophilic). تتمتع هذه الجزيئات، مثل الدهون الفسفورية، بطبيعة مزدوجة: مجموعة "رأس" قطبية محبة للماء، ومجموعة "ذيل" واحدة أو أكثر غير قطبية كارهة للماء[37]. يمكن أن تختلف المجموعة الرئيسة في طبيعتها الكيميائية، إذ تحتوي على جزيء فوسفات مرتبط بكحول (في
الدهون الفسفورية المشتقة من الغليسرول (غليسروفسفوليبيدات، Glycerophospholipids)، أو
كربوهيدرات (في
الدهون السكرية، Glycolipids)، أو مجموعة
هيدروكسيل بسيطة (في
الستيرولات أو
السيراميد (Ceramide). عادةً ما تكون الذيول سلاسل طويلة من الأحماض الدهنية، التي تحتوي على روابط كربون - كربون أحادية وثنائية[38]. في البيئة المائية، تتجمع هذه الدهون تلقائيًا في هياكل منظمة لحماية ذيولها الكارهة للماء وحفظها بعيدًا عنه، مع تعريض رؤوسها المحبة للماء له (الشكل 3)[39]. تتأثر الخصائص الفيزيائية للدهون بشكل كبير ببنية سلاسلها الهيدروكربونية، ولا تحتوي الأحماض الدهنية المشبعة على روابط مزدوجة بين ذرات الكربون. يسمح غياب هذه الروابط المزدوجة لسلاسل الهيدروكربون المستقيمة بالتجمع معًا بترابط وترتيب مُحكَم، ما يزيد من
قوى ڤان دير ڤالس {{قوى ڤان دير ڤالس: (Van der Waals forces) مصطلح شامل لقوى التجاذب الضعيفة بين الجزيئات، التي تشمل قوى لندن، وتجاذبات ثنائي القطب-ثنائي القطب، وقوى ثنائي القطب المُستحثة. تعرّف هذه القوى بأنها تجاذبات ضعيفة وقصيرة المدى بين الجزيئات غير المشحونة، تنشأ عن عدم تماثل الإلكترونات العابرة في الذرات.}} إلى أقصى حد. ينتج من هذا التجمع المحكم درجة انصهار أعلى، ما يجعلها صلبة عادة في درجة حرارة الغرفة (مثلما هو موجود في الزبدة والشحوم الحيوانية). في المقابل، تحتوي الأحماض الدهنية غير المشبعة على رابطة مزدوجة واحدة (أحادية غير مشبعة، monounsaturated) أو أكثر (متعددة غير مشبعة، polyunsaturated). تحدث هذه الروابط المزدوجة، بسبب أنها في
التركيب المقرون (Cis)، انحناءات حادة في سلسلة الهيدروكربون، تمنع هذه الانحناءات التكتل المحكم، وتخفض درجة الانصهار، وتجعلها سائلة عادةً في درجة حرارة الغرفة (مثل الأحماض الدهنية الموجودة في زيت الزيتون وزيت السمك، والزيوت النباتية بشكل عام). كذلك يؤثر طول سلسلة الهيدروكربون في درجة الانصهار، إذ تكون درجات انصهار السلاسل الأطول أعلى[40].
[الشكل 3]
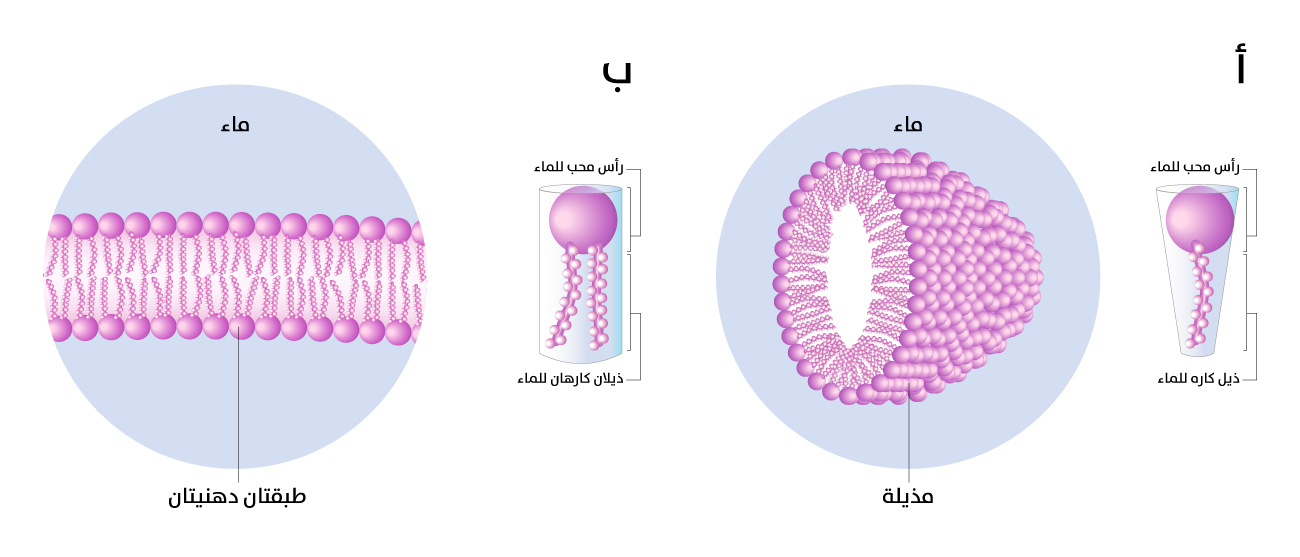 تتشكل المذيلة عندما يكون الدهن مكونًا من ذيل واحد، في حين تتشكل طبقات من الدهون عندما يكون الجزيء الدهني يحتوي على ذيلين
تتشكل المذيلة عندما يكون الدهن مكونًا من ذيل واحد، في حين تتشكل طبقات من الدهون عندما يكون الجزيء الدهني يحتوي على ذيلين
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تصنيف الدهون
استلزم التنوع البنيوي والوظيفي الهائل للدهون تطوير نظام تصنيف شامل ومنهجي، وقد طور
اتحاد استراتيجيات المستقلَبات الدهنية ومساراتها {{اتحاد استراتيجيات المستقلبات الدهنية ومساراتها:
Lipid Metabolites and Pathway Strategy, LIPID MAPS: بوابة إلكترونية مصممة لتكون مرجعًا لموارد علم الليبدوميكس. وقد قادت هذه المبادرة التي أسست عام 2003، إلى تصنيفات حديثة للدهون البيولوجية، مقسّمةً إياها إلى ثماني فئات عامة.}} الدولي هذا النظام ونقحه، إذ تُقسّم الدهون إلى ثماني فئات رئيسة بناءً على تركيبها الكيميائي وأصلها الحيوي[41]. يُعد هذا النظام معيارًا عالميًا لأبحاث الدهون وإدارة بياناتها، وهو يتجاوز التصنيف التقليدي القديم للدهون على أنها إما "دهون بسيطة" وإما "دهون معقدة". وبحسب التصنيف الحديث، فإن الدهون تنتمي إلى المجموعات التالية:
- الأسيلات الدهنية (Fatty acyls): تُعدّ هذه الأسيلات اللبنات الأساسية لمعظم الدهون المعقدة، وهي أحماض كربوكسيلية ذات سلسلة هيدروكربونية أليفاتية طويلة وغير متفرعة. تشمل هذه الفئة الأحماض الدهنية المشبعة، والأحادية غير المشبعة، والمتعددة غير المشبعة. من الأسيلات الدهنية
أحماض أوميغا 3 الدهنية وأحماض أوميغا 6، التي تشكل النسبة بينهما مؤشرًا لصحة القلب والأوعية الدموية. كذلك تشمل هذه الفئة جزيئات إشارة مهمة، مثل الأيكوسانويدات والدوكوسانويدات، المشتقة من الأحماض الدهنية المتعددة غير المشبعة ذات 20 و22 ذرة كربون، على التوالي. وتشمل المجموعة أيضًا مشتقات الأحماض الدهنية، مثل الشموع، وهي إسترات ناتجة من تفاعل الأحماض الدهنية طويلة السلسلة مع الكحوليات طويلة السلسلة[42].
- الدهون الغليسرولية (Glycerolipids): تشمل هذه الفئة الدهون التي تحتوي على هيكل يتكون من الكحول الثلاثي الغليسرول (Glycerol). أكثر أعضائها وفرةً هي
ثلاثي أسيل الغليسرول (الدهون الثلاثية {{الدهون الثلاثية: المكونات الرئيسة للدهون في الجسم، وتتكون من جزيء غليسيرول مُؤستر بثلاثة أحماض دهنية؛ وهي جزيئات فعالة لتخزين الطاقة على المدى الطويل، يؤدي تراكمها في الدم إلى مشكلات صحية كبيرة.}})، التي تتكون من جزيء غليسرول مؤستر (Esterified)، مع ثلاث سلاسل من الأحماض الدهنية. وظيفتها الأساسية تخزين الطاقة على المدى الطويل في
قطرات الدهون {{قطرات الدهون: هياكل ديناميكية داخل الخلايا، تخزن الدهون المحايدة مثل الدهون الثلاثية، ما يوفر مخزونًا للطاقة، وينظم توازن الدهون، لمنع السمية الخلوية للدهون.}} الموجودة في الأنسجة الدهنية وبذور النباتات[43].
- الدهون الفسفورية (Glycerophospholipids): وتُعرف أيضًا باسم الدهون الغليسروفسفورية أو الفوسفوليبيدات، هي مكونات أساسية للطبقة الدهنية الثنائية في الخلايا، علاوة على دورها في عمليات الأيض وانتقال الإشارة. تشكل الدهون الفسفورية المكونات الهيكلية الأساسية للأغشية الخلوية وأغشية العضيات جميعها، وهي جزيئات أمفيباثية مبنية على هيكل من الغليسرول، تتكون من مجموعة رأسية محبة للماء (تحتوي على مجموعة فوسفات مرتبطة بجزيئات أخرى)، وذيلين من بقايا الأحماض الدهنية الكارهة للماء، وتُحدد طبيعة مجموعة الرأس النوع المحدد من الدهن الفسفوري (مثل فوسفاتيديل كولين (Phosphatidylcholine)). وعلاوة على أنها مكون أساسي للأغشية الخلوية، ومواقع ارتباط للبروتينات داخل الخلايا وبينها، فإن بعضها في الخلايا حقيقية النواة، مثل
فوسفاتيديل إينوسيتول (Phosphatidylinositol) وأحماض الفوسفاتيديك (Phosphatidic acids)، إما أن تكون سلائف لرسل ثانوية (Second messengers) مشتقة من الغشاء، وإما هي نفسها هذه الرسل، ما يسهم في انتقال الإشارة في داخل الخلية[44].
- الدهون السفينغولية (Sphingolipids): ترتكز هذه الفئة المتنوعة من الدهون على الكحول الأميني سفينغوسين (Sphingosine) بدلًا من الغليسرول. يرتبط حمض دهني بمجموعة الأمين من السفينغوسين لتكوين السيراميد (Ceramide)، وهو الوحدة الهيكلية المركزية لهذه الدهون. تشمل هذه الفئة السفينغوميالين (Sphingomyelin)، وهو مكون رئيس لغمد الميالين الموجود في الخلايا العصبية، والدهون السفينغولية السكرية (مثل السيريبروسيدات والغانغليوسيدات)، وهي دهون مهمة توجد على سطح الخلايا، تساعد الخلايا على التعرف على بعضها والالتصاق بها وبالأسطح[45].
-
الستيرولات (Sterols): تُعرف هذه الفئة ببنيتها المكونة من أربع حلقات هيدروكربونية مُدمجة (ثلاث حلقات سداسية وواحدة خماسية). الكوليسترول هو الستيرول الأساسي في الخلايا الحيوانية، ويؤدي كثيرًا من الأدوار، مثل تعديل سيولة الأغشية وتنظيمها، وكونه المركب الأساسي الذي يؤدي لتكوين الهرمونات الستيرويدية جميعها (مثل الكورتيزولCortisol ، والإستروجينEstrogen ، والتستوستيرونTestosterone )، والأحماض الصفراوية (Bile acids)، وفيتامين د (Vitamin D). وتحتوي النباتات على ستيرولات أخرى، مثل الفيتوستيرولات (Phytosterols)[46].
- البرينولات (Prenols): مشتقة من وحدات آيزوبرين خماسية الكربون، وتشمل هذه الفئة الفيتامينات القابلة للذوبان في الدهون، مثل
فيتامين هـ، وفيتامين ك، وفيتامين أ، علاوة على
اليوبيكوينون (Ubiquinone، المشارك في سلسلة نقل الإلكترونات في الميتوكوندريا) والكاروتينات[47].
- الدهون السكّارية (Saccharolipids): ترتبط الأحماض الدهنية مباشرة بسلسلة سكرية، وهي نادرة نسبيًا في أنظمة الثدييات، ولكنها مكونات أساسية للغشاء الخارجي للبكتيريا سالبة الغرام {{البكتيريا سالبة الغرام: (Gram negative bacteria) فئة من البكتيريا ذات غلاف خلوي معقد، تتكون من طبقة رقيقة من الببتيدوغليكان وغشاء خارجي، ما يجعلها مقاومة لكثير من المضادات الحيوية. ولا تحتفظ بصبغة الكريستال البنفسجي المستخدمة في صبغة غرام.}}، مثل
ليبو بوليسكاريد (LPS) والدهن أ (Lipid A)[48].
-
متعددات الكيتيد (Polyketides): فئة واسعة ومتنوعة من المستقلَبات الثانوية التي تُصنّعها
البكتيريا والفطريات والنباتات والحيوانات، تشمل هذه الفئة كثيرًا من المركبات المهمة سريريًا، مثل
المضادات الحيوية (مثل الإريثروميسين والتتراسيكلين) ومضادات الفطريات[49].
[الشكل 4]
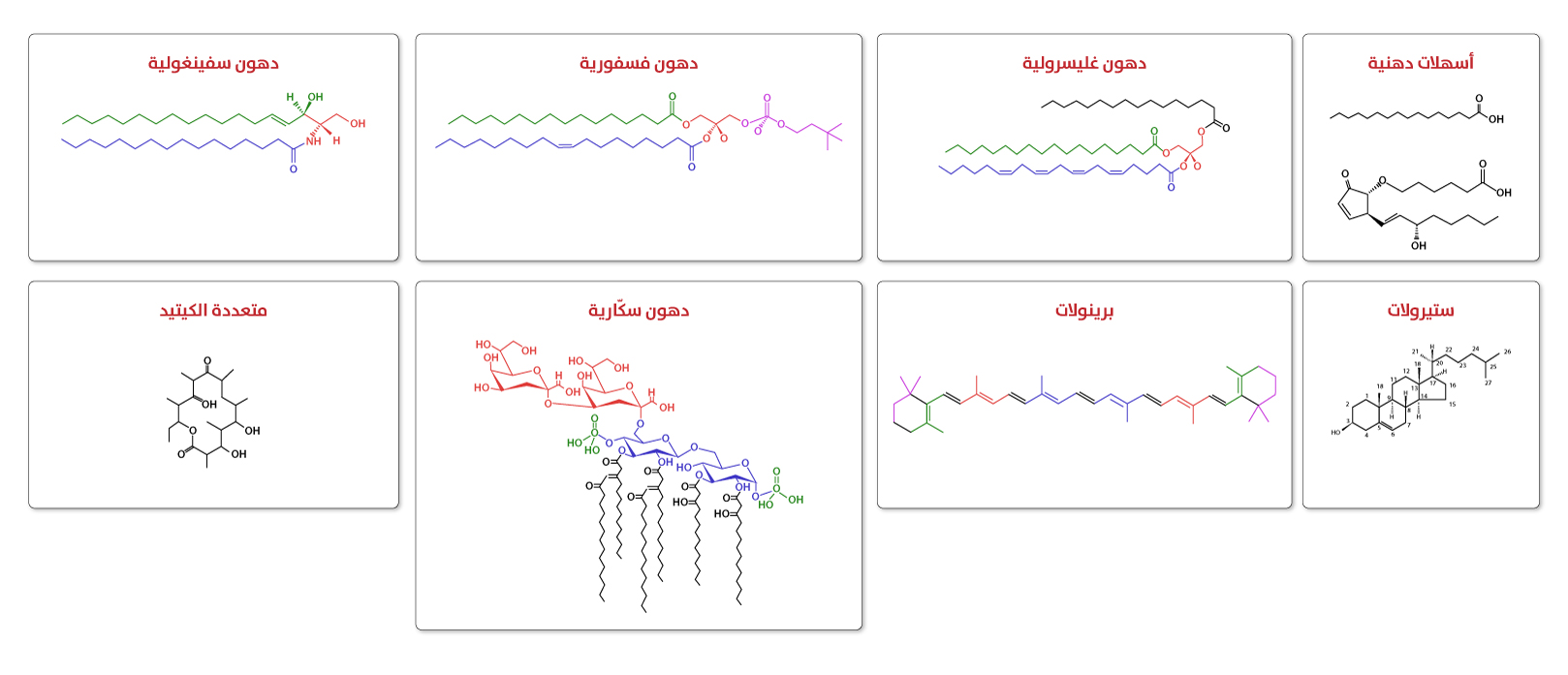 أمثلة على أشكال الدهون من المجموعات التصنيفية المختلفة
أمثلة على أشكال الدهون من المجموعات التصنيفية المختلفة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
وظائفها البيولوجية
كانت الدهون في السابق تعتبر دعامات هيكلية للخلايا تشكل الأغشية الخلوية ومن ثم حدودها فقط، إلا أن التقدم الكبير في علوم الدهون، كشف عن تنوع وظائفها بقدر تنوع بنيتها (الشكل 5)، ما يدعم استمرار الحياة المعقدة[50]. من وظائف الدهون الرئيسة ما يلي:
- تخزين الطاقة: تُعد الدهون الثلاثية أكثر أشكال تخزين الطاقة كفاءة في الجسم، إذ توفر نحو 9 كيلو كالوري من الطاقة لكل غرام، أي أكثر من ضعف تخزين الطاقة من الكربوهيدرات أو البروتينات (يوفر كلاهما نحو 4 كيلو كالوري/ غرام). تُخزن الدهون الثلاثية في الخلايا المتخصصة للأنسجة الدهنية من دون تخزين الماء معها، بسبب طبيعتها الكارهة للماء، ما يوفر احتياطيًا طويل الأمد من الوقود، خفيف الوزن وصغير الحجم، ومخزّن بطريقة متراصة. يستعمل هذا المخزون من الطاقة في أثناء الصيام أو التجويع، أو ممارسة التمارين الرياضية الشاقة لفترات طويلة[51].
- تكوين الأغشية: يُعد التجميع الذاتي التلقائي للدهون الفسفورية والسفينغولية والكوليسترول في طبقة دهنية ثنائية مزدوجة، المبدأ الأساسي لتكوين الأغشية البيولوجية جميعها، وتعمل هذه الطبقة الثنائية شبه النفاذة بوصفها حاجزًا يمنع مرور
الأيونات ومعظم
الجزيئات القطبية (ويسمح به انتقاءً)، ما يحافظ على التدرجات الكيميائية الأساسية، ويخلق حجيرات مميزة للتفاعلات الكيميائية الحيوية المتخصصة. إنه الأساس الهيكلي للغشاء البلازمي ولأغشية العضيات جميعها داخل الخلايا[52].
- الإشارات الخلوية: تؤدي الدهون أدوار ناقلات كيميائية أساسية في كثير من مسارات الإشارة داخل الخلايا، فالهرمونات الستيرويدية (المشتقة من الكوليسترول)، مثل البروجستيرون والكورتيزول والألدوستيرون والإستروجين والتستوستيرون، هي هرمونات صماء تنتقل عبر مجرى الدم، لتنظيم التعبير الجيني والأيض، والوظائف التناسلية في الخلايا المستهدفة البعيدة. أما الأيكوسانويدات (مثل البروستاغلاندينات واللوكوترينات)، فتعمل بوصفها إشارات قوية موضعية التأثير، تتوسط الاستجابات الموضعية، مثل الالتهابات والألم، وارتفاع درجة حرارة الجسم (الحمى)[53]. أما الدهون السفينغولية، ولا سيما السيراميد والسفينغوسين 1-فوسفات، فهي جزيئات إشارة مهمة تشارك في انقسام الخلايا ونموها، والشيخوخة الخلوية، وموت الخلايا المبرمج[54].
- العزل والحماية: يعمل النسيج الدهني تحت الجلد بوصفه عازلًا حراريًا، ما يساعد على الحفاظ على درجة حرارة الجسم. كذلك يوفر حماية ميكانيكية، ويخفف الصدمات، ويحمي الأعضاء الحيوية مثل الكلى والقلب من الصدمات الجسدية. توفر الأغلفة الشمعية على أوراق النباتات وريش الطيور حاجزًا مقاومًا للماء[55]، ويمثل النسيج الدهني البني (Brown adipose tissue) نوعًا من الدهون التي تحرق السعرات الحرارية لإنتاج الحرارة لتدفئة الجسم، وينشط بشكل رئيس عند التعرض للبرد، وقد كان يُعتقد سابقًا أنه موجود فقط لدى الرضع من
الثدييات، إلا أنه موجود أيضًا لدى البالغين، ولا سيما في منطقة الرقبة وأعلى الظهر، ويؤدي دورًا في تنظيم درجة حرارة الجسم وتحسين الصحة الأيضية. ويمكن أن يؤدي تنشيطه عند التعرض للبرد إلى زيادة استهلاك الطاقة، وله آثار إيجابية في مكافحة السمنة والأمراض المرتبطة بها[56].
- تسهيل الهضم: يتحول الكوليسترول في الكبد إلى أحماض صفراوية، تُخزن في المرارة وتُفرز في الأمعاء الدقيقة بعد وجبات غذائية غنية بالدهون، تسمح طبيعتها الكارهة للماء لها بالعمل بوصفها منظفات بيولوجية، إذ تُحوّل الدهون الغذائية إلى مُذيلات مختلطة. تزيد هذه العملية بشكل كبير من مساحة سطح الدهون، ما يُمكّنها من التحلل المائي بكفاءة بوساطة
إنزيمات هضمية مثل الليباز البنكرياسي (Pancreatic lipase)[57].
[الشكل 5]
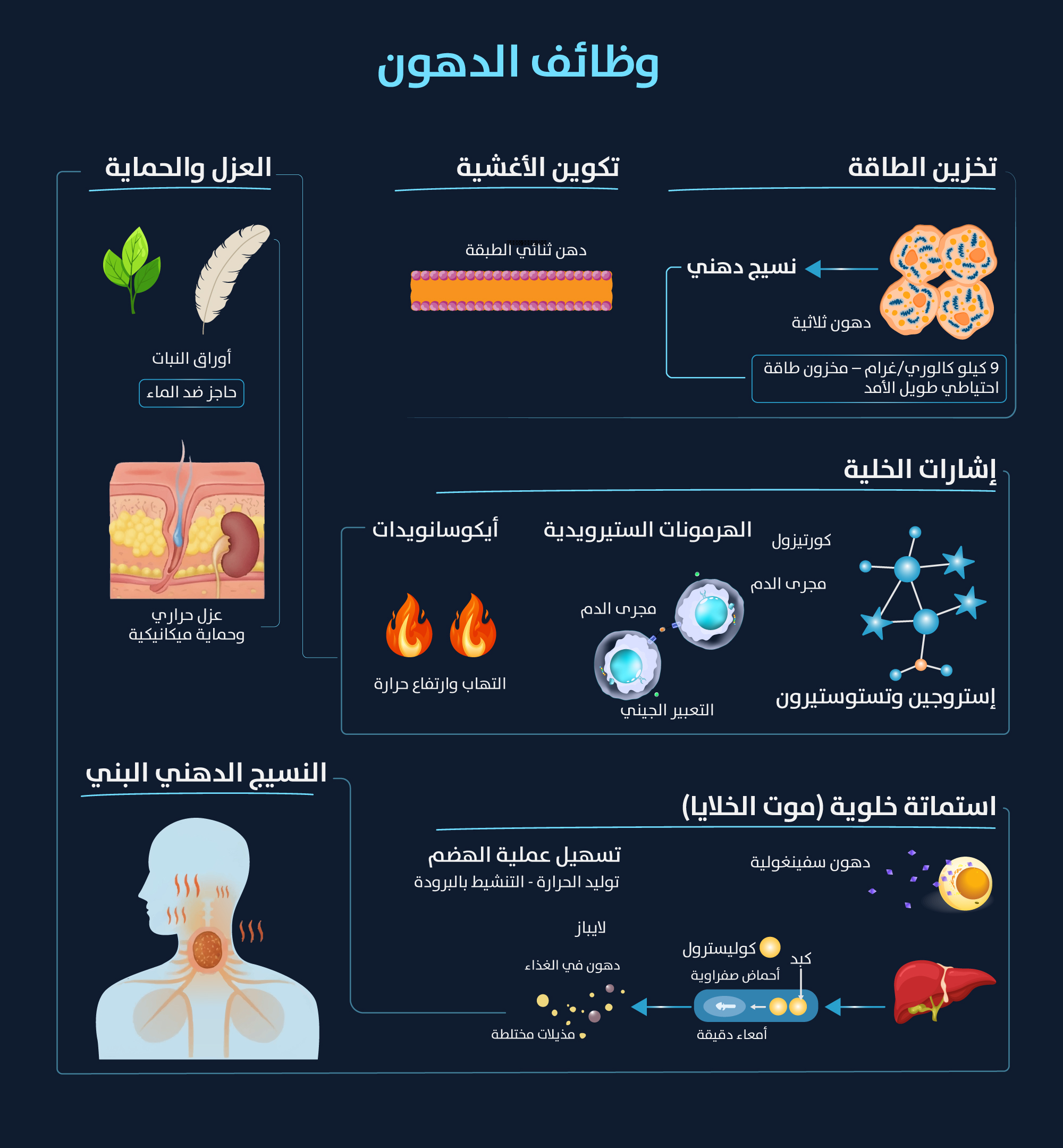 وظائف الدهون المختلفة
وظائف الدهون المختلفة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
أيض الدهون ونقلها
يشكل أيض (استقلاب) الدهون مجموعة معقدة ومنظمة للغاية من العمليات التي تشمل اصطناع الدهون (عمليات بنائية)، وتكسيرها (عمليات هدمية) ونقلها (الشكل 6). ونظرًا لأن الدهون كارهة للماء، تُنقل في مجرى الدم والسائل اللمفاوي معبأة في البروتينات الدهنية، وهي مجمعات من الدهون مع البروتينات. وتاليًا ملخص للعمليات الضرورية المتعلقة بالدهون في الجسم:
- تحلل الدهون (Lipolysis): هو المسار الهدمي الذي تحلل من خلاله الدهون الثلاثية المخزنة في الأنسجة الدهنية بوساطة إنزيمات الليباز، إلى أحماض دهنية حرة وغليسرول. تُطلق هذه المكونات في مجرى الدم، وتمتص الأنسجة الأحماض الدهنية التي تخضع لاحقًا لأكسدة بيتا (Beta oxidation) داخل
الميتوكوندريا لتوليد كميات كبيرة من أسيتيل مرافق الإنزيم أ (Acetyl CoA)، الذي يدخل بدوره في دورة حمض الستريك (حلقة كربس، Citric acid cycle)، لإنتاج الطاقة الحيوية على شكل أدينوسين ثلاثي الفوسفات (ATP)[58].
- تكوين الدهون (Lipogenesis): هي العملية البنائية لتكوين الأحماض الدهنية من الكربوهيدرات الغذائية الزائدة أو سلائف البروتين، ولا سيما في الكبد والأنسجة الدهنية. يحفز إنزيم سينثاز الأحماض الدهنية (Fatty acid synthase) عملية البناء التدريجي لحمض البالمتيك (Palmitic acid) من أسيتيل مرافق الإنزيم أ، وتُؤستر هذه الأحماض الدهنية بعد ذلك مع الغليسرول 3-فوسفات لتكوين ثلاثي أسيل غليسرول (دهون ثلاثية) للتخزين[59].
- نقل البروتينات الدهنية (Lipoprotein transport): نظرًا لعدم ذوبانها في الماء، يجب تجميع الدهون في بروتينات دهنية لنقلها في بلازما الدم، وهو وسط مائي. كان اكتشاف البروتينات الدهنية بحد ذاته نقطة تحول في علم الدهون، إذ وصفها الفرنسي ميشيل ماشيبوف (Michel Macheboeuf) لأول مرة عام 1929 بأنها مُركبات تتكون من الدهون والبروتينات[60]. تُعرف البروتينات الدهنية بأنها جسيمات كروية مُعقدة، ذات نواة كارهة للماء، من ثلاثي أسيل غليسرول وإسترات الكوليسترول (Cholesteryl esters)، محاطة بغلاف مُزدوج من الدهون الفسفورية والكوليسترول الحر، وبروتينات مُحددة تُسمى البروتينات الدهنية (Apolipoproteins). تختلف الفئات الرئيسة في الكثافة والحجم والتركيب، وهي:
أ. الكيلوميكرونات (Chylomicrons) التي تنقل الدهون الثلاثية الغذائية من الأمعاء إلى الأنسجة.
ب. البروتين الدهني منخفض الكثافة جدًا (VLDL)، الذي ينقل الدهون الثلاثية المُصنّعة حديثًا من الكبد إلى الأنسجة.
ج. البروتين الدهني منخفض الكثافة (LDL) الذي يتشكل من استقلاب البروتين الدهني منخفض الكثافة جدًا، وهو الناقل الرئيس للكوليسترول إلى الأنسجة الطرفية. ترتبط مستوياته المرتفعة في البلازما ارتباطًا وثيقًا بتصلب الشرايين، ما أكسبه الاسم الدارج "الكوليسترول السيء".
د. البروتين الدهني عالي الكثافة (HDL)، الذي يقوم بالنقل العكسي للكوليسترول، على النحو الذي يزيل الكوليسترول الزائد من الأنسجة الطرفية والشرايين، ويعيده إلى الكبد للتخلص منه، ويرتبط ارتفاع مستوياته إحصائيًا بانخفاض خطر الإصابة بأمراض القلب والأوعية الدموية، ما أكسبه اسم "الكوليسترول الجيد"، إلا أن الأبحاث الحديثة تُظهر أن العلاقة أكثر تعقيدًا، إذ إن النسبة بين البروتين الدهني منخفض الكثافة وعالي الكثافة هي ما تؤثر في خطر الإصابة بأمراض القلب[61].
- تكوين الكيتون (Ketogenesis): خلال فترات انخفاض مستوى الغلوكوز (مثل الصيام أو اتباع نظام غذائي منخفض الكربوهيدرات)، يُكثّف الكبد أكسدة بيتا للأحماض الدهنية، ويُحوّل الأسيتيل مرافق الإنزيم أ الناتج لإنتاج
أجسام كيتونية (Ketone bodies) (وهي أسيتو أسيتات Acetoacetate، بيتا هيدروكسي بيوتيرات يوتيراتNK \l "a"، وأسيتون Acetone). تُصدّر هذه الجزيئات القابلة للذوبان في الماء من الكبد، فتكون مصدرًا بديلًا لطاقة للدماغ والقلب والعضلات الهيكلية، ما يُحافظ على الغلوكوز، ويمنع التحلل المفرط لبروتينات
العضلات[62].
[الشكل 6]
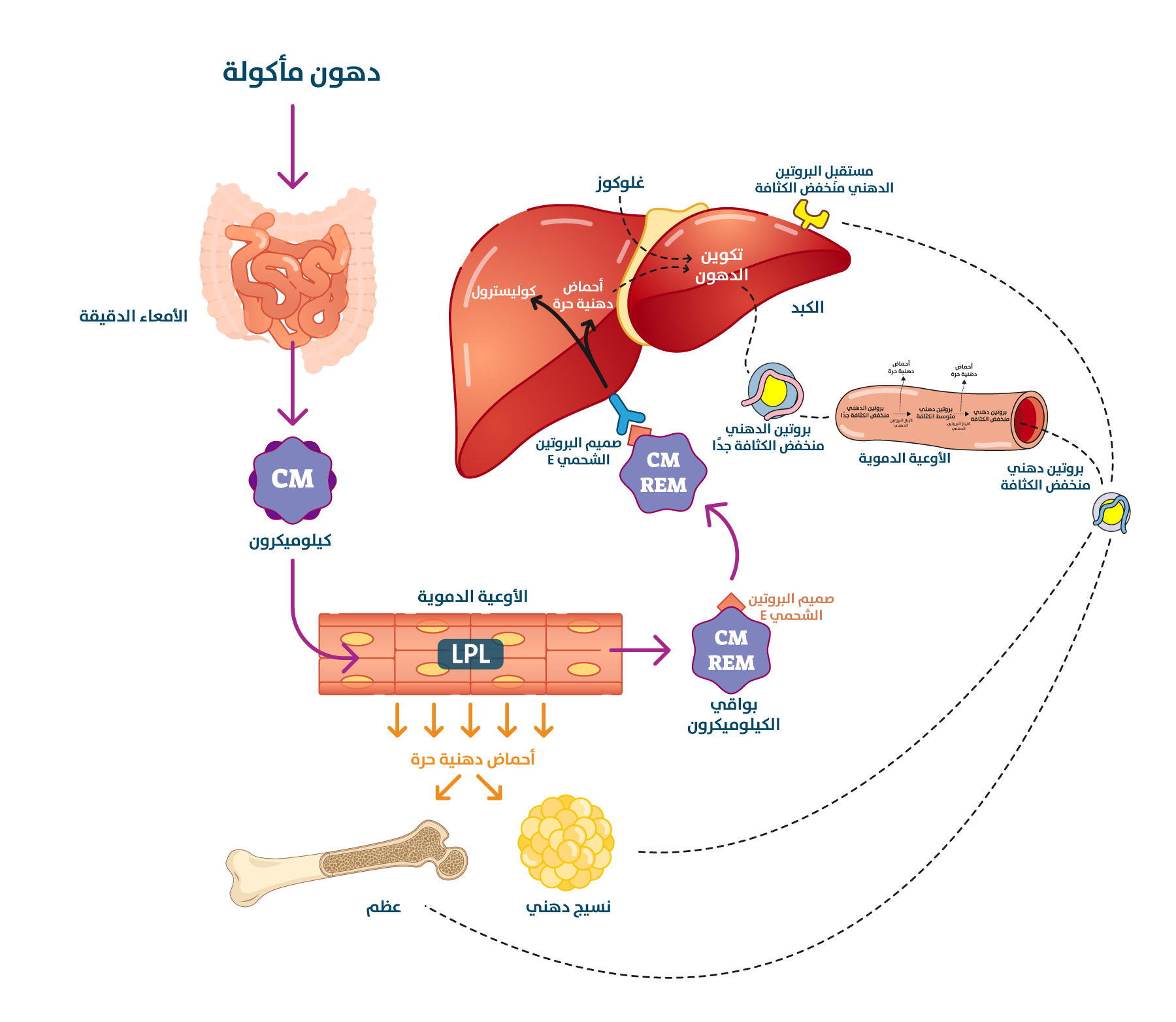 استقلاب الدهون
استقلاب الدهون
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
الدهون في الصحة والمرض
يُعد اختلال استقلاب الدهون عاملًا رئيسًا في كثير من الأمراض الخطرة، ما يجعل دراسة علوم الدهون والأبحاث فيها محورية لدعم صحة الإنسان. من الأمراض المرتبطة باستقلاب الدهون ما يلي:
- أمراض القلب والأوعية الدموية: يُعد تراكم كوليسترول من البروتين الدهني منخفض الكثافة داخل جدار الشرايين، حدثًا مُبكرًا حاسمًا في تطور مرض تصلب الشرايين، فبعد دخولها إلى جدار الشرايين، يمكن أن تتأكسد جزيئات البروتين الدهني منخفض الكثافة أو تُعدَّل بطريقة أخرى، ثم تلتقطها الخلايا البلعمية (Macrophages)، التي تُصبح مُمتلئة بالدهون، وتتحول إلى خلايا رغوية {{الخلايا الرغوية: (Foam cells) خلايا بلعمية محملة بالدهون، تتراكم على جدران الشرايين قبل تطور مرض تصلب الشرايين، وتتشكل بسبب زيادة البروتين الدهني منخفض الكثافة وتأكسده.}}[63]. تُشكل هذه الخلايا خطوطًا دهنية، ومع مرور الوقت، لويحات مُعقدة يمكن أن تُضيِّق الشرايين (مُسببة نقص التروية) أو تُمزِّقها، مُحفِّزةً خثرة (جلطة)، يُمكن أن تسبب احتشاء عضلة القلب (نوبة قلبية) أو
سكتة دماغية. يُعدُّ التحكم في مستويات البروتين الدهني منخفض الكثافة من خلال النظام الغذائي وممارسة الرياضة، وأدوية
الستاتينات، حجر الزاوية في طب القلب الوقائي.
-
السمنة المفرطة: تنشأ هذه الحالة نتيجة توازن طاقة إيجابي مُزمن، إذ يتجاوز مُتناوَل الطاقة مُستهلَك الطاقة باستمرار. تُخزَّن الطاقة الزائدة على شكل ثلاثي أسيل الغليسرول في الأنسجة الدهنية، ما يؤدي إلى تمددها. تُعدّ السمنة عامل خطر رئيسًا لمجموعة من الحالات الأخرى، بما في ذلك داء السكري من النوع الثاني، وأمراض القلب والأوعية الدموية، وبعض أنواع
السرطان.
- المتلازمة الاستقلابية (Metabolic syndrome): هي مجموعة من الاضطرابات (السمنة البطنية، وارتفاع سكر الدم، وارتفاع نسبة الدهون الثلاثية في الدم، وارتفاع ضغط الدم)، التي تزيد مجتمعةً خطر الإصابة بأمراض القلب وتصلب الشرايين، ومقاومة الإنسولين، ومرض السكري. ترتبط المتلازمة الاستقلابية بالدهون ارتباطًا وثيقًا، إذ يتميز كلٌّ منها بتركيبة دهون محددة، ويسهم اضطراب استقلاب الدهون في تطورها. تشمل الاضطرابات الدهنية الرئيسة في المتلازمة الاستقلابية ارتفاع الدهون الثلاثية في الدم (Hypertriglyceridemia)، وانخفاض البروتين الدهني عالي الكثافة، وارتفاع كل من البروتين الدهني منخفض الكثافة والكوليسترول الكلي في كثير من الأحيان، ما يزيد من خطر الإصابة بأمراض القلب والأوعية الدموية[64].
- أمراض تخزين الدهون: هي مجموعة من الاضطرابات الأيضية الوراثية النادرة، الناتجة من طفرات في الجينات التي تُشفِّر الإنزيمات اللازمة لتكسير دهون مُحددة، يؤدي هذا إلى تراكم سام للركائز غير المُستقلَبة داخل الليسوسومات، ما يؤدي إلى خلل في وظائف الخلايا وتلف الأعضاء. ومن الأمثلة على ذلك،
مرض تاي ساكس ومرض نيمان بيك، ومرض غوشيه[65].
- التغذية والدهون الغذائية: لطالما كان الفهم العلمي للآثار الصحية لمختلف الدهون الغذائية، مصدرًا للجدل التاريخي، وتوصي الإرشادات الحالية بالحد من تناول الدهون المشبعة (الموجودة في اللحوم الحمراء والزبدة ومنتجات الألبان كاملة الدسم)، وتجنب الدهون المتحولة الصناعية تمامًا (الموجودة في الزيوت المهدرجة جزئيًا)، لأنها ترفع مستويات الكوليسترول الضار، وقد كان للخلط التاريخي بين هذه الدهون المختلفة في رسائل الصحة العامة عواقب وخيمة[66]. ويرتبط استبدال الدهون المشبعة والمتحولة بالدهون غير المشبعة (غير المشبعة الأحادية وغير المشبعة المتعددة ولا سيما
الأوميغا 3، الموجودة في زيت الزيتون والمكسرات والأفوكادو والأسماك الدهنية)، بتحسين صحة القلب والأوعية الدموية وتقليل الالتهابات[67].
المراجع
Abed Rabbo, Muna et al. "Sphingolipid Lysosomal Storage Diseases: From Bench to Bedside."
Lipids in Health and Disease. vol. 20, no. 1 (2021). p. 44.
"About the FHS."
Framingham Heart Study. at:
https://acr.ps/1L9F2rg
Al-Awqati, Qais. "One Hundred Years of Membrane Permeability: Does Overton Still Rule?"
Nature Cell Biology. vol. 1, no. 8 (1999). pp. E201–E202.
Bazan, Nicolas G., David T. Stark & Nicos A. Petasis. "Lipid Mediators: Eicosanoids, Docosanoids and Platelet-Activating Factor." In: Brady, Scott T. et al. (ed.).
Basic Neurochemistry. 8th ed. London: Academic Press, 2012. pp. 62-643.
Becker, W. Mayne, Lewis J. Kleinsmith & Jeff Hardin.
The World of the Cell. 6th ed. San Francisco: Pearson/ Benjamin Cummings, 2006.
Bertrand, G. "Projet de reforme de la nomenclature de Chimie biologique."
Bulletin de la Société de Chimie Biologique. vol. 5 (1923).
Calder, P. C. "Functional Roles of Fatty Acids and Their Effects on Human Health."
Journal of Parenteral and Enteral Nutrition. vol. 39, no. 1 Suppl (2015). pp. 18S–32S.
Chevreul, Michel Eugène.
Recherches chimiques sur les corps gras d'origine animale. Paris: F. G. Levrault, 1823.
CrossFit. "Keys' Scientific Abandon." 31/12/2018. at:
https://acr.ps/1L9F2eM
Davson, Hugh, & James Frederic Danielli. "A Contribution to the Theory of Permeability of Thin Films."
Journal of Cellular and Comparative Physiology. vol. 5, no. 4 (1935). pp. 495–508.
Denisenko, Yulia K. et al. "Lipid-Induced Mechanisms of Metabolic Syndrome."
Journal of Obesity. vol. 2020 no. 1. (2020).
Endo, Akira. "A Historical Perspective on the Discovery of HMG-CoA Reductase Inhibitors."
Archives of Biochemistry and Biophysics. vol. 298, no. 2 (1992). pp. 350–52.
Endo, Akira, Masao Kuroda & Yoshio Tsujita. "ML-236A, ML-236B, and ML-236C, New Inhibitors of Cholesterogenesis Produced by Penicillium citrinium."
The Journal of Antibiotics. vol. 29, no. 12 (1976). pp. 1346–1348.
Fahy, Eoin et al. "Update of the LIPID MAPS Comprehensive Classification System for Lipids."
Journal of Lipid Research. vol. 50, no. Suppl (2009). pp. S9–S14.
"Fats, Oils and Heart Health."
Heart Foundation. at:
https://acr.ps/1L9F2XC
Goñi, Félix M. "Celebrating 100 Years of the Term 'Lipid'."
ASBMB Today. 3/10 2023. at:
https://acr.ps/1L9F2MP
Hannun, Yusuf A., & Lina M. Obeid. "The Ceramide-centric Universe of Lipid-mediated Cell Regulation: Stress Encounters of the Lipid Kind."
Journal of Biological Chemistry. vol. 277, no. 29 (2002). pp. 25847–25850.
Issleny, Batoul M. et al. "Sphingolipids: From Structural Components to Signaling Hubs."
The Enzymes. vol. 54 (2023). pp. 171–201.
Jayadev, Supriya et al. "Role for Ceramide in Cell Cycle Arrest."
Journal of Biological Chemistry. vol. 270, no. 5 (1995). pp. 2047–2052.
Keys, Ancel. "Atherosclerosis: A Problem in Newer Public Health."
Journal of the Mount Sinai Hospital, New York. vol. 20, no. 2 (1953). pp. 118–39.
________ . "Coronary Heart Disease in Seven Countries."
Circulation. vol. 41, no. 1 (1970). pp. 186–95.
Kresge, Nicole, Robert D. Simoni & Robert L. Hill. "The Biosynthetic Pathway for Cholesterol: Konrad Bloch."
Journal of Biological Chemistry. vol. 280, no. 10 (2005). pp. e7–e9.
Leray, Claude. "Contribution of Chevreul to Lipid Chemistry."
OCL. vol. 30 (2023). P 9.
"Lipid Classification System."
LIPID MAPS. at:
https://acr.ps/1L9F2Bj
Liu, Xiaomeng et al. "An Update on Brown Adipose Tissue and Obesity Intervention: Function, Regulation and Therapeutic Implications."
Frontiers in Endocrinology. vol. 13 (2023). p. 1065263.
Macheboeuf, Michel A. "Recherches sur les phosphoaminolipides et les sterides du serum et du plasma sanguins."
Bulletin de la Société de Chimie Biologique. vol. 11 (1929). pp. 268–93.
Nelson, David L. & Michael M. Cox.
Lehninger's Principles of Biochemistry. 8th ed. New York: W. H. Freeman, 2021.
Newport, Mary T. & Fabian M. Dayrit. "The Lipid–Heart Hypothesis and the Keys Equation Defined the Dietary Guidelines but Ignored the Impact of Trans-Fat and High Linoleic Acid Consumption."
Nutrients. vol. 16, no. 10 (2024).
Obeid, Lina M. et al. "Programmed Cell Death Induced by Ceramide."
Science. vol. 259, no. 5102 (1993). pp. 1769–71.
O'Donnell, Christopher J. & Roberto Elosua. "Cardiovascular Risk Factors: Insights From Framingham Heart Study."
Revista Española de Cardiología. vol. 61, no. 3 (2008). pp. 299–310.
"Press Release: The Nobel Prize in Physiology or Medicine 1982."
NobelPrize.org. at:
https://acr.ps/1L9F3d7
"Press Release: The Nobel Prize in Physiology or Medicine 1985."
NobelPrize.org. at:
https://acr.ps/1L9F3d7
Rieck, J. "Adolf Otto Reinhold Windaus."
European Heart Journal. vol. 40, no. 32 (2019). p. 2659.
Singer, S. J. & Garth L. Nicolson. "The Fluid Mosaic Model of the Structure of Cell Membranes."
Science. vol. 175, no. 4023 (1972). pp. 720–731.
Takagi, H., K. K. Matsuno, K. Umemoto, T. Hara, K. Saito, K. Shimada, Y. Saito, et al. "The Discovery of Statins." Journal of Atherosclerosis and Thrombosis, vol. 29, no. 1 (2022). pp. 1–16.
"The Nobel Prize in Chemistry 1927."
NobelPrize.org. at:
https://acr.ps/1L9F2h8
"The Nobel Prize in Chemistry 1928."
NobelPrize.org. at:
https://acr.ps/1L9F2yN
"The Nobel Prize in Physiology or Medicine 1964."
NobelPrize.org. at:
https://acr.ps/1L9F2py
Thudichum, J. L. W.
A Treatise on the Chemical Constitution of the Brain. London: Baillière, Tindall, and Cox, 1884.
Vance, Dennis E. & Jean E. Vance (ed.).
Biochemistry of Lipids, Lipoproteins and Membranes. 5th ed. New York: Elsevier Science, 2008.
- Euler, U. S. "Über die Spezifische Blutdrucksenkende Substanz des Menschlichen Prostata- und Samenblasensekretes."
Klinische Wochenschrift. vol. 14 (1935). pp. 1182–1183.
[1] Dennis E. Vance & Jean E. Vance )eds.(, Biochemistry of Lipids,
Lipoproteins and Membranes, 5th ed. (New York: Elsevier Science, 2008).
[2] E. Fahy et al., "Update of the LIPID MAPS Comprehensive Classification System for Lipids,"
Journal of Lipid Research, vol. 50, no. Suppl (2009), p. S10.
[3] Michel Eugène Chevreul,
Recherches chimiques sur les corps gras d'origine animale (Paris: F. G. Levrault, 1823).
[4] Ibid.
[5] Claude Leray, "Contribution of Chevreul to Lipid Chemistry,"
OCL, vol. 30 (2023), p. 9.
[6] J. L. W. Thudichum,
A Treatise on the Chemical Constitution of the Brain (London: Baillière, Tindall & Cox, 1884).
[7] G. Bertrand, "Projet de reforme de la nomenclature de Chimie biologique,"
Bulletin de la Société de Chimie Biologique, vol. 5 (1923).
[8] Félix M. Goñi, "Celebrating 100 Years of the Term 'Lipid',"
ASBMB Today, 3/10/ 2023, accessed on 20/1/2026, at:
https://acr.ps/1L9F2MP
[9] "The Nobel Prize in Chemistry 1927,"
NobelPrize.org, accessed on 20/1/2026, at:
https://acr.ps/1L9F2h8
[10] "The Nobel Prize in Chemistry 1928,"
NobelPrize.org, accessed on 20/1/2026, at:
https://acr.ps/1L9F2yN
[11] Mark Nicholls, "Adolf Otto Reinhold Windaus,"
European Heart Journal, vol. 40, no. 32 (2019), p. 2659.
[12] "The Nobel Prize in Physiology or Medicine 1964,"
NobelPrize.org, accessed on 20/1/2026, at:
https://acr.ps/1L9F2py
[13] Nicole Kresge, Robert D. Simoni & Robert L. Hill, "The Biosynthetic Pathway for Cholesterol: Konrad Bloch,"
Journal of Biological Chemistry, vol. 280, no. 10 (2005), p. e7.
[14] Qais Al-Awqati, "One Hundred Years of Membrane Permeability: Does Overton Still Rule?,"
Nature Cell Biology. vol. 1, no. 8 (1999), p. E201.
[15] W. Mayne Becker, Lewis. J. Kleinsmith & Jeff Hardin,
The World of the Cell, 6th ed. (San Francisco: Pearson/ Benjamin Cummings, 2006).
[16] Hugh Davson & James Frederic Danielli, "A Contribution to the Theory of Permeability of Thin Films,"
Journal of Cellular and Comparative Physiology, vol. 5, no. 4 (1935), p. 495.
[17] Becker, Kleinsmith & Hardin.
[18] S. J. Singer & Garth L. Nicolson, "The Fluid Mosaic Model of the Structure of Cell Membranes,"
Science, vol. 175, no. 4023 (1972), p. 720.
[19] "About the FHS,"
Framingham Heart Study, accessed on 20/1/2026, at:
https://acr.ps/1L9F2rg
[20] Christopher J. O'Donnell & Roberto Elosua, "Cardiovascular Risk Factors: Insights From Framingham Heart Study,"
Revista Española de Cardiología, vol. 61, no. 3 (2008), p. 299.
[21] Ancel Keys, "Coronary Heart Disease in Seven Countries,"
Circulation, vol. 41, no. 1 (1970), p. 186.
[22] Ancel Keys, "Atherosclerosis: A Problem in Newer Public Health,"
Journal of the Mount Sinai Hospital,
New York, vol. 20, no. 2 (1953), p. 118.
[23] CrossFit, "Keys' Scientific Abandon," 31/12/2018, accessed on 20/1/2026, at:
https://acr.ps/1L9F2eM
[24] Mary T. Newport & Fabian M. Dayrit, "The Lipid–Heart Hypothesis and the Keys Equation Defined the Dietary Guidelines but Ignored the Impact of Trans-Fat and High Linoleic Acid Consumption,"
Nutrients, vol. 16, no. 10 (2024), p. 1447.
[25] H. Takagi et al., "The Discovery of Statins,"
Journal of Atherosclerosis and Thrombosis, vol. 29, no. 1 (2022), p. 1.
[26] Akira Endo, Masao Kuroda & Yoshio Tsujita, "ML-236A, ML-236B, and ML-236C, New Inhibitors of Cholesterogenesis Produced by Penicillium citrinium,"
Journal of Antibiotics, vol. 29, no. 12 (1976), p. 1346.
[27] Akira Endo, "A Historical Perspective on the Discovery of HMG-CoA Reductase Inhibitors," Archives of Biochemistry and Biophysics, vol. 298, no. 2 (1992), p. 350.
[28] U. S. V. Euler, "Über die Spezifische Blutdrucksenkende Substanz des Menschlichen Prostata- und Samenblasensekretes,"
Klinische Wochenschrift, vol. 14 (1935), p. 1182.
[29] "Press Release: The Nobel Prize in Physiology or Medicine 1982,"
NobelPrize.org, accessed on 20/1/2026, at:
https://acr.ps/1L9F3d7
[30] "Press Release: The Nobel Prize in Physiology or Medicine 1985,"
NobelPrize.org, accessed on: 20/1/2026, at:
https://acr.ps/1L9F3d7
[31] Lina M. Obeid et al., "Programmed Cell Death Induced by Ceramide,"
Science, vol. 259, no. 5102 (1993), p. 1769.
[32] Supriya Jayadev et al., "Role for Ceramide in Cell Cycle Arrest,"
Journal of Biological Chemistry, vol. 270, no. 5 (1995), p. 2047.
[33] P. C. Calder, "Functional Roles of Fatty Acids and Their Effects on Human Health,"
Journal of Parenteral and Enteral Nutrition, vol. 39, no. 1 Suppl (2015), p. 18S.
[34] Fahy et al., p. S9.
[35] "Lipid Classification System,"
LIPID MAPS, accessed on 20/1/2026, at:
https://acr.ps/1L9F2Bj
[36] Daived L. Nelson & Michael M. Cox,
Lehninger's Principles of Biochemistry, 8th ed. (New York: W. H. Freeman, 2021)
[37] Ibid.
[38] Ibid.
[39] Ibid.
[40] Ibid.
[41] Fahy et al.
[42] Ibid.
[43] Ibid.
[44] Ibid.
[45] Ibid.
[46] Ibid.
[47] Ibid.
[48] Ibid.
[49] Ibid.
[50] Batoul M. Issleny et al. "Sphingolipids: From Structural Components to Signaling Hubs." The Enzymes, vol. 54 (2023), pp. 171–201.
[51] Nelson & Cox.
[52] Becker, Kleinsmith & Hardin.
[53] Nicolas G. Bazan, David T. Stark & Nicos A. Petasis, "Lipid Mediators: Eicosanoids, Docosanoids and Platelet-Activating Factor," in: Scott T. Brady et al. (ed.),
Basic Neurochemistry, 8th ed. (London: Academic Press, 2012), p. 643.
[54] Yusuf A. Hannun & Lina M. Obeid, "The Ceramide-centric Universe of Lipid-mediated Cell Regulation: Stress Encounters of the Lipid Kind,"
Journal of Biological Chemistry, vol. 277, no. 29 (2002), p. 25847.
[55] Nelson & Cox.
[56] Xiaomeng Liu et al., "An Update on Brown Adipose Tissue and Obesity Intervention: Function, Regulation and Therapeutic Implications,"
Frontiers in Endocrinology, vol. 13 ( 2023), p. 1065263.
[57] Nelson & Cox.
[58] Ibid.
[59] Ibid.
[60] Michel A. Macheboeuf, "Recherches sur les phosphoaminolipides et les sterides du serum et du plasma sanguins,"
Bulletin de la Société de Chimie Biologique, vol. 11 (1929), p. 268.
[61] Nelson & Cox.
[62] Ibid.
[63] Ibid.
[64] Yulia K. Denisenko et al., "Lipid-Induced Mechanisms of Metabolic Syndrome,"
Journal of Obesity, vol. 2020, vol. 1, no. 5762395 (2020).
[65] M. Abed Rabbo, Y. Khodour, L. S. Kaguni & J. Stiban, "Sphingolipid Lysosomal Storage Diseases: From Bench to Bedside,"
Lipids in Health and Disease, vol. 20, no. 1 (2021), p. 44.
[66] Newport, Mary T. & Fabian M. Dayrit. "The Lipid-Heart Hypothesis and the Keys Equation Defined the Dietary Guidelines but Ignored the Impact of Trans-Fat and High Linoleic Acid Consumption,"
Nutrients, vol. 16, no. 10 (2024), p. 1447.
[67] "Fats, Oils and Heart Health,"
Heart Foundation, accessed on 30/1/2026, at:
https://acr.ps/1L9F2XC