أدوية خفض الدهون هي علاجات تُستخدم لتقليل مستويات الدهون والبروتينات الدهنية في الدم، مما يسهم في تقليل خطر الإصابة بالأمراض القلبية الوعائية. تستهدف هذه الأدوية أنواعًا مختلفة من الدهون والبروتينات الدهنية، مثل البروتينات الدهنية منخفضة الكثافة، والدهون الثلاثية، والبروتينات الدهنية عالية الكثافة. ويُعدّ اضطراب الدهون في الدم عامل خطر رئيس لأمراض القلب التاجية، إذ يرتبط ارتفاع البروتين الدهني منخفض الكثافة بشكل مباشر بأمراض القلب والأوعية الدموية الناتجة عن تصلب الشرايين، وهي من الأسباب الرئيسة للوفيات عالميًّا. ومن الأمثلة على الأدوية التقليدية التي تخفض مستويات الكوليسترول المرتبط بالبروتينات الدهنية منخفضة الكثافة الستاتينات، والإيزيتيميب، ومُنحِّيات الأحماض الصفراوية. إضافة إلى أدوية حديثة مثل مثبطات أبولايبوبروتين سي 3، ومثبطات البروتينات المشابهة للأنجيوبويتين.
التعريف
أدوية خفض الدهون (Lipid-lowering agents)، والمعروفة أيضًا بالعوامل الخافضة لمستوى الدهون في الدم (Hypolipidemic agents)، أو أدوية خفض الكوليسترول (Cholesterol-lowering drugs)، أو الأدوية المضادة لفرط شحميات الدم (Antihyperlipidemic agents)، هي أدوية تُعطى لغاية خفض مستويات الدهون والبروتينات الدهنية (Lipoproteins) في الدم، ما يقلل من خطر الإصابة بالأمراض القلبية الوعائية الضارة. يُعتقد أن هذه الأدوية تعمل من خلال تقليل إنتاج البروتينات الدهنية وزيادة تحطيمها، إضافة إلى تحفيز الجسم على التخلص من
الكوليسترول (Cholesterol)[1].
الفسيولوجيا الحيوية للدهون
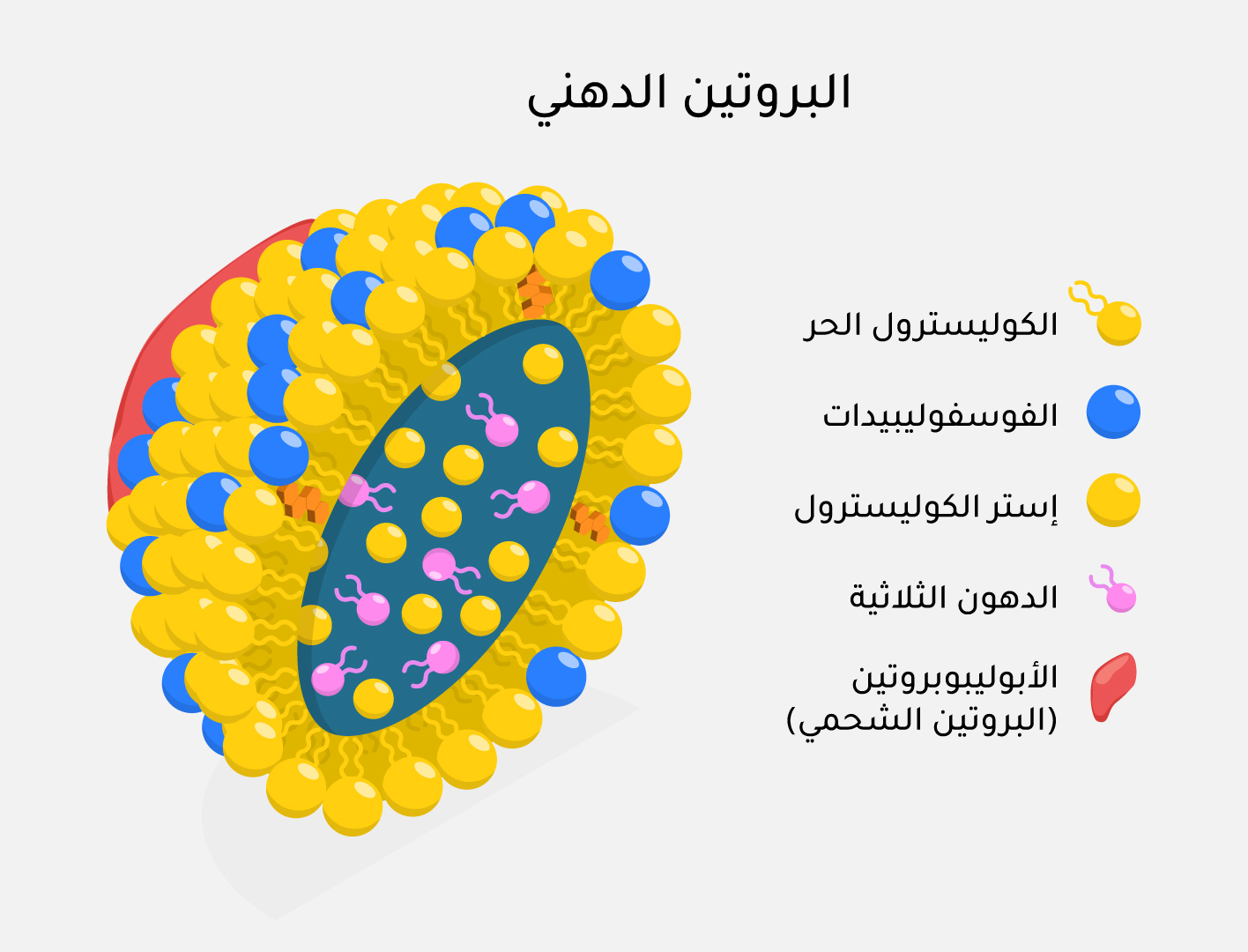 هيكل البروتين الدهني
هيكل البروتين الدهني
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يُعدّ
الكوليسترول والدهون الثلاثية (Triglycerides – TGs) والفوسفوليبيدات (Phospholipids) من الدهون الرئيسة في البلازما[2]. تعمل البروتينات الدهنية التي تتشكل في الكبد والأمعاء على ربط هذه الدهون ونقلها في الدم. تُعدّ هذه البروتينات جزيئات معقدة لاحتوائها على نواة من إسترات الكوليسترول والدهون الثلاثية إضافة إلى تغليفها بطبقة من الكوليسترول الحر، والفوسفوليبيدات، والأبوليبوبروتينات (Apolipoproteins).
في الأمعاء، تُعبأ الدهون الغذائية بالكيلومكرونات الغنية بالدهون الثلاثية، ثم تُطلق في الدورة الدموية عبر القناة الصدرية. بينما في مجرى الدم، تتحلل الكيلومكرونات بوساطة إنزيم
الليباز البروتيني الدهني (Lipoprotein lipase)، ما يساعد في إطلاق الدهون الثلاثية، وتنتج بقايا الكيلومكرونات التي تمتصها خلايا الكبد، وهذه العملية تسهم في تكوين البروتينات الدهنية عالية الكثافة[3]. يُعدّ الكوليسترول ضروريًّا لوظيفة غشاء الخلية وإنتاج أغلفة الميالين (Myelin sheaths) والهرمونات الستيرويدية. ويعمل
إنزيم 3-هيدروكسي 3-ميثيل جلوتاريل كو إنزيم أ ريديكتاز (3-hydroxy-3-methylglutaryl coenzyme A – HMG-CoA Reductase) على تنظيم معدل إنتاج الكوليسترول في الكبد. يمكن تنظيم نقل الكوليسترول من مجرى الدم إلى الخلايا المشبعة بالكوليسترول عن طريق تعديل عدد مواقع الامتصاص مستقبلات البروتين الدهني منخفض الكثافة (Low-density lipoprotein – LDL) على أغشية خلايا الكبد[4].
الأنواع المختلفة للبروتينات الدهنية وقيمها
الوحدة |
الطبيعي |
غير الطبيعي |
المرتفع |
الكوليسترول الكلي (Total cholesterol) | ملّغرام/ ديسيلتر
(mg/dL) | أقل من 200 | 200-239 | أكثر من 239 |
البروتينات الدهنية منخفضة الكثافة (Low-density lipoprotein – LDL) | أقل من 130 | 130-159 | أكثر من 159 |
البروتينات الدهنية عالية الكثافة (High-density lipoprotein – HDL) | أكثر من 60 | 60-40 | أقل من 40 |
الدهون الثلاثية (TGs) | أقل من 150 | 150-199 | أكثر من 199 |
البروتينات الدهنية منخفضة الكثافة جدًا (Very-low-density lipoprotein – VLDL) | من 2 إلى 30 | | أكثر من 30 |
مضاعفات فرط الدهون
تُعدّ أمراض القلب والأوعية الدموية الناتجة عن
تصلب الشرايين (Atherosclerotic cardiovascular disease – ASCVD) من الأسباب الرئيسة للوفيات عالميًّا. يحدث
تصلب الشرايين بسبب تراكم الترسبات في جدران الشرايين، ما يؤدي إلى أمراض القلب التاجية (Coronary heart disease – CHD). وثمة عدة عوامل تسهم في حدوث هذه الأمراض وتطورها، مثل السلوكيات الأيضية، والعوامل البيئية، وأنماط الحياة غير الصحية. يُعدّ ارتفاع ضغط الدم الانقباضي، والمخاطر الغذائية، وارتفاع مستويات
الكوليسترول الضار (LDL-C) من بين أهم ثلاثة عوامل تشكل خطرًا على القلب[5].
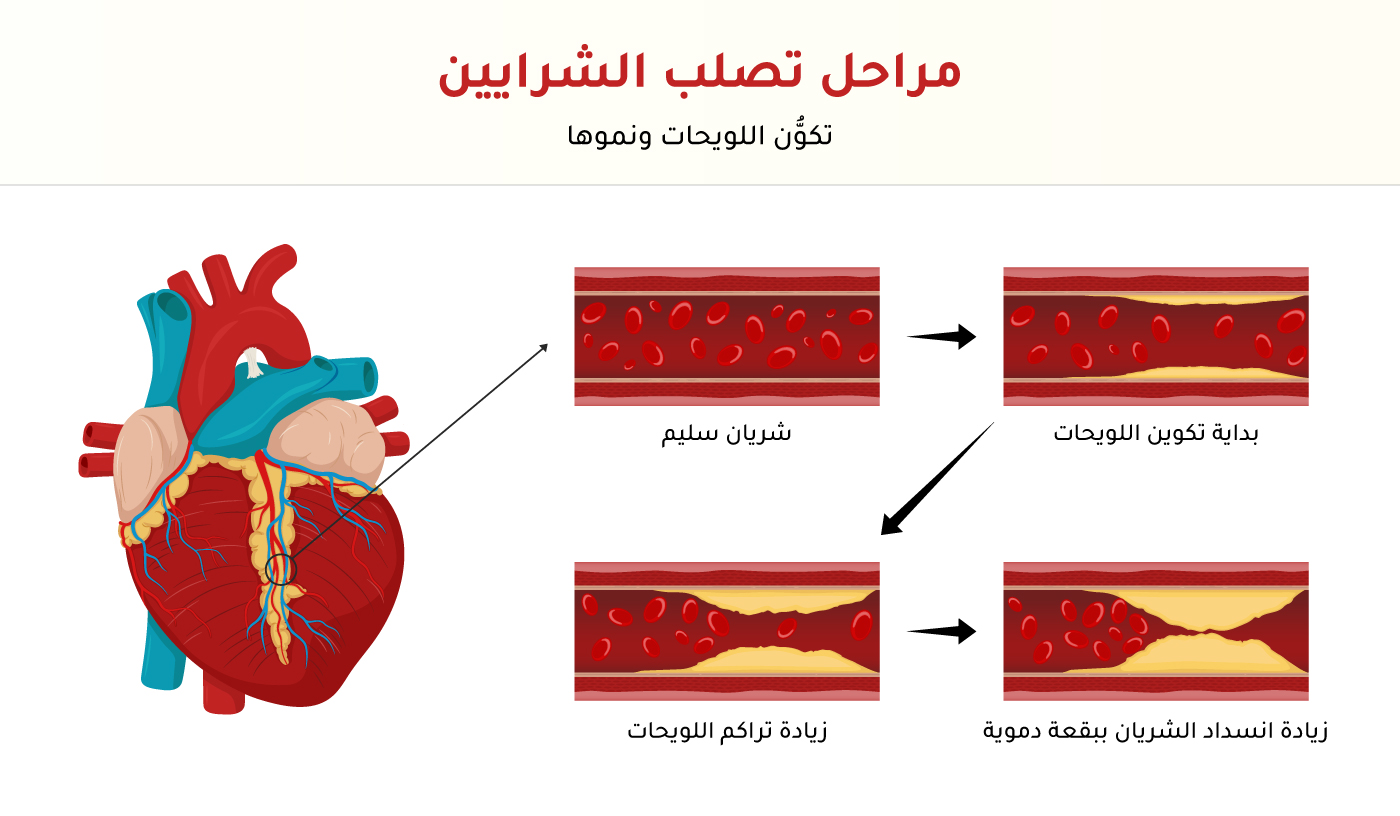 تصلب الأوعية الدموية والشرايين
تصلب الأوعية الدموية والشرايين
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
كما يعتبر
ارتفاع الكوليسترول في الدم (Hypercholesterolemia) (أعلى من 239 ملّغرام/ ديسيلتر) عامل خطر رئيس لتطور أمراض القلب التاجية. وقد أظهرت الأبحاث وجود علاقة مباشرة بين ارتفاع تركيز الكوليسترول الكلي في الدم وزيادة مستويات البروتينات الدهنية، خاصة البروتينات الدهنية منخفضة الكثافة وتصلب الشرايين (Atherosclerosis). لذا، فمن الضروري خفض مستويات الكوليسترول من خلال اتباع نظام غذائي صحي واستخدام الأدوية المناسبة، والحفاظ على مستوى الكوليسترول في الدم ضمن التركيز المثالي (أقل من 200 ملّغرام/ ديسيلتر)[6]. على النقيض من ذلك، تبين أن المستويات المرتفعة من الكوليسترول المرتبط بالبروتينات الدهنية عالية الكثافة ترتبط بانخفاض خطر الإصابة بأمراض القلب التاجية. أما
الدهون الثلاثية (TGs) فترتبط بعلاقة ضعيفة مع تصلب الشرايين. ومع ذلك، يُعدّ التهاب البنكرياس الحاد المتكرر (Recurrent acute pancreatitis) من المضاعفات المرتبطة بفرط الدهون الثلاثية (Hypertriglyceridemia) (أعلى من 150 ملّغرام/ ديسيلتر) والمرتبطة بالشحميات الكيلوسية الدقيقة (Chylomicronemia). لذا، فمن الضروري الحفاظ على مستوى الدهون الثلاثية ضمن التركيز المثالي (أقل من 150 ملّغرام/ ديسيلتر)[7]. وتُعدّ الإصابة بمرض السكري، وقصور الغدة الدرقية، وأمراض الكلى من الحالات الشائعة التي تسبب فرط الدهون في الدم. إضافة إلى ذلك، ثمة بعض أنواع العلاجات والمواد التي تعمل على زيادة الدهون في الدم مثل الثيازيدات (Thiazides)، ومثبطات البيتا (β-blockers)، والإستروجينات (Estrogens)، والرتينويدات (Retinoids)، وتناول الكحول بكميات كبيرة.
العلاجات الدوائية التقليدية
يهدف العلاج بأدوية خفض الدهون إلى تقليل خطر الإصابة بأمراض القلب والأوعية الدموية الناتجة عن تصلب الشرايين، وخاصة أمراض القلب التاجية. تم تصنيف أدوية خفض الدهون بناءً على آلية عملها الدوائية وتأثيرها على أنواع مختلفة من الدهون في الدم إلى الآتي:
الستاتينات
تعمل الستاتينات (Statins) على تقليل مستوى الكوليسترول عن طريق تثبيط إنزيم 3-هيدروكسي 3-ميثيل جلوتاريل كو إنزيم أ ريديكتاز reductase) HMG-CoA)، وهو إنزيم رئيس لتصنيع الكوليسترول، ويؤدي هذا التثبيط إلى زيادة تواجد مستقبلات الكوليسترول المرتبطة بالبروتينات الدهنية منخفضة الكثافة (LDL-Cholesterol – LDL-C) على سطح الخلايا، ما يؤدي إلى انخفاض مستويات البروتين الدهني منخفض الكثافة، والبروتينات الدهنية (Apolipoprotein B-100 – ApoB 100)، والدهون الثلاثية في الدم[8]، تساهم أيضًا هذه الفئة في تقليل الدهون الثلاثية بشكل معتدل.
تعتمد فعالية الستاتينات على الجرعة؛ إذ يمكن للستاتينات ذات الشدة المنخفضة إلى المتوسطة تقليل البروتين منخفض الكثافة بنسبة تتراوح بين 30 في المئة إلى 50 في المئة، والدهون الثلاثية بنسبة 20 في المئة، في حين تقلل الستاتينات عالية الشدة البروتين نفسه بأكثر من 50 في المئة، والدهون الثلاثية بنسبة تصل إلى 40 في المئة. إضافة إلى أن الستاتينات تعزز
مستويات الكوليسترول الجيد (HDL-C) بنسبة تصل إلى 10 في المئة[9].
تبين أن للستاتينات عدة فوائد إضافية إلى جانب تخفيض الكوليسترول، مثل حماية القلب من خلال تحسين وظائف بطانة عضلة القلب، وزيادة أكسيد النيتريك، وتقليل الاستجابة للالتهابات، والعمل على استقرار اللويحات التصلبية (Plaque stabilization)، وبعض الصفات المضادة للأكسدة. ومع ذلك، قد تتسبب الستاتينات في بعض الآثار الجانبية مثل آلام العضلات، وارتفاع إنزيمات الكبد، وارتفاع مستوى السكر في الدم، وظهور النوع الثاني من مرض السكري، ووجود البروتينات في البول[10].
الإيزيتيميب
الإيزيتيميب (Ezetimibe) هو دواء يهدف إلى خفض الكوليسترول عن طريق تثبيط امتصاصه بشكل انتقائي في الأمعاء الدقيقة، دون التأثير في امتصاص العناصر الغذائية والفيتامينات الأخرى. يعمل الإيزيتيميب على خفض الكوليسترول المرتبط بالبروتينات الدهنية منخفضة الكثافة بنسبة 24 في المئة، وتقليل أبوليبوبروتين ب-100 (ApoB-100) بنسبة 14 في المئة، وتراجع الدهون الثلاثية بنسبة 12 في المئة، وتقليص مستوى البروتين سي التفاعلي عالي الحساسية (High-sensitivity C-reactive protein – HsCRP) إلى 13 في المئة، مع الحفاظ على مستويات الكوليسترول المرتبط بالبروتينات الدهنية منخفضة الكثافة ثابتة. وبالمقارنة مع العلاج الأحادي بالستاتين، فإن استخدام الإيزيتيميب المساعد لا يؤدي إلى زيادة الآثار الجانبية أو التسبب في وقف العلاج. ومن أبرز الآثار الجانبية للإيزيتيميب آلام البطن، والإسهال، وآلام المفاصل، والتهابات الجهاز التنفسي العلوي[11].
مُنحيات الأحماض الصفراوية
تعمل مُنحيات الأحماض الصفراوية (Bile acid binding resins)، مثل كوليستيرامين (Cholestyramine)، وكوليسيفيلام (Colesevelam)، وكوليستيبول (Colestipol)، على الارتباط بالأحماض الصفراوية في تجويف الأمعاء، ما يعطل دورانها المعوي الكبدي ويقلل مخزون
الأحماض الصفراوية. نتيجة لذلك، يحفز الكبد على استخدام الكوليسترول لتصنيع المزيد من الأحماض الصفراوية، ما يزيد من امتصاص الكوليسترول الضار (LDL-C) ويخفض مستواه في الدم بشكل كبير، ما يعني التقليل من معدل الإصابة بأمراض القلب التاجية[12].
تُعدّ مُنحيات الأحماض الصفراوية مناسبة للأطفال الذين لديهم
فرط كوليسترول الدم العائلي متغاير الجينات (Heterozygous familial hypercholesterolemia) أو للنساء في مرحلة الإنجاب، لكن لا يُفضل استخدامها في أثناء الحمل.
قد تحفز هذه العوامل أيضًا إنتاج
البروتينات الدهنية ذات الكثافة المنخفضة جدًا (VLDL) في الكبد، وقد يزيد ذلك من تركيز الدهون الثلاثية. لذلك، يُفضل أن يستخدم المرضى الذين لديهم فرط في الكوليسترول مصحوبًا بزيادة ملحوظة في مستوى البروتينات الدهنية ذات الكثافة المنخفضة جدًا (VLDL) دواءً آخر، مثل حمض النيكوتينيك (Nicotinic acid) أو الفايبرات مع مُنحيات الأحماض الصفراوية.
من أبرز الآثار الجانبية لمُنحيات الأحماض الصفراوية الانتفاخ البطني، والتجشؤ، والغازات، والإمساك، إضافة إلى أنه يمكن أن تتداخل مُنحيات الأحماض الصفراوية مع امتصاص الأدوية الأنيونية (Anionic drugs) مثل الديجوكسين (Digoxin)، والوارفارين (Warfarin)، والثيروكسين (Thyroxine)، ومدرات البول الثيازيدية (Thiazide diuretics)، ولذلك يُفضّل تناول الأدوية الأنيونية قبل مُنحيات الأحماض الصفراوية أو بعدها بفترات زمنية محددة لضمان الامتصاص الفعّال.
حمض النيكوتينيك
حمض النيكوتينيك (Nicotinic acid) والمعروف أيضًا باسم النياسين (Niacin)، وهو فيتامين ب 3(Vitamin B3) يعمل على تقليل مستويات البروتينات الدهنية ذات الكثافة المنخفضة جدًا (VLDL)، والبروتينات الدهنية منخفضة الكثافة (LDL) عند استخدامه بجرعات دوائية. يُخفض حمض النيكوتينيك إنتاج الدهون الثلاثية من خلال تقليل
الأحماض الدهنية الحرة (Free Fatty acids) اللازمة لتكوين
البروتينات الدهنية ذات الكثافة المنخفضة جدًا في الكبد. ومن الجدير بالذكر أن الانخفاض في إنتاج البروتينات الدهنية ذات الكثافة المنخفضة جدًا (VLDL) يؤدي إلى تقليل مستويات
البروتينات الدهنية منخفضة الكثافة (LDL).
يُستخدم حمض النيكوتينيك كخيار علاجي لفرط كوليسترول الدم (Hypercholesterolemia) وفرط دهون الدم المختلط (Combined hyperlipidemia). ومع ذلك، يقل استخدامه حاليًا بسبب الآثار الجانبية المحتملة، وتشمل زيادة نشاط إنزيمات الكبد، وفرط حمض يوريك الدم، وضعف تحمل الجلوكوز (Impaired glucose tolerance) عند استخدامه بجرعات عالية، وقد يُسبب أيضًا تنشيط القرحة المعوية، وفرط تصبغ الجلد، وعدم وضوح الرؤية.
على الرغم من أن مركب نيكوفورانوز (Nicofuranose) وعقار أسيبيموكس (Acipimox) مشتقان من حمض النيكوتينيك، فهما يعملان عن طريق منع تحلل الدهون في الأنسجة الدهنية، ما يخفض مستويات الدهون والبروتينات الدهنية في البلازما ويزيد من مستويات
البروتينات الدهنية عالية الكثافة (HDL).
من الجدير بالذكر أن النيكوتيناميد (Nicotinamide) أو نياسيناميد (Niacinamide) أو أميد حمض النيكوتينيك (Nicotinamide acid amide) غير فعّال في خفض مستويات الدهون[13].
الفايبرات
تنشط الفايبرات (Fibrates) مثل الفينوفيبرات (Fenofibrate)، والبيزافيبريت (Bezafibrate)، والجيمفبروزيل (Gemfibrozil) مستقبلات البيروكسيسوم ألفا (Peroxisome proliferator Activated receptor alpha PPAR-α)، ما يسهم في تقليل مستويات الدهون الثلاثية في الدم وتقليل خطر الإصابة بأمراض القلب والأوعية الدموية التصلبية (ASCVD). بناءً على نوع الفايبرات المستخدم، يمكن أن تُخفض هذه الأدوية مستويات الدهون الثلاثية بنسبة تصل إلى 50 في المئة والكوليسترول الضار بنسبة تصل إلى 20 في المئة، بينما تزيد من الكوليسترول الضار بنسبة تصل إلى 20 في المئة. يرتبط استخدام الفايبرات بزيادة حدوث الأعراض المعوية، والطفح الجلدي، واعتلال العضلات، وارتفاع إنزيمات الكبد. أما البيمافيبرات (Pemafibrate)، وهو أول مُعدِّل انتقائي لمستقبلات بيروكسيسوم المنشأ ألفا (PPAR-α)، فيتميز بقدرة تفعيل تزيد بأكثر من 2500 مرة مقارنةً بحمض الفينوفبريك (Fenofibric acid)، وهو الشكل النشط من الفينوفيبرات. يُخفض البيمافيبرات مستويات الدهون الثلاثية في البلازما بشكل أكثر فعالية من الفينوفيبرات، مع آثار جانبية أقل مقارنةً بمجموعة الفينوفيبرات
[14].
الأحماض الدهنية أوميغا-3
ترتبط المستويات المرتفعة من
الأحماض الدهنية أوميغا-3 (Omega-3 fatty acids) بانخفاض كبير في خطر الإصابة بالأمراض القلبية الوعائية والوفاة. يُنصح المرضى الذين يعانون من فرط الدهون الثلاثية في الدم بتناول أحماض أوميغا-3 الدهنية الموجودة في زيت السمك مثل
حمض الدوكوساهيكسانويك (Docosahexaenoic acid – DHA)، وحمض الإيكوسابنتانويك (Eicosapentaenoic acid – EPA)، وحمض الدوكوسابنتانويك (Docosapentaenoic acid – DPA)، نظرًا إلى تأثيرها الملحوظ في تقليل الأمراض القلبية الوعائية التصلبية[15].
تعمل الأحماض الدهنية أوميغا-3 على تقليل مستويات الدهون الثلاثية في البلازما من خلال منع تصنيع البروتينات الدهنية منخفضة الكثافة جدًا وإفرازها، وزيادة إزالة الدهون الثلاثية من جزيئات البروتينات الدهنية منخفضة الكثافة جدًا والكيلومكرونات عبر زيادة نشاط إنزيم الليبيز البروتيني الدهني (Lipoprotein lipase – LPL). تشمل آلية عملها أيضًا تثبيط
إنزيم داي أسيل جليسيرول أسيل ترانسفيراز (Diacylglycerol acyltransferase) و/أو
إنزيم الفوسفاتيتيك أسيد فوسفوهيدراز (Phosphatidic acid phosphohydrolase)، وتنشيط مستقبلات بيروكسيسوم المنشأ ألفا (PPARα)، وتقليل توفر الأحماض الدهنية لتصنيع الدهون الثلاثية، وزيادة نشاط تحلل الدهون في البلازما.
تُظهر الأبحاث أن
أحماض الإيكوسابنتانويك (EPA) لها تأثيرات مفيدة في صحة القلب والأوعية الدموية تتجاوز مجرد خفض الدهون الثلاثية. فهي تمتلك خصائص مضادة للالتهاب، ومضادة للتخثر، وتساعد في استقرار الأغشية واللويحات (Plaque stabilizing)، وتسهم في مكافحة عدم انتظام ضربات القلب وارتفاع ضغط الدم.
على الرغم من ذلك، ارتبط استخدام الإيكوسابنتانويك بزيادة نسبة الاصابة بالرجفان الأذيني (Atrial fibrillation)، وحدوث النزيف الخطر، والوذمة الطرفية (Peripheral edema)، ولكن مع انخفاض معدل الإصابة بالإسهال وآلام الجهاز الهضمي، وفقر الدم مقارنة بالعلاج الأحادي بالستاتينات.
يُعدّ
الإيكوسابنت إيثيل، وهو شكل من أشكال حمض الإيكوسابنتانويك، علاجًا فعالًا للوقاية من أمراض القلب والأوعية الدموية لدى المرضى الذين يعانون من اضطرابات الدهون في الدم (Dyslipidemia)[16].
إن التوصيات الأميركية والأوروبية تحث على استخدام الفايبرات (Fibrates) أو أحماض أوميغا-3 الدهنية (Omega-3 fatty acids) للمرضى الذين يعانون من ارتفاع مستمر في مستويات الدهون الثلاثية (أكثر أو يساوي 500 ملّغرام/ ديسيلتر) وسيلةً للوقاية من التهاب البنكرياس (Pancreatitis). إضافة إلى ذلك، تنصح التوصيات الأوروبية باستخدام الأحماض الدهنية المتعددة غير المشبعة مثل
إيكوسابنت إيثيل (Icosapent ethyl) مع الستاتين للمرضى المعرضين لخطر مرتفع، أي الذين تتراوح مستويات الدهون الثلاثية لديهم بين 135 و499 ملّغرام/ ديسيلتر[17].
كما يُوصى بعلاج
فرط كوليسترول الدم (Hypercholesterinemia) باستخدام الستاتينات (Statins)، وإيزيتيميب (Ezetimibe)، ومثبطات بروتين المحول سبتيليسين-كيكسين من النوع 9 PCSK9)). وفي حالة فرط الدهون الثلاثية بالدم (Hypertriglyceridemia)، تُعدّ الستاتينات العلاج الأولي، مع إضافة إيكوسابينت إيثيل (Icosapent ethyl) و/أو الفايبرات (Fibrates) بوصفها علاجات في الخط الثاني.
العلاجات الدوائية الحديثة
الأجسام المضادة وحيدة النسيلة
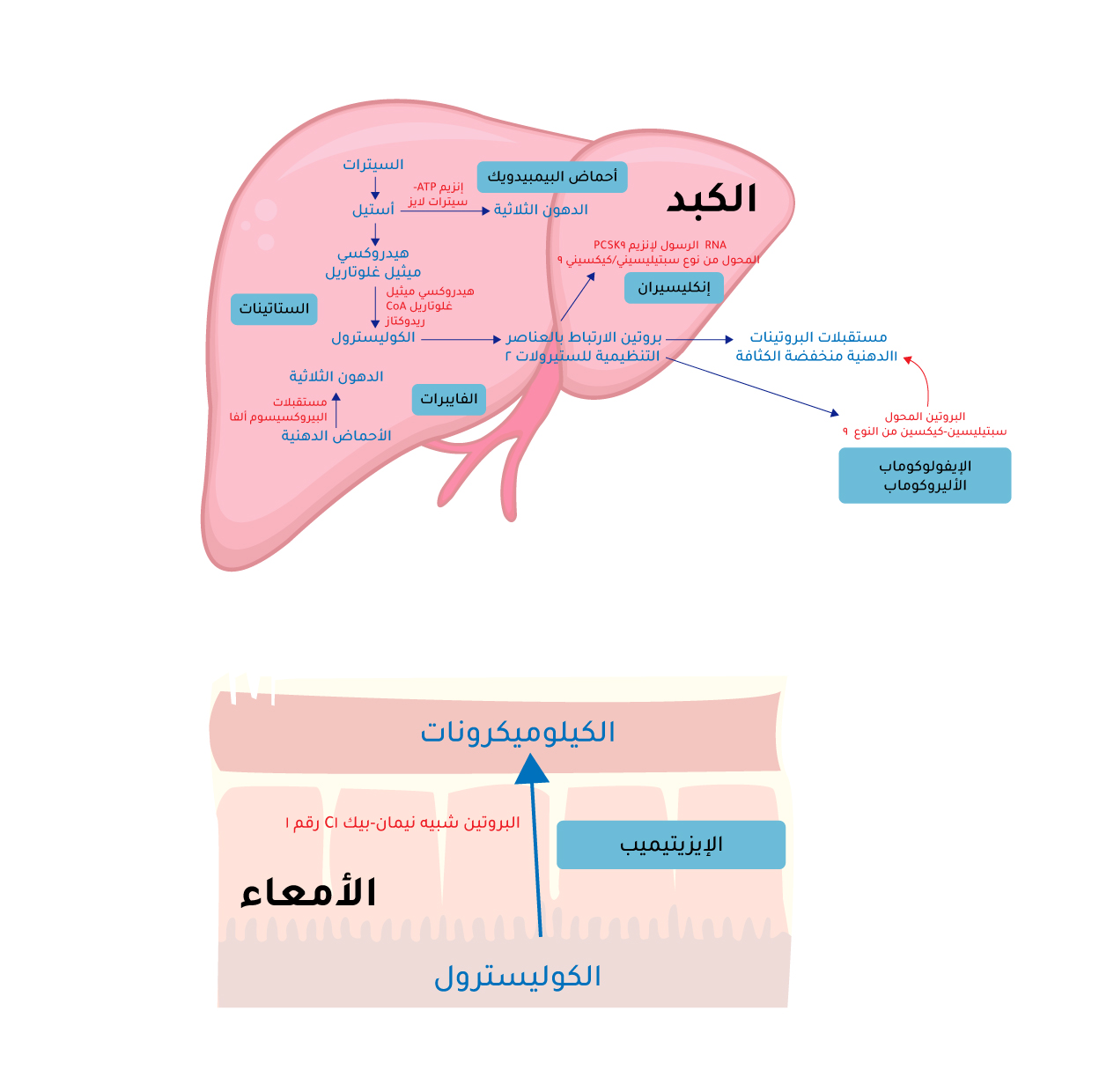 الأدوية الخافضة للدهون وآلية عملها
الأدوية الخافضة للدهون وآلية عملها
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تُعدّ الإيفولوكوماب (Evolocumab) والأليروكوماب (Alirocumab) أجسامًا مضادة وحيدة النسيلة (Monoclonal antibodies) تعمل على تثبيط
إنزيم البروتين المحول سبتيلسين-كيكسين من النوع 9 (PCSK9) الذي يُنتج في الكبد، ويرتبط بمستقبلات الكوليسترول الضار (LDL Receptors – LDLR) على سطح خلايا الكبد. تقلل هذه الأجسام المضادة من مستويات بروتين المحول سبتيلسين-كيكسين من النوع 9 في البلازما، ما يؤدي إلى زيادة التعبير عن مستقبلات الكوليسترول الضار. إن العلاج بهذه المثبطات قد يخفض الكوليسترول الضار بنسبة تقارب 60 في المئة. إضافة إلى أن هذه المثبطات تخفض من مستويات الدهون الثلاثية والبروتينات الدهنية أ (Lipoprotein a – Lp [a])، في حين تزيد من البروتينات الدهنية من النوع أبوليبوبروتين A1 (Apolipoprotein A1 – ApoA1). لذلك يوصى باستخدام هذه المثبطات للمرضى الذين لديهم مستويات كوليسترول الضار في البلازما أكثر من 70 ملّغرام/ ديسيلتر، ومعرضين لخطر مرتفع للإصابة بأمراض تصلب الشرايين القلبية (ASCVD)[18].
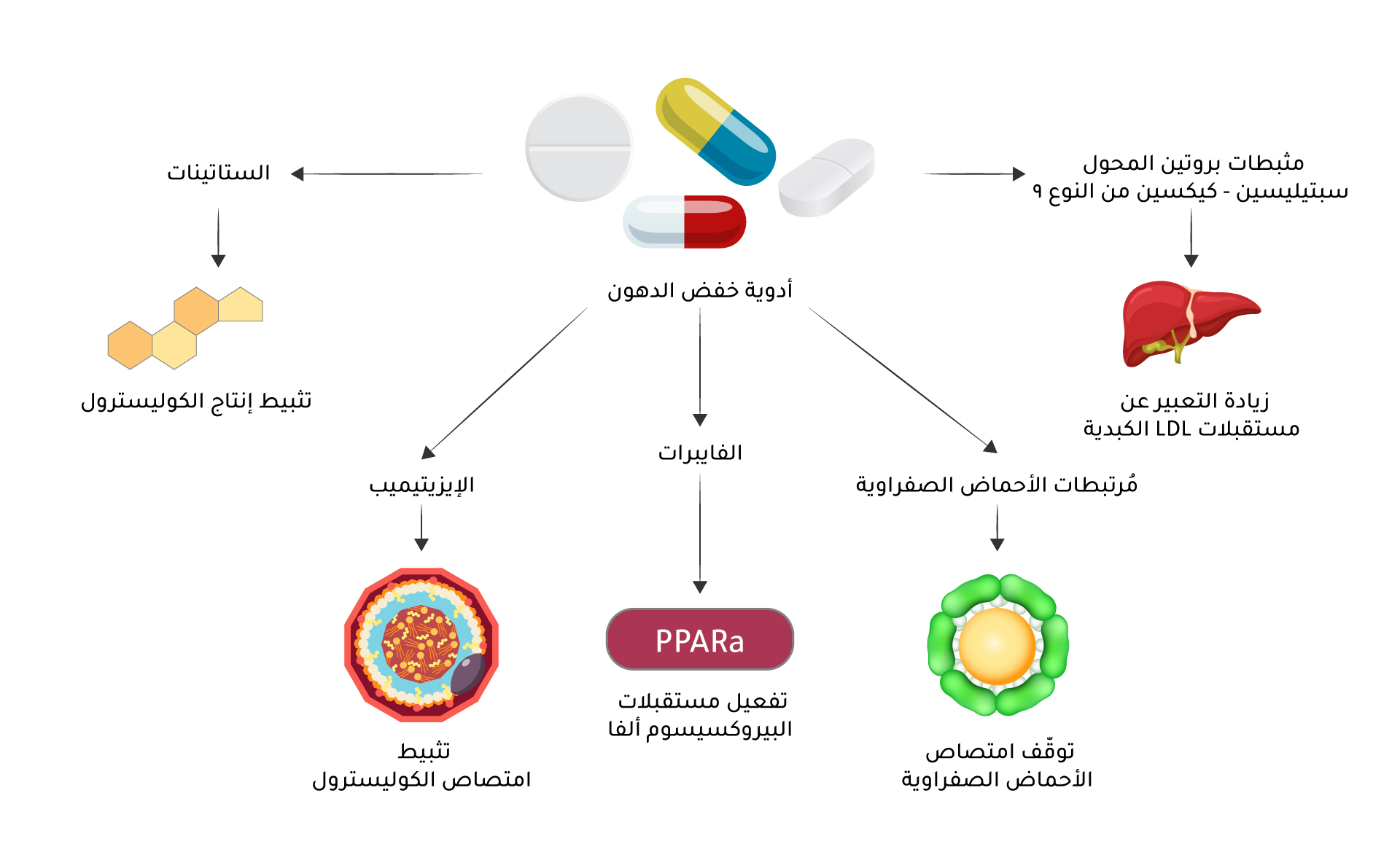 الأدوية الخافضة للدهون وآلية عملها
الأدوية الخافضة للدهون وآلية عملها
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تعمل هذه المثبطات على تقليل خطر الأمراض القلبية الوعائية للمرضى الذين يعانون من متلازمة القلب الحاد بنسبة تتراوح 15 في المئة. يتسبب حقن الأجسام المضادة وحيدة النسيلة تحت الجلد في تأثيرات موضعية في موقع الحقن. وينجم عن الاستخدام المتزايد منها احتمالية إنتاج الأجسام المضادة الذاتية، وارتفاع خطر الإصابة بمرض السكري[19].
دواء إنكليسيران
إنكليسيران (Inclisiran) هو علاج يعتمد على الحمض النووي الريبوزي الصغير المتداخل (Small interfering RNA – siRNA)، ويستهدف الحمض النووي الريبوزي المرسال (mRNA) لبروتين المحول سبتيليسين-كيكسين من النوع 9 (PCSK9) في الكبد. يقلل إنكليسيران مستويات الكوليسترول الضار في البلازما بنسبة 47.9 في المئة لدى المرضى الذين يعانون من فرط كوليسترول الدم العائلي متخالف الجينات (Heterozygous familial hypercholesterolemia – HeFH)، وكذلك للأفراد الذين لديهم مستويات الكوليسترول الضار في البلازما أكثر من 100 ملّغرام/ ديسيلتر في أثناء تلقيهم العلاج بالستاتين. ومن أبرز الآثار الجانبية شيوعًا الإرهاق، وآلام في العضلات، وتورم في موضع الحقن[20].
مثبطات سكوالين سينثاز
مثبطات سكوالين سينثاز (Squalene synthase inhibitors) تعمل على منع إنتاج الكوليسترول دون التأثير في تكوين منتجات الإيزوبرينويد (Isoprenoid products) الحيوية المهمة. أحد الأمثلة على مثبطات سكوالين سينثاز هو أسيتات لاباكويستات (Lapaquistat acetate). تتميز هذه المثبطات بقدرتها على خفض مستويات الكوليسترول والدهون الثلاثية في البلازما دون تعطيل إنتاج الإيزوبرينويد، أما عملها فتقليل الدهون الثلاثية في البلازما إما عن طريق خفض إفرازها أو زيادة التخلص منها، وقد ثبت أن مثبطات سكوالين سينثيز تخفض الدهون الثلاثية في البلازما من خلال مسارات مستقلة عن مستقبلات LDL، وهي آلية مختلفة عن تلك التي تستخدمها الستاتينات أو الفايبرات[21].
حمض بيمبيدويك
حمض بيمبيدويك (Bempedoic acid) هو جزيء صغير يعمل مثبطًا انتقائيًّا لإنزيم ATP سيتريت لاياز (ATP-citrate lyase – ACLY). يُستخدم هذا الحمض بصورة
دواء أولي (Prodrug)، ويحتاج إلى تفعيل بوساطة إنزيم طويل السلسلة من
أسيل-كو A سينثيتاز1 (Acyl-CoA synthetase-1)، الذي يُعبَّر عنه بشكل رئيس في الكبد[22]. يحفز إنزيم
سيتريت لاياز (ACLY) التحويل المعتمد على جزئيات الطاقة للسيتريت والإنزيم المساعد (CoA) إلى أوكسالوأسيتات وأستيل-CoA. يُعدّ أستيل-CoA مقدمة لثلاثي هيدروكسي-3-ميثيل جلوتاريل-كو A-(3-Hydroxy-3-methylglutaryl-CoA – HMG-CoA)، وهو ضروري لتصنيع الكوليسترول. ما يعني أن تثبيط سيتريت لاياز يؤدي إلى انخفاض في إنتاج أستيل كو أ والكوليسترول، ما يزيد من عدد
مستقبلات البروتينات الدهنية منخفضة الكثافة (LDLR) ويقلل من مستويات الكوليسترول في البلازما.
على الرغم من أن حمض بيمبيدويك يمكن أن يقلل من مستويات الكوليسترول الضار في البلازما بنسبة تصل إلى 14 في المئة، إلا أنه لا يُلاحظ انخفاض كبير في حدوث الأمراض القلبية الوعائية الضارة. يرتبط استخدام حمض بيمبيدويك بزيادة مستويات نيتروجين اليوريا في الدم (Blood urea nitrogen)، والكرياتينين (Creatinine)، وحمض اليوريك (Uric acid)، إضافة إلى انخفاض مستويات الهيموغلوبين وزيادة خطر الإصابة بالنقرس ومن الجدير بالذكر أنه من الممكن استخدام حمض بيمبيدويك وحده أو بالجمع مع أدوية أخرى مثل الستاتينات أو الإزيتيميب لتحقيق أفضل خفض للكوليسترول (LDL)[23].
مثبطات أبولايبوبروتين سي 3
إن
أبولايبوبروتين C3 (Apolipoprotein C3 – ApoC3) هو منظم لاستقلاب الدهون الثلاثية عن طريق تثبيط انزيم الليباز البروتيني (Lipoprotein lipase – LPL) المسؤول عن تحلل الدهون الثلاثية في البروتينات الدهنية منخفضة الكثافة جدًا وجزيئات الكيلومكرون. إضافة إلى أن أبوليبوبروتين يثبط إزالة بقايا البروتينات الدهنية منخفضة الكثافة جدًا (VLDL) والكيلومكرون في الكبد من خلال مسارات مستقلة عن إنزيم الليباز البروتيني الدهني. يرتبط ارتفاع مستويات أبوليبوبروتين في البلازما بزيادة احتمالية الإصابة بأمراض القلب والأوعية الدموية.
يُستخدم دواء فولانيسورسن (Volanesorsen)، وهو نوع من الأليغنوكليوتيد المعاكس لاتجاه النسخ (Antisense oligonucleotide – ASO)، الذي يستهدف الحمض النووي الريبوزي المرسال للحمض النووي الريبوزي المرسال الخاص بأبوليبوبروتين سي 3. يُعطى فولانيسورسن للمرضى الذين يعانون من فرط مستويات الدهون الثلاثية في البلازما، وأيضًا للأفراد المصابين بمتلازمة الكيلومكرون العائلية (Familial chylomicronemia syndrome – FCS)[24]. وأبرز الآثار الجانبية لعلاج الفولانيسورسن؛ التعب، وآلام الجهاز العضلي الهيكلي، والغثيان، والقشعريرة، وآلام العضلات[25].
مثبطات البروتينات المشابهة للأنجيوبويتين
البروتينات المشابهة للأنجيوبويتين 3 (ANGPTL3 – Angiopoietin-like protein inhibitors) مثل إيفيناكوماب (Evinacumab) تُنتج وتُفرز من الكبد، وتعمل على تنظيم مستويات الدهون الثلاثية في البلازما. البروتينات المشابهة للأنجيوبويتين 3 لها تأثير كبير في تركيز الدهون الثلاثية والكوليسترول عالي الكثافة (HDL-C) عن طريق تثبيط إنزيم الليباز البروتيني الدهني والليباز البطاني (Endothelial lipase)[26]. ومن الآثار الجانبية لهذا الدواء زيادة الدهون في الكبد بشكل يعتمد على الجرعة[27].
المراجع
Cordero, Alberto, et al. “Estimation of the major cardiovascular events prevention with Inclisiran.”
Atherosclerosis. no. 313 (2020). pp. 76-80.
Ferri, Nicola, and Alberto Corsini. “Clinical Pharmacology of Statins: An Update.”
Current Atherosclerosis Reports. vol. 22(7), no. 26 (2024).
Ferri, Nicola, et al. “Low-density lipoprotein cholesterol-lowering drugs: a narrative review.”
Journal of Clinical Medicine. vol. 13, no. 4, article no. k943 (2024).
Gibson, C. Michael, et al. “Rationale and design of ApoA-I Event Reducing in Ischemic Syndromes II (AEGIS-II): A phase 3, multicenter, double-blind, randomized, placebo-controlled, parallel-group study to investigate the efficacy and safety of CSL112 in subjects after acute myocardial infarction.”
American Heart Journal. vol. 23, no. 1 (2021). pp. 121-127.
Graham, Mark J., et al. “Cardiovascular and metabolic effects of ANGPTL3 antisense oligonucleotides.”
New England Journal of Medicine. vol. 377, no. 3 (2017). pp. 222-232.
Hadjiphilippou, Savvas, and Kausik K. Ray. “Cholesterol-lowering agents.”
Circulation Research. vol. 124, no. 3 (2019). pp. 354-363.
Ishihara, Tsukasa, et al. “Synthesis and Biological Evaluation of Quinuclidine Derivatives Incorporating Phenothiazine Moieties as Squalene Synthase Inhibitors.”
Chemical and Pharmaceutical Bulletin. vol. 52, no. 10 (2004). pp. 1204-1209.
Kim, Kyuho, Henry N. Ginsberg, and Sung Hee Choi. “New, Novel Lipid-lowering Agents for Reducing Cardiovascular Risk: Beyond Statins.”
Diabetes & Metabolism Journal. vol. 46, no. 4 (2022). pp. 517-532.
Khvorova, Anastasia. “Oligonucleotide therapeutics—a new class of cholesterol-lowering drugs.”
New England Journal of Medicine. vol. 376, no. 1 (2017). pp. 4-7.
Koren, Michael J., et al. “Preclinical Development and Phase 1 Trial of a Novel siRNA Targeting Lipoprotein (a).”
Nature Medicine. vol. 28, no. 1 (2022). pp. 96-103.
Michaeli, Daniel Tobias, et al. “Established and Emerging lipid-lowering drugs for primary and secondary cardiovascular prevention.”
American Journal of Cardiovascular Drugs. vol. 23, no. 5 (2023). pp. 477-495.
Ng, Dominic S., Norman C.W. Wong, and Robert A. Hegele. “HDL—is it too Big to Fail?”
Nature Reviews Endocrinology. vol. 9, no. 5 (2013). pp. 308-312.
Nissen, Steven E., et al. “Single Ascending dose Study of a Short Interfering RNA Targeting Lipoprotein (a) Production in Individuals with Elevated Plasma Lipoprotein (a) Levels.”
JAMA. vol. 327, no. 17 (2022). pp. 1679-1687.
Phan, Binh An P., Thomas D. Dayspring, and Peter P. Toth. “Ezetimibe therapy: Mechanism of action and clinical update.”
Vascular Health Risk Management. vol. 8 (2012). pp. 415–427.
Robinson, Jennifer G., et al. “Effect of Evolocumab or Ezetimibe Added to Moderate- or High-intensity Statin Therapy on LDL-C Lowering in Patients with Hypercholesterolemia: The LAPLACE-2 Randomized Clinical Trial.”
JAMA. vol. 311, no. 18 (2014). pp. 1882-1870.
Rosenson, Robert S., et al. “Evinacumab in Patients with Refractory Hypercholesterolemia.”
New England Journal of Medicine. vol. 383, no. 24 (2020). pp. 2307-2319.
Reyes-Soffer, Gissette, et al. “Lipoprotein (a): A Genetically Determined, Causal, and Prevalent Risk Factor for Atherosclerotic Cardiovascular Disease: A Scientific Statement from the American Heart Association.”
Arteriosclerosis, Thrombosis, and Vascular Biology. vol. 42, no. 1 (2022). pp. e48-e60.
Ruscica, Massimiliano, et al. “Side Effects of Statins: From Pathophysiology and Epidemiology to Diagnostic and Therapeutic Implications.”
Cardiovascular Research. vol. 117, no. 17 (2023). pp. 3288–3304.
Salakhutdinov, Nariman F., and Sergey S. Laev. “Triglyceride-lowering agents.”
Bioorganic & Medicinal Chemistry. vol. 22, no. 14 (2014). pp. 3551-3564.
Shriver, Kylee. “Bempedoic Acid: A Novel LDL Cholesterol–Lowering Agent.”
Clinical Diabetes. vol. 38, no. 4 (2020). pp. 405-407.
Tardif, Jean-Claude, et al. “Apolipoprotein C-III Reduction in Subjects with Moderate Hypertriglyceridaemia and at High Cardiovascular Risk.”
European Heart Journal. vol. 43, no. 14 (2022). pp. 1401-1412.
Wang, Helen H., et al. “Cholesterol and Lipoprotein Metabolism and Atherosclerosis: Recent Advances in Reverse Cholesterol Transport.”
Annals of Hepatology. vol. 16, suppl. 1 (2018). pp. 27-42.
Wang, Nan, et al. “ATP-binding Cassette Transporters G1 and G4 Mediate Cellular Cholesterol Efflux to Eigh-density Lipoproteins.”
Proceedings of the National Academy of Sciences. vol. 101, no. 26 (2004). pp. 9774-9779.
Yamashita, Shizuya, Daisaku Masuda, and Yuji Matsuzawa. “Pemafibrate, a new Selective PPARα Modulator: Drug Concept and its Clinical Applications for Dyslipidemia and Metabolic Diseases.”
Current Atherosclerosis Reports. vol. 22(1), no. 5 (2020). pp. 1-17.
Yamashita, Shizuya, et al. “Probucol Trial for Secondary Prevention of Atherosclerotic Events in Patients with Coronary Heart Disease (PROSPECTIVE).”
Journal of Atherosclerosis and Thrombosis. vol. 28, no. 2 (2021). pp. 103-123.
[1] Nicola Ferri et al., “Low-density lipoprotein cholesterol-lowering drugs: a narrative review,” Journal of Clinical Medicine, vol. 13, no. 4, article no. k 943 (2024).
[2] Nariman F. Salakhutdinov & Sergey S. Laev, “Triglyceride-lowering agents,” Bioorganic & Medicinal Chemistry, vol. 22, no. 14 (2014), pp. 3551-3564.
[3] Ibid.
[4] Ibid.
[5] Savvas Hadjiphilippou & Kausik K. Ray, “Cholesterol-lowering agents,” Circulation Research, vol. 124, no. 3 (2019), pp. 354-363; Kim Kyuho, Henry N. Ginsberg & Sung Hee Choi, “New, Novel Lipid-lowering Agents for Reducing Cardiovascular Risk: Beyond Statins,” Diabetes & Metabolism Journal, vol. 46, no. 4 (2022), pp. 517-532.
[6] Kim, Ginsberg & Choi,
op. cit.
[7] Salakhutdinov & Laev,
op. cit.
[8] Nicola Ferri & Alberto Corsini, “Clinical Pharmacology of Statins: An Update,”
Current Atherosclerosis Reports, vol. 22(7), no. 26 (2024).
[9] Daniel Tobias Michaeli et al., “Established and Emerging lipid-lowering drugs for primary and secondary cardiovascular prevention,” American Journal of Cardiovascular Drugs, vol. 23, no. 5 (2023), pp. 477-495.
[10] Massimiliano Ruscia et al., “Side effects of statins: From pathophysiology and Epidemiology to Diagnostic and Therapeutic Implications,”
Cardiovascular Research, vol. 118, no. 17 (2022), pp. 118, 3288–3304.
[11] Ferri et al.,
op. cit.; Binh An P. Phan, Thomas D. Dayspring & Peter P. Toth, “Ezetimibe therapy: Mechanism of action and clinical update,”
Vascular Health Risk Manag, vol. 8 (2012), pp. 415-427.
[12] Ibid.
[13] Salakhutdinov & Laev,
op. cit.
[14] Phan, Dayspring & Toth, op. cit.; Shizuya Yamashita, Daisaku Masuda & Yuji Matsuzawa, "Pemafibrate, A new Selective PPARα Modulator: Drug Concept and its Clinical Applications for Dyslipidemia and Metabolic Diseases," Current Atherosclerosis Reports, vol. 22(1), no. 5 (2020), pp. 1-17.
[15] Kim, Ginsberg & Choi,
op. cit.
[16] Phan, Dayspring & Toth.
op. cit.
[17] Kim, Ginsberg & Choi,
op. cit.
[18] Jennifer G. Robinson et al., “Effect of evolocumab or ezetimibe added to moderate- or high-intensity statin therapy on LDL-C lowering in patients with hypercholesterolemia: the LAPLACE-2 randomized clinical trial,”
JAMA, vol. 311. no. 18 (2014), pp.1882-1870.
[19] Kim, Ginsberg & Choi,
op. cit.
[20] Anastasia Khvorova, “Oligonucleotide Therapeutics—a New Class of Cholesterol-lowering Drugs,” New England Journal of Medicine, vol. 376, no. 1 (2017), pp. 4-7; Alberto Codero et al., “Estimation of the Major Cardiovascular Events Prevention with Inclisiran,” Atherosclerosis, vol. 313 (2020), pp. 76-80.
[21] Salakhutdinov & Laev,
op. cit.; Tsukasa Ishihara et al., “Synthesis and biological evaluation of quinuclidine derivatives incorporating phenothiazine moieties as squalene synthase inhibitors,” Chemical and Pharmaceutical Bulletin, vol. 52, no. 10 (2004), pp. 1204-1209.
[22] Ferri et al,
op. cit.
[23] Kylee Shriver, “Bempedoic Acid: A Novel LDL Cholesterol–Lowering Agent,” Clinical Diabetes, vol. 38, no. 4 (2020), pp. 405-407.
[24] Ibid.
[25] Jean-Claude Tardif et al., “Apolipoprotein C-III Reduction in Subjects with Moderate Hypertriglyceridaemia and at high Cardiovascular Risk.” European Heart Journal, vol. 43, no. 14 (2022), pp. 1401-1412.
[26] Kim, Ginsberg & Choi,
op. cit.
[27] Robert S. Rosenson et al., “Evinacumab in patients with refractory hypercholesterolemia,” New England Journal of Medicine, vol. 383, no. 24 (2020), pp. 2307-2319.