جون دالتون (John Dalton، 1766-1844) عالم كيميائي بريطاني، كان رائدًا في تطور
علم بنية الذرة واشتُهر بتقديم نظريته الذرية التي قدمت أول تفسير علمي مقبول ومتماسك لبنية المادة، وأحدثت ثورة علمية هائلة في تقدم
علم الكيمياء ولا سيما في مجال
الكيمياء العضوية، فقد شكلت هذه النظرية حجر الأساس الذي بُنيت عليه مفاهيم الكيمياء الحديثة وقوانينها، بما في ذلك فهم
التركيب الذري {{التركيب الذري: البنية الداخلية للذرة، التي تُعَدّ أصغر وحدة بنائية للمادة تحتفظ بخواص العنصر. تتكون الذرة من جزأين أساسيين: النواة، وهي تحتوي على البروتونات والنيوترونات؛ والإلكترونات، وهي جسيمات صغيرة ذات شحنة سالبة تدور حول النواة.}} للجزيئات البسيطة والمعقدة. وكان للعالم دالتون أيضًا اهتمامات كبيرة في علم الأرصاد الجوية، إذ كان ذلك أساسًا في اكتشافاته عن الغازات وصياغة
قانون الضغوط الجزيئية {{قانون الضغوط الجزيئية: أو ما يُعرف بقانون دالتون للضغوط الجزئية، هو قانون فيزيائي ينص على أن الضغط الكلي لخليط من الغازات يساوي مجموع الضغوط الجزئية لكل غاز على حدة، بشرط ألّا تتفاعل الغازات مع بعضها كيميائيًا.}}. ومن إنجازاته البارزة أيضًا، أنه يعد أول من قدم تفسيرًا علميًا لداء
عمى الألوان {{عمى الألوان: اضطراب بصري يُفقد الشخص القدرة على التمييز بين بعض الألوان أو رؤيتها رؤيةً طبيعيةً. يحدث عادة بسبب خلل في الخلايا المخروطية، وهي المستقبلات الضوئية الموجودة في شبكية العين والمسؤولة عن إدراك الألوان. وقد تكون هذه الحالة وراثية أو مكتسبة.}}، وهو الاضطراب في تمييز الألوان الذي كان هو وأخوه يعانيان منه.
حياته المبكرة وتعليمه
ولد العالم جون دالتون في أيلول/ سبتمبر عام 1766، في إيغلزفيلد (Eaglesfield) بمقاطعة كمبرلاند (Cumberland) في إنكلترا، وتوفي بسبب سكتة دماغية في تموز/ يوليو عام 1844 بمدينة مانشستر. انتمى أبواه لعائلة من طائفة الكويكرز (الصورة 1)، والتحق في طفولته بمدرسة جون فليتشر في إيغلزفيلد، وبدأ في سن الثانية عشر بمساعدة شقيقه الأكبر جوناثان في التدريس فيها، وبعد عامين انتقل جون دالتون إلى العمل في مدرسة أخرى، حيث تطورت مهاراته التعليمية تدريجيًا أولًا بوصفه مساعدًا ثم بصفته مديرًا. اكتسب خلال مدة تدريسه خبرة من أبرز المشرفين والمرشدين على المدرسة وهم: إيليهو روبنسون (Elihu Robinson)، وجون غوف (John Gough)، واكتسب منهم معرفة علمية في مجال استخدام أدوات الأرصاد الجوية، وكيفية الاحتفاظ بسجلات الطقس اليومية، وتعلم منهم أيضًا المهارات الأساسية للتعليم في مجال علم الرياضيات، واللغتين اللاتينية واليونانية. في عام 1793، انتقل دالتون إلى مانشستر لتولي منصب مدرس رياضيات في أكاديمية مستقلة، وفي أثناء انتقاله كان يعمل على النسخة الأولية في كتابه الأول الذي حمل العنوان (Metrological Observations and Essays)، والذي ضم موضوعات ومقالات عن الأرصاد الجوية التي كتبها جرّاء خبرته في الملاحظة، وتسجيل المعطيات اليومية لكل من
الضغط الجوي {{الضغط الجوي: الضغط الناتج من وزن عمود الهواء الواقع فوق وحدة المساحة عند مستوى سطح الأرض. ونظرًا إلى أن الهواء له كتلة، فإنه يؤثر بقوة في كل ما يوجد على سطح الأرض، وتتأثر قيمته بتغيّرات درجة الحرارة والرطوبة.}} وكمية الأمطار والرطوبة والرياح وغيرها. كذلك كان يفكر بعمق في أهمية البيانات التي كان يجمعها ويدرجها في الكتاب[1]. نُشر هذا الكتاب عام 1793 ولم يحظ بالقبول بشكل جيد في البداية، إلا أنه احتوى على أفكار كانت بمنزلة تطور علمي جديد في مجال الأرصاد الجوية، ونقل
علم الأرصاد من موضوع الفولكلور الشعبي العام إلى مسعى وبحث علمي جاد[2].
وبعد مدة وجيزة من وصوله إلى مانشستر، انتُخِب دالتون عضوًا في جمعية مانشستر الأدبية والفلسفية، وكانت إسهاماته الأولى في هذه الجمعية عبارة عن وصف للعيوب التي اكتشفها دالتون في بصره وبصر أخيه، إذ كان ذلك أول منشور عن
عمى الألوان، وعرف فيما بعد باسم الدالتونية نسبة إلى العالم دالتون[3].
وظيفته وإسهاماته العلمية
علم الأرصاد الجوية
ولد جون دالتون ونشأ في منطقة جبلية في إنكلترا منحته إطلالة جيدة لمراقبة مختلف الظواهر الجوية، وظل مهتمًا بالأرصاد الجوية طيلة حياته، فقسّم كتابه
ملاحظات ومقالات في علم الأرصاد إلى جزأين[4]، عرض الجزء الأول معلومات متنوعة تصف الأدوات التي كان يستخدمها في جمع المعطيات اليومية للطقس، مثل
الباروميتر {{الباروميتر: جهاز علمي يُستخدم لقياس الضغط الجوي الذي يُحدثه الهواء على سطح الأرض. ويُعدّ هذا الجهاز عنصرًا أساسيًا في محطات الأرصاد الجوية، وله تطبيقات حيوية في التنبؤ بالطقس وفي مجالات أخرى.}} ومقاييس الحرارة والرطوبة وهي أدوات صنعها دالتون بنفسه، فقد اكتسب المعرفة العملية في استخدام أدوات الأرصاد الجوية من مرشديه روبونسون وجوف وبنائها. كذلك اشتمل هذا الجزء على البيانات التي كان يجمعها بشأن الضغط الجوي ودرجة الحرارة والرطوبة وكميات الأمطار، وضمّ تقارير عن الرياح والثلوج والعواصف الرعدية. أما الجزء الثاني فتناول مقالات نظرية بشأن الظواهر الجوية تشمل مكونات الغلاف الجوي ومقالات عن
التبخر {{التبخر: عملية فيزيائية يتحول فيها السائل إلى غاز (بخار) من دون الحاجة إلى بلوغ درجة الغليان. تحدث هذه العملية على سطح السائل، إذ تكتسب بعض جزيئاته طاقة كافية للتغلب على قوى التجاذب بينها، فتهرب إلى الغلاف الجوي بشكل غاز.}} والأمطار. وكان يدرس البيانات التي كان يجمعها ويبني فرضيات وعلاقات بينها، ففي مقالة تتحدث عن التبخر والمطر والبرد والثلج والندى، بعنوان: "On Evaporation, Rain, Hail, Snow and Dew"، أدرج بيانات تجريبية بشأن درجة الحرارة التي يغلي عندها الماء تحت ضغوط مختلفة، وافترض في هذا المقال أن الحد الأقصى لكمية بخار الماء التي يمتصها حجم الهواء تعتمد على درجة الحرارة فقط بغض النظر عن كثافته، وأثبتت تجاربه الرائدة أن تكاثف البخار المعرض للهواء لا يعتمد بأي حال من الأحوال على ضغط الهواء. كرّس دالتون اهتمامه أيضًا في تفسير ظاهرة الشفق القطبي (Aurora Borealis) بوصفها ظاهرة مرتبطة بحدوث المغناطيسية في الغلاف الجوي (Atmospheric magnetism) وكتب عنها مقالة في كتابه. وفي مرحلة لاحقة، تناول العالم
مايكل فارادي (Michael Faraday، 1791-1867) موضوع المغناطيسية الجوية مستندًا إلى اكتشافه أن غاز الأكسجين يمتلك خصائص بارامغناطيسية، وهو ما مثل دليلًا باكرًا على قابلية بعض الغازات للتأثر في المجالات المغناطيسية. وقد وصف العالم البريطاني
جون فريدريك دانييل (John Frederic Daniell، 1790-1845) العالم دالتون بـأبي الأرصاد الجوية (Father of meteorology)[5].
 غلاف كتاب ملاحظات ومقالات في علم الأرصاد
غلاف كتاب ملاحظات ومقالات في علم الأرصاد
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
وكان تفكير دالتون في فيزياء الغلاف الجوي بمنزلة مقدمة لأبحاثه المخبرية في مانشستر في الفترة 1799- 1803، وقد أكد أن الغلاف الجوي هو خليط فيزيائي يتكون من نحو 80 في المئة نيتروجين و20 في المئة أكسجين، وتوصل دالتون إلى
قانون الضغط الجزئي (Partial Pressure) الذي ينص على أن الضغط الكلي لمزيج من الغازات يساوي مجموع الضغوط الجزئية للغازات المكونة لهذا المزيج، فالمكونات الأربعة للغلاف الجوي التي افترضها دالتون (النيتروجين، والأكسجين، وثاني أكسيد الكربون، وبخار الماء) تضغط على سطح الأرض بشكل مستقل عن بعضها ولا يؤثر اختفاء أي غاز منها في الكثافة والضغط اللذين تمارسهما بقية المكونات الأخرى. وأوضح دالتون أن قوى التنافر تنشأ فقط بين الذرات من النوع نفسه وأن الذرات داخل الخليط تختلف في الوزن والنوع والكثافة، وأن الضغط يرجع فقط إلى قوى التنافر بين الجسيمات. في عام 1800، أجرى تجارب عدة على تأثير التمدد الحراري للغازات وأوضح أن الموائع المختلفة أظهرت التباين نفسه في ضغط البخار مع التباين نفسه في درجة الحرارة، إذ إن الموائع المرنة جميعها تتمدد بالتساوي بفعل الحرارة تحت الضغط نفسه، وقدّم تجاربه وأبحاثه إلى جمعية مانشستر الأدبية والفلسفية، إذ افترض دالتون أنه عندما تتمدد الغازات عند درجة حرارة معينة تزداد المسافة بين الجسيمات المكونة للخليط ويضعف التنافر وينخفض الضغط بين الجسيمات، ومن ثم توصل إلى أنه عند زيادة درجة الحرارة في حجم ثابت من الغازات يزداد التنافر بين الجسيمات ويرتفع الضغط. وقاس دالتون الرطوبة باستخدام مقياس الندى لتحديد كيفية تأثير درجة الحرارة في مستوى بخار الماء الموجود في الغلاف الجوي[6].
نشر دالتون في عام 1803 ورقة علمية عن امتصاص الغازات بوساطة الماء والسوائل الأخرى، بعنوان: "On the Absorption of Gases by Water and other Liquids"، فسر فيها ذائبية الغازات في الماء بمصطلحات ميكانيكية فكتب: "إن الغازات جميعها التي تدخل إلى الماء والسوائل الأخرى بفعل الضغط، تتحرر كليًا مرة أخرى عند إزالة هذا الضغط"؛ إذ إن الغازات تكون ممتزجة ميكانيكيًا في السوائل، وليست مرتبطة كيميائيًا بها، وتوصل دالتون إلى أن الجسيمات الأخف وزنًا تكون أقل قابلية للذوبان في الماء، في حين الجسيمات الأكثر وزنًا تكون أكثر قابلية للذوبان[7]. وفي عام 1838 أسهم دالتون في ورقة بحثية عن الأرسينات والفوسفات، بعنوان: "On the Arsenate and Phosphate"[8].
النظرية الذرية
وضع دالتون في عام 1808 نظريته الذرية تحت عنوان (A New System of Chemical Philosophy). تصنف
النظرية الذرية (Atomic theory) بأنها العمل الأكثر تأثيرًا الذي قدمه دالتون في علم
الكيمياء والذي يعد من أعظم إنجازاته. استند في نظريته بشأن الضغوط الجزيئية إلى فكرة أن
الذرات المتشابهة في خليط من الغازات تتنافر مع بعضها، والذرات غير المتشابهة تكون في حالة تفاعل دائم مع بعضها، واستخدم هذا المفهوم لتفسير تصرف كل غاز في المزيج بشكل مستقل، إلا أن هذا الاعتقاد ثبُت عدم صحته فيما بعد، ولكنه خدم غرضًا مفيدًا حينئذٍ، إذ ساعده على إلغاء الفكرة التي تبناها كثير من العلماء السابقين بأن ذرات أنواع المادة جميعها متشابهة[9].
نصت
النظرية الذرية على نقاط أساسية، وهي:
- تتكون المواد جميعها من جسيمات صغيرة جدًا، تُعرف بالذرات، وتعد هذه الذرات غير قابلة للانقسام.
- تتميز ذرات كل
عنصر كيميائي بكونها متشابهة تمامًا في الشكل والكتلة والخواص الكيميائية، وتختلف عن ذرات أي عنصر آخر.
- تؤكد النظرية أن الذرات لا تُخلق ولا تفنى في أثناء
التفاعلات الكيميائية، بل يعاد ترتيبها لتكوين مواد جديدة[10].
وكانت السمة الأساسية لنظرية دالتون وصفه بأن ذرات العناصر المختلفة تختلف في الشكل والحجم والكتلة، إذ كانت حجته بأن كل عنصر له ذراته الخاصة به وتختلف عن ذرات أي عنصر آخر. ناقضت هذه النظرية أفكار أولئك الذين اعتقدوا أن وجود كثير من الجسيمات المختلفة يتعارض مع مبدأ بساطة الطبيعة، فقد رأى بعض المفكرين والعلماء ومنهم العالم اليوناني ديموقرطس (Democritus، نحو 460-360ق.م.)، وعالم الرياضيات والفلك روجريرو جوزيبي بوسكوڤيتش (Ruggero Giuseppe Boscovich، 1711-1787) أن الذرات الموجودة في الطبيعة جميعها متشابهة، وأن تنوع الذرات يؤدي إلى تدمير الطبيعة بسهولة. لكن دالتون رفض تلك الاعتراضات بوصفها افتراضات خيالية، ولا تستند إلى أساس علمي تجريبي، وبدلًا من ذلك فقد ركز على تحديد الكتل الذرية النسبية لذرات
العناصر المختلفة من خلال البحث في عدد
الذرات لكل عنصر موجود في
المركبات الكيميائية المختلفة[11].
[الشكل1]
 الرموز التصويرية التي رسمها دالتون للعناصر الكيميائية
الرموز التصويرية التي رسمها دالتون للعناصر الكيميائية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل2]
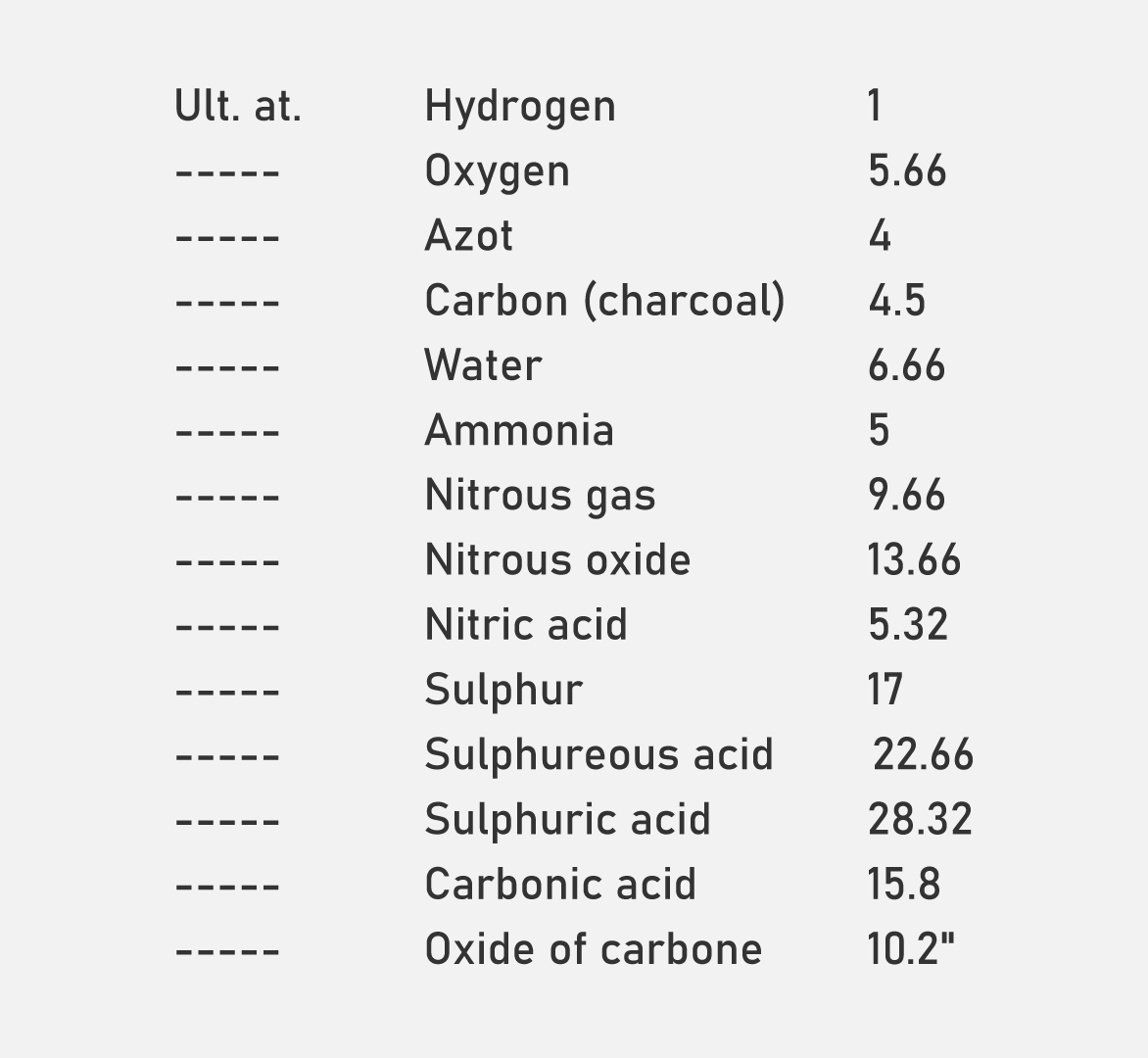 الجدول الأول للأوزان الذرية النسبية للعناصر والمركبات التي وضعها دالتون
الجدول الأول للأوزان الذرية النسبية للعناصر والمركبات التي وضعها دالتون
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
اعتمدت
النظرية الذرية على خصيصة ذرية واحدة وهي وزن
الذرة، فقد وجد دالتون أن ذرات
العناصر المختلفة يمكن تمييزها عن غيرها بناء على أوزانها الذرية، إذ كان أول من حسب الأوزان الذرية لعدد من
العناصر الكيميائية. شملت هذه
العناصر الهيدروجين والأكسجين والنيتروجين والكربون. وأعطى رموزًا تصويرية لتمثيل هذه
العناصر الكيميائية وذلك في جزء من النظرية الذرية. كانت هذه الرموز هي دوائر ذات أجزاء داخلية مميزة لكل عنصر، وكان الاختيار الأولي لذرة الهيدروجين دائرة مفتوحة في حين كانت ذرة الأكسجين دائرة منقطة (الشكل 1). ووضع دالتون هذه الرموز مع أوزانها في جداول (الشكل 2)، وقدم
الأوزان الذرية على أنها نسب أوزان
الذرات المختلفة مقارنة بذرة الهيدروجين التي اختارها دالتون بوصفها وحدة أساسية لقياس الأوزان، وقد وصف طريقته في قياس كتل العناصر المختلفة وفقًا لطريقة يجري من خلالها اتحاد ذرات عناصر مختلفة مع بعضها بنسب ثابتة بسيطة. واتبع قاعدة البساطة القصوى (Rule of Greatest Simplicity)، وبذلك صاغ دالتون قانون النسب الثابتة (Law of Fixed Proportions) الذي ينص على أن العناصر تتحد مع بعضها بنسب ثابتة مماثلة للنسب الوزنية لذراتها مكونة
مركبات جديدة. عدّ دالتون قانون النسب الثابتة أمرًا مفروغًا منه، وتجاهل الجدل الذي كان يتناوله بعض العلماء الكيميائيين الفرنسيين، ومنهم جوزيف لويس بروست (Joseph-Louis Proust، 1754-1826)، وكلود لويس بيرتوليه (Claude-Louis Berthollet، 1748-1822) بشأن قانون النسب الثابتة[12].
وصاغ دالتون قانون النسب المتضاعفة (Law of multiple proportions) بناءً على قياساته، الذي ينص على أنه إذا اتحد عنصران لتكوين أكثر من مركب، فتكون نسبة كتل مختلفة من العنصر الأول عند إضافته على كتلة ثابتة من العنصر الثاني تأخذ نسبة عددية صحيحة بسيطة. على سبيل المثال، إذا أخذنا العنصرين A وB، فإنهما يتحدان مع بعضهما وفقًا لنسبة الكتلة A: B = (x: y) أو (x : 2y) أو (2x :y)، وهكذا فأي نسبة لكتلة العنصرين تكون نسبة عددية صحيحة بسيطة، وهذا يعني أنه بالإمكان تكوين مركبات مختلفة ناتجة من اتحاد العنصرين بنسب كتلية مختلفة[13].
ومن التحديات التي واجهت نظرية دالتون أن معرفة النسب الوزنية للعناصر في المركبات المختلفة لم تكن كافية لتحديد العدد الفعلي لذرات
العناصر في كل مركب. على سبيل المثال، لاحظ دالتون أن الميثان يحتوي على ضعف كمية الهيدروجين الموجودة في الإيثيلين، فافترض بناءً على بياناته أن الميثان يتكون من ذرة كربون واحدة وذرتين من الهيدروجين وذلك يكون بالصيغةCH2 ، في حين وجد أن الإيثيلين يتكون من ذرة كربون واحدة وذرة هيدروجين واحدة. وجد لاحقًا أن هذه التقديرات كانت غير دقيقة، لأن جزيء الميثان بالحقيقة يتكون من أربع ذرات هيدروجين ويكون بالصيغة (CH4)، في حين يتكون الإيثيلين من ذرتي كربون وأربع ذرات من الهيدروجين ويكون بالصيغة (C2H4). وعلى الرغم من افتقار
النظرية الذرية حينئذٍ لبعض الدقة التجريبية ومحدودية التفسير، فإنها شكلت نقطة انطلاق أساسية نحو فهم طبيعة المادة. لأنها كانت المرة الأولى التي تُطرح فيها أن العناصر تتكون من ذرات صغيرة جدًا غير قابلة للانقسام، وأن ذرات العنصر الواحد فريدة ومتمايزة في الكتلة والحجم عن غيرها. ولم تُصحَّح بعض أوجه القصور في نظرية دالتون إلا تدريجيًا، ولا سيما في الفترة التي أشار فيها العالم الكيميائي الإيطالي ستانيسلاو كانيزارو (Stanislao Cannizzaro، 1826-1910) إلى أهمية فرضية
أميديو أڤوغادرو في تحديد
الكتل الجزيئية. ومنذ ذلك الحين عد الكيميائيون أن نظرية دالتون الذرية، رغم نقائضها الأولية، العامل الرئيس وراء التقدم في مجال البنية الذرية والكيمياء الحديثة، لا سيما
الكيمياء العضوية التي شهدت تطورًا هائلًا بعد ترسيخ المفهوم الذري. ونتيجةً للإسهامات الكبيرة في الكيمياء الذرية التي قدمها العالم دالتون وتأسيسه لنظرية متماسكة بشأن طبيعة المادة، ولتطوير التصوّر الذرّي، حاز دالتون لقبَ أبي الكيمياء (Father of chemistry)[16].
التحديات وأوجه القصور في نظرية دالتون
على الرغم من أن النظرية الذرية لدالتون مثلت حجر الأساس في تطور علم
الكيمياء، فقد واجهت تحديات عدة ظهرت مع تقدم المعرفة العلمية وتطوير أدوات البحث ووسائله.
وكان من أبرز هذه التحديات التي واجهت دالتون (وقد خضعت للتطوير لاحقًا) افتراضه أن الذرات تعد أصغر وحدة في المادة ومن ثم تكون غير قابلة للانقسام. ومع أن هذا الافتراض كان مقبولًا في زمنه، فإنه بعد اكتشاف
الإلكترونات على يد العالم
جوزيف جون ثومسون (Joseph John Thomson، 1856-1940) والبروتونات على يد العالم
إرنست رذرفورد (Ernest Rutherford، 1871-1937) والنيوترونات على يد العالم
جيمس تشادويك (James Chadwick، 1891-1974) تبيّن أن الذرة نفسها تحتوي على جسيمات أصغر ما يجعلها قابلة للتجزئة.
افترض دالتون أن ذرات العنصر الواحد جميعها متشابهة تمامًا في الكتلة والخصائص الكيميائية، ولكن مع اكتشاف
النظائر (Isotopes) تبيّن أن للعنصر الواحد ذرات تختلف في الكتلة وذلك بسبب اختلاف عدد
النيوترونات في أنويتها. لم يتمكن دالتون من تحديد العدد الفعلي للذرات في المركبات والجزيئات الكيميائية، كذلك لم توفر نظرية دالتون تفسيرًا واضحًا لكيفية اتحاد الذرات مع بعضها لتشكيل مركبات مختلفة، ولم تفسر النظرية حينئذٍ التفاعلات الكيميائية المختلفة بشكل علمي، إذ اقتصر التفسير على وصف التفاعلات الكيميائية على أنها إعادة ترتيب للذرات فقط[17].
انتقد السير همفري ديڤي (Sir Humphry Davy، 1778-1829) مكتشف الصوديوم والبوتاسيوم، جون دالتون لكونه "مجربًا فظًا للغاية"، وذلك لأن دالتون لم يستخدم الأدوات في تجاربه وأبحاثه وكان يفضل الثقة في مهاراته وحدسه في التوصل إلى النتائج، ولكنه كان غالبًا ما يحصل على النتائج التي يريدها[18].
عمى الألوان (الدالتونية)
 نُصب نصفي لجون دالتون
نُصب نصفي لجون دالتون
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
علاوة على تفوقه في علم
الكيمياء واهتمامه في علم الأرصاد الجوية، طوّر دالتون نظرية لتفسير السبب وراء نقص رؤية الألوان الذي كان يعاني منه هو وشقيقه. أدرك دالتون عدم مقدرته على التمييز بين الألوان حين أرسلته والدته ليشتري لها خيطًا يتناسب مع لون فستانها الرمادي الخاص بطائفة الكويكرز، لأنه اختار خيطًا لونه قرمزي (أحمر فاتح)، وقد بدا له مشابهًا للون الرمادي. فدرس بشكل علمي أسباب اضطراب الرؤية اللونية لديه وقدّم أول تفسير علمي للظاهرة، ثم نشر في عام 1798 ورقة علمية بحثية عُنيت بعمى الألوان (color Blindness)، وصف فيها تسميته غير المعتادة للألوان بشكل مختلف عن معظم الأشخاص الآخرين، إذ كان يخلط بين اللون القرمزي واللون الأزرق والأخضر، وحاول وضع فرضيات وراثية لتفسير ذلك. فافترض أن لون السائل في العينين المعروف بالجسم الزجاجي (Vitreous humor) في عينه كان ملونًا باللون الأزرق، ما جعل الجسم الزجاجي يمتص بشكل انتقائي أطوالًا موجية أطول مما هي عليه، لكن هذا الاستنتاج أُثبت فيما بعد أنه خاطئ. وقد أوصى دالتون بفحص عينه وتحليلها بعد وفاته، وفعلًا أجرى الأطباء فحوصات وتحليلات على عينه في اليوم التالي لوفاته. وفي سنوات لاحقة أظهر فحص
الحمض النووي (DNA) المستخرج من أنسجة عينه المحفوظة أنه يفتقر إلى الصبغة الضوئية ذات الموجة المتوسطة في شبكية العين، وهذا ما جعله غير قادر على التمييز بين اللون الأحمر واللونين الأزرق والأخضر[19].
التكريمات التي حازها
انتُخب دالتون عضوًا في زمالة الجمعية الملكية في لندن (Royal Society of London)، والجمعية الملكية في إدنبرة (Royal Society of Edinburgh). وحاز أيضًا درجةً فخرية من جامعة أكسفورد، وانتُخب عضوًا من بين ثمانية أعضاء أجانب في الأكاديمية الفرنسية للعلوم (French Academy of Sciences) ليشغل المنصب الذي شَغَر بعد وفاة السير همفري ديڤي. وفي عام 1817، انتُخب دالتون رئيسًا للجمعية الأدبية والفلسفية (Literary and Philosophical Society) واستمر في هذا المنصب بقية حياته، وبعد انتقاله إلى الكلية الجديدة في مانشستر زودته الجمعية بمختبر ليستمر بأبحاثه.
تقديرًا له ولإنجازاته وإسهاماته في علم الأرصاد الجوية والنظرية الذرية، خصصت الحكومة الإنكليزية للعالم جون دالتون راتبًا تقاعديًا. وكان من أبرز مظاهر التكريم التي حصل عليها دالتون خلال حياته، إنشاء تمثال له في لندن. وبعد وفاته، أُطلق اسمه على
وحدة قياس الكتلة الذرية (ورمزها Da)، تكريمًا له واعترافًا بجهوده الكبيرة التي ظلت حجر الأساس التي بُنيت عليها مفاهيم
الكيمياء الحديثة[20].
المراجع
Constable, Edwin C. “John Dalton–The Man and The Myth.” Dalton Transactions. vol. 51, no. 3 (2022). pp. 768-776.
Dalton, John. Meteorological Observations and Essays. London: Harrison & Crosfield, 1834.
Hunt, David M. et al. “The Chemistry of John Dalton's Color Blindness.” Science. vol. 267, no. 5200 (1995). pp. 984-988.
“John Dalton.” Biography. 21/5/2021. at: https://acr.ps/1L9F2MJ
“John Dalton Biography.” Biography Online. 8/1/2020. at: https://acr.ps/1L9F3dP
Peterman, Keith & Matthew Cordes (eds.). Contextualizing Climate Change: Linking Science and Culture. Washington: American Chemical Society, 2021.
Ross, Sydney. “John Dalton | Biography, Discoveries, Atomic Model, & Facts.” Encyclopedia Britannica. 12/2/2025. at: https://acr.ps/1L9F2I1
Salvi, Pier Remigio. “Dalton’s Long Journey from Meteorology to the Chemical Atomic Theory.” Substantia. vol. 7, no. 2 (2023). pp. 101-119.
Stewart, Ken. “Atomic Model | Definition, History, Development, Examples, & Facts.” Encyclopedia Britannica. 7/2/2025. at: https://acr.ps/1L9F2uq
Woody, Andrea I., Robin Findlay Hendry & Paul Needham (eds.). Handbook of The Philosophy of Science, Volume 6: Philosophy of Chemistry. [Oxford]: North-Holland, 2012.
Zwier, Karen R. “John Dalton’s Puzzles: From Meteorology to Chemistry.” Studies in History and Philosophy of Science. vol. 42, no. 1 (2011). pp. 58-66.
[1]Sydney Ross, “John Dalton | Biography, Discoveries, Atomic Model, & Facts,” Encyclopedia Britannica, 12/2/2025, accessed on 18/9/2025, at: https://acr.ps/1L9F2I1
[2] Edwin C. Constable, “John Dalton–The Man and The Myth,” Dalton Transactions, vol. 51, no. 3 (2022), p. 768.
[3] Ross, op. cit.
[4] John Dalton, Meteorological Observations and Essays (London: Harrison & Crosfield, 1834).
[5] Pier Remigio Salvi, “Dalton’s Long Journey from Meteorology to the Chemical Atomic Theory,” Substantia, vol. 7, no. 2 (2023), p. 101; Karen R. Zwier, “John Dalton’s Puzzles: From Meteorology to Chemistry,” Studies in History and Philosophy of Science, vol. 42, no. 1 (2011), p. 58.
[6] Ibid.; Salvi, p. 102; Ross; “John Dalton Biography,” Biography Online, 8/1/2020, accessed on 18/9/2025, at: https://acr.ps/1L9F2BK
[7] Salvi, p. 102.
[8] Ross, op. cit.
[9] Ibid.
[10] Keith Peterman & Matthew Cordes, “England: John Dalton and the Atomic Theory,” in: Keith Peterman & Matthew Cordes (eds.), Contextualizing Climate Change: Linking Science and Culture (Washington: American Chemical Society, 2021), p. 37.
[11] Ross, op. cit.
[12] Ibid.; Salvi, p. 102.
[13] Ross, op. cit.
[14] Salvi, p. 102.
[15] Ibid.
[16] Ross, op. cit.
[17] Ken Stewart, “Atomic Model | Definition, History, Development, Examples, & Facts,” Encyclopedia Britannica, 7/2/2025, accessed on 18/9/2025, at: https://acr.ps/1L9F2uq
[18] “John Dalton,” Biography, 21/5/2021, accessed on 18/9/2025, at: https://acr.ps/1L9F2MJ
[19] David M. Hunt et al., “The Chemistry of John Dalton's Color Blindness,” Science, vol. 267, no. 5200 (1995), p. 984; David Knight, “John Dalton (1766-1844),” in: Andrea I. Woody, Robin Findlay Hendry & Paul Needham (eds.), Handbook of The Philosophy of Science, Volume 6: Philosophy of Chemistry ([Oxford]: North-Holland, 2012), p. 71.
[20] “John Dalton Biography”.