البروتينات غير المرتبة (أو المضطربة) جوهريًا، بروتينات لا تحتوي كلها أو مجالات معينة منها على بنية مرتبة كغيرها من
البروتينات، وتكون ذات مرونة هيكلية واسعة، ما يجعلها متحركة بشكل كبير. لا تتخذ البروتينات غير المرتبة جوهريًا شكلًا ثلاثي الأبعاد ثابتًا في الظروف الطبيعية في
الخلايا، وبدلًا من ذلك، تكون في حالة توازن حركي بين هياكل متعددة غير مطوية، يمليها تسلسل
الأحماض الأمينية. ترتبط الديناميكيات الهيكلية والمرونة الموجودة في البروتينات غير المرتبة جوهريًا، بالعمليات البيولوجية الرئيسة، التي تتضمن وظائف تنظيمية وإشارات خلوية. يمثل اكتشاف هذه البروتينات نقلة نوعية في فهم العلاقة بين بنية البروتين ووظيفته، ما يتحدى وجهات النظر التقليدية القائلة بأن البروتينات تتطلب بنية ثلاثية الأبعاد ثابتة، حتى تؤدي أي نشاط بيولوجي. تُظهر هذه البروتينات قدرة ملحوظة على التكيف هيكليًا، فتتخذ أشكالًا مختلفة متعددة اعتمادًا على الظروف الخلوية، وتتميز بوجود مناطق مرنة خالية من البنية البروتينية الثانوية المنظمة، وبأحماض أمينية قطبية ومشحونة، وبعدم وجود مناطق عدة كارهة للماء. ومن الناحية الوظيفية، تعمل البروتينات غير المرتبة جوهريًا بوصفها مُعدِّلات جزيئية في
مسارات الإشارة، وتشارك في استتباب التوازن الخلوي. إن قدرتها العالية على الارتباط بكثير من الجزيئات داخل الخلية، تتيح لها أداء التفاعلات السريعة واللحظية الحاسمة في عمليات التعرف الجزيئي، وتنظيم المسارات الأيضية. للبروتينات غير المرتبة جوهريًا تأثيرات مهمة في الصحة والمرض، فهي تؤثر في تطور
السرطان وانتشاره، وفي
الأمراض التنكسية العصبية، وفي أمراض القلب والأوعية الدموية، وبناء عليه، فإنها تعد أهدافًا محتملة لاكتشاف أدوية وعلاجات جديدة مبتكرة.
تاريخ اكتشافها
يرجع تاريخ اكتشاف البروتينات غير المرتبة جوهريًا (IDPs)، إلى بدايات التجارب لتحديد بنية البروتينات في أوائل القرن العشرين وفي منتصفه، وقد شهد مجال تحديد بنية البروتين تقدمًا كبيرًا مع ظهور علم دراسة بلورات البروتين بالأشعة السينية (Protein X-ray crystallography). أدت هذه الجهود إلى حل أول هياكل للبروتينات، وهذه الهياكل بدت أنها تدعم فكرة أن بنية البروتين ثلاثية الأبعاد ثابتة وضرورية، لكي تؤدي وظائفها البيولوجية، وتفترض هذه الفكرة أن تسلسل الأحماض الأمينية لأي بروتين، يحدد بنيته ثلاثية الأبعاد، التي بدورها تحدد وظيفته. وفي عام 1950، تحدى فريد كاروش (1914-1994) هذه الفرضية، واقترح مفهوم "القدرة على التكيّف البنيوي" (configurational Adaptability). أشار كاروش إلى أنه على عكس البروتينات الأخرى كلها المعروفة في ذلك الوقت، أظهر بروتين ألبومين (Albumin) قدرة عالية جدًا على الارتباط بقوة وسرعة بكثير من الجزيئات الصغيرة ذات الأشكال المختلفة، والكارهة للماء وذات الشحنة السالبة (الأنيونية)، فاقترح أن لدى البروتينات تكوينات متعددة في مستوى الطاقة نفسه، ويمكنها أن تتبنى أشكالًا مختلفة عند ارتباطها مع جزيئات محددة[1] ألمحت هذه الفكرة إلى احتمال وجود بروتينات ذات هياكل ديناميكية ومرنة. علاوة على ذلك، عززت تجربة كريستيان آنفينسن (Christian Anfinsen، 1916-1995) في إعادة الطبيعة التلقائية لإنزيم ريبونيوكلياز أ (Ribonuclease A)[2]، التي منحته جائزة نوبل في الكيمياء عام 1972 (الشكل 1)، مفهوم أن البنية الثابتة ثلاثية الأبعاد للبروتين (الشكل الثلاثي، Tertiary structure)، تُشفَّر في شكله الأولي (Primary structure)، وهي بنية مستقرة في ظل الظروف الفيزيولوجية. أدى هذا الاكتشاف إلى تأسيس نظرية آنفينسن أو عقيدته (Anfinsen’s dogma)، وطُبقت في المقام الأول على البروتينات "المنظمة" ذات الهياكل المحددة[3].
مع تقدم التقنيات البيوكيميائية لتحديد بنية البروتينات، من خلال تقنيات الرنين المغناطيسي النووي (Nuclear magnetic resonance, NMR) والأشعة السينية، وتشتت الأشعة السينية ذات الزاوية الصغيرة (Small-angle X-ray scattering)، وازدواجية اللون الدائرية (Circular dichroism)، ونقل الطاقة برنين فورستر (Förster resonance energy transfer)، واجه العلماء كثيرًا من مناطق البروتين، التي لا يمكن تعيينها بدقة مثل غيرها، فعند تحليل بيانات الأشعة السينية لبلورات البروتين المختلفة، وجد العلماء أن ثمة مناطق تشغل مواقع متعددة، وليست محددة في خرائط كثافة الإلكترون، ما يشير إلى مرونتها الهيكلية والعشوائية في شكلها. وقد شهد العقد الأول من القرن الحادي والعشرين مزيدًا من التحليلات الكمية، والاكتشاف المتزايد بانتشار بروتينات غير مرتبة كغيرها[4]، واكتُشفت بروتينات غير مرتبة جوهريًا في الكائنات الحية[5] جميعها وفي الأمراض[6]. ومما يُذكر، أنه عبْر استخدام تقنيات الحوسبة والتنبؤ بالأشكال، فإنه من المتوقع أن البروتينات الموجودة في الطبيعة أكثر مرونة، وأقل استقرارا (في شكلها) من تلك الموجودة في
بنك بيانات البروتين {{بنك بيانات البروتين(PDB) : (Protein data bank) مستودع عالمي للبيانات البنيوية ثلاثية الأبعاد للجزيئات الحيوية الكبيرة، كالبروتينات والأحماض النووية ومعقداتها، ويعد موردًا أساسيًا لعلوم الأحياء والكيمياء الحيوية وتصميم الأدوية، إذ يوفر بيانات للباحثين مجانًا، وإن البيانات الموجودة فيه ناتجة من تجارب مخبرية، تتضمن تصوير البلورات بالأشعة السينية، وطيف الرنين المغناطيسي النووي، والمجهر الإلكتروني فائق البرودة.}}، كذلك فإن البروتينات الموجودة في
الخلايا حقيقية النوى(Eukaryotes)، فيها نسبة أكبر من الاضطراب الجوهري، من تلك الموجودة في
البكتيريا (Bacteria) أو العتائق (Archaea). ومن خلال هذه الاكتشافات، يعكس تاريخ البروتينات غير المرتبة جوهريًا تحولًا في التوجه العام للعلماء، من الالتزام الصارم بالنظرية التي أخذ عليها آنفينسن جائزة نوبل، إلى الاعتراف بأهمية مرونة نسبة مهمة من البروتينات وتعدد أشكالها، وقدرتها على التكيف في الوظائف البيولوجية وفي آليات المرض.
وجودها
الشكل[1]
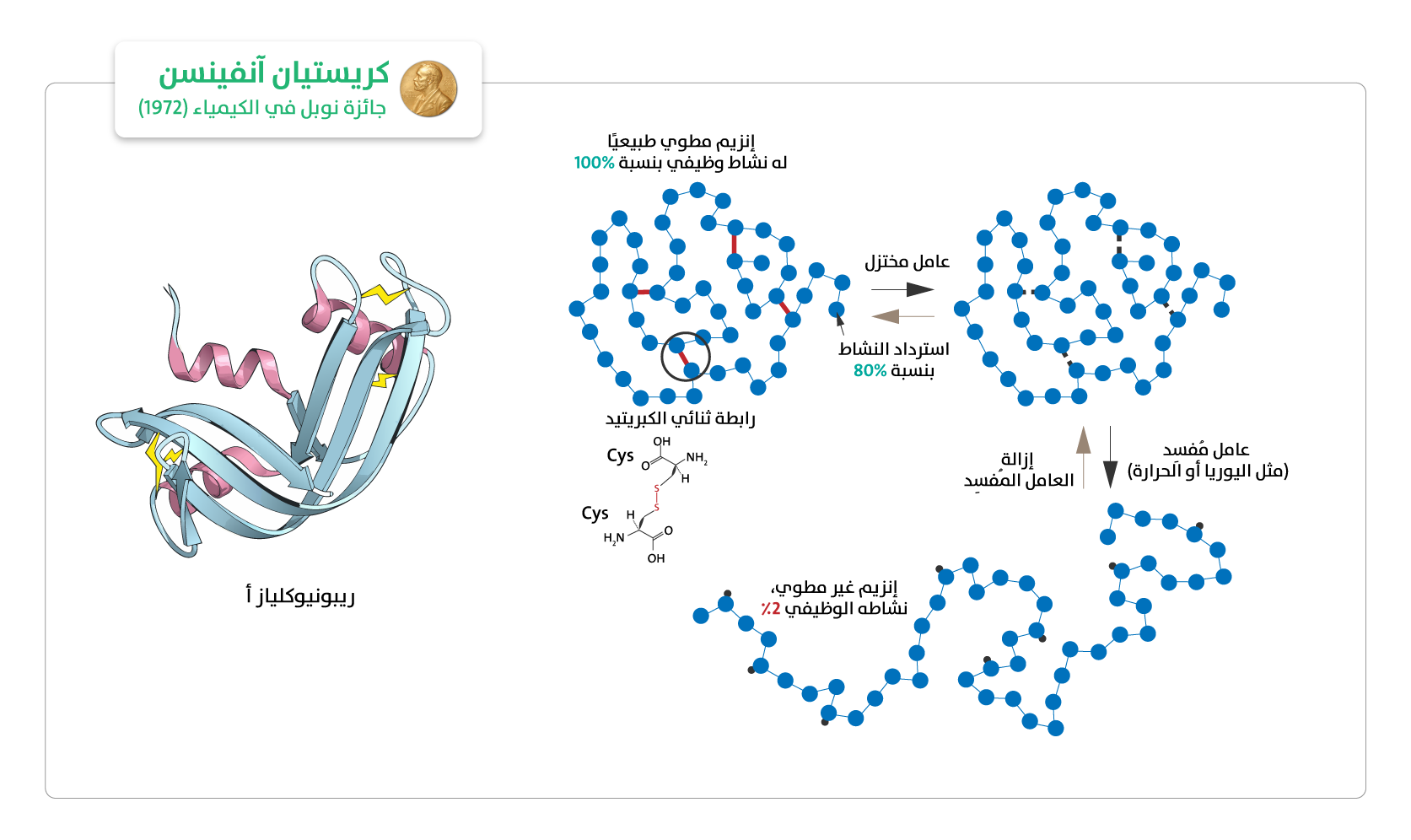 تجربة كريستيان آنفينسن التي حصل من خلالها على جائزج نوبل في الكيمياء عام 1972
تجربة كريستيان آنفينسن التي حصل من خلالها على جائزج نوبل في الكيمياء عام 1972
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
مع تطور برمجيات
المعلوماتية الحيوية (Bioinformatics)، أصبح بالإمكان التنبؤ بمدى انتشار البروتينات غير المرتبة، بالمقارنة بالبروتينات المعروفة هياكلها البنائية. ثمة كثير من البرمجيات التي أجمعت على أن البروتينات في الخلايا حقيقية النوى، أكثر اضطرابًا من بروتينات
الخلايا بدائية النوى (Prokaryotes)[7]. ووفقًا لتنبؤات برمجية DISOPRED2، وُجِدت أجزاء طويلة غير مرتبة تحتوي على أكثر من 30 وحدة
حمض أميني، في نحو 2 في المئة من بروتينات العتائق (Archaea)، و4.2 في المئة من بروتينات البكتيريا، و33 في المئة من بروتينات
الخلايا حقيقية النواة[8]. تشير هذه النتائج وغيرها، إلى أن هذه البروتينات أكثر شيوعًا مما كان مقدرًا سابقًا، وهي مكونات أساسية للعمليات الخلوية في الكائنات الحية المتنوعة جميعها، وبناء عليه، أضحت البروتينات غير المرتبة جوهريًا تعد من الأنواع الأساسية من البروتينات، بعكس ما كان يُنظر إليها سابقًا، فالبروتينات مرنة بصورة عامة، ولها درجات متفاوتة من المرونة بحسب نوع البروتين وهيكليته. تمثّل البروتينات غير المرتبة جوهريًا النهاية القصوى من طيف المرونة، إذ تُظهر بعض المجالات فيها (أو معظم شكل البروتين في عدد من الأحيان)، ميلًا كبيرًا للفوضوية وعدم انتظام الشكل. توجد البروتينات غير المرتبة جوهريًا بشكل واسع في مختلف الوظائف والأنظمة البيولوجية، وتنتشر بشكل خاص بين عائلات البروتين المشاركة في تنظيم
الكروماتين {{الكروماتين: (Chromatin) معقّد يتكون من الحمض النووي الريبي منقوص الأكسجين (DNA)، والبروتينات (ولا سيما بروتينات الهستون)، التي تغلف المادة الوراثية وتنظمها داخل النواة. يتكثف الكروماتين مُشكِّلًا الكروموسومات في أثناء انقسام الخلايا، وينفكّ عند حاجة الخلية لنسخ الحمض النووي. الوحدة التركيبية الأساسية للكروماتين تدعى النيوكليوسوم.}} ، وعمليات نسخ الحمض النووي (Transcription)، وعمليات
نقل الإشارة الخلوية (Signal transduction)[9]، إذ إن مرونتها الهيكلية قد تسهل الارتباطات الديناميكية والآليات التنظيمية الخاصة بهذه العمليات[10]،[11]. ولا يقتصر وجود البروتينات غير المرتبة جوهريًا في الوظائف الخلوية العادية، بل يمتد أيضًا إلى اشتراك بعضها بكثير من الأمراض أو ارتباطها بها، كالسرطان والسكري، واضطرابات الأعصاب والقلب والأوعية الدموية. في دراسة في جامعة كاليفورنيا/ سان دييغو، وجد الباحثون أن نحو 20 في المئة من الطفرات في مجالات الاضطراب الجوهري في البروتينات غير المرتبة جوهريًا، تؤدي إلى تحويل البروتين من عشوائي إلى مرتب ما يجعله مُمْرضًا[12]. إن ارتباط البروتينات غير المرتبة جوهريًا بالأمراض المختلفة، يؤكد أهميتها في النظم البيولوجية وصلتها بالحالات المرضية.
خصائصها الهيكلية
[الشكل2]
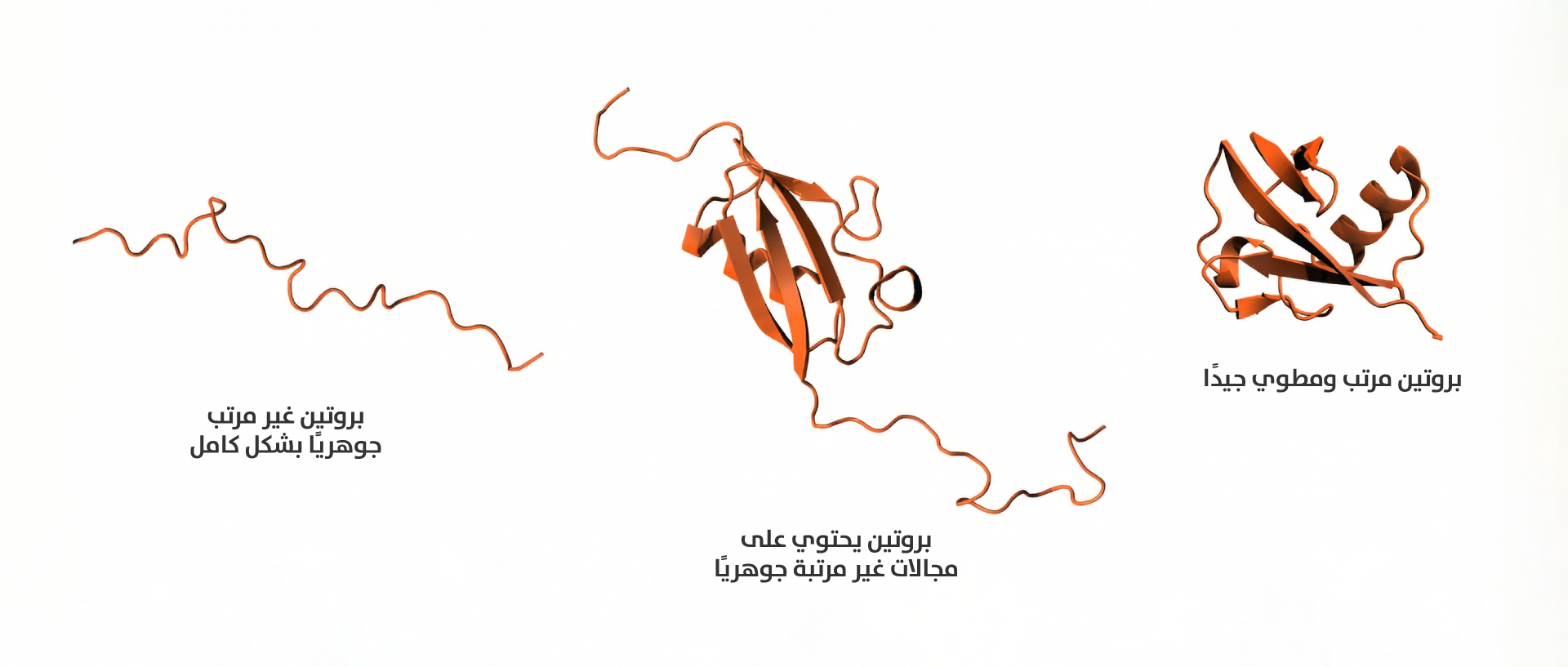 أنواع البروتينات غير المرتبة جوهريًا
أنواع البروتينات غير المرتبة جوهريًا
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل3]
-موجودة-الطرفين-الأميني-والكربوكسيلي.png) المرونة في بروتين سومو-1 (SUMO-1) موجودة الطرفين الأميني والكربوكسيلي، في حين يُظهر الجزء المركزي بنية مُرتبة نسبيًا
المرونة في بروتين سومو-1 (SUMO-1) موجودة الطرفين الأميني والكربوكسيلي، في حين يُظهر الجزء المركزي بنية مُرتبة نسبيًا
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
مع أن ثمة عددًا ملحوظًا من البروتينات المصنفة بأنها غير مرتبة جوهريًا في الكائنات الحية، إلا أن أقلية منها فقط تكون غير مرتبة بشكل كامل في حالتها الطبيعية، ومعظم هذه البروتينات فيها مجالات غير مرتبة (Intrinsically disordered regions, IDRs) داخل بروتين لديه هيكل ثلاثي الأبعاد واضح وجيد التنظيم. تندرج البروتينات التي تحتوي على مجالات غير مرتبة ضمن الفئة الأوسع للبروتينات غير المرتبة جوهريًا[13] (الشكل 2). تُظهِر البروتينات غير المرتبة جوهريًا قدرة هيكلية ملحوظة على التكيّف في خلايا الكائن الحي، فتتخذ هياكل وأشكالًا متنوعة اعتمادًا على الظروف الخلوية، ومن ثم، لديها مجموعة من الأشكال بينها توازن حركي[14] (الشكل 3)، ويرتبط هذا التنوع ارتباطًا وثيقًا بأدوارها الوظيفية.
يحدد تسلسل الأحماض الأمينية في البروتين نوع عدم ترتيب البروتين في طبيعته الخلوية ومداه، وتمتاز البروتينات غير المرتبة جوهريًا، بكمية منخفضة من الأحماض الأمينية الكبيرة الكارهة للماء، وبالمقابل، تحتوي على نسبة أعلى من الأحماض الأمينية القطبية والمشحونة، ما يسهل ارتباطها وتفاعلها بصورة جيدة مع الماء، فتكون أكثر مرونة وحركية. علاوة على ذلك، فإن وجود الأحماض الأمينية المشحونة يرفع من محصلة الشحنات على البروتين، ما يعزز الاضطراب الشكلي عن طريق التسبب في التنافر الكهروستاتيكي (Electrostatic repulsion) بين الأحماض الأمينية المشحونة بالشحنات نفسها[15]. إن هذا التنافر علاوة على عدم وجود أحماض أمينية غير قطبية بشكل كافٍ، يمنع تشكيل النواة الكارهة للماء (Hydrophobic core) اللازمة لطي
البروتينات الكروية (Globular proteins) المستقرة شكليًا. في بعض الحالات، توجد تجمعات كارهة للماء ضمن التسلسلات غير المرتبة، وتوفر هذه التجمعات أدلة عن المناطق والمجالات داخل البروتين، التي تخضع للطي الجزئي أو الكلي، وأيضًا لها علاقة بالارتباط مع الجزيئات الأخرى، وهو أمر بالغ الأهمية لتبيان أدوارها البيولوجية. وفي حين أن البروتينات المستقرة ذات الهياكل المحددة لها أشكال ثانوية (Secondary structure) محددة، وبين أحماضها الأمينية توجد مجموعة واحدة من
زوايا راماشاندران {{زوايا راماشاندران (فاي φ، وساي ψ): (Ramachandran angles) تصف دوران روابط العمود الفقري الببتيدي حول الروابط بين النيتروجين والكربون ألفا ((φ، وبين الكربون ألفا والكربون ((ψ في البروتينات. تحدد هذه الزوايا البنية الثانوية (مثل: لولب ألفا، وصفائح بيتا المُتثنِّية)، وتُعرض هذه الزوايا في مخطط راماشاندران، الذي يُقيِّم هندسة البروتين ويُثبِّت صحة البنى ثلاثية الأبعاد، من خلال تحديد التوافقات الفراغية المسموح بها وغير المسموح بها.}} تظهر كثير من البروتينات غير المرتبة مناطق تخلو من البنية الثانوية المنتظمة، التي تسمى المناطق المرنة. تتضمن البروتينات غير المرتبة جوهريًا مجموعات متعددة من زوايا راماشاندران، ما يؤكد طبيعتها الديناميكية والمرنة[16]، وتختلف هذه المرونة في البروتينات غير المرتبة جوهريًا عن تلك الموجودة في البروتينات المستقرة شكليًا، بأن البروتينات غير المرتبة لها كثير من الأشكال الأصلية التي تكون في حالة توازن بينها، في حين أن البروتينات المستقرة لها شكل أو بضعة أشكال أصلية، ينتقل البروتين بينها لإحلال التوازن.
علاوة على خصائصها الهيكلية، تتميز البروتينات غير المرتبة جوهريًا بقدرتها العالية على التكيّف، لتؤدي إلى مجموعة متنوعة من أوضاع الارتباط (Binding modes)، فنظرًا لافتقارها إلى بنية صلبة وأشكال محددة، تمتلك البروتينات غير المرتبة جوهريًا قدرة كبيرة على تعديل أشكالها، لتوائم بنية شريكها في الارتباط (Binding partner)[17]. إن المرونة غير المقيدة تقريبًا تسمح للبروتينات غير المرتبة جوهريًا بتكوين عدد كبير من الارتباطات غير المتوقعة، التي لا يمكن تحقيقها بوساطة البروتينات المرتبة. وبناء عليه، فإن البروتينات غير المرتبة جوهريًا قادرة على تكوين معقدات ديناميكية أو عشوائية، أو غير مرتبة مع جزيئات حيوية مختلفة مثل البروتينات الأخرى (سواء المرتبة أم غير المرتبة)، أو الأحماض النووية أو
الأغشية البيولوجية أو الجزيئات الصغيرة. تتميز هذه المعقدات بوجود مواقع ربط متعددة منخفضة الألفة (Multiple low-affinity binding sites)، ما يتيح للبروتينات غير المرتبة جوهريًا التفاعل مع شركاء متنوعين بطريقة ديناميكية[18]. إن وجود عدد كبير من مواقع الارتباط المماثلة، والطبيعة المرنة والديناميكية للبروتينات غير المرتبة جوهريًا، يخلق وضعًا فريدًا، إذ يمكن لأي موقع ارتباط على بروتين غير مرتب جوهريًا، أن يتفاعل مع أي موقع ربط لشريكه باحتمالات متساوية تقريبًا. وبما أن الارتباطات ضعيفة ومنخفضة الألفة داخل هذه المعقّدات، فإن كل ارتباط يمكن عدّه عابرًا وقابلًا للكسر بسهولة، ومن ثم، تستكشف البروتينات غير المرتبة جوهريًا، وتغير مواقع الارتباط المتعددة الخاصة به بشكل مستمر، في أثناء فحص مواقع الارتباط مع شركائها. إن هذه التفاعلات الديناميكية والقدرة على التكيّف مهمة في العمليات الخلوية، إذ تكون التفاعلات السريعة والمتعددة الاستخدامات ضرورية للإشارات والتنظيم والوظائف البيولوجية الأخرى.
وظائفها
تعد البروتينات غير المرتبة جوهريًا جزيئات محورية في مختلف العمليات البيولوجية، وتظهر خصائص تميزها عن البروتينات ذات الأشكال المنتظمة. تُنظَّم كثير من الظواهر والعمليات البيولوجية مثل
التنظيم التفارغي {{التنظيمالتفارغي: (Allosteric regulation) هو عملية تؤدي للتحكم في نشاط الإنزيم، من خلال ارتباط جزيء بموقع على الإنزيم غير الموقع النشط. يُحفِّز هذا الارتباط تغييرات تكوينية تُعزِّز وظيفة الإنزيم (عند ارتباط مُنشِّط) أو تُثبِّطها (عندما يرتبط جزيء مُثبِّط). يُتيح التنظيم التفارغي التحكّم الدقيق بعمليات الأيض وتثبيط التغذية الراجعة، والتأثيرات التعاونية في البروتينات، كما في الهيموغلوبين والبروتينات التنظيمية.}} للبروتينات، وتحفيز
الإنزيمات[19] والإشارات الخلوية، وعمليات نسخ الحمض النووي، وإعادة تشكيل الكروماتين، وغيرها من الوظائف الخلوية، من خلال المجالات غير المرتبة التي لها ديناميكية ومرونة عاليتان[20]. وبسبب مرونتها الهيكلية التي تتيح لها حرية التغييرات الشكلية استجابة للإشارات الخلوية، تعمل البروتينات غير المرتبة جوهريًا بوصفها مفاتيح أو مُعدِّلات جزيئية (molecular switches)، في تنشيط مسارات الإشارات المختلفة أو تثبيطها. علاوة على ذلك، فإن
الجينات التي تطورت حديثًا (de novo genes)، تميل إلى إظهار مستويات أعلى من الاضطراب، ما يعكس الطبيعة الديناميكية والأهمية التطورية للبروتينات غير المرتبة جوهريًا في النظم البيولوجية[21]. تاليًا بعض من وظائف هذه البروتينات:
- 1. الارتباطات المتنوعة والمختلفة: تُظهر البروتينات غير المرتبة جوهريًا درجة عالية من القدرة على الارتباط والتفاعل ديناميكيًا مع مجموعة واسعة من الشركاء. ويسهّل عدم وجود شكل محدد لهذه البروتينات، على أداء هذه التفاعلات السريعة والعابرة مع جزيئات مختلفة، مثل البروتينات الأخرى والأحماض النووية والدهون والجزيئات الصغيرة.
- 2. الأدوار التنظيمية في مسارات الإشارة: تعمل البروتينات غير المرتبة جوهريًا مُعدِّلات جزيئية في تنظيم مسارات الإشارات المختلفة، وتسمح مرونتها الهيكلية لها بالخضوع لتغييرات تكوينية استجابة للإشارات الخلوية، ما يؤثر في الأحداث النهائية لهذه الإشارة، التي تؤدي إلى تغييرات في
التعبير الجيني، والاستجابة الخلوية وقرارات الخلية المصيرية.
- 3. تفاعلات البروتين-بروتين: تتوسط البروتينات غير المرتبة جوهريًا في
تفاعلات البروتين-بروتين {{تفاعلات البروتين-بروتين: (protein-protein interactions) هي اتصالات فيزيائية بين بروتينَين أو أكثر، تتم بوساطة روابط غير تساهمية. تُعد هذه التفاعلات أساسية في الإشارات الخلوية، والنشاط الإنزيمي، والدعم الهيكلي، والعمليات الخلوية المختلفة. ويمكن أن تكون تفاعلات البروتين-البروتين مؤقتة أو ثابتة، ويرتبط اختلال تنظيمها بالأمراض المختلفة.}} ، ما يسهم في تكوين معقدات البروتينات المتعددة، وتشكيل الشبكات التنظيمية المختلفة. تتيح مرونتها ارتباطات سريعة وعابرة وقابلة للعكس مع شركاء متعددين، ما يؤدي للحفاظ على
الاستتباب البروتيني {{الاستتباب البروتيني: (proteostasis) أو التوازن البروتيني، وهو عملية خلوية تحافظ على توازن البروتين، من خلال تخليقه وطيه ونقله وتحلله. تضمن هذه العملية وظائف البروتينات وصحة الخلايا. تؤدي الاضطرابات في الاستتباب البروتيني إلى وجود تكتلات غير طبيعية، ترتبط بأمراض تنكسية عصبية مثل ألزهايمر.}}، والخلوي {{الاستتباب الخلوي: (homeostasis) أو التوازن الخلوي، وهو العملية البيولوجية التي تحافظ بها الكائنات الحية على استقرارها الداخلي رغم التغيرات الخارجية، ويشمل آليات التغذية الراجعة التي تنظم درجة الحرارة ودرجة الحموضة، وتوازن السوائل ومستويات العناصر الغذائية. تُنسق الأنظمة الرئيسة في الجسم استجاباتها للتغيرات التي قد تؤدي إلى المرض، ما يضمن وظائف خلوية مثالية.}}.
- 4. تكويم البروتين المرضي: على الرغم من تنوع وظائفها الحيوية، فإن البروتينات غير المرتبة جوهريًا لها أدوار مرضية أيضًا، فيمكن أن يؤدي اختلال البروتينات غير المرتبة جوهريًا وتكويمها، إلى إنشاء مجمعات بروتينية غير قابلة للذوبان في الوسط المائي في الخلية، ترتبط بالاضطرابات التنكسية العصبية مثل مرض
ألزهايمر (Alzheimer's) ومرض باركنسون {{مرضباركنسون: (Parkinson's disease) ويطلق عيه أيضًا مرض الشلل الرعاش، هو فقدان المريض للقدرة على التحكم في وتنسيق عمل العضلات الهيكلية. يحدث ذلك بسبب تلف تدريجي، ومن ثم موت الخلايا العصبية المفرزة للناقل العصبي الدوبامين في منطقة المادة السوداء، التي هي جزء من العقد القاعدية في الدماغ والموجودة قرب مركز الدماغ.}}. إن التوازن الدقيق بين المرونة الوظيفية للبروتينات غير المرتبة جوهريًا والعواقب المرضية لها، محط دراسات بيوكيميائية كثيرة في هذا المجال.
جوانبها الهيكلية والوظيفية
أولًا: تحتوي معظم البروتينات الكروية المستقرة شكليًا على روابط مرنة (Flexible linkers) بين مجالات مختلفة، وتتكون هذه الروابط المرنة في العادة من مناطق غير مرتبة، وتتميز باختلاف طولها من بروتين لآخر، وبوفرة الأحماض الأمينية القطبية غير المشحونة. تمكِّن هذه الروابط المرنة المجالات البروتينية من الالتواء والدوران بحريّة، ما يسهل ربط الجزيئات الشريكة على البروتين. كذلك تسمح للجزيئات الشريكة بإحداث تغييرات شكلية واسعة النطاق عبر عمليات التفارغ، ما يسهم في تنظيم تفاعلات البروتين والعمليات الخلوية المرتبطة به[22].
ثانيًا: في بعض البروتينات غير المرتبة جوهريًا، توجد تسلسلات خطية فيها ما بين 3 إلى 10 أحماض أمينية، تسمى الطوابع البنائية الخطيّة القصيرة (Short linear motifs)، وهي شرائح قصيرة مضطربة من البروتينات التي تتوسط التفاعلات الوظيفية مع الجزيئات الحيوية الأخرى. وقد تُنُبِّئ بوجود ما يقارب المليون منها في البروتينات البشرية، ولكن لم يُستكشَف سوى جزء صغير منها بالتفصيل[23]. تنظم هذه الطوابع الخلايا بوساطة التحكم في شكل الخلية وتوطين البروتينات فيها، وتنظيم دوران البروتين واستتبابه. ولهذه الطوابع أهمية في بعض الأمراض أيضًا، إذ تنتشر البروتينات غير المرتبة جوهريًا بشكل عام، والطوابع البنائية الخطية القصيرة بشكل خاص، في
ڤيروساتالحمض النووي الريبي، ما يتيح الارتباط الفعال والتلاعب ببروتينات الخلية المضيفة، لذا لها أدوار في استراتيجيات العدوى الڤيروسية، إذ تحاكي كثير من الڤيروسات الطوابع البنائية الخطية القصيرة، لتستطيع إصابة الخلايا والتكاثر فيها[24].
ثالثًا: الطوابع البنائية المنظَّمة سابقًا (Pre-structured motifs): عناصر هيكلية ثانوية توجد في بعض البروتينات غير المرتبة جوهريًا، وهي غير مرتبطة بالجزيء المستهدف، التي تصبح هياكل ثانوية مستقرة عند الارتباط به، وتعمل هذه العناصر بوصفها مواقع نشطة مفترضة في البروتينات غير المرتبة جوهريًا. تسهّل عملية الربط المقترنة بطيّ بعض البروتينات غير المرتبة جوهريًا، الانتقالَ إلى الحالات المنظمة عند ربط الجزيء المستهدف، وعلاوة على ذلك، يمكن للمناطق غير المرتبة أن تعمل بوصفها مفاتيح جزيئية، تتحول إلى نطاقات مرتبة عند ارتباط الجزيئات، مثل ارتباط الأحماض النووية. إن قدرة البروتينات غير المرتبة جوهريًا على الارتباط وأداء أدوارها البيولوجية، تتحدى فكرة أن الاستقرار في البروتينات هو دائمًا الشرط الأساسي للوظيفة البيولوجية[25].
أمثلة
تاليًا بعض أبرز البروتينات غير المرتبة جوهريًا، المعروفة في خلايا الإنسان:
بروتين بي 53
[الشكل4]
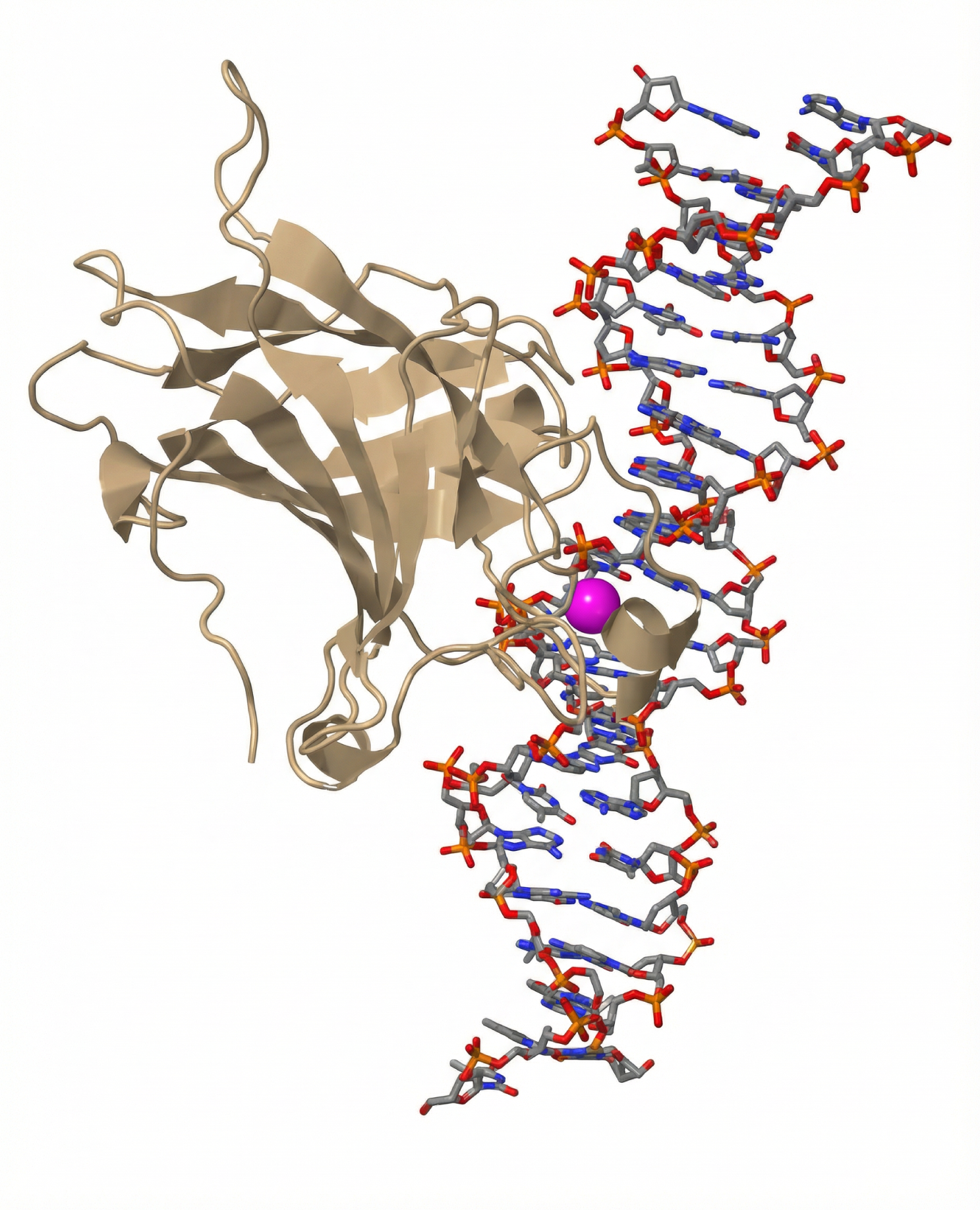 ارتباط بروتين بي 53 مع جزيء من الحمض النووي (DNA)
ارتباط بروتين بي 53 مع جزيء من الحمض النووي (DNA)
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
بروتين بي 53 (p53) هو منظّم مهم لـدورة حياة الخلية، وله أدوار أساسية في
إصلاح الحمض النووي، وبناء عليه، يكنّى بحارس الجينوم، وهو بروتين
كابت للورم (Tumor suppressor). يجسّد هذا البروتين أهمية عدم الترتيب الداخلي في الوظيفة الجزيئية، فعلى عكس كثير من البروتينات جيدة التنظيم، يفتقر البروتين بي53 بنية محددة ثلاثية الأبعاد، ويحتوي على عدد من المجالات غير المرتبة، ما يسمح له بتبني عدد كبير من الأشكال اعتمادًا على شركائه في الربط. تتيح هذه المرونة الارتباط والتفاعل مع الحمض النووي والبروتينات الأخرى والعوامل الخلوية المختلفة، بطريقة ديناميكية للغاية (الشكل 4)، ما يسهّل أدواره في تنشيط
نسخ الحمض النووي وإصلاحه، وفي حالات عدم القدرة على الإصلاح، يسهل دوره في تحفيز بداية الاستماتة الخلوية (موت الخلايا المبرمج، Apoptosis) وتثبيط الورم. يعد عدم وجود بنية ثابتة في هذا البروتين أمرًا ضروريًا لوظيفته، لأنه يسمح بالاستجابات السريعة للضغط والتلف الخلوي، وعلى الرغم من عدم وجود بنية مستقرة، فإن المناطق المضطربة في بي 53، تحتوي على طوابع بنائية وظيفية، ومجالات ارتباط محددة للربط مع الجزيئات الشريكة، وتعد هذه المناطق المضطربة ضرورية لتنسيق العمليات الخلوية المعقدة، فمن خلالها تتجمع المعقدات متعددة البروتينات، المشارِكة في
إصلاح الحمض النووي وموت الخلايا المبرمج[26]. يمكن أن تؤدي الطفرات في بي 53 أو التغيرات في مناطقه المضطربة، إلى نمو الخلايا غير المنضبط وتكوين الأورام.
ألفا-سينوكلين
ألفا-سينوكلين (α-Synuclein) بروتين ذائب متوفر بكثرة في
الخلايا العصبية (الشكل 5)، يفتقر إلى بنية محددة في حالته الطبيعية، إذ يوجد بوصفه مجموعة من الأشكال بدرجات متفاوتة من عدم الترتيب[27]. تعد الطبيعة الديناميكية وغير المرتبة لهذا البروتين ضرورية لوظائفه في
الخلايا العصبية، فيرتبط مع
الأغشية الخلوية وحويصلات الشق التشابكي {{حويصلات الشق التشابكي: (synaptic vesicles) إفرازات صغيرة محاطة بغشاء، تفرز من جهاز غولجي من الخلية العصبية الأولى، وتوجد في نهاية محورها عند مكان ارتباطها بالخلية التالية، وتحتوي على الناقل العصبي الذي ينطلق من تلك الخلية عند وصول النبضة العصبية إلى نهايتها، فيؤثر على الخلية التالية.}}، وبروتينات أخرى للإسهام في إطلاق
الناقل العصبي {{الناقلالعصبي: (neurotransmitter) مادة كيميائية مخزنة في حويصلات الشق التشابكي للخلايا العصبية، تنطلق هذه المادة من الخلية العصبية عند وصول النبضة العصبية من الخلية الأولى، وترتبط بمستقبِلات تتأثر بها فقط، وتسبب تغييرًا في الجهد الكهربي لغشاء الخلية التالية. يتكسر الناقل العصبي بعد ارتباطه بالمستقبِل، أو يُعاد امتصاصه بوساطة الخلايا الدبقية أو الخلية الأولى ليعاد استخدامه.}}، ووظائف
الشقوق التشابكية {{الشقالتشابكي: (synapses) هو المنطقة التي تتصل بها الخلية العصبية بالخلية التالية، وهي فراغ صغير جدًا (أصغر من الفراغ بين الخلايا العادية). يشمل الشق التشابكي كلًا من نهاية محور الخلية العصبية المؤثِّرة (الأولى)، والجزء المقابل من الخلية المتأثرة (الثانية)، التي تمكن أن تكون خلية عصبية أو عضلية أو غدية، والفراغ بينهما.}}. عندما يتعرض ألفا-سينوكلين لخلل في الطي، يتكتّل ويتجمّع مشكّلًا جزيئات بروتينية سامة، تسهم في إحداث اختلال في
الخلايا العصبية، مؤدية إلى
التنكّس العصبي {{التنكسالعصبي: (neurodegeneration) يشير إلى بعض الأمراض التي تصيب الجهاز العصبي، بسبب موت الخلايا العصبية في أحد أجزاء الجهاز العصبي المركزي. يسبب موت الخلايا العصبية فقدان الوظيفة، التي كان من المفترض أن يؤديها ذلك المركز أو الجزء من الجهاز العصبي المركزي، والتي قد تكون وظيفة حركية أو تحليلية أو إدراكية.}}.
[الشكل5]
 ألفا-سينوكلين
ألفا-سينوكلين
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تتورط المعقّدات الناجمة عن تكتّلات ألفا-سينوكلين في إحداث مرض باركنسون، وهو أحد
الأمراض التنكسيّة العصبية {{الأمراضالتنكسيةالعصبية: (neurodegenerative diseases) مجموعة من الأمراض التي تصيب الإنسان بسبب تلف تدريجي، أو موت لخلايا عصبية معينة في الجهاز العصبي المركزي، ما يؤدي إلى فقدان الدماغ وظيفة معينة كانت تؤديها تلك الخلايا. تعتمد الوظيفة المفقودة على أي مركز من مراكز الدماغ الذي تلفت وماتت خلاياه.}}. إن الأجزاء غير المرتبة جوهريًا من ألفا-سينوكلين، تتعرّض لتعديلات لاحقة للترجمة (post-translational modifications)، تكون خاطئة أو مختلة، فتؤدي إلى تكتّل البروتين وتجميعه في ألياف (fibrils) غير قابلة للذوبان، وأجسام ليوي {{أجسامليوي: (Lewy bodies) اكتشف العالم الألماني فريدريك هنري ليوي في عام 1912، وجود تراكم غير طبيعي لبعض البروتينات (مثل بروتين ألفا-سينوكلين) داخل الخلايا العصبية، للمصابين ببعض أنواع الأمراض التنكسية العصبية مثل مرض باركنسون، سميت هذه التراكمات بأجسام ليوي نسبة إليه. وتؤدي هذه التراكمات غير الطبيعية إلى تعطيل وظائف هذه الخلايا أو موتها.}} المميّزة لمرض باركنسون. إن دراسة الديناميكيات الهيكلية لهذا البروتين، وآليات انتقاله من بروتين وظيفي غير مرتب جوهريًا إلى كيان ممرض، أمر أساسي لتطوير استراتيجيات علاجية تهدف إلى منع
التنكس العصبي في
مرض باركنسون، والاضطرابات الأخرى ذات الصلة[28].
بروتين تاو
[الشكل6]
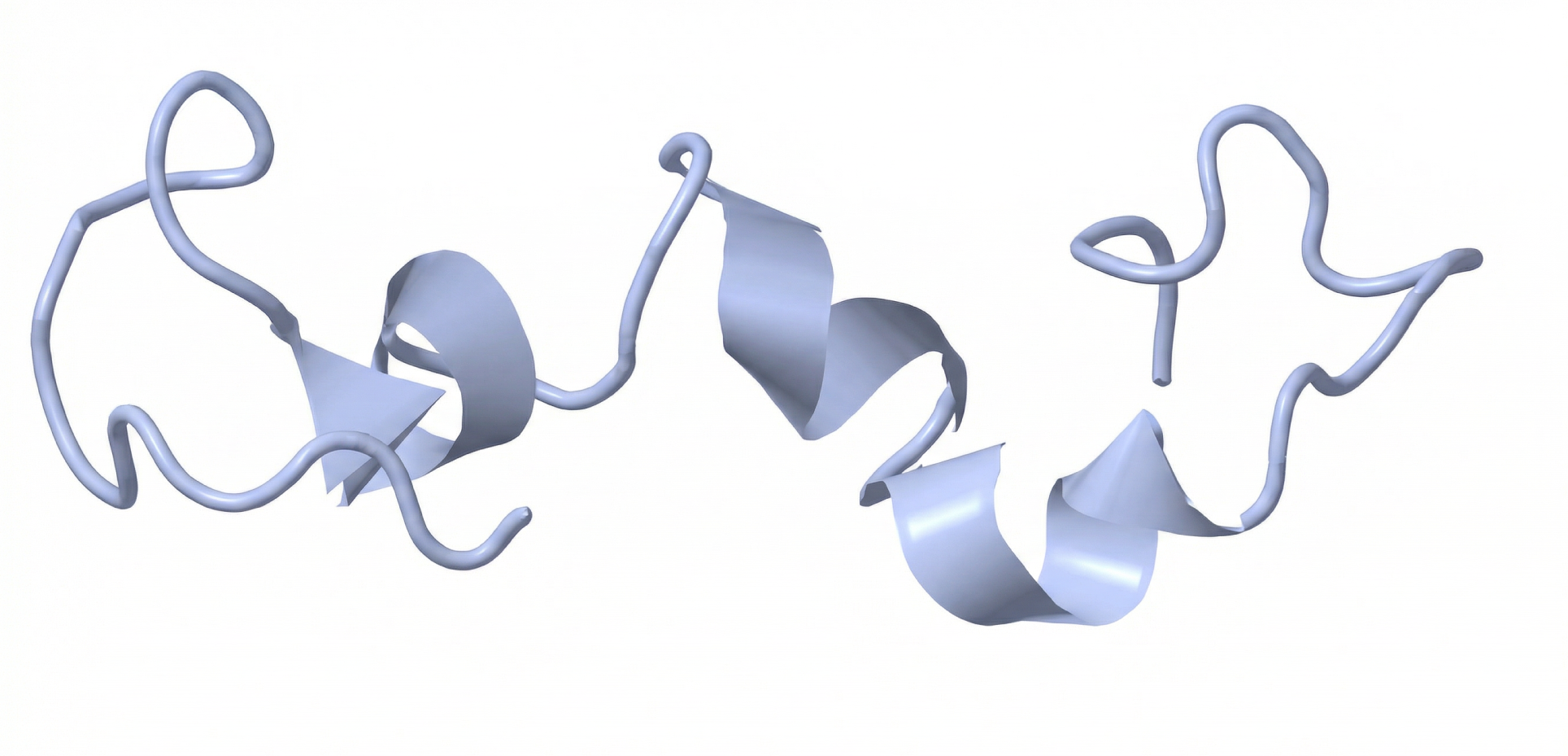 بروتين تاو
بروتين تاو
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل7]
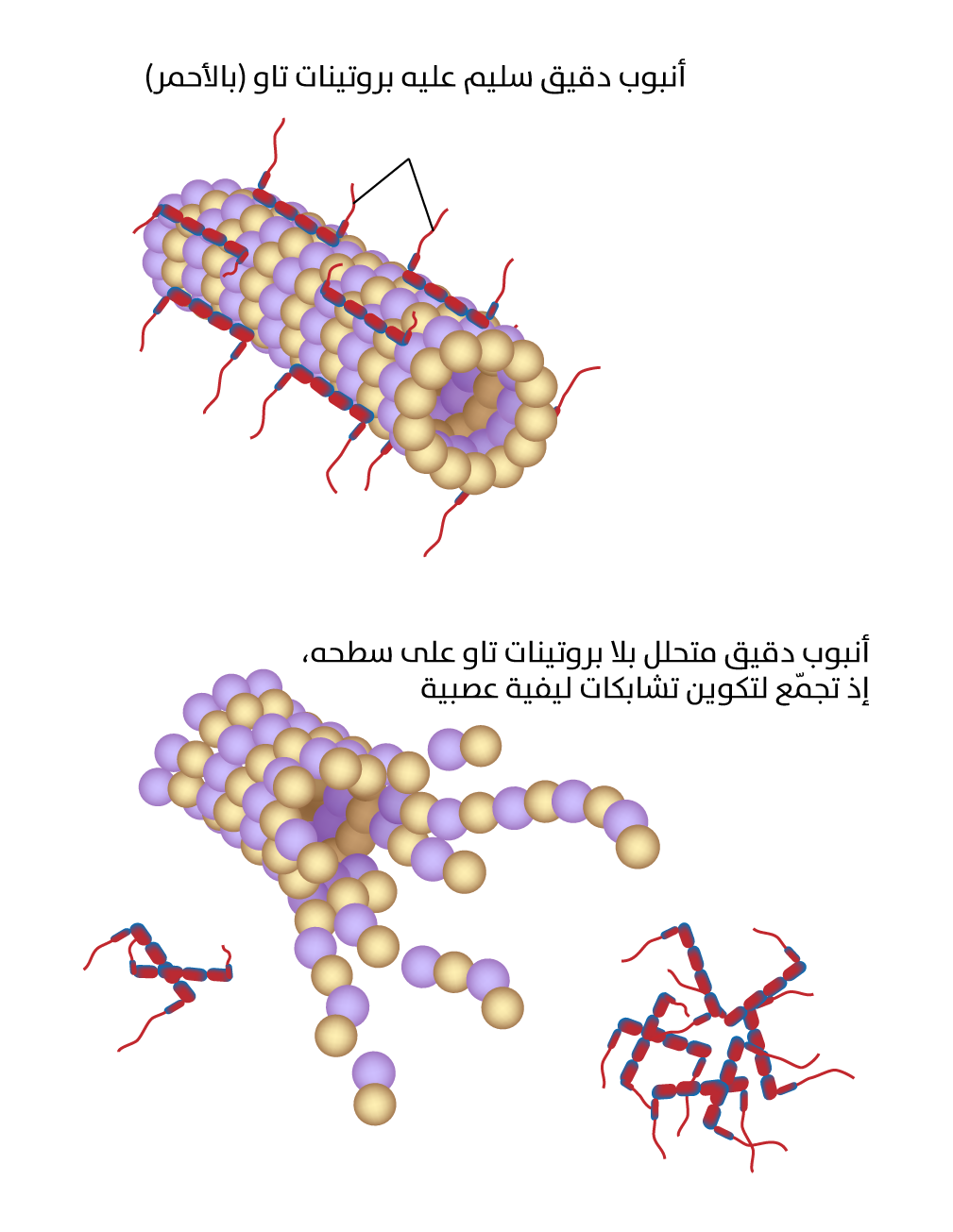 يتجمع بروتين تاو على الأنيبيبات الدقيقة ليمنحها بنية صلبة واستقرارًا. أما بروتين تاو المطوي بشكل خاطئ فيشكل تشابكات تاو، ثم تشابكات ليفية عصبية، ما يؤدي إلى عدم استقرار الأنيبيبات الدقيقة وتفككها
يتجمع بروتين تاو على الأنيبيبات الدقيقة ليمنحها بنية صلبة واستقرارًا. أما بروتين تاو المطوي بشكل خاطئ فيشكل تشابكات تاو، ثم تشابكات ليفية عصبية، ما يؤدي إلى عدم استقرار الأنيبيبات الدقيقة وتفككها
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يوجد بروتين تاو (Tau) بشكل أساسي في
الخلايا العصبية (الشكل 6)، ويحافظ على ثبات
الأنيبيبات الدقيقة {{الأنابيبالدقيقة: (microtubules) أو الأنيبيبات الدقيقة، وهي تشكيلات بروتينية مجوفة تتكون من بروتين التوبيولين، وهي واحدة من ثلاثة مكونات للهيكل الخلوي. تُوفر هذه الأنابيب دعمًا هيكليًا، وتُساعد الخلايا على الانقسام (فالخيوط المغزلية أنابيب دقيقة)، وتعمل بوصفها مسارات للنقل داخل الخلايا. يُنظم تحللُ مركب غوانوسين ثلاثي الفوسفات عدمَ استقرارها الديناميكي، ما يؤدي إلى تفككها. ويعتمد ثباتها أيضًا على وجود بعض البروتينات المرتبطة بالأنابيب الدقيقة.}}، التي هي جزء من
الهيكل الخلوي {{الهيكلالخلوي: (cytoskeleton) شبكة من الخيوط البروتينية (الأنابيب الدقيقة، والخُيَيْطيَّات، والخيوط المتوسطة)، التي تحافظ على شكل الخلية وتُسهل حركتها، وتُنظم حركة العضيّات ووظائفها. كذلك تُمكّن من المقاومة الميكانيكية والنقل داخل الخلايا وانقسام الخلايا. تُحرك عمليات إعادة الترتيب الديناميكية عمليات مثل هجرة الخلايا وانقسامها، وانتقال الإشارات.}}. وبناء عليه، ينظّم تاو ديناميكيات الهيكل الخلوي، ومن ثم وظائف
الخلايا العصبية كلها. يفتقر تاو إلى بنية محددة، ويُظهر اضطرابًا جوهريًا في حالته الأصلية، يسمح هذا الاضطراب الجوهري لتاو بالتفاعل ديناميكيًا مع
الأنيبيبات الدقيقة، ما يعزز استقرارها ويسهل
النقل المحوري السريع {{النقلالمحوريالسريع: (fast axonal transport) الحركة السريعة المعتمدة على البروتينات الحركية للحويصلات والعضيات، على طول الأنيبيبات الدقيقة في الخلايا العصبية. تضمن هذه الحركة السريعة اتصالًا فعالًا بين المشابك العصبية والجسم الخلوي، وهو أمر بالغ الأهمية لوظيفة الخلايا العصبية وبقائها.}}. في
الأمراض التنكسية العصبية مثل مرض ألزهايمر، يخضع تاو لعمليات
فسفرة {{الفسفرة: (phosphorylation) هي إضافة مجموعة فوسفات إلى جزيء (مثل البروتين أو الدهون)، بوساطة بروتينات الكيناز، ما يُغيّر وظيفتها في الغالب. في البروتينات، تصنف الفسفرة بأنها تعديل لاحق للترجمة، وتُنظّم نشاط الإنزيمات وانتقال الإشارات ومعظم العمليات الخلوية. تُؤدي إنزيمات الفوسفاتاز عمليات إزالة الفوسفات.}} تؤدي إلى تجمّعات غير طبيعية، ما يؤدي إلى تكوين تشابكات ليفية عصبية (neurofibrillary tangles) (الشكل 7). كذلك تحتوي المناطق المضطربة في تاو على مواقع ربط متعددة، تتفاعل مع كثير من المكونات الخلوية المختلفة كالبروتينات وجزيئات الإشارة، هذه الارتباطات ديناميكية للغاية وعابرة، ما يسمح لتاو بتعديل العمليات الخلوية مثل
اللدونة التشابكية {{اللدونة التشابكية (أو المرونة المشبكية): (synaptic plasticity) هي قدرة الشق التشابكي الموجود بين الخلايا العصبية على زيادة قوة الإشارة العصبية أو إضعفها مع مرور الوقت، استجابة لنشاط معين. تعد هذه العملية الديناميكية جزءًا أساسيًا في عمليات التعلم وحفظ المعلومات في مراكز الذاكرة، علاوة على أهميتها في وظائف الدماغ بشكل عام، ما يسمح للدماغ بالتكيف مع التجارب وإعادة تنظيم الدوائر العصبية.}}، وتنظيم الهيكل الخلوي. لذا، تعتمد الوظيفة الطبيعية للخلايا العصبية على أن تاو بروتين غير مرتب جوهريًا، لأن أي خلل في شكله المرن، يمكن أن يؤدي إلى آثار ضارة في سلامة الخلايا العصبية ويسهم في
التنكس العصبي[29].
عوامل النسخ وبروتينات الإشارة
تحتوي كثير من
عوامل النسخ {{عواملالنسخ: هي بروتينات ترتبط بالحمض النووي الريبي منقوص الأكسجين (DNA)، لتنظيم التعبير الجيني، عن طريق تعزيز استقطاب بوليميراز الحمض النووي الريبي (RNA) أو تثبيطه، وغيرها من الآليات. تحتوي هذه العوامل على مجالات ربط الحمض النووي الريبي (مثل: أصابع الزنك) ومجالات التنشيط/ التثبيط.}} وبروتينات الإشارة على مناطق غير مرتبة لها أدوار محورية في تنظيم الجينات والإشارات الخلوية. يساعد افتقار هذه البروتينات لبنية محددة التفاعل مع الحمض النووي والبروتينات الأخرى والعوامل المساعدة بطريقة مرنة وسريعة مطلوبة، في التنظيم الدقيق للتعبير الجيني ومسارات نقل الإشارة. فمثلًا، هاكس 1 (HAX1)، بروتين صغير نسبيًا وغير مرتب جوهريًا، له علاقة مباشرة في كثير من الوظائف الخلوية[30]، مثل تنظيم
موت الخلايا المبرمج، وهجرة الخلايا (Cell migration)، والاستتباب البروتيني، وتولد الأوعية الدموية {{تولدالأوعيةالدموية: (Angiogenesis) عملية أساسية في النمو، إذ يبني الجسم أوعية دموية جديدة، لتمد الأنسجة والخلايا الجديدة بما يلزمها للاستمرار بالحياة. يسهم في البدء بهذا التخليق الأنسجة التي ينقص لديها الأكسجين، وسرعة هذه العملية مرتبطة بالانتشار السرطاني.}}، والبلعمة الذاتية (Autophagy) والترجمة[31].
غالبًا ما تحتوي المناطق المضطربة في عوامل النسخ على طوابع بنائية ومجالات وظيفية، ترتبط مع العناصر التنظيمية (Regulatory elements) في الحمض النووي والبروتينات الأخرى، المشارِكة في تنظيم عمليات النسخ والترجمة[32]. وكذلك، فإن المناطق غير المحددة شكليًا في بروتينات الإشارة، تسهّل التفاعلات بين البروتين والبروتين، وتساعد في نقل الإشارة، وتسمح الطبيعة الديناميكية والمرنة لهذه المناطق المضطربة لعوامل النسخ وبروتينات الإشارة، بالاستجابة بسرعة للإشارات الخلوية والتغيرات البيئية.
البروتينات غير المرتبة جوهريًا في الصحة والمرض
البروتينات غير المرتبة جوهريًا لها تأثيرات عميقة في الصحة والمرض، ما يؤثر في مجموعة واسعة من العمليات الفيزيولوجية والفيزيولوجية المرضية. إن البروتينات غير المرتبة جوهريًا، تتسبب في
الأمراض التنكسية العصبية، مثل ألزهايمر وباركنسون، وأمراض هنتنغتون {{أمراضهنتنغتون: يتسبب هذا المرض بتلف خلايا عصبية، تؤدي إلى تدهور الصحة العقلية، بما في ذلك القدرة على الحركة والوعي، وهو ناتج من طفرة تحدث في أحد جينات الكروموسوم 4 المسؤول عن إنتاج بروتين هنتنغتين (Huntingtin) ما يتسبب في تدهور وضع الخلايا المكونة للعقد القاعدية في الدماغ.}}، من خلال اختلال أشكال البروتينات وتراكمها في خلايا الدماغ. وبالمثل، في أمراض السرطان، تعد البروتينات غير المرتبة جوهريًا ضرورية لتطور المرض، من خلال مشاركتها في العمليات الخلوية الرئيسة، مثل تنظيم
دورة الخلية، وإصلاح الحمض النووي، وموت الخلايا المبرمج، وغيرها. تشارك البروتينات غير المرتبة جوهريًا في مسارات الإشارة المعروفة في السرطان، مثل مسار م-تور (mTOR)، إذ تنظّم البروتينات غير المرتبة مثل أكت (AKT) وم-تور نمو
الخلايا وتكاثرها، وبقاءها على قيد الحياة.
إن مرونة البروتينات غير المرتبة، وقدرتها على التكيّف والتغير من شكل لآخر بسرعة، تجعلها أهدافًا مهمة لعلاجات السرطان، إذ إن استهداف المجالات المضطربة الضرورية لبقاء الخلايا السرطانية، يمكن أن يعطّل مسارات الإشارات الجينية ويمنع نمو الورم. وفي الأمراض التنكسية العصبية، من الممكن تطوير علاجات مستهدفة نحو هذه البروتينات، على النحو الذي تمنع فيه اختلال البروتين وتجميعه، التي تؤدي إلى السمية العصبية. لقد أتاح التقدم في مجالات النمذجة الحاسوبية (Computational modeling)، ودراسات التعديل التفارغي (Allosteric modification)، وغيرها من التقنيات البيوكيميائية الحديثة، تحديد بعض الجزيئات الصغيرة والببتيدات التي ترتبط بالبروتينات غير المرتبة جوهريًا، من خلال المناطق المضطربة بشكل انتقائي، أو تُعطّل تفاعلاتها مع شركائها. يمكن لهذه الجزيئات تعديل وظائف البروتينات غير المرتبة جوهريًا لاستعادة
التوازن الخلوي، وربما علاج الأمراض المرتبطة بها.
المراجع
Anfinsen, C. B. “Principles That Govern the Folding of Protein Chains.”
Science. vol. 181, no. 4096 (1973). pp. 223-230.
________. et al. “The Kinetics of Formation of Native Ribonuclease during Oxidation of the Reduced Polypeptide Chain.”
Proc Natl Acad Sci U S A. vol. 47, no. 9 (1961). pp. 1309-1314.
Berlow, R. B., H. J. Dyson & P. E. Wright. “Expanding the Paradigm: Intrinsically Disordered Proteins and Allosteric Regulation.”
J Mol Biol. vol. 430, no. 16 (2018). pp. 2309-2320.
Bianchi, G. et al. “Relevance of Electrostatic Charges in Compactness, Aggregation, and Phase Separation of Intrinsically Disordered Proteins.”
Int J Mol Sci. vol. 21, no. 17 (2020).
Bisi, N. et al. “α-Synuclein: An All-Inclusive Trip Around Its Structure, Influencing Factors and Applied Techniques.”
Front Chem. vol. 9 (2021).
Bornberg-Bauer, E., K. Hlouchova & A. Lange. “Structure and Function of Naturally Evolved de Novo Proteins.”
Curr Opin Struct Biol. vol. 68 (2021). pp. 175-183.
Chakrabarti, Pinak & Devlina Chakravarty. “Intrinsically Disordered Proteins/Regions and Insight into Their Biomolecular Interactions.”
Biophysical Chemistry. vol. 283 (2022).
Dittmar, G. et al. “PRISMA: Protein Interaction Screen on Peptide Matrix Reveals Interaction Footprints and Modifications- Dependent Interactome of Intrinsically Disordered C/EBPβ.”
IScience. vol. 13 (2019). pp. 351-370.
Dunker, A. K. et al. “Intrinsically Disordered Protein.”
J Mol Graph Model. vol. 19, no. 1 (2001). pp. 26-59.
Fung, H. Y. J., M. Birol & E. Rhoades. “IDPs in Macromolecular Complexes: The Roles of Multivalent Interactions in Diverse Assemblies.”
Curr Opin Struct Biol. vol. 49 (2018). pp. 36-43.
Karush, Fred. “Heterogeneity of the Binding Sites of Bovine Serum Albumin.”
Journal of the American Chemical Society. vol. 72, no. 6 (1950). pp. 2705-2713.
Katuwawala, A., S. Ghadermarzi & L. Kurgan. “Computational Prediction of Functions of Intrinsically Disordered Regions.”
Prog Mol Biol Transl Sci. vol. 166 (2019). pp. 341-369.
Khare, S. D., P. Chinchilla & J. Baum. “Multifaceted Interactions Mediated by Intrinsically Disordered Regions Play Key Roles in Alpha Synuclein Aggregation.”
Curr Opin Struct Biol. vol. 80 (2023).
Kim, D. H. & K. H. Han. “Target-Binding Behavior of IDPs via Pre-Structured Motifs.”
Prog Mol Biol Transl Sci. vol. 183 (2021). pp. 187-247.
Midic, U. et al. “Unfoldomics of Human Genetic Diseases: Illustrative Examples of Ordered and Intrinsically Disordered Members of the Human Diseasome.”
Protein Pept Lett. vol. 16, no. 12 (2009). pp. 1533-1547.
Mishra, P. M. et al. “Intrinsically Disordered Proteins of Viruses: Involvement in the Mechanism of Cell Regulation and Pathogenesis.”
Prog Mol Biol Transl Sci. vol. 174 (2020). pp. 1-78.
Morris, O. M., J. H. Torpey & R. L. Isaacson. “Intrinsically Disordered Proteins: Modes of Binding with Emphasis on Disordered Domains.”
Open Biol. vol. 11, no. 10 (2021). 210222.
Trębińska-Stryjewska, A. et al. “HAX1: A versatile, intrinsically disordered regulatory protein.”
Biochim Biophys Acta Mol Cell Res. vol. 1870, no. 7 (2023).
Trivedi, R. & H. A. Nagarajaram. “Intrinsically Disordered Proteins: An Overview.”
Int J Mol Sci. vol. 23, no. 22 (2022).
Uversky, V. N. “P53 Proteoforms and Intrinsic Disorder: An Illustration of the Protein Structure-Function Continuum Concept.”
Int J Mol Sci. vol. 17, no. 11 (2016).
Uversky, V. N., C. J. Oldfield & A. K. Dunker. “Intrinsically Disordered Proteins in Human Diseases: Introducing the D2 Concept.”
Annu Rev Biophys. vol. 37 (2008). pp. 215-246.
Vacic, V. et al. “Disease-Associated Mutations Disrupt Functionally Important Regions of Intrinsic Protein Disorder.”
PLoS Comput Biol. vol. 8, no. 10 (2012).
Ward, J. J. et al. “Prediction and Functional Analysis of Native Disorder in Proteins from the Three Kingdoms of Life.”
J Mol Biol. vol. 337, no. 3 (2004). pp. 635-645.
Wright, P. E. & H. J. Dyson. “Intrinsically Disordered Proteins in Cellular Signalling and Regulation.”
Nat Rev Mol Cell Biol. vol. 16, no. 1 (2015). pp. 18-29.
Zheng, H. et al. “The Enigma of Tau Protein Aggregation: Mechanistic Insights and Future Challenges.”
Int J Mol Sci. vol. 25, no. 9 (2024).
[1] Fred Karush, “Heterogeneity of the Binding Sites of Bovine Serum Albumin,”
Journal of the American Chemical Society, vol. 72, no. 6 (1950), pp. 2705-2713.
[2] C. B. Anfinsen et al., “The Kinetics of Formation of Native Ribonuclease during Oxidation of the Reduced Polypeptide Chain,”
Proc Natl Acad Sci U S A, vol. 47, no. 9 (1961), pp. 1309-1314.
[3] C. B. Anfinsen, “Principles That Govern the Folding of Protein Chains,”
Science, vol. 181, no. 4096 (1973), pp. 223-230.
[4] A. K. Dunker et al., “Intrinsically Disordered Protein,”
J Mol Graph Model, vol. 19, no. 1 (2001), pp. 26-59.
[5] J. J. Ward et al., “Prediction and Functional Analysis of Native Disorder in Proteins from the Three Kingdoms of Life,”
J Mol Biol, vol. 337, no. 3 (2004), pp. 635-645.
[6] V. N. Uversky, C. J. Oldfield & A. K. Dunker, “Intrinsically Disordered Proteins in Human Diseases: Introducing the D2 Concept,”
Annu Rev Biophys, vol. 37 (2008), pp. 215-246.
[7] A. Katuwawala, S. Ghadermarzi & L. Kurgan, “Computational Prediction of Functions of Intrinsically Disordered Regions,”
Prog Mol Biol Transl Sci, vol. 166 (2019), pp. 341-369.
[8] Ward et al.
[9] U. Midic et al., “Unfoldomics of Human Genetic Diseases: Illustrative Examples of Ordered and Intrinsically Disordered Members of the Human Diseasome,”
Protein Pept Lett, vol. 16, no. 12 (2009), pp. 1533-1547.
[10] P. E. Wright & H. J. Dyson, “Intrinsically Disordered Proteins in Cellular Signalling and Regulation,”
Nat Rev Mol Cell Biol, vol. 16, no. 1 (2015), pp. 18-29.
[11] G. Dittmar et al., “PRISMA: Protein Interaction Screen on Peptide Matrix Reveals Interaction Footprints and Modifications- Dependent Interactome of Intrinsically Disordered C/EBPβ,”
IScience, vol. 13 (2019), pp. 351-370.
[12] V. Vacic et al., “Disease-Associated Mutations Disrupt Functionally Important Regions of Intrinsic Protein Disorder,”
PLoS Comput Biol, vol. 8, no. 10 (2012).
[13] Wright & Dyson.
[14] Midic et al.
[15] G. Bianchi et al., “Relevance of Electrostatic Charges in Compactness, Aggregation, and Phase Separation of Intrinsically Disordered Proteins,”
Int J Mol Sci, vol. 21, no. 17 (2020).
[16] R. Trivedi & H. A. Nagarajaram, “Intrinsically Disordered Proteins: An Overview,”
Int J Mol Sci, vol. 23, no. 22 (2022).
[17] H. Y. J. Fung, M. Birol & E. Rhoades, “IDPs in Macromolecular Complexes: The Roles of Multivalent Interactions in Diverse Assemblies,”
Curr Opin Struct Biol, vol. 49 (2018), pp. 36-43.
[18] Wright & Dyson.
[19] R. B. Berlow, H. J. Dyson & P. E. Wright, “Expanding the Paradigm: Intrinsically Disordered Proteins and Allosteric Regulation,”
J Mol Biol, vol. 430, no. 16 (2018), pp. 2309-2320.
[20] Wright & Dyson.
[21] E. Bornberg-Bauer, K. Hlouchova & A. Lange, “Structure and Function of Naturally Evolved de Novo Proteins,”
Curr Opin Struct Biol, vol. 68 (2021), pp. 175-183.
[22] O. M. Morris, J. H. Torpey & R. L. Isaacson, “Intrinsically Disordered Proteins: Modes of Binding with Emphasis on Disordered Domains,”
Open Biol, vol. 11, no. 10 (2021).
[23] Trivedi & Nagarajaram.
[24] P. M. Mishra et al., “Intrinsically Disordered Proteins of Viruses: Involvement in the Mechanism of Cell Regulation and Pathogenesis,”
Prog Mol Biol Transl Sci, vol. 174 (2020), pp. 1-78.
[25] D. H. Kim & K. H. Han, “Target-Binding Behavior of IDPs via Pre-Structured Motifs,”
Prog Mol Biol Transl Sci, vol. 183 (2021), pp. 187-247.
[26] V. N. Uversky, “P53 Proteoforms and Intrinsic Disorder: An Illustration of the Protein Structure-Function Continuum Concept,”
Int J Mol Sci, vol. 17, no. 11 (2016).
[27] N. Bisi et al., “α-Synuclein: An All-Inclusive Trip Around Its Structure, Influencing Factors and Applied Techniques,”
Front Chem, vol. 9 (2021).
[28] S. D. Khare, P. Chinchilla & J. Baum, “Multifaceted Interactions Mediated by Intrinsically Disordered Regions Play Key Roles in Alpha Synuclein Aggregation,”
Curr Opin Struct Biol, vol. 80 (2023).
[29] H. Zheng et al., “The Enigma of Tau Protein Aggregation: Mechanistic Insights and Future Challenges,”
Int J Mol Sci, vol. 25, no. 9 (2024).
[30] A. Trębińska-Stryjewska, et al., “HAX1: A versatile, intrinsically disordered regulatory protein.”
Biochim Biophys Acta Mol Cell Res. vol. 1870, no. 7 (2023).
[31] Pinak Chakrabarti & Devlina Chakravarty, “Intrinsically Disordered Proteins/Regions and Insight into Their Biomolecular Interactions,”
Biophysical Chemistry, vol. 283 (2022).
[32] Ibid.