أدوية المناعة (Immunomodulatory drugs) هي أدوية يمكنها تعديل الاستجابة المناعية، إما عن طريق تحفيز الجهاز المناعي أو تثبيطه أو تعزيزه، وتُصنف هذه الأدوية إلى علاجات مناعية تحفيزية، وغالبًا ما تُستخدم في اللقاحات أو عوامل مكافحة السرطان؛ أو علاجات مناعية تثبيطية، وتُستخدم عادةً في علاج الحساسية والحالات الالتهابية مثل التهاب المفاصل الروماتويدي أو الأمراض المناعية الذاتية، بالإضافة إلى معززات المناعة التي تساعد في دعم وظائف الجهاز المناعي وتحسينها عمومًا، من دون أن تسبب تنشيطًا مباشرًا أو مفرطًا.
يُعد النظام المناعي أساسيًّا لمنع العدوى والأمراض وللمحافظة على التوازن الداخلي للجسم. وتنشأ أمراض المناعة عندما يحصل خلل أو توجيه خاطئ للاستجابة المناعية، ما يؤدي إلى حالات مثل أمراض المناعة الذاتية، والحساسية، ونقص المناعة. إن البحث المستمر والتقدم في العلاج المناعي يبشر بعلاجات أكثر فاعلية، ما يمهد الطريق إلى تحسين النتائج الصحية وتحسين نوعية الحياة للمرضى.
تعريفها
أدوية المناعة هي أدوية يمكنها تعديل الاستجابة المناعية، إما عن طريق تحفيز الجهاز المناعي أو تثبيطه أو تعزيزه، وتُصنف هذه الأدوية إلى عدة فئات بناءً على آلية عملها، ومنها: العلاجات المناعية التحفيزية، والعلاجات المناعية التثبيطية، ومعززات المناعة[1].
الجهاز المناعي
الجهاز المناعي (The Immune system) هو النظام الدفاعي الأساسي في الجسم البشري، ويُعد المسؤول الرئيس عن الوقاية من الأمراض والعدوى، ويتكون من شبكة معقدة من الأعضاء والخلايا والبروتينات والأنسجة التي تعمل بتكامل لحماية الجسم من الكائنات الحية الضارة والمواد التي تسبب الضرر له. ويُعد الجلد والطبقة القرنية والأغشية المخاطية للجهاز التنفسي والجهاز الهضمي والجهاز البولي حاجزًا فيزيائيًّا (Physical barrier)، أما هو فيُعد الخط الأول للدفاع عن الجسم[2].
أنواع الاستجابات المناعية
يستطيع الجسم حماية نفسه من مجموعة واسعة من الأمراض، بسبب الحواجز الفيزيائية والاستجابات المناعية المتنوعة، ما يعزز صحته وسلامته، وقد يؤدي اختراق الحواجز التشريحية إلى استجابتين مناعيتين: المناعة الفطرية (Innate immunity) والمناعة المكتسبة (Acquired Immunity)[3]، مثلما هو موضح في (الشكل 1) و(الشكل 2).
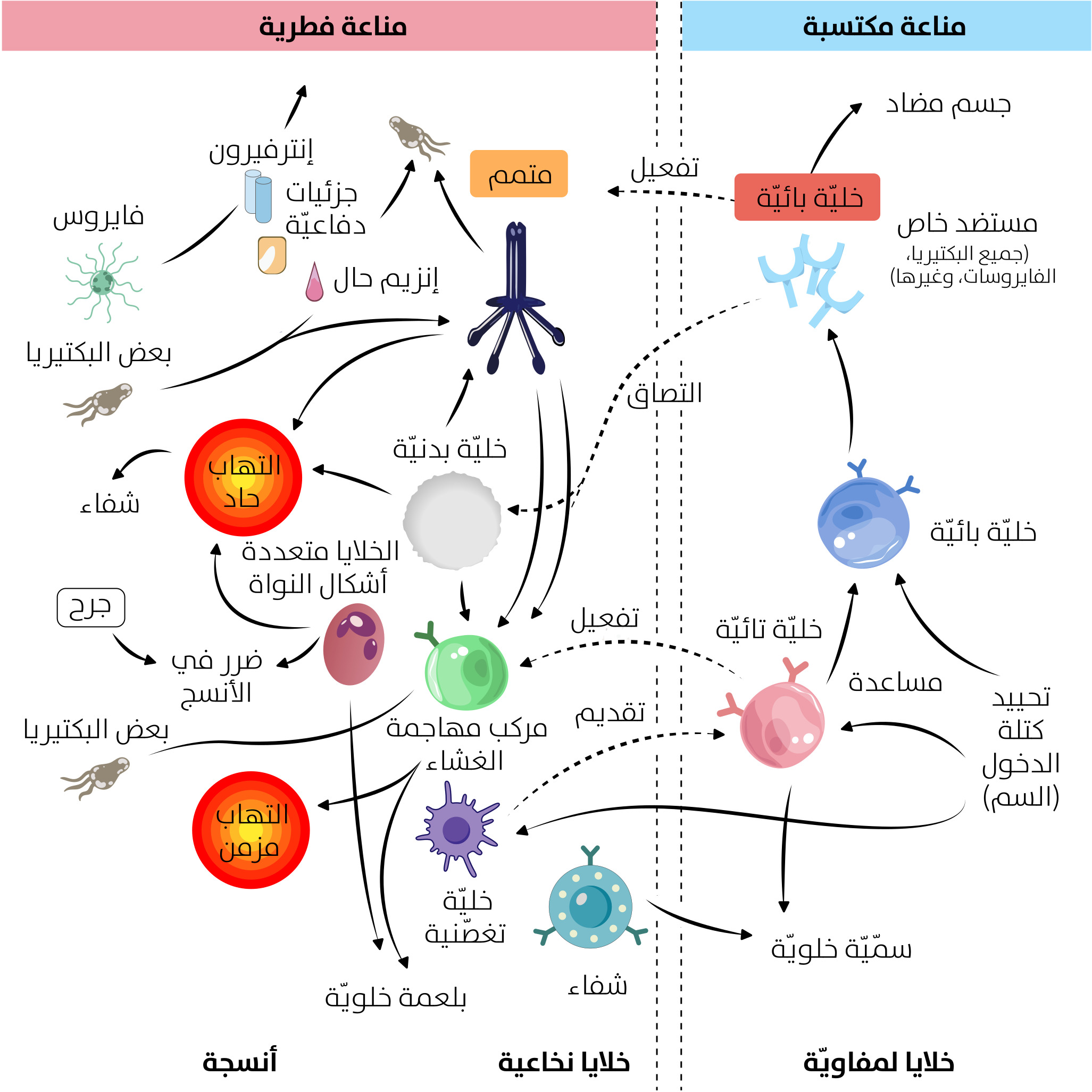 [الشكل 1]
[الشكل 1]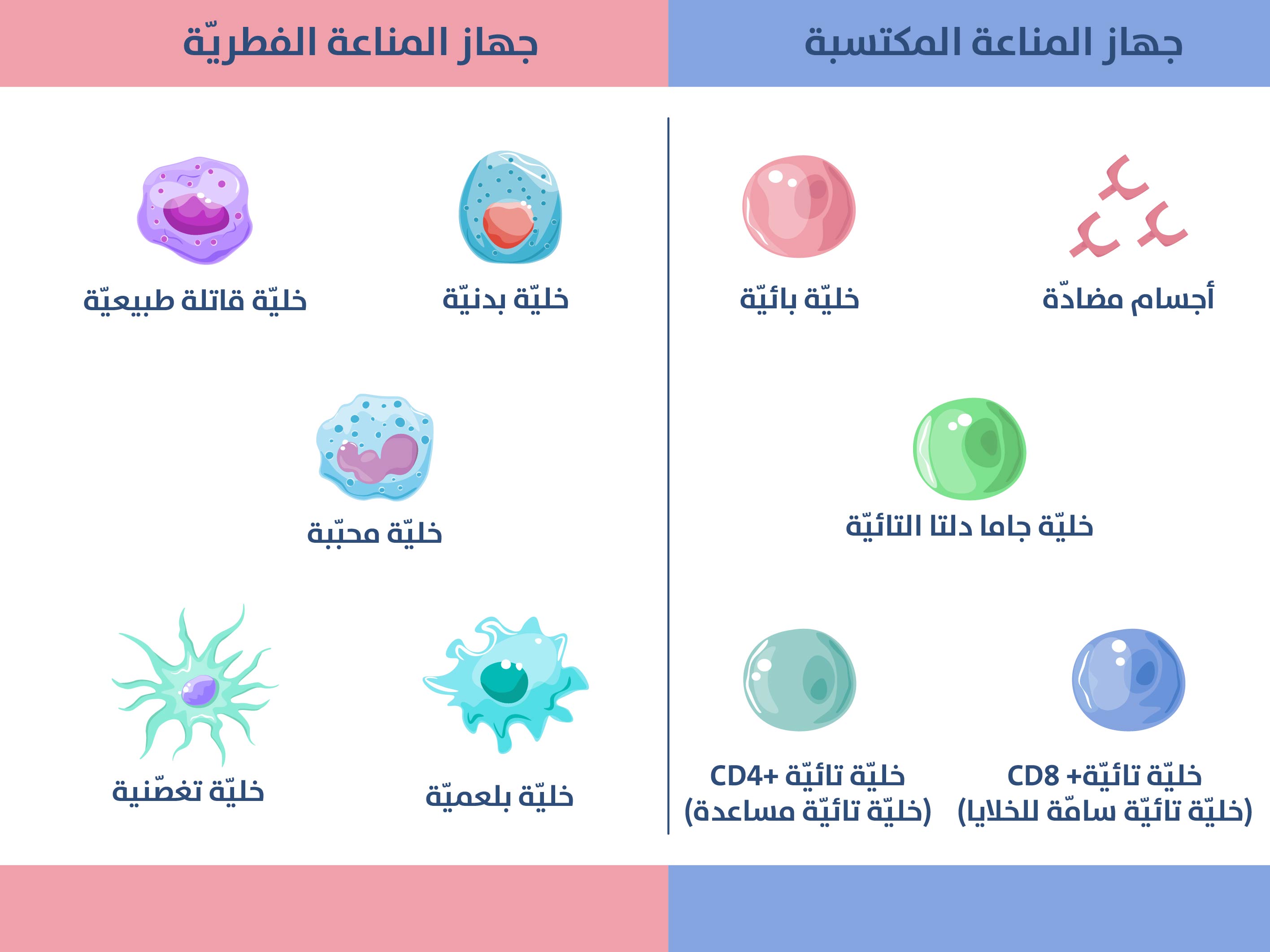 [الشكل 2]
[الشكل 2]
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
المناعة الكامنة أو الفطرية
تعمل المناعة الكامنة أو الفطرية (The Innate immunity)، التي تُعرف أيضًا باسم "المناعة الطبيعية"، من دون الحاجة إلى التعرض المسبق لمستضد، ما يجعلها فاعلة فورًا ضد الأجسام الغريبة، وتَستخدم هذه المناعة مستقبلات التعرف على الأنماط (Pattern Recognition Receptors, PRPs) لتحديد أنواع الجزيئات الغريبة المرتبطة بالممرضات (Pathogen Associated Molecular Patterns, PAMPs)، وأنماط الجزيئات المرتبطة بإحداث الضرر في المضيف (Damage Associated Molecular Patterns, DAMPs)[4].
تُصنف المناعة الكامنة إلى أربعة أنواع حسب الحواجز الدفاعية التي تعتمد عليها، وهذه الأنواع هي: أولًا، الحواجز التشريحية (Anatomical barriers)، مثل الجلد والأغشية المخاطية، التي تعمل بصفتها خط دفاع ميكانيكي ضد دخول الكائنات الممرضة. وثانيًا، الحواجز الفيزيولوجية (Physiological barriers) التي تشمل ارتفاع درجة حرارة الجسم، وانخفاض الرقم الهيدروجيني، والعوامل الكيميائية مثل الإنزيمات والبروتينات المضادة للميكروبات. وثالثًا، عمليات البلعمة والاحتواء (Phagocytosis and Containment) التي تؤديها خلايا مثل البلعميات الكبيرة والخلايا المتعادلة، إذ تبتلع الكائنات الممرضة وتمنع انتشارها. ورابعًا، الاستجابات الالتهابية (Inflammatory responses) التي تنشط عند الإصابة، وتُسهّل وصول خلايا الدم البيضاء إلى موقع العدوى. تمثل هذه الآليات معًا استجابة مناعية فورية وفعالة، وتُعدّ الخط الأول للدفاع عن الجسم قبل تفعيل المناعة المكتسبة (يُنظر الجدول 1)[5].
تُعتبر المناعة الطبيعية ضرورية للحفاظ على التوازن الداخلي، ويؤدي هذا النوع من المناعة دورًا مهمًا في تنشيط المناعة التكيفية وتنظيمها. وعلى الرغم من بساطة مكوناتها، فإن آليات الدفاع الفطرية تمتلك القدرة على تطوير استجابة مستحثه أثناء العدوى الأولية والظروف الالتهابية، وتتحدد هذه الاستجابة بفضل التعبير عن مستقبلات التعرف على الأنماط الموجودة على سطح الخلية. إضافة إلى أن هذه المستقبلات قادرة على التعرف على العديد من الجزيئات المعقدة مثل: عديدات السكريات، والغليكوليبيدات، والبروتينات الدهنية، والنوكليوتيدات، والأحماض النووية[6].
[الجدول 1]
أنواع المناعة الكامنة حسب الحواجز الدفاعية
الحاجز |
نوع الحاجز |
آلية العمل |
الحاجز التشريحي | الجلد | أ. الحاجز الميكانيكي يبطئ دخول الميكروبات. ب. البيئة الحمضية ((pH من 3-5 تبطئ نمو الميكروبات. |
الغشاء المخاطي | أ. البكتيريا النافعة تتنافس مع الميكروبات على مواقع الارتباط ب. المخاط يحبس الميكروبات الغريبة. ت. الأهداب تدفع الميكروبات خارج الجسم. |
الحاجز الفيزيولوجي | درجة الحرارة | أ. ارتفاع درجة حرارة الجسم، إذ تثبط الحمى نمو بعض مسببات الأمراض. |
الرقم الهيدروجيني المنخفض | أ. الرقم الهيدروجيني الحمضي للمعدة يقتل معظم الميكروبات غير المهضومة. |
العوامل الكيميائية | أ. الليزوزيم (Lysosomes) يحلل جدار الخلية البكتيرية ب. الإنترفيرون (Interferon) يحفز الدفاعات المضادة للفيروسات في الخلايا غير المصابة. ت. المكملات تحلل الميكروبات أو تسهل عملية البلعمة. |
البلعمة والاحتواء الداخلي | | أ. تقوم خلايا متنوعة عن طريق الاحتواء الداخلي بتفكيك الجزيئات الكبيرة والغريبة. ب. تقوم خلايا متخصصة (الخلايا الوحيدة في الدم، والبلاعم، والبلاعم النسيجية) عن طريق البلعمة بقتل وهضم الكائنات الحية بالكامل. |
الحواجز الالتهابية | | أ. يسبب الضرر النسيجي والعدوى تسربَ السائل الوعائي الذي يحتوي على بروتينات المصل ذات النشاط المضاد للبكتيريا، ما يؤدي إلى تدفق الخلايا البلعمية إلى المنطقة المتضررة. |
المناعة المكتسبة
المناعة المكتسبة (Acquired immunity)، التي تُعرف أيضًا باسم "المناعة التكيفية" (Adaptive immunity)، هي ضرورية لمحاربة الكائنات المعدية التي لا يلتقطها الجهاز المناعي الكامن، وتستهدف هذه الاستجابة الدقيقة مسببات أمراض معينة وتتميز بذاكرتها، ما يمكّن الجهاز المناعي من تذكر المسببات التي تعامل معها مسبقًا، فيستجيب لها بكفاءة أكبر، وتتكون هذه الاستجابات في المناعة المكتسبة عن طريق خلايا الدم البيضاء المعروفة باسم اللمفاويات (Lymphocytes)، وهناك نوعان رئيسان منها - أي الاستجابات المكتسبة - وهي: استجابات الأجسام المضادة التي تقوم بها الخلايا البائية (B cells)، واستجابات المناعة المتوسطة الخلوية التي تقوم بها الخلايا التائية (T cells)، وتشكل هذه الجهود المنسقة بين الخلايا البائية والتائية العمود الفقري لقدرة الجهاز المناعي المكتسب على توفير حماية طويلة الأمد[7].
- استجابات الخلايا البائية (المناعة الخلطية) (Humoral Immunity)
في استجابات الأجسام المضادة، تُنشط الخلايا البائية لإنتاج بروتينات تُعرف باسم "الأجسام المضادة" (Antibodies) وإفرازها (يُنظر الشكل 3)، تنتشر هذه الأجسام المضادة في الدورة الدموية وتخترق السوائل الجسمية الأخرى، وتتصل بشكل محدد بالمستضدات الأجنبية (Antigen, Ag) التي تحفز إنتاجها من خلال الربط بتلك المستضدات. تُحيِّد الأجسام المضادة الفيروسات والسموم الميكروبية (مثل سم الكزاز أو سم الدفتيريا) عن طريق منعها من الالتصاق بمستقبلات الخلايا المضيفة. إضافة إلى ذلك، تغزو الأجسام المضادة مسببات الأمراض لتدميرها من خلال تيسير ابتلاعها من قبل خلايا البلعمة المختصة في الجهاز المناعي الكامن، ويعزز هذا العمل المزدوج للتعطيل بشكل كبير قدرة الجسم على القضاء على الأجسام الضارة[8].
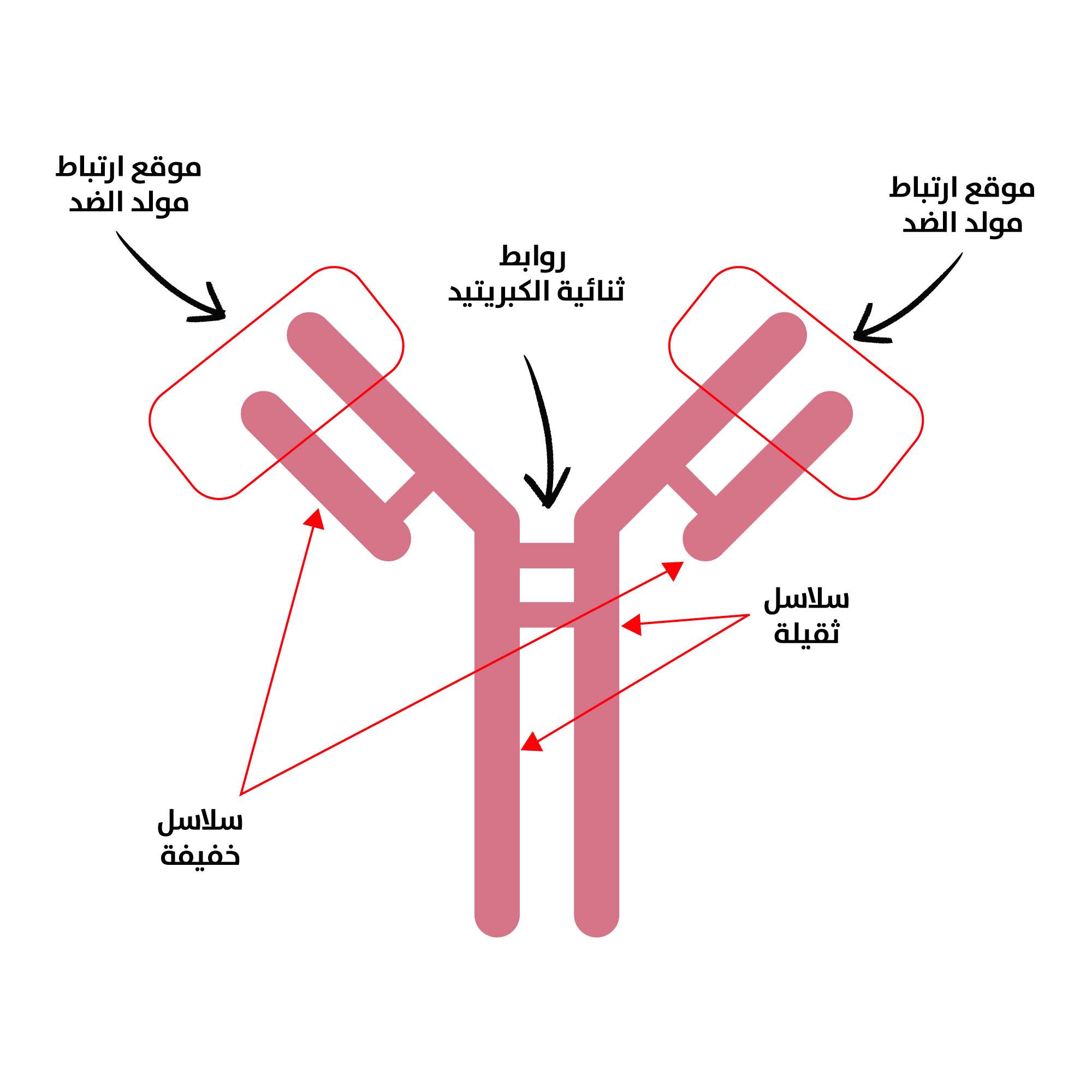 [الشكل 3]
[الشكل 3]
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
- استجابات الخلايا التائية (المناعة الخلوية) (Cell-mediated immunity)
في الاستجابات المناعية الخلوية، تستهدف خلايا T المنشطة مباشرة المستضدات الأجنبية التي تُعرض على سطح الخلايا المضيفة. مثلًا: قد تقضي خلية T على خلية مضيفة مصابة بالفيروس تعرض على سطحها مستضدات فيروسية، ما يمنع تكاثر الفيروس. وفي حالات أخرى، تنتج خلايا T جزيئات إشارية تنشط البلاعم (Macrophages)، ما يعزز قدرتها على تدمير الميكروبات التي ابتُلعت. هذا النهج المستهدف يضمن القضاء الفاعل على الخلايا المصابة أو غير الطبيعية، ما يعزز دفاعات الجسم ضد العدوى[9].
- خلايا الذاكرة (Memory Cells)
تتحول بعض الخلايا البائية والتائية إلى خلايا ذاكرة بعد الإصابة، ما يوفر مناعة طويلة الأمد، وتستجيب هذه الخلايا بسرعة وفاعلية أكبر عند التعرض لنفس المسببات مرة أخرى[10].
الاستجابة المناعية
يتطلب الدفاع المناعي الناجح تفعيل الاستجابة المناعية وتنظيمها وحلها، وذلك من خلال:
التنشيط
تُنشط خلايا الجهاز المناعي عندما تتعرف على مستضد أجنبي (Ag) عبر مستقبلات سطحية على الخلايا، ويمكن أن تكون هذه المستقبلات محددة لـ:
- أنماط الجزيئات الغريبة المرتبطة بالممرضات (PAMPs) وهي الهياكل المرتبطة بمختلف الأمراض، ويُتعرف عليها من خلال مستقبلات التعرف على أنماط الجزيئات (PRRs) مثل مستقبلات تول (Toll-like Receptors, TLRs) الشبيهة بالفطريات، ومستقبلات المانوز (Mannose Receptors, MRs)، ومستقبلات البحث عن الخلايا العصبية (Neurotrophic Receptors) وغيرها من الخلايا المناعية.
- هياكل محددة مسببة للأمراض: تخص أنواعًا معينة من مسببات الأمراض، وتتعرف عليها الأجسام المضادة التي توجد على الخلايا البائية أو بوساطة مستقبلات الخلايا الموجودة على الخلايا التائية. هذه الآلية المزدوجة للتعرف، تسمح للجهاز المناعي بالاستجابة بفاعلية لمجموعة واسعة من العوامل الممرضة. ويمكن أن تُنشط الخلايا المناعية أيضًا عندما ترتبط مجمعات الأجسام المضادة والمستضدات ومجمعات الكائنات الحية الدقيقة التكميلية بمستقبلات سطحية معينة[11].
- مستقبلات Fc-gamma (Future constant gamma receptor, FcγR): ترتبط هذه المستقبلات بمنطقة البروتين البلورية (Fc) من الأجسام المضادة التي تنتمي إلى النوع (الغلوبولين المناعي ج) (Immunoglobulin G, IgG). ويؤدي ربط أجسام IgG بمستقبلات FcγR على الخلايا المناعية إلى تفعيل استجابات مناعية متنوعة، مثل البلعمة، والسمية الخلوية المعتمدة على الأجسام المضادة (Antibody-dependent celular cytotoxicity, ADCC) وإفراز وسطاء الالتهاب[12].
- مستقبلات C3b وiC3b: ترتبط هذه المستقبلات بالأجزاء التكميلية C3b وiC3b التي تُعد جزءًا من النظام المكمل (Complement system)، وإن ربط هذه الأجزاء المتممة بمستقبلاتها على الخلايا المناعية يعزز البلعمة لمسببات الأمراض المزعجة ويحفز الاستجابات الالتهابية[13]. وتؤدي هذه التفاعلات التي تتوسطها المستقبلات أدوارًا حاسمة في ربط الاستجابات المناعية التكيفية والفطرية، ما يضمن التعرف الفاعل على مسببات الأمراض والخلايا المصابة والقضاء عليها.
عند التعرف على المستضد، أو مركب المستضد والجسم المضاد، أو مركب الكائنات الحية الدقيقة التكميلية، يُبلعم عادةً بوساطة الخلايا المناعية، ويقتل معظم الكائنات الحية الدقيقة بفاعلية خلال هذه العملية، ولكن بعضها يمكن أن يثبط آليات القتل داخل الخلايا البلعمية، مثل المتفطرات ((Mycobacteria داخل الخلايا البلعمية[14].
في الحالات التي تكون فيها القدرة على القتل الخلوي الداخلي متأثرة، تؤدي السيتوكينات المشتقة من الخلايا T، وخاصة الإنترفيرون جاما Interferon gamma, IFNγ)) دورًا حاسمًا، إذ يحفز IFNγ الخلايا البلعمية لإنتاج مزيد من الإنزيمات المحللة (Lysosomal enzymes) والمواد المضادة للميكروبات الأخرى، ما يعزز قدرتها على القضاء على الكائنات الدقيقة أو احتجازها[15]. إذا لم يُحلل المستضد بسرعة، ويُزال عن طريق البلعمة، وهذا يحدث بطريقة أقل شيوعًا، تُنشط الاستجابة المناعية المكتسبة، وتبدأ هذه الاستجابة في الأنسجة اللمفاوية الثانوية، إذ يتعامل كل عضو مع نوع محدد من المستضدات. ويتولى الطحال معالجة المستضدات المتداولة في الدم، في حين تستجيب العقد اللمفاوية الإقليمية للمستضدات القادمة من الأنسجة المختلفة. أما الأنسجة اللمفاوية المرتبطة بالمخاط، مثل اللوزتين والغدد الليمفاوية الموجودة في الأغشية المخاطية، فهي تتعامل مع المستضدات التي يُتَعرَّض لها عند السطوح المخاطية.
وفي هذه الأنسجة اللمفاوية، تتعرف الخلايا B والخلايا T ذات المستقبلات المحددة للغاية على المستضد، ويؤدي هذا التعرف إلى استجابات مناعية تكيفية تتضمن إنتاج الأجسام المضادة بوساطة الخلايا B وتنشيط الخلايا T للقضاء على المستضد، وتضمن هذه الاستجابة المنسقة تعبئة الدفاعات المناعية الجهازية والمخاطية ضد مسببات الأمراض الغازية[16].
التنظيم
تُنظم الاستجابة المناعية بدقة لمنع الضرر على المضيف، الذي يمكن أن يظهر على شكل حالات مثل فقر الدم الشديد، ومتلازمة إطلاق السيتوكينات (Cytokines)، أو التدمير الواسع للأنسجة. وتعبر الكثير من خلايا T التنظيمية عن عامل التكيف Foxp3، وتؤدي دورًا حاسمًا في الحفاظ على التوازن المناعي، وتمارس الخلايا التائية التنظيمية (Regulatory T-cells, Tregs) وظيفتها من خلال عدة آليات[17]:
- إفراز السيتوكينات المناعية المثبطة: تنتج الخلايا التائية التنظيمية سيتوكينات مثل الإنترلوكين-10 (IL-10-Interleukin-10,) وعامل نمو التحول بيتا (Transforming growth factor beta, TGF-β) وتثبط هذه السيتوكينات تنشيط الخلايا المناعية الأخرى ووظائفها، ما يخفف من استجابة المناعة ويمنع الالتهاب الزائد.
- آليات تعتمد على اتصال الخلايا: يمكن لـخلايا T التنظيمية التفاعل مباشرة وتثبيط وظائف الخلايا المناعية الأخرى من خلال اتصال خلية بخلية، ما يعدل استجابات المناعة محليًا.
هذه الآليات التنظيمية التي تتوسطها الخلايا التائية التنظيمية (Tregs) ضرورية لمنع التفاعلات الذاتية المناعية، إذ يستهدف الجهاز المناعي بشكل خاطئ أنسجة الجسم. إضافة إلى إن الخلايا التائية التنظيمية تؤدي دورًا محتملًا في حل الاستجابات المناعية ضد المستضدات الأجنبية عند تثبيط التهديد، ما يعزز التوازن المناعي ويقلل من الضرر التابع للأنسجة السليمة[18].
التحلل
عندما يُعزل أو يُزال المستضد من الجسم، تتحلل الاستجابة المناعية تدريجيًّا[19]:
- توقف إفراز السيتوكينات: إذ لم تُحفز الخلايا المناعية باستمرار فإنها تتوقف، لا سيما الخلايا T، عن إفراز السيتوكينات التي تحفز الالتهاب وتنشط المناعة.
- التخزين الخلوي للخلايا T ذات السمية الفاعلة: تخضع الخلايا T ذات السمية الفاعلة، والتي أدّت دورًا في القضاء على الخلايا المصابة أو غير الطبيعية، لعملية التخزين الخلوي (الوفاة المبرمجة للخلية، Apoptosis)، وتضمن عملية التخزين الخلوي أن تُزال هذه الخلايا الفاعلة بأمان عن طريق الخلايا الناقلة، ما يمنع من إفراز محتوياتها الخلوية التي يمكن أن تثير الالتهاب.
- البلعمة للخلايا السمية: يُتعرف على الخلايا السمية وتُبتلع سريعًا بوساطة الخلايا الناقلة، وتُسمى هذه العملية بالبلعمة النهائية، وتعمل على إزالة الخلايا السمية بفاعلية قبل أن تنفجر وتنسكب محتوياتها، ما يتجنب إحداث ضرر محتمل للأنسجة وحدوث الالتهاب.
- بقاء خلايا الذاكرة: تظل خلايا T وخلايا B التي تمايزت في خلايا الذاكرة خلال الاستجابة المناعية على قيد الحياة، وتوفر خلايا الذاكرة استجابات سريعة وفاعلة عند التعرض للمستضد نفسه في المستقبل، وإن هذه الخاصية مهمة وتعبّر عن قدرة الجهاز المناعي على إطلاق استجابة أسرع وأكثر فاعلية خلال العدوى اللاحقة.
الأمراض المناعية
الأمراض المناعية والتي تُعرف أيضًا بالاضطرابات المناعية، وهي الحالات التي تنجم عن نشاط غير طبيعي لجهاز المناعة في الجسم. ويمكن تصنيفها عمومًا إلى ثلاثة أنواع رئيسة:
- الأمراض المناعية الذاتية: في هذه الحالات، يهاجم الجهاز المناعي بشكل خاطئ أنسجة الجسم الخاصة به، معتبرًا إياها غريبة. من الأمثلة على ذلك التهاب المفاصل الروماتويدي، والذئبة الحمامية النظامية (Systemic Lupus Erythematosus, SLE)، والتصلب المتعدد (Multiple sclerosis)، والسكري من النوع الأول[20].
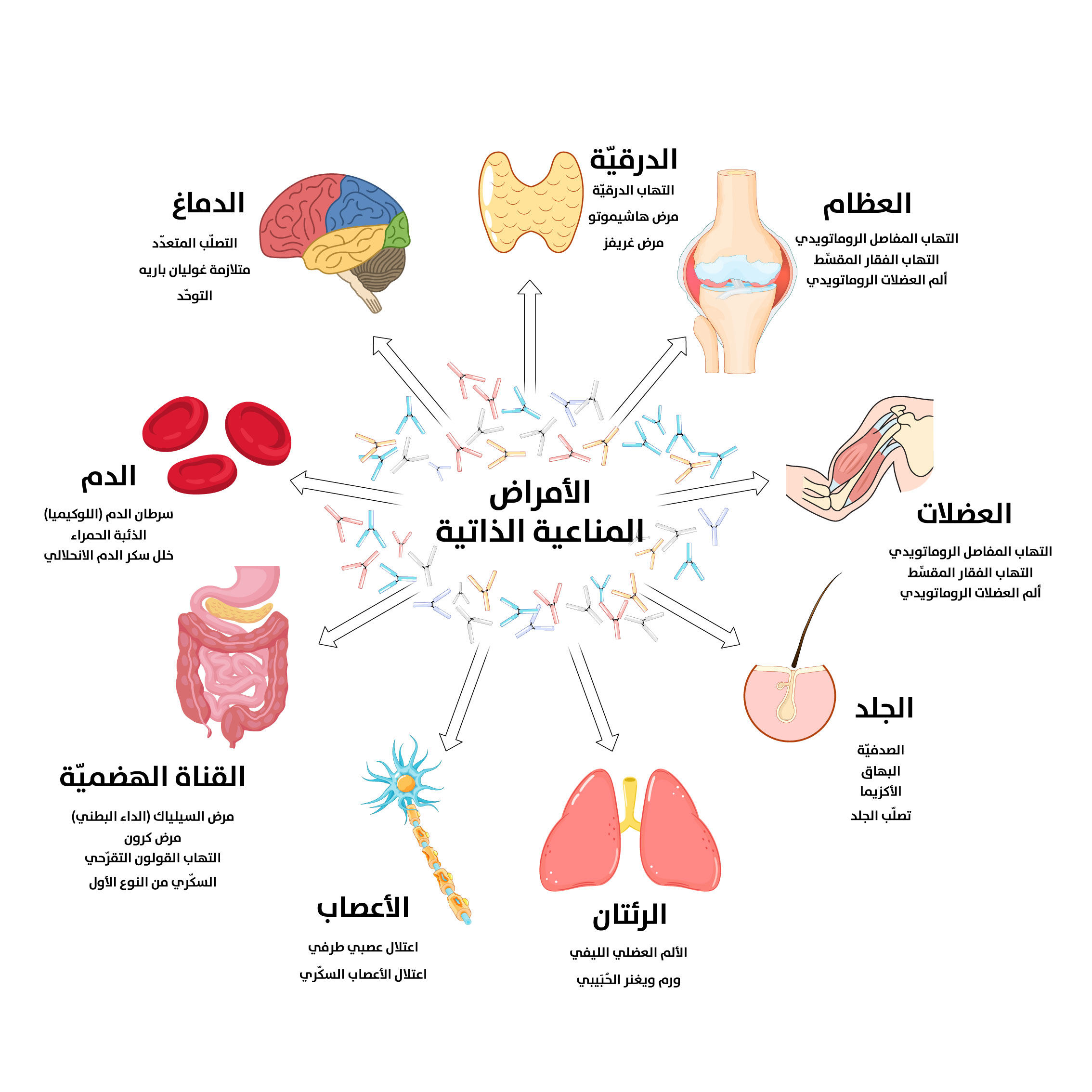 [الشكل 4]
[الشكل 4]
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
- اضطرابات نقص المناعة: تحدث هذه الاضطرابات عندما يكون الجهاز المناعي إما غائبًا أو ناقصًا، ما يجعل الجسم أكثر عرضة للإصابة بالعدوى، يمكن أن يكون نقص المناعة خُلقيًا (أولي)، مثل
نقص المناعة المشترك الوخيم (Severe combined immunodeficiency (SCID) أو مُكتسبًا (ثانوي)، مثل
مرض الإيدز الناجم عن فيروس نقص المناعة البشرية[21].
- تفاعلات الحساسية والتحسسات الزائدة: ينطوي هذا النوع من الاضطرابات المناعية على استجابة مبالغ فيها من جهاز المناعة لمادة خارجية تكون عادةً غير ضارة، وتشمل الحالات الشائعة الربو، والإكزيما، وحمى القش، وحساسية الطعام[22].
في هذه الأنواع جميعها، يؤدي تعرض جهاز المناعة إلى أعراض مختلفة ومشاكل صحية، اعتمادًا على الاضطراب المحدد والأعضاء المتأثرة، ويتضمن العلاج غالبًا إدارة الأعراض، وفي بعض الحالات، تنظيم نشاط جهاز المناعة[23].
أدوية المناعة
تُصنف الأدوية المناعية التي تهدف إلى استحداث استجابة مناعية أو تعزيزها تحت فئة العلاجات المناعية التحفيزية، وغالبًا ما تُستخدم في اللقاحات أو عوامل مكافحة السرطان، بينما تُصنف العلاجات المناعية التي تقلل أو تثبط جهاز المناعة تحت فئة العلاجات المناعية التثبيطية، وغالبًا ما تُستخدم في علاج الحساسية والحالات الالتهابية مثل التهاب المفاصل الروماتويدي أو الأمراض المناعية الذاتية. وتشتمل الأدوية المستخدمة لمنع المناعة على أدوية منع رفض العضو المزروع.
ويُعد ظهور عوامل جديدة وتحسينات في أنظمة تثبيط المناعة بعد الزرع من العوامل المهمة التي تؤدي إلى تقدم كبير في هذا المجال. ومع ذلك، تزيد هذه الأدوية أيضًا من خطر الإصابة بالعدوى والسرطانات والآثار الجانبية الأخرى[24].
العلاجات المناعية التحفيزية
يمكن تعزيز الجهاز المناعي من خلال مجموعة متنوعة من الأدوية والتدخلات، ويمكن تصنيفها عمومًا إلى لقاحات ومناعيات[25].
اللقاحات
تحفز اللقاحات الجهاز المناعي للتعرف على المسببات المحددة ومحاربتها، وتُعد من أكثر الطرق الفاعلة لمنع الأمراض العدوانية، وتنقسم إلى:
- اللقاحات الحية المضعفة (Live attenuated vaccines): تنشأ اللقاحات الحية من الفيروسات أو البكتيريا البرية الحية (Wild-type live bacteria)، وتُضاعف هذه الفيروسات أو البكتيريا البرية في المختبر عادةً عن طريق الزراعة المتكررة. مثلًا: عُزِل فيروس الحصبة – الذي نستخدمه الآن لقاحًا - من طفل أصيب بمرض الحصبة عام 1954، واستغرق نحو 10 سنوات من المرور المتسلسل باستخدام وسائط زراعة الأنسجة لتحويل الفيروس البريّ الحي (Wild type live virus) إلى الفيروس المطعَّم المضعف؛ لتحفيز استجابة مناعية، لأن اللقاحات الحية المضعفة عند الشخص المطعم يجب أن تتكاثر منها جرعة صغيرة نسبيًا من الفيروس أو البكتيريا المحقونة في الجسم، وتنشئ ما يكفي من الكائنات الحية لتحفيز استجابة مناعية. وتستخدم اللقاحات الحية المضعفة للحماية ضد الحصبة (Measles)، والنكاف (Mumps)، والحصبة الألمانية (Rubella)، بما يعرف بـ "اللقاح الثلاثي" (Measles-Mumps-Rubella vaccine, MMR vaccine)، وفيروسات الروتا (Rotaviruses)، والجدري (Smallpox)، والحماق (Chickenpox)، والحمى الصفراء.
- اللقاحات غير الحية: تُعد هذه اللقاحات غير حية، ولا يمكن أن تتكاثر، وبذلك لا تستطيع أن تسبب المرض، حتى عند الأشخاص الذين يعانون من نقص المناعة. اللقاحات الميتة أقل تأثيرًا مقارنة باللقاحات الحية، وتُعطى عندما تكون الأجسام المضادة موجودة في الدم (على سبيل المثال، في الطفولة أو بعد الحصول على منتجات الدم المحتوية على الأجسام المضادة). الحصانة التي توفرها اللقاحات غير الحية عمومًا لا تدوم مثل اللقاحات الحية المضعفة. وتستخدم اللقاحات غير الحية للحماية ضد التهاب الكبد A، والإنفلونزا، وشلل الأطفال، وداء الكَلب.
- اللقاحات الفرعية، والجينية المعاد تكوينها والموحدة: تُستخدم في هذه اللقاحات قطع محددة من الجرثومة، مثل بروتينها أو سكرياتها أو كبسيدها (الغلاف الخارجي للجرثومة). ونظرًا إلى أن هذه اللقاحات تَستخدم فقط أجزاءً معينة من الجرثومة، فإنها توفر استجابة مناعية قوية جدًا وتَستهدف أجزاءً رئيسة من الجرثومة، ويمكن استخدامها للأشخاص الذين يعانون من أنظمة مناعية ضعيفة ومشاكل صحية طويلة الأمد. ومن القيود على هذه اللقاحات أنها قد تحتاج إلى لقاحات معززة للحصول على حماية دائمة ضد الأمراض، وتستخدم هذه اللقاحات للحماية ضد مرض الإنفلونزا النزلية النوع ب، والتهاب الكبد B، وفيروس الورم الحليمي البشري (Human Papillomavirus, HPV)، والسعال الديكي، ومرض الالتهاب الرئوي، والسل، والتهاب الدماغ والسحايا، والحزام الناري.
- لقاحات الحمض النووي الريبي المرسال (mRNA): يقومالحمض النووي الريبي المرسال بإنتاج بروتينات لتحفيز استجابة مناعية، ولها فوائد عديدة مقارنة بأنواع اللقاحات الأخرى، بما في ذلك قصر وقت التصنيع وتفادي خطر التسبب بأمراض للشخص المتلقي للتطعيم بسبب خلوه من الفيروس الحي، وتُستخدم هذه اللقاحات للحماية من
الكوفيد 19 (COVID -19).
- لقاحات الحمض النووي الريبي منقوص الأكسجين DNA: تتألف هذه اللقاحات من قطعة صغيرة دائرية من الحمض النووي تُسمى بلازميد، وتحمل الجينات التي تُشفر البروتينات من الكائن المسبب للمرض. إن عملية تصنيع اللقاحات الجينية DNA وطيدة، ما يسمح بتطوير اللقاحات التجريبية بسرعة لمعالجة الأمراض المعدية الناشئة أو المعاودة، إذ طوّر مركز أبحاث اللقاحات التابع للمعهد الوطني للحساسية والأمراض المعدية (National Institute of Allergy and Infectious Diseases, NIAID) لقاحات الحمض النووي لمعالجة العديد من الأمراض الفيروسية، مثل
فيروس السارس التاجي (SARS-CoV)، وإنفلونزا الطيور، وإنفلونزا الخنازيرH1N1، وفيروس زيكا[26].
المحفزات المناعية
المحفزات المناعية هي المواد التي تعدل استجابة الجهاز المناعي؛ إذ يمكن أن تعزز أو تثبط الجهاز المناعي، وتستخدم لعلاج مجموعة متنوعة من الحالات، مثل: الأمراض المناعية الذاتية، والعدوى، والأورام السرطانية. وتشمل الأنواع الرئيسة من المحفزات المناعية النشطة[27]:
- السيتوكينات (Cytokines): وهي جزيئات تنظم نضج الخلايا المناعية ونموها واستجابتها. يوجد حاليًا أربعة محفزات مناعية تعتمدها إدارة الغذاء والدواء الأمريكية (FDA) لعلاج مجموعات محددة من المرضى المصابين بسرطان الكلى، واللوكيميا (Leukemia)، واللمفوما (Lymphoma)، والميلانوما (Melanoma)، والسركوما (Sarcoma).
- الدسلوكين (Aldesleukin) (بروليوكين®، Proleukin®): سيتوكين يستهدف مسار الإنترلوكين IL-2/IL-2R؛ وهو مُعتمد لمجموعات محددة من المرضى المصابين بسرطان الكلى والميلانوما.
- عامل تحفيز مستعمرات الخلايا الحبيبية والبلعمية (Granulocyte-macrophage colony stimulating factor, GM-CSF): هو سيتوكين منظم مناعي؛ ومُعتمد لمجموعات محددة من المرضى المصابين بورم الخلايا العصبية النخاعي.
- إنترفيرون ألفا-2أ (Interferon alfa-2a): هو سيتوكين يستهدف مسار IFNAR1/2؛ وهو معتمد لمجموعات محددة من المرضى المصابين باللوكيميا والسركوما.
- إنترفيرون ألفا-2ب (Interferon alfa-2b) إنترون أ (Intron A®): سيتوكين يستهدف مسار IFNAR1/2؛ وهو مُعتمد لمجموعات محددة من المرضى المصابين باللوكيميا، واللمفوما، والميلانوما، والسركوما.
- بيغ إنترون سيلاترون (Sylatron®/PEG-Intron®)، (بيغ إنترفيرون-ألفا-2ب) (Peginterferon alfa-2): سيتوكين يستهدف مسار IFNAR1؛ وهو معتمد لمجموعات محددة من المرضى المصابين بالميلانوما.
- الأجسام المضادة وحيدة النسيلة (Monoclonal Antibodies): تعتمد علاجات الأجسام المضادة وحيدة الخلايا على نسخ مخبرية من الأجسام المضادة لمحاربة السرطان.
- مثبطات نقاط التحكم المناعية (Immune Checkpoint Inhibitors): تعمل مثبطات نقاط التحكم عن طريق حجب نقاط التحكم الناقلة للمناعة "الفرامل" التي تستخدمها الأورام مرارًا لإيقاف استجابات المناعة وحماية أنفسها. ونتيجة لذلك، تستطيع مثبطات نقاط التحكم أن تحرر استجابات مناعية جديدة ضد السرطان، إضافة إلى تعزيز الاستجابات الموجودة للمساعدة في القضاء على خلايا السرطان. وحتى عام 2020، اكتسبت مثبطات نقاط التحكم شهرةً ونجاحًا واسع الانتشار.
- الأتيزوليزوماب (Atezolizumab) (تنسينريك®) (®Tecentriq): مثبط نقطة التحكم الذي يستهدف مسار PD-1/PD-L1؛ وهو معتمد للمرضى المصابين بسرطان المثانة، وسرطان الثدي، وسرطان الكبد، وسرطان الرئة، والميلانوما، والسركوما.
- فيلوماب (Velumab) (بافينسيو أ®) (Bavencio A®): مثبط نقطة التحكم الذي يستهدف مسار PD-1/PD-L1؛ وهو معتمد للمصابين بسرطان المثانة، وسرطان الكلى، وسرطان الخلايا الظهارية العدائية.
- سيميبليماب (Cemiplimab) (ليبتايو®) (Libtayo®): مثبط نقطة التحكم الذي يستهدف مسار PD-1/PD-L1؛ وهو معتمد لعلاج سرطان الخلايا القرنية الجلدية، وسرطان الخلية القاعدية، وسرطان الرئة.
- دوستارليماب (Dostarlimab) (جيمبرلي®) (Jemperli®): مثبط نقطة التحكم الذي يستهدف مسار PD-1؛ وهو معتمد لمجموعات محددة من المرضى المصابين بسرطان الرحم.
- دورفالوماب (Durvalumab) (إيمفينزي®) (Imfinzi®): مثبط نقطة التحكم الذي يستهدف مسار PD-1/PD-L1؛ وهو معتمد للمرضى المصابين بسرطان المثانة، وسرطان الكبد، وسرطان الرئة.
- إبيليموماب (Ipilimumab) (ييرفوي®)(Yervoy®) : مثبط نقطة التحكم الذي يستهدف مسار CTLA-4؛ وهو معتمد للمرضى المصابين بميلانوما، والميزوثيليوما، وسرطان الكبد، وسرطان الرئة.
- نيفولوماب (Nivolumab) (أوبديفو®) (Opdivo®): مثبط نقطة التحكم الذي يستهدف مسار PD-1/PD-L1؛ وهو معتمد في حالات سرطان المثانة، وسرطان القولون والمستقيم، وسرطان المريء، وسرطان المعدة، وسرطان الرأس والعنق، وسرطان الكلى، وسرطان الكبد، وسرطان الرئة، واللمفوما، والميلانوما، والميزوثيليوما.
- بيمبروليزوماب (Pembrolizumab) (كيترودا®) (Keytruda®) : مثبط نقطة التحكم الذي يستهدف مسار PD-1/PD-L1؛ وهو معتمد للمصابين بسرطان المثانة، وسرطان الثدي، وسرطان عنق الرحم، وسرطان القولون والمستقيم، وسرطان الخلايا القرنية الجلدية، وسرطان المريء، وسرطان الرأس والعنق، وسرطان الكلى، وسرطان الكبد، وسرطان الرئة، واللمفوما، والميلانوما، وسرطان خلايا ميركل، وسرطان المعدة.
- ريلاتليماب (Relatlimab): مثبط نقطة التحكم الذي يستهدف مسار LAG-3؛ وهو جزء مكون من مزيج مع نيفوليماب (المعروفان معًا باسم أوبدوالاغ™)؛ وهو معتمد لمرضى الميلانوما.
- ريتيفانليماب (Retifanlimab®) (Zynyz®) )زينيز® (: مثبط نقطة التحكم الذي يستهدف مسار PD-1/PD-L1؛ وهو معتمد للمصابين بسرطان خلايا ميركل المتقدم.
- تريميليموماب (Tremelimumab) (إيمجودو®) (Imjudo®): مثبط نقطة التحكم الذي يستهدف مسار CTLA-4؛ وهو معتمد بوصفه جزءًا من مزيج مع دورفاليماب والعلاج الكيميائي لسرطان الكبد وسرطان الرئة[28].
العلاجات المثبطة للمناعة
تُستخدم مثبطات المناعة أو ما تسمى بكابتات المناعة لعلاج مجموعة متنوعة من الأمراض الالتهابية وأمراض المناعة الذاتية، أو تُقلل من الاستجابة المناعية الطبيعية لمنع رفض الأعضاء أو الخلايا المزروعة مثل الكورتيزون، وأدوية العلاج الكيماوي، والأجسام المضادة وحيدة النسيلة (Monoclonal Antibodies)[29].
العلاج المناعي للحساسية
عندما يواجه الجسم مسببًا للحساسية، تُفرز الخلايا البدينة (Mast cells) الهيستامين ومواد كيميائية أخرى سريعًا، ما يسبب أعراض الحساسية خلال 15 إلى 30 دقيقة، وتؤثر هذه الأعراض في العيون، والجلد، والجهاز التنفسي، وتفرز الخلايا البدينة أيضًا وسطاء يعملون على زيادة نفاذية الأوعية الدموية وتجذب خلايا المناعة الأخرى، ما يؤدي إلى موجة ثانية من الالتهاب بعد 6 إلى 12 ساعة، تشمل هذه المرحلة اللاحقة خلايا (CD4+) T، والخلايا القاعدية (Basophils)، والخلايا المحببة (Granulocytes)، والعدلات(Neutrophils) ، التي تفرِز مواد مختلفة تسبب تلف الأنسجة.
يعمل العلاج المناعي للحساسية عن طريق الحد من الاستجابات الحساسية المبكرة والمتأخرة، ويقمع استجابات الخلايا التائية المساعدة 2Th المدفوعة بالمسببات الحساسية، ما يقلل من مستويات الإنترلوكينات (IL-4, IL-5, IL-9, IL-13) ويحول الاستجابة المناعية نحو مسارات الخلايا التائية المساعدة Th1 (T helper cells, Th1) الواقية. وينشط العلاج خلايا الرقابة اللمفاوية (T regulatory cells) ويفرز IL-10 وTGF-β لقمع استجابات Th2 والمساعدة في تحويل أنماط الأجسام المناعية إلى IgG4 وIgA، ما يؤدي إلى زيادة مستويات IgA، IgG1، وIgG4، وتقليل IgE. ونتيجة لذلك، تُقلل عدد الخلايا المناعية التي تتسلل إلى الأنسجة، ويُحقق تقليل طويل الأمد في مستويات IgE الخاصة بالمسببات الحساسية في المصل، ما يقلل من الاستجابات في المرحلة المبكرة[30].
العلاج المناعي لمرضى زرع الأعضاء
يجب على المرضى الذين يتلقون زرعًا غريبًا أو نسيجًا أخذ عوامل مثبطة للمناعة لمنع أجسامهم من مهاجمة الأنسجة المزروعة، ويُعد التخفيض الطويل الأمد في نظام المناعة أمرًا حاسمًا لنجاح الزرع الغريب، ويتعين على علاج المثبطات المناعية أن تقمع الاستجابة المناعية للزرع الغريب انتقائيًّا مع السماح بالتعامل مع الاستجابات المناعية الأخرى بفاعلية.
ثمة ثلاث اعتبارات رئيسة لعلاجات مثبطات المناعة، وهي: ضمان ما يكفي من التثبيط المناعي لحماية العضو المزروع من الهجوم المناعي، والحفاظ على حملة منخفضة للتثبيط المناعي الكلي بحيث يمكن للجهاز المناعي محاربة العدوى واكتشاف خلايا الأورام، إضافة إلى استخدام مثبطات المناعة ذات الآليات المكملة لتعزيز الفاعلية وتقليل التأثيرات السامة[31].
تستهدف الأدوية المثبطة للمناعية، بخلاف الكورتيكوستيرويدات، نقاطًا محددة في مسارات تنشيط الخلايا T وB، لمنع رفض الزرع الغريب، ومن الأمثلة على ذلك:
- سيكلوسبورين أ (Cyclosporin) وتاكروليموس (Tacrolimus): يمنعان تكرار السيتوكينات.
- أزاثيوبرين (Azathioprine) وميكوفينولات الموفيتيل (Mycophenolate mofetil) اللذان يعيقان تخليق النوكليوتيدات.
- داكليزوماب (Daclizumab) وبازيليكسيماب (Basiliximab): يحظران تحفيز IL-2لمستقبلات IL-2 في خلايا T.
- سيروليموس (Sirolimus): يعيق نقل إشارة عامل النمو.
- الكورتيكوستيرويدات (Corticosteroids): تؤثر الكورتيكوستيرويدات في جميع مراحل الاستجابات الالتهابية والمناعية؛ بسبب وجود مستقبلات الكورتيكوستيرويدات الواسعة الانتشار، ووجِد أنها تعطل عرض الأجسام المضادة، وتمنع إنتاج السيتوكينات، وكذلك تعيق انقسام الخلايا اللمفاوية أيضًا. وإن إعطاء الكورتيكوستيرويدات يؤدي إلى تقليل عدد الخلايا اللمفاوية، والخلايا الأحادية، والخلايا القاعدية، ولكنه يزيد عدد خلايا العدلات[32].
العلاج المناعي للأمراض المناعية الذاتية
يمكن أن تؤدي اضطرابات الجهاز المناعي إلى نشاط زائد أو نشاط غير كاف، أما النشاط الزائد فإنه يؤدي إلى الأمراض المناعية الذاتية، إذ يهاجم الجهاز المناعي أنسجة الجسم بدلًا من محاربة العدوى.
في التهاب المفاصل الروماتويدي، تستهدف الأجسام المضادة بطانات المفاصل، ما يسبب الألم والالتهاب. تبدأ العلاجات بمضادات الالتهاب غير الستيرويدية ((NSAIDs, Non-steroidal Anti-inflammatory Drugs، وقد تتقدم إلى الأدوية المضادة للروماتيزم المعدلة للمرض ((Disease Modifying Antirheumatic Drugs, DMARDs مثل الميثوتريكسيت، أما إذا فشلت (DMARDs) فقد يقوم العلاج المثبط للمناعة بحجب استجابات الالتهاب المناعي، مثل: أباتاسيبت (Abatacept)، وريتوكسيماب Aituximab))، وإيتانيرسبت ((Etanercept.
أما
أمراض الأمعاء الالتهابية (Inflammatory bowel diseases) فإنها تشمل غالبًا العلاجات الأولية: أمينوساليسيلات (Aminosalicylates) مثل السلفازالازين (Sulfasalazine) لتخفيف الأعراض، وقد تستخدم الستيرويدات الكورتيكوستيرويدية ((Steroids Corticosteroids أيضًا، ولكنها غير مثالية للاستخدام على المدى الطويل؛ بسبب الآثار الجانبية. وفي حالات أكثر حدة، قد يكون العلاج المثبط للمناعة ضروريًّا، فتستهدف هذه الأدوية، مثل السيكلوسبورين (Cyclosporine)، والأزاثيوبرين (Azathioprine)، والإنفليكسيماب Infliximab)) الاستجابة المناعية التي تسبب الالتهاب في بطانة الأمعاء، وقد يكون العلاج المتكامل مفيدًا لبعض الأفراد[33].
تعزيز جهاز المناعة
يؤدي جهاز المناعة دورًا مهمًّا في الدفاع عن الإنسان ضد الكائنات الحية الدقيقة المسببة للأمراض. ومع ذلك، قد يفشل أحيانًا، إذ تغزو البكتيريا الإنسان أو الحيوان بنجاح وتجعله مريضًا.
تُعد فكرة تعزيز جهاز المناعة مهمة، ولكن القدرة على تحقيق ذلك تبدو بعيدة المنال؛ إذ أن جهاز المناعة هو نظام معقد يتطلب التوازن والانسجام، وليس كيانًا بسيطًا يمكن تعديله بسهولة. ومع ذلك، لا يعني هذا أن تأثيرات نمط الحياة في الجهاز المناعي ليست مهمة أو لا تستحق الدراسة، فالعلماء يبحثون تأثيرات النظام الغذائي، وممارسة الرياضة، والعمر، والإجهاد النفسي، وعوامل أخرى في الاستقرار المناعي لدى الحيوانات والبشر.
تشير بعض الأدلة التجريبية إلى أن نقص بعض المغذيات الدقيقة، مثل الزنك، والسيلينيوم، والحديد، والنحاس، وحمض الفوليك، وفيتامينات أ، ب6، ج، يمكن أن يؤثر في الاستجابات المناعية؛ لذلك، يُعد تعزيز الجهاز المناعي من خلال التغذية الجيدة علاجًا مهمًا لتقوية جهاز المناعة[34].
لقد برز العلاج المناعي بوصفه منهجًا رائدًا في الطب الحديث، إذ يقدم علاجات مستهدفة لمختلف الحالات المرتبطة بالمناعة، ويؤدي الخوض في هذه الجوانب إلى فهم شامل للدور المحوري الذي يؤديه جهاز المناعة في الصحة والمرض، وإن البحث المستمر والتقدم في العلاج المناعي يبشر بعلاجات أكثر فاعلية، ما يمهد الطريق إلى تحسين النتائج الصحية وتحسين نوعية الحياة للمرضى في جميع أنحاء العالم.
المراجع
Abbas, Abdul K., Andrew H. Lichman & Shiv Pillai.
Cellular and Molecular Immunology. HBJ International edition. Philadelphia: Saunders, 1991.
Ahmad, Hafiz Ishfaq et al. “Immune Tolerance vs. Immune Resistance: The Interaction Between Host and Pathogens in Infectious Diseases.”
Frontiers in Veterinary Science. vol. 9, article no. 827407 (2022).
Alberts, Bruce et al. “From DNA to RNA.” in: Bruce Alberts et al.
Molecular Biology of the Cell. 4th ed. New York: Garland Science, 2002. at: https://acr.ps/1L9F2kD
Bluestone, Jeffrey A. & Abul K. Abbas. “Natural Versus Adaptive Regulatory T Cells.”
Nature Reviews Immunology. vol. 3, no. 3 (2003), pp. 253-257.
Dinarello, Charles A. “Overview of the IL‐1 Family in Innate Inflammation and Acquired Immunity.”
Immunological Reviews. vol. 281, no. 1 (2018). pp. 8-27.
Disis, Mary L. “Mechanism of Action of Immunotherapy.”
Seminars in Oncology. vol. 41, suppl. 5 (2014). pp. S3-S13.
Felippe, M. Julia B. (ed.).
Equine Clinical Immunology. Chichester: Wiley Blackwell, 2015.
Fulton, Kelly M. & Susan M. Twine (eds.).
Immunoproteomics: Methods and Protocols. vol. 2024. 2nd ed. New York: Humana, 2019.
Hussain, Yaseen & Haroon Khan. “Immunosuppressive Drugs.”
Encyclopedia of Infection and Immunity. vol. 4 (2022). pp. 726-740.
Iwasaki, Akiko & Ruslan Medzhitov. “Control of Adaptive Immunity by the Innate Immune System.”
Nature Immunology. vol. 16, no. 4 (2015). pp. 343-353.
Janeway, Charles A. et al.
Immunobiology - The Immune System in Health and Disease. 5th ed. New York: Garland Science, 2001.
Marshall, Jean S. et al. “An Introduction to Immunology and Immunopathology.”
Allergy, Asthma & Clinical Immunology, vol. 14, suppl. 2 (2018).
Nicholson, Lindsay B. “The Immune System.”
Essays in Biochemistry. vol. 60, no. 3 (2016). pp. 275-301.
Pagliari, Sthefany et al. “DNA Vaccines: History, Molecular Mechanisms and Future Perspectives.”
Journal of Molecular Biology. vol. 435, no. 23, article no. 168297 (2023).
Pardoll, Drew M. “The Blockade of Immune Checkpoints in Cancer Immunotherapy.”
Nature Reviews Cancer. vol. 12, no. 4 (2012). pp. 252-264.
Romo, Mario Riera, Dayana Pérez-Martínez & Camila Castillo Ferrer. “Innate Immunity in Vertebrates: An overview.”
Immunology, vol. 148, no. 2 (2016). pp. 125-139.
Shoenfeld, Yehuda & Eric M. Gershwin.
Cancer and Autoimmunity. Amsterdam: Elsevier, 2000.
William B. Grant, “Vitamins and Minerals,”
Reference Module in Life Sciences (2022).
[1] Hafiz Ishfaq Ahmad et al., “Immune Tolerance vs. Immune Resistance: The Interaction Between Host and Pathogens in Infectious Diseases,”
Frontiers in Veterinary Science,
vol. 9, article no. 827407 (2022).
[2] Jean S. Marshall et al., “An Introduction to Immunology and Immunopathology,”
Allergy, Asthma & Clinical Immunology,
vol.
14, suppl. 2 (2018).
[3] Scott McComb et al., “Introduction to the Immune System,” in: Kelly M. Fulton & Susan M. Twine (eds.),
Immunoproteomics: Methods and Protocols, vol. 2024, 2nd ed. (New York: Humana, 2019); Charles A. Janeway et al.,
Immunobiology - The Immune System in Health and Disease, 5th ed. (New York: Garland Science, 2001).
[4] Mario Riera Romo, Dayana Pérez-Martínez & Camila Castillo Ferrer, “Innate Immunity in Vertebrates: An overview,”
Immunology,
vol.
148, no. 2 (2016), pp. 125-139.
[5] Ibid.; Bruce Alberts et al., “From DNA to RNA,” in: Bruce Alberts et al., Molecular Biology of the Cell, 4th ed. (New York: Garland Science, 2002), at:
https://acr.ps/1L9F2kD
[6] Mario et al.; Akiko Iwasaki & Ruslan Medzhitov, “Control of Adaptive Immunity by the Innate Immune System,”
Nature Immunology, vol. 16, no. 4 (2015), pp. 343-353.
[7] Iwasaki & Medzhitov; Abdul K. Abbas, Andrew H. Lichman & Shiv Pillai,
Cellular and Molecular Immunology, HBJ International edition (Philadelphia: Saunders, 1991), pp. 226-242.
[8] McComb et al.; Lindsay B. Nicholson, “The Immune System,”
Essays in Biochemistry, vol. 60, no. 3 (2016), pp. 275-301.
[9] Ibid.
[10] Iwasaki & Medzhitov.
[11] Mario et al.
[12] Ibid.
[13] Ibid
[14] Iwasaki & Medzhitov.
[15] Nicholson.
[16] Ibid.; Iwasaki & Medzhitov.
[17] Jeffrey A. Bluestone & Abul K. Abbas, “Natural Versus Adaptive Regulatory T Cells,”
Nature Reviews Immunology, vol. 3, no. 3 (2003), pp. 253-257.
[18] Nicholson; Mary L. Disis, “Mechanism of Action of Immunotherapy,”
Seminars in Oncology,
vol. 41, suppl. 5 (2014), pp. S3-S13.
[19] Yehuda Shoenfeld & Eric M. Gershwin,
Cancer and Autoimmunity (Amsterdam: Elsevier, 2000).
[20] Disis.
[21] Yaseen Hussain & Haroon Khan, “Immunosuppressive Drugs,”
Encyclopedia of Infection and Immunity, vol. 4 (2022), pp. 726-740.
[22] Marshall et al.
[23] Disis; Hussain & Khan.
[24] Ahmad et al.
[25] Noah D. Cohen & Angela I. Bordin, “Principles of Vaccination,” in: M. Julia B. Felippe (ed.),
Equine Clinical Immunology(Chichester: Wiley Blackwell, 2015), pp. 263-278.
[26] Sthefany Pagliari et al., “DNA Vaccines: History, Molecular Mechanisms and Future Perspectives,” Journal of Molecular Biology, vol. 435, no. 23, article no. 168297 (2023).
[27] Disis; Drew M. Pardoll, “The Blockade of Immune Checkpoints in Cancer Immunotherapy,”
Nature
Reviews Cancer, vol. 12, no. 4 (2012), pp. 252-264.
[28] Charles A. Dinarello, “Overview of the IL‐1 Family in Innate Inflammation and Acquired Immunity,” Immunological Reviews, vol. 281, no. 1 (2018), pp. 8-27.
[29] Hussain & Khan.
[30] Marshall et al.
[31] Hussain & Khan.
[32] Disis; Hussain & Khan.
[33] Bluestone & Abbas; Hussain & Khan.
[34] William B. Grant, “Vitamins and Minerals,”
Reference Module in Life Sciences (2022).