المثبط الإنزيمي (Enzyme Inhibitor) هو مركب كيميائي يؤثر في حركية التفاعلات البيوكيميائية بخفض سرعتها أو إيقافها كليًا، وذلك عبر تداخله مع آلية التفاعل أو مع
الموقع النشط {{الموقع النشط: منطقة محددة في الإنزيم ترتبط فيها جزيئات الركيزة وتخضع لتفاعل كيميائي، غالبًا من خلال ترتيبات دقيقة للأحماض الأمينية التي تحفز التفاعل الكيميائي.}} للإنزيم أو مواقع ارتباط أخرى عليه. تُقسَّم المثبطات الإنزيمية إلى مثبطات عكوسة، يمكن عكس تأثيرها بإزالة المثبط أو بتغيير شروط التفاعل، ومثبطات غير عكوسة، تُحدث ارتباطًا دائمًا أو تعديلًا كيميائيًا ثابتًا. تؤدي المثبطات دورًا محوريًا في تنظيم النشاط الإنزيمي والتحكم في العمليات الحيوية، إذ يمكنها تعديل سرعة التفاعلات أو إيقافها مؤقتًا أو دائمًا حسب طبيعتها.
يشمل التثبيط أنماطًا مختلفة مثل التثبيط التنافسي، واللاتنافسي، والمختلط، والتثبيط الانتحاري، مع اختلاف تأثير كل نمط على الثوابت الحركية للإنزيم.
ويمثل فهم البنية الجزيئية وآليات التثبيط أساسًا لتفسير انتقائية المثبطات وكفاءتها، وهي حجر الزاوية في تصميم أدوية دقيقة وفعّالة. كما تُعدّ المثبطات أدوات أساسية في البحث العلمي لفهم وظيفة البروتينات والمسارات الخلوية، وتطبيقاتها العلاجية واسعة، بدءًا من ضبط ضغط الدم إلى مكافحة السرطان.
تكتسب المثبطات أهمية تطبيقية واسعة في مجالات
الكيمياء الصناعية والصيدلة والتكنولوجيا الحيوية، وحماية المواد من التآكل، وتنظيم العمليات الحيوية. ومع تقدم التقنيات البنيوية والحاسوبية، تزداد قدرة العلماء على تصميم مثبطات أكثر انتقائية ودقة، ما يعزز من دورها في الطب الدقيق والعلاجات الموجهة، ويجعلها عنصرًا أساسيًا في مستقبل العلوم البيولوجية والكيميائية الحيوية.
التعريف العام
المُثبِّطات الإنزيمية هي جزيئات أو أيونات تُقلِّل نشاط جزيئات حيوية أخرى أو توقفه، وغالبًا ما تؤثر في البروتينات الوظيفية، لا سيما الإنزيمات، ما يؤثر في قدرتها على تحفيز
التفاعلات الحيوية. يتحقق هذا التأثير من خلال ارتباط المثبط بالموقع النشط (Active Site) أو بمواقع تنظيمية أخرى، ما يغيّر البنية الفراغية أو الديناميكية الجزيئية للبروتين. تؤدي المثبطات دورًا محوريًا في تنظيم العمليات الحيوية داخل الخلية، إذ تُسهم في ضبط سرعة
المسارات الأيضية، ودعم
الاستتباب (Homeostasis)، ومنع التفاعلات غير المرغوبة أو المفرطة. كما تُعدّ آلية أساسية في التحكم الخلوي، إذ تسمح للخلايا بالاستجابة السريعة للتغيرات البيئية أو الفيزيولوجية. تُعدّ دراسة المثبطات أداة أساسية في
الكيمياء الحيوية لفهم آليات عمل الإنزيمات وتحديد وظائفها بدقة، إضافةً إلى أهميتها التطبيقية في مجالات
الطب والصيدلة، إذ يعتمد العديد من الأدوية على مبدأ التثبيط الانتقائي لنشاط إنزيمات أو بروتينات مستهدفة[1].
أساسه وآلياته البنيوية
تعتمد آلية التثبيط الجزيئي بشكل مباشر على البنية الفراغية لكلٍّ من المثبط والبروتين الهدف، إذ يُحدِّد التركيب ثلاثي الأبعاد طبيعة الارتباط وقوته وانتقائيته. تمتلك البروتينات، وخصوصًا الإنزيمات، مواقع ارتباط محددة صُممت بنيويًا لاستقبال
الركائز (Substrates) أو الجزيئات المنظمة، ويؤدي ارتباط المثبط بهذه المواقع إلى إعاقة الوظيفة التحفيزية أو التنظيمية للبروتين[2]. يُثبَّط نشاط الإنزيمات عبر آليات بنيوية وكيميائية متعددة يمكن تصنيفها بصورة عامة إلى تثبيط عكوس (Reversible inhibition) وتثبيط غير عكوس (Irreversible inhibition)، ويختلف تأثير كلٍّ منهما تبعًا لطبيعة ارتباط المثبط بالإنزيم. في التثبيط العكوس، يرتبط المثبط بالإنزيم بروابط غير تساهمية ضعيفة نسبيًا، مثل
الروابط الهيدروجينية أو
التآثرات الكهروستاتيكية، ما يسمح بانفصال المثبط عند إزالة ظروف التثبيط[3].
في المقابل، يتميز التثبيط غير العكوس بارتباط المثبط بالإنزيم ارتباطًا قويًا ودائمًا، غالبًا عبر
روابط تساهمية مع
مجموعات وظيفية أساسية في الموقع النشط، مثل مجموعات
الهيدروكسيل، أو
الأمين، أو السلفهيدريل. يؤدي هذا الارتباط إلى تعطيل دائم للنشاط التحفيزي للإنزيم، ولا يمكن عكسه بزيادة تركيز الركيزة أو إزالة المثبط. ومن أبرز أمثلة هذا النوع المثبطات الانتحارية (Suicide inhibitors)، إذ يعمل المثبط في البداية بوصفه ركيزةً طبيعيةً، ثم يتحول أثناء التفاعل التحفيزي إلى ناتج تفاعلي يرتبط تساهميًا بالإنزيم ويُثبطه ذاتيًا. كما قد يحدث التثبيط غير العكوس نتيجة التعرض لمركبات كيميائية سامة، أو
أيونات معادن ثقيلة، أو ظروف فيزيائية قاسية تؤدي إلى تشوه البنية البروتينية (Denaturation) وفقدان الإنزيم لوظيفته[4]. وبذلك، يعتمد نوع التثبيط وتأثيره البيوكيميائي على طبيعة التفاعل بين المثبط والإنزيم، سواء كان ارتباطًا عكوسًا يؤثر مؤقتًا في النشاط التحفيزي، أو تثبيطًا غير عكوس يؤدي إلى فقدان دائم لوظيفة الانزيم.
أنواع التثبيط
التثبيط العكوس
التثبيط العكوس هو نوع من التثبيط الإنزيمي يتميز بقدرة المثبط على الارتباط بالإنزيم ارتباطًا غير دائم، قابلًا للفك بحسب
ألفة (Affinity) الإنزيم للمثبط. يمكن للإنزيم استعادة نشاطه التحفيزي عند إزالة المثبط، أو عند تغيير الظروف الفيزيائية أو الكيميائية. يعتمد هذا النمط على تآثرات غير تساهمية تسمى قوى ڤان دير ڤالز (Van Der Waals Forces)، مثل
الروابط الهيدروجينية (Hydrogen bonds) والتآثرات الكهروستاتيكية (Electrostatic interaction) والتآثرات الكارهة للماء (Hydrophobic interactions). للتثبيط العكوس دور رئيس في تنظيم النشاط الإنزيمي بشكل عام والتحكم في سرعة وتدفق المسارات الأيضية داخل الخلايا[5]. ينقسم التثبيط العكوس إلى ثلاثة أنواع رئيسة: التثبيط التنافسي (Competitive inhibition)، والتثبيط اللاتنافسي (Uncompetitive inhibition)، والتثبيط المختلط (Mixed inhibition).
التثبيط التنافسي
التثبيط التنافسي هو نمط من التثبيط العكوس يتنافس فيه المثبط مع الركيزة على الارتباط بالموقع النشط للإنزيم. يرتبط المثبط فقط بالإنزيم الحر (E). يمكن أن يكون التنافس مباشرًا على نفس المنطقة من الموقع النشط، أو ناتجًا من تداخل جزئي في مواقع الارتباط، أو عن إعاقة فراغية تمنع ارتباط الركيزة والمثبط في الوقت نفسه (الشكل 1). من الناحية الحركية، يؤدي التثبيط التنافسي إلى زيادة
ثابت ميكاليس ((Km، في حين تبقى
السرعة العظمى ((Vmax من دون تغيير[6]. بحسب قوة المثبط، فإن ثابت ميكاليس يزيد بمقدار كمية تُسمّى ألفا، بحيث تساوي 1 + نسبة تركيز المثبط إلى ثابت اتزان التثبيط (Ki) (الشكل 2). كلما زادت ألفا، زادت قيمة ثابت ميكاليس الظاهرية وزادت قوة التثبيط. ينعكس هذا التثبيط بزيادة تركيز الركيزة، إذ تتنافس مع المثبط وتزيحه من الموقع النشط.
[الشكل1]
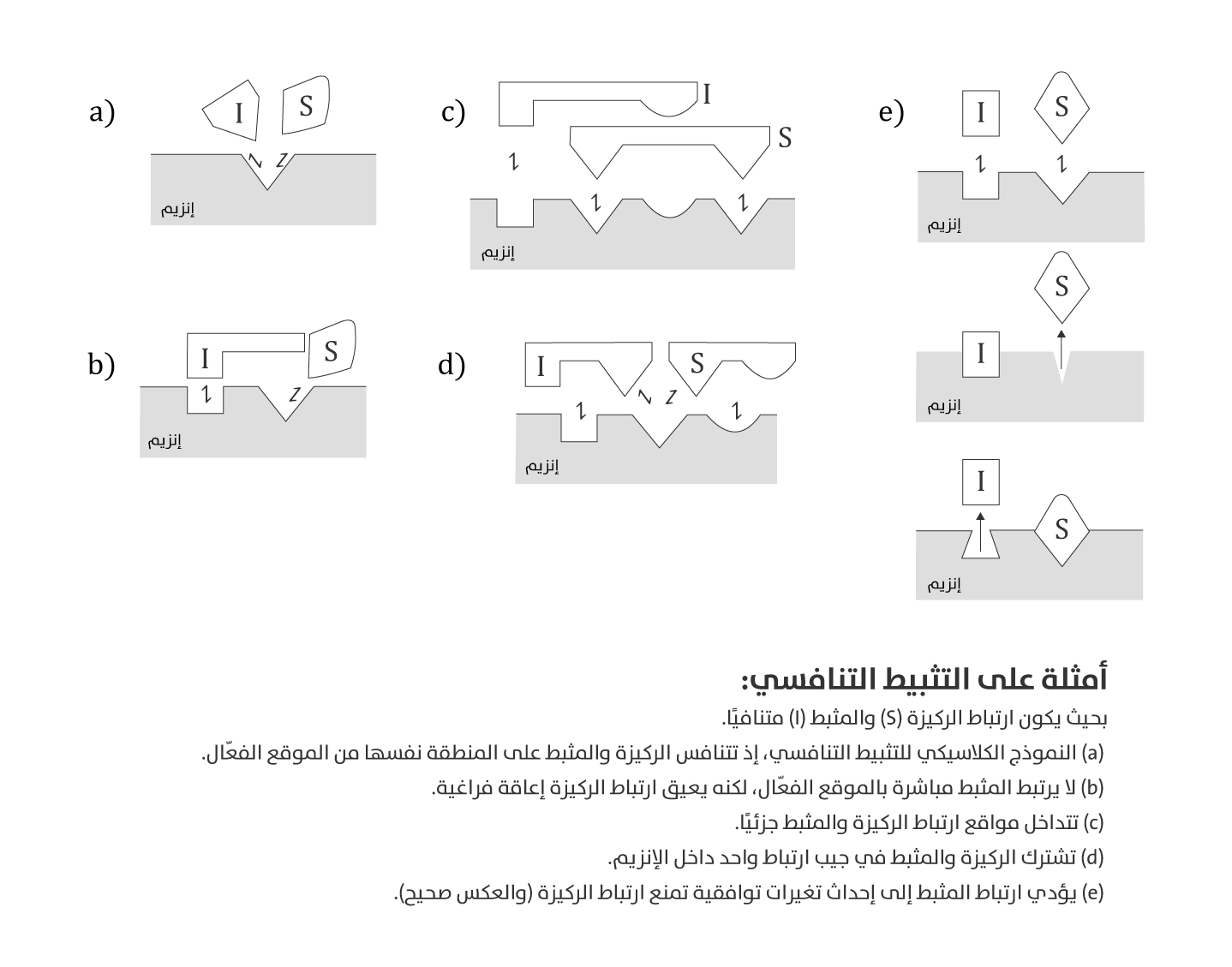 أمثلة على التثبيط التنافسي
أمثلة على التثبيط التنافسي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل 2]
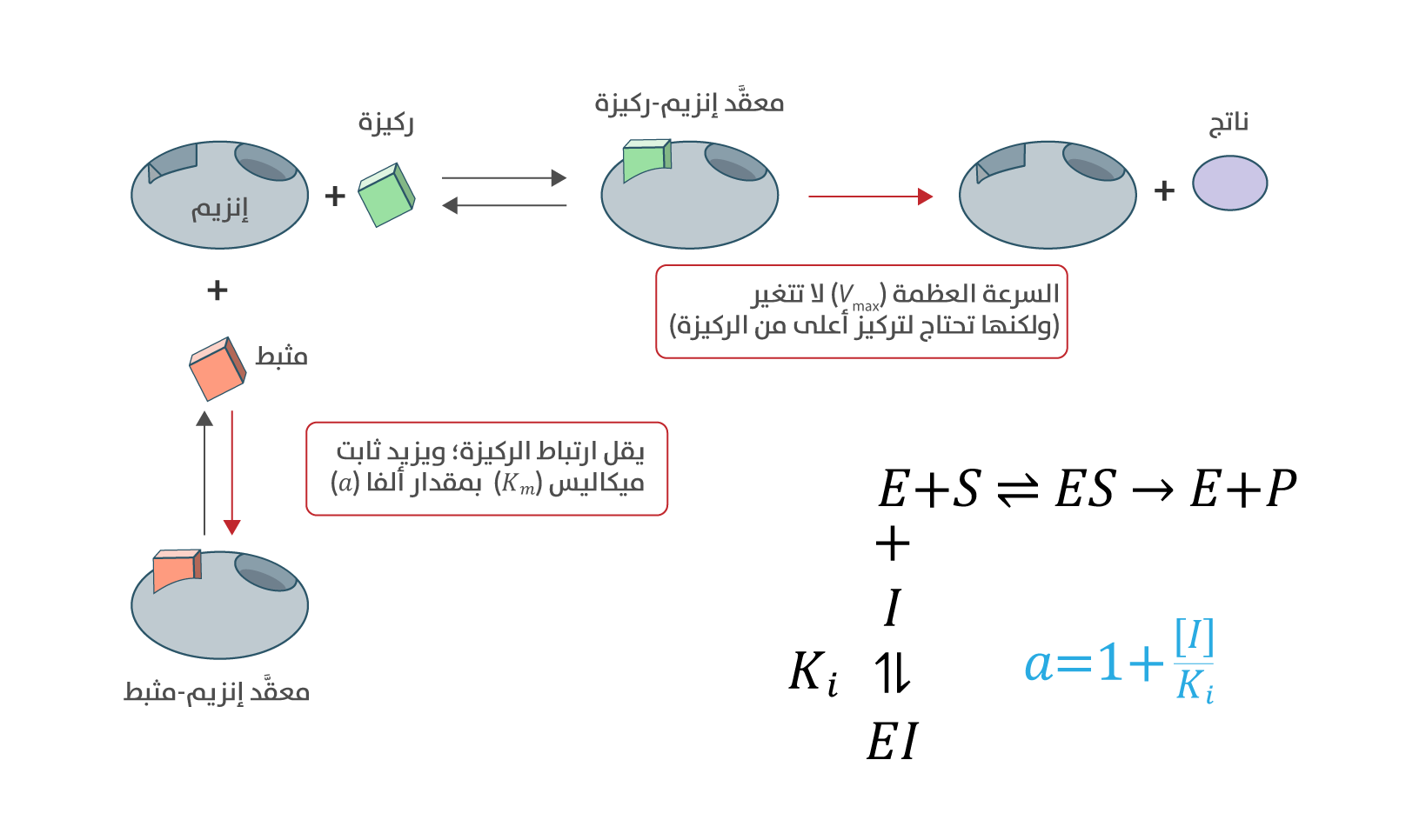 التثبيط التنافسي
التثبيط التنافسي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
التثبيط اللاتنافسي
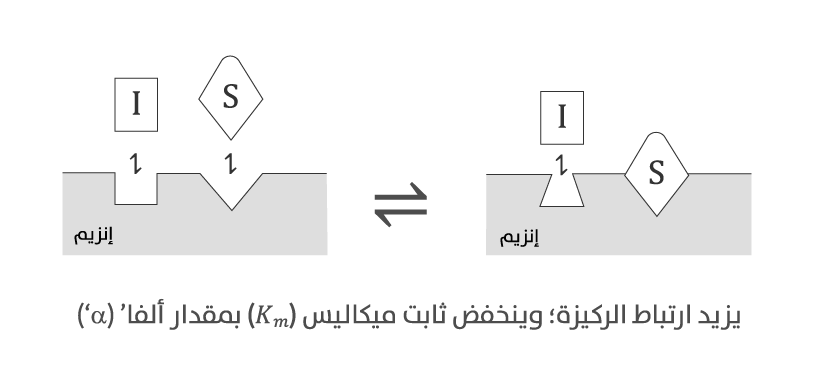
التثبيط اللاتنافسي (Uncompetitive inhibition) هو تثبيط إنزيمي قابل للعكوس، يختلف عن التثبيط التنافسي بأن المثبط يرتبط فقط بمعقّد الإنزيم - الركيزة (ES complex)، وليس بالإنزيم الحر، مُكوّنًا معقّدًا بين الإنزيم والركيزة والمثبط (ESI complex)، وهذا المعقد غير نشط، ما يقلل كلًا من سرعة التفاعل العظمى (Vmax) وثابت ميكاليس (Km) معًا بحسب قوة المثبط. تنخفض القيمتان بمقدار كمية تسمى ألفا'، بحيث تساوي 1 + نسبة تركيز المثبط إلى ثابت اتزان التثبيط (K’i) (الشكل 3). كلما زادت ألفا'، قلت قيمتا ثابت ميكاليس الظاهرية والسرعة العظمى. يُلاحظ أن هذا النوع من التثبيط لا ينعكس بزيادة تركيز الركيزة، وإنما يزداد التثبيط مع زيادة تركيز الركيزة.
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل 4]
 أمثلة على التثبيط غير التنافسي
أمثلة على التثبيط غير التنافسي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
التثبيط المختلط
في التثبيط المختلط يرتبط المثبط بموقع مختلف عن الموقع النشط، سواء أكان الإنزيم حرًا أم مرتبطًا بالركيزة، فيرتبط المثبط بالإنزيم الحر (تكون له مقدار ألفا) أو بمعقد الإنزيم - الركيزة (تكون له مقدار ألفا')، فهو بالتالي له خصائص من التثبيط التنافسي واللاتنافسي. يؤدي هذا الارتباط إلى انخفاض الكفاءة التحفيزية للإنزيم من دون منافسة مباشرة على الموقع النشط. من الناحية الحركية، تنخفض السرعة العظمى للإنزيم، في حين من الممكن أن تزيد قيمة ثابت ميكاليس أو تقل بحسب قيم ألفا و ألفا'. وفي حالة خاصة، عندما تكون قيمة ألفا تساوي قيمة ألفا' بقيمة أكبر من 1، تنخفض السرعة العظمى، في حين تبقى قيمة ثابت ميكاليس من دون تغيير. تُسمى هذه الحالة الخاصة من التثبيط المختلط التثبيط غير التنافسي (Non-competitive inhibition).
[الشكل 5]
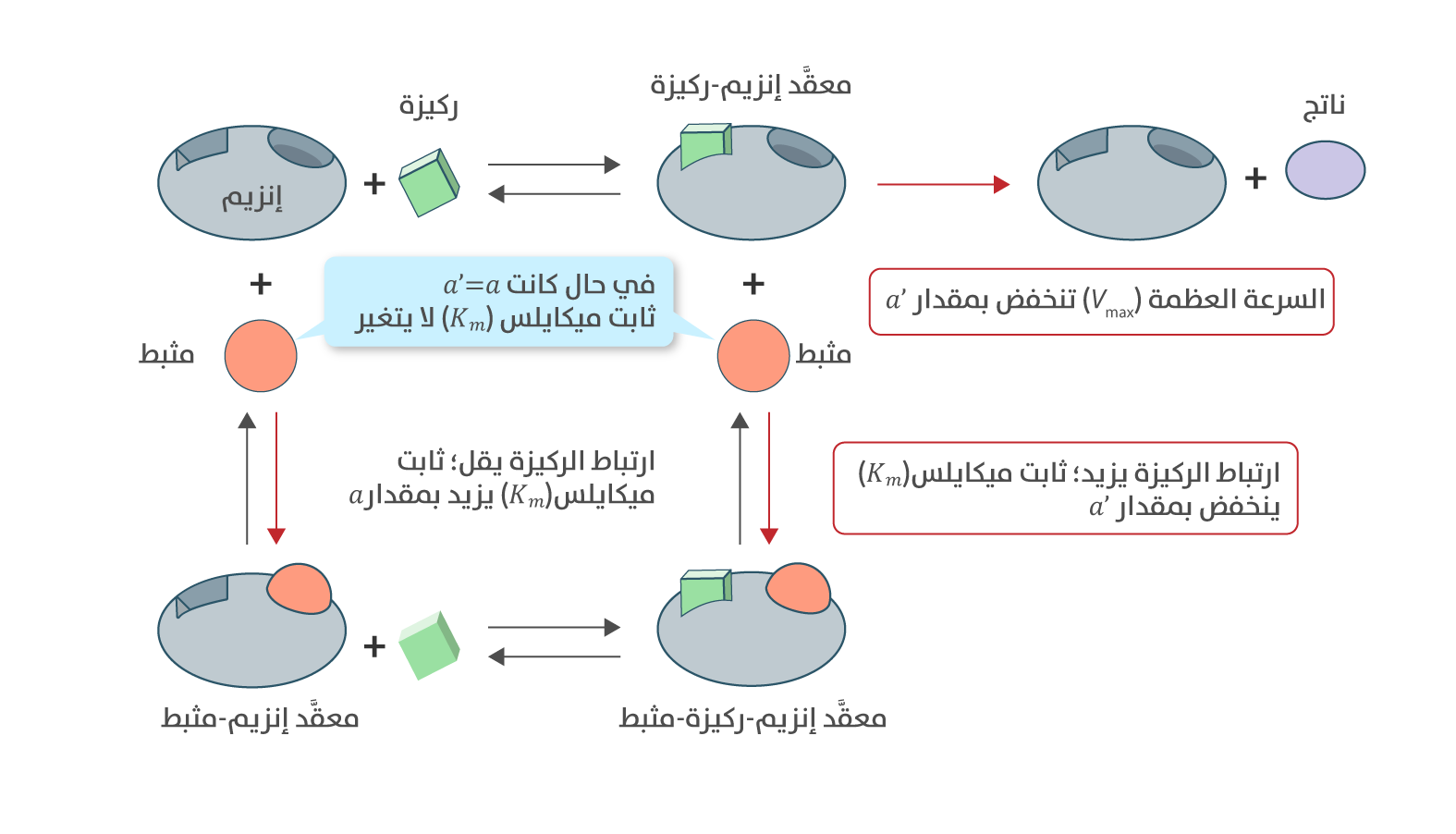 التثبيط المختلط
التثبيط المختلط
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل 6]
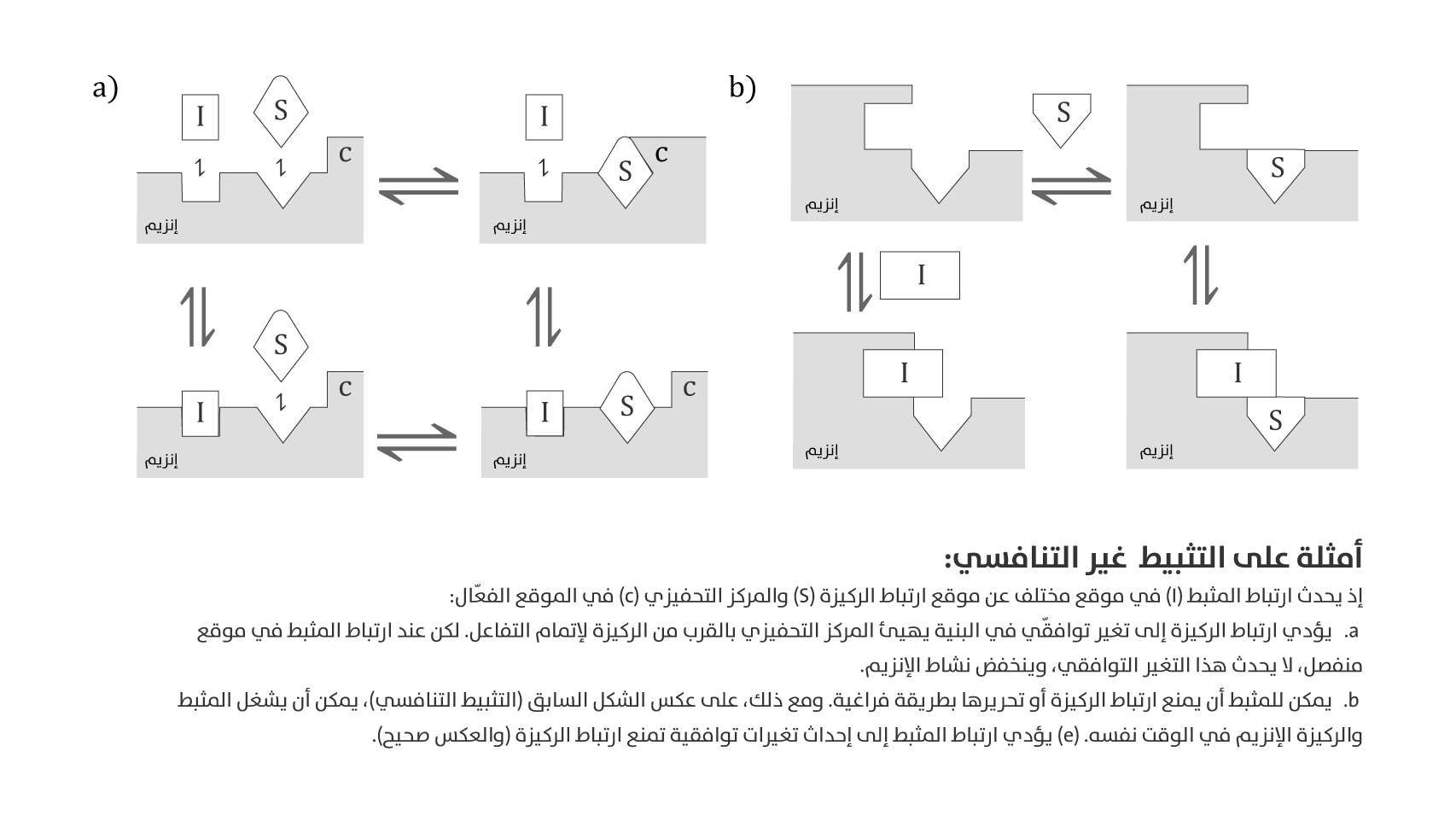 أمثلة على التثبيط غير التنافسي
أمثلة على التثبيط غير التنافسي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
التثبيط غير العكوس
التثبيط غير العكوس هو نمط من التثبيط الإنزيمي يؤدي إلى فقدان دائم أو شبه دائم لنشاط الإنزيم نتيجة ارتباط قوي بين المثبط والإنزيم، غالبًا عبر تعديل تساهمي (Covalent modification) لمواضع حاسمة في الموقع النشط أو في مواقع أخرى مهمة في بنية الإنزيم. وبخلاف التثبيط العكوس[7]، لا يكفي إزالة المثبط لاستعادة النشاط، وقد يستلزم الأمر تصنيع إنزيمات جديدة لاستعادة الوظيفة.
قد يحدث التعديل التساهمي عندما يتفاعل المثبط مع مجموعات وظيفية نشطة في الإنزيم، مثل مجموعات
الكبريت في بعض
الأحماض الأمينية أو مجموعات
الهيدروكسيل في أخرى، ما قد يؤدي إلى إيقاف التحفيز مباشرة. يتميز هذا النوع من التثبيط بدرجة عالية من الخصوصية البنيوية، إذ يعتمد على التوافق الكيميائي والفراغي بين المثبط والإنزيم المستهدف[8].
المثبطات الانتحارية
تُعدّ المثبطات الانتحارية، أو المثبطات المعتمدة على الآلية، فئةً خاصةً من المثبطات غير العكوسة، إذ يحوِّل الإنزيم المثبط أثناء التفاعل إلى شكل تفاعلي عالي النشاط قبل تثبيطه بشكل تام. يرتبط الشكل التفاعلي الناتج تساهميًا بالإنزيم، ما يؤدي إلى تعطيله. تكتسب هذه المثبطات أهميةً خاصةً في تصميم الأدوية نظرًا لانتقائيتها العالية واعتمادها على آلية التحفيز الخاصة بالإنزيم الهدف، ويُعدّ
البنسيلين مثالًا كلاسيكيًا على ذلك، إذ يعمل بوصفه مثبطًا انتحاريًا لإنزيم
الترانسبيبتيداز المسؤول عن بناء
جدار الخلية البكتيرية؛ إذ يتعامل الإنزيم مع البنسيلين بوصفه ركيزةً، ثم يتحول أثناء التفاعل إلى وسيط تفاعلي يرتبط تساهميًا بالإنزيم، ما يؤدي إلى تثبيطه ومنع تكوين الجدار.
تطبيقات المثبطات
تُستخدم المثبطات على نطاق واسع في البحث العلمي، لا سيما في مجالات
البيولوجيا الجزيئية والكيمياء الحيوية، لدراسة وظيفة البروتينات وتحديد دورها في المسارات الخلوية المعقّدة. يتيح التثبيط الانتقائي تعطيل نشاط إنزيم أو مستقبِل معيّن بصورة مضبوطة، ما يساعد على تفسير الأثر الناتج واستنتاج العلاقات السببية داخل الشبكات التنظيمية الخلوية، كما يُستخدم لفهم الآليات التحفيزية للإنزيمات والتحقق التجريبي من النماذج البنيوية والآلية المقترحة[9].
أما من منظور علاجي، فتمثل المثبطات مبدأً محوريًا في تطوير الاستراتيجيات الدوائية الحديثة، إذ يُبنى كثير من التدخلات العلاجية على خفض أو إيقاف نشاط أهداف جزيئية مرتبطة بحالات مرضية محددة، مع الحفاظ قدر الإمكان على الوظائف الفيزيولوجية السليمة[10]. ومن الأمثلة البارزة:
- إينالابريل (Enalapril): مثبط إنزيم تحويل الأنجيوتنسين (Angiotensin-converting enzyme - ACE) يُستخدم لخفض ضغط الدم، ويُعدّ مثالًا على التثبيط التنافسي.
- تاموكسيفين (Tamoxifen): يرتبط بمستقبلات
الإستروجين ويُستخدم في علاج بعض أنواع
سرطان الثدي، ويظهر مبدأ التثبيط اللاتنافسي أو التغايري بشكل انتقائي من دون إيقاف كامل للوظيفة الطبيعية في الأنسجة الأخرى.
يسهم التقدم في فهم الأسس البنيوية والآلية للتثبيط في تحسين انتقائية المثبطات وتقليل آثارها غير المرغوبة، ما عزز دورها في الطب الدقيق والعلاجات الموجهة.
ويرتكز اكتشاف المثبطات وتصميمها على فهم عميق للعلاقة بين البنية الجزيئية والوظيفة الحيوية للأهداف، ولا سيما الإنزيمات والبروتينات التنظيمية. تقليديًا، اعتمد اكتشاف المثبطات على فحص تجريبي واسع النطاق لمكتبات المركبات الكيميائية، ثم تطورت المقاربات إلى استراتيجيات عقلانية تستند إلى المبادئ البنيوية والحركية، ما زاد من كفاءة تحديد مركبات فعالة وانتقائية. تُستخدم هذه المقاربات أيضًا لتقليل احتمالية التأثيرات الجانبية غير المرغوبة وتحسين الانتقائية تجاه البروتين المستهدف. كما أصبح من الشائع دمج نتائج التجارب المخبرية مع التقنيات الحاسوبية لتسريع اختيار المركبات المرشحة قبل اختبارها تجريبيًا، ما يزيد من فرص الوصول إلى مثبطات واعدة بأقل تكلفة وزمن ممكن[11].
تصميم المثبطات
يمثل التصميم الدوائي المعتمد على البنية أحد الركائز الأساسية لتطوير المثبطات الحديثة. في هذا السياق، تُستخدم بيانات بنيويّة مستخلصة من تقنيات، مثل
البلورة بالأشعة السينية (X-ray Crystallography) أو
الرنين المغناطيسي النووي (Nuclear magnetic resonance - NMR) لتحليل مواقع الارتباط الجزيئي بدقة. تتيح هذه المقاربة تصميم مثبطات قادرة على التفاعل النوعي مع المواقع النشطة أو المواقع التغايرية، من خلال تحسين التوافق الفراغي والتآثرات الكيميائية، مثل الروابط الهيدروجينية والتآثرات الكارهة للماء[12]. كما أسهم دمج الأدوات الحاسوبية، مثل
النمذجة الجزيئية والمحاكاة (Simulations) والالتحام الجزيئي (Molecular Docking) في تسريع عملية التصميم وتحسين التنبؤ بفعالية المثبطات قبل اختبارها تجريبيًا، ما يقلل الوقت والكلفة ويزيد فرص الوصول إلى مرشحات دوائية واعدة.
الاتجاهات المستقبلية
تتجه أبحاث المثبطات نحو تطوير جزيئات أكثر انتقائية ودقة، مع التركيز على استهداف مواقع تغايرية، والتعامل مع أهداف بروتينية كانت تُعدّ سابقًا غير قابلة للاستهداف الدوائي. كما تتجه الدراسات الحديثة إلى فهم الديناميكيات البنيوية للبروتينات بدل الاكتفاء بالبنى الساكنة، ما يفتح آفاقًا جديدة لتصميم مثبطات تتلاءم مع التحولات التوافقية أثناء الوظيفة البيولوجية. يتنامى دور
التقنيات الحاسوبية وأساليب
الذكاء الاصطناعي في أبحاث المثبطات، خاصة في تحليل البيانات البنيوية للبروتينات. تُستخدم هذه الأدوات بشكل عام للتنبؤ بمواقع ارتباط الركائز أو المثبطات، وتحسين اختيار المركبات المرشحة قبل التجارب المعملية، ما يسهم في توجيه جهود اكتشاف وتصميم المثبطات بشكل أكثر فعالية ودقة[13].
المراجع
Anderson, Amy C. “The Process of Structure-Based Drug Design.”
Chemistry & Biology. vol. 10, no. 9 (2003). pp. 787-797.
Berg, Jeremy M. et al.
Biochemistry. 9th ed. New York: WH Freeman, 2019.
Boué-Grabot, Eric, David Blum, & Stefania Ceruti. “Editorial: Purinergic Signaling in Health and Disease.” Frontiers in Cellular Neuroscience. vol. 14, article no. 15 (2020). pp. 1-2.
Copeland, Robert A.
Evaluation of Enzyme Inhibitors in Drug Discovery: A Guide for Medicinal Chemists and Pharmacologists. 2nd ed. Hoboken, NJ: Wiley, 2013.
Cornish-Bowden, Athel. Fundamentals of Enzyme Kinetics. 4th ed. Weinheim: Wiley-Blackwell, 2012.
Cesco, Stefano De et al. “Covalent Inhibitors Design and Discovery.” European Journal of Medicinal Chemistry. vol. 138 (2017). pp. 96-114.
Kitchen, Douglas B. et al. “Docking and Scoring in Virtual Screening for Drug Discovery: Methods and Applications.”
Nature Reviews Drug Discovery. vol. 3 (2004). pp. 935-949.
Nelson, David L. et al.
Lehninger Principles of Biochemistry. 8th ed. New York: Macmillan Learning, 2021.
Singh, Juswinder et al. “The Resurgence of Covalent Drugs.”
Nature Reviews Drug Discovery. vol. 10 (2011). pp. 307-317.
Williams, Jon et al. “Generative AI: A Generation‑Defining Shift for Biopharma Regulatory Affairs.”
Nature Reviews Drug Discovery. vol. 24 (2025). pp. 651-652.
[1] David L. Nelson et al.,
Lehninger Principles of Biochemistry, 8th ed. (New York: Macmillan Learning, 2021).
[2] Ibid.
[3] Ibid.
[4] Robert A. Copeland, “Irreversible Enzyme Inactivators,” in: Evaluation of Enzyme Inhibitors in Drug Discovery: A Guide for Medicinal Chemists and Pharmacologists, 2nd ed. (Hoboken, NJ: Wiley, 2013).
[5] Athel Cornish-Bowden, Fundamentals of Enzyme Kinetics, 4th ed. (Weinheim: Wiley-Blackwell, 2012).
[6] Nelson et al.,
op. cit.
[7] Jeremy M. Berg et al.,
Biochemistry, 9th ed. (New York: WH Freeman, 2019).
[8] Juswinder Singh et al., “The Resurgence of Covalent Drugs,”
Nature Reviews Drug Discovery, vol. 10 (2011), pp. 307-317.
[9] Eric Boué-Grabot, David Blum, & Stefania Ceruti, “Editorial: Purinergic Signaling in Health and Disease,” Frontiers in Cellular Neuroscience, vol. 14, article no. 15 (2020), pp. 1-2.
[10] Stefano De Cesco et al., “Covalent Inhibitors Design and Discovery,” European Journal of Medicinal Chemistry, vol. 138 (2017), pp. 96-114.
[11] Douglas B. Kitchen et al., “Docking and Scoring in Virtual Screening for Drug Discovery: Methods and Applications,”
Nature Reviews Drug Discovery, vol. 3 (2004), pp. 935-949.
[12]Amy C. Anderson, “The Process of Structure-Based Drug Design,”
Chemistry & Biology, vol. 10, no. 9 (2003), pp. 787-797.
[13] Jon Williams et al., “Generative AI: A Generation‑Defining Shift for Biopharma Regulatory Affairs,”
Nature Reviews Drug Discovery, vol. 24 (2025), pp. 651-652.