علم الخلية البِنيوي، المعروف أيضًا باسم "علم الخلايا" والمعرّب أحيانًا بـ "السيتولوجيا"، هو علم يختصّ بدراسة الخلايا بوصفها الوحدات البنائية الأساسية للحياة، ويعدّ فرعًا من فروع علم بيولوجيا الخلية الحديث (Cell Biology) الثلاثة الذي يضم – إضافة إلى علم الخلية البنيوي - علمَي الوراثة (Genetics) والكيمياء الحيوية (Biochemistry). يدرس هذا العلم بِنية الخلايا ووظائفها وتكاثرها وأمراضها، ويستخدم علماء الخلايا مجموعة واسعة من التقنيات القديمة والحديثة لدراسة بنية الخلايا ووظيفتها وسلوكها، بما في ذلك الفحص المجهري وأساليب الكيمياء الحيوية وعلم الوراثة والبيولوجيا الجزيئية.
تاريخ علم الخلية البنيوي
يختصّ علم الخلية البنيوي، أو علم الخلايا، بدراسة الخلايا دراسة علمية باعتبارها الوحدات البنائية الأساسية للكائن الحي، وترتبط نشأة هذا العلم باختراع المجهر؛ ففي عام 1665، أجرى العالم الإنكليزي روبرت هوك (Robert Hooke، 1635-1703) أبحاثًا مجهرية على الفِلِّين، وكان لملحوظاته للحجيرات الفارغة في الفِلِّين (وهي لخلايا الفِلِّين الميتة) أثر مهم في نشأة علم الخلايا، إذ اعتمد مصطلح "خلية" (Cell) لوصف هذه الوحدات الهيكلية[1]. وبصورة شبه متزامنة، قدّم العالم الهولندي أنتوني ڤان ليفينهوك (Antonie van Leeuwenhoek، 1632-1723) إسهامًا كبيرًا في تطوير علم الخلية في أواخر القرن السابع عشر، وذلك حين استخدم عام 1674 مجهرًا أحادي العدسة - كان قد صمّمه بنفسه - وشاهد به عدة كائنات حية دقيقة وكائنات وحيدة الخلية لأول مرة، بخلاف هوك الذي عاين الخلايا الميتة[2].
وفي القرن التاسع عشر، حقق العالمان الألمانيان، ماتياس شلايدن (Matthias Schleiden، 1804-1881) وثيودور شڤان (Theodore Schwann، 1810-1882)، قفزة نوعية في هذا المجال؛ ففي عام 1838، قدّم عالم النبات شلايدن نظرية مفادها أن كل جزء هيكلي من النبات يتكون من خلايا أو ناتج الخلايا، مؤكدًا أن الخلايا تشكل اللّبِنات الأساسية للنباتات. وبعد ذلك بوقت قصير، في عام 1839 تحديدًا، توصّل عالم الأحياء شڤان إلى أن الحيوانات أيضًا مكونة من خلايا. وبذلك نشأ أساس ما عُرف في ما بعد باسم "نظرية الخلية" (Cell Theory). وفي عام 1858، أضاف العالم الألماني رودولف ڤيرخوف (Rudolf Virchow، 1821-1902) عمود النظرية الخلوية الثالث الذي ينصّ على أن كل الخلايا تنشأ من خلايا أخرى[3]. ويزخر تاريخ البيولوجيا الحديثة بنقاشات حول الادعاءات القائلة إن ڤيرخوف استقى هذه الفكرة المركزية وأساسها العلمي من أعمال عالم آخر يدعى روبرت ريماك (Robert Remak،1815 -1865)[4].
في عام 1876، كان عالم الأجنة الألماني، أوسكار هيرتڤيغ (Oscar Hertwig، 1849-1922)، من أوائل العلماء الذين أثبتوا أن اتحاد الحيوان المنوي بالبويضة هو أساس الإخصاب (سبقه إلى هذه النتيجة عالمان على الأقل، ورغم ذلك اشتُهر بـ "أبي الإخصاب")[5]. وفي عام 1892، أسَّس هيرتڤيغ علم الخلية البنيوي بوصفه فرعًا مستقلًا من علم الأحياء، بعد أن وجد أنّ العمليات التي لوحظت على المستوى العضوي هي مظاهر للعمليات الخلوية الأساسية، وذلك ما يُبرز أهمية علم الخلايا في السياق البيولوجي الأوسع[6]. أدت التطورات المتتابعة في علم الخلية البنيوي إلى إنشاء علم الوراثة الخلوية (Cytogenetics) عام 1903 بناءً على أعمال العالم الألماني ثيودور بوڤيري (Theodor Boveri، 1862-1915)، وعالم الوراثة الأميركي والتر ساتون (Walter Sutton، 1877-1916) اللذين أوضحا العلاقة بين انقسام الخلايا والوراثة كلّ على حدة[7]. وفي منتصف القرن العشرين، أحدث تطوير المجهر الإلكتروني وتقنيات التصوير المتقدمة الأخرى ثورة في مجال علم الخلايا البنيوي، فيسّر ذلك للعلماء دراسة بنية الخلايا بدقة كبيرة غير مسبوقة.
[الشكل 1]
 ساعد تطور المجهر على فهم الخلايا وأنواعها ومكوناتها وكيفية حل المشكلات في شتى المجالات
ساعد تطور المجهر على فهم الخلايا وأنواعها ومكوناتها وكيفية حل المشكلات في شتى المجالات
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
ومع تقدم العلوم البيوكيميائية، تطوّر عن علم الخلية البنيوي علمُ الأمراض الخلوي (Cytopathology) بوصفه فرعًا متخصصًا في مجال علم الأمراض (Pathology)، ووضع أركان هذا العلم العالم اليوناني جورجيوس بابانيكولاو (Georgios Papanicolaou،1883 -1962) عام 1928، وذلك حين عرض أبحاثه حول تمييز الخلايا السرطانية في عنق الرحم (لطاخة باب Pap smear[8]). وفي حين شكّل علم الخلايا أساس هذا المجال، وسّع علم الأمراض الخلوي مجال بحثه ليختص في فحص وتشخيص الأمراض على المستوى الخلوي بطريقة تختلف عن علم أمراض الأنسجة (Histopathology) الذي يشمل تحليل عينات الأنسجة الكاملة. لذا، فإن علم الأمراض الخلوي ينطوي - كسابقه - في المقام الأول على فحص الخلايا الفردية وشظايا الأنسجة الصغيرة. ويُعدّ هذا المجال الحديث المنبثق عن علم الخلية البنيوي أداة حيوية للتحقيق في مجموعة واسعة من الأمراض، ويؤدي دورًا بارزًا في تشخيص السرطان، والأمراض المُعْدية، والحالات الالتهابية، وغيرها.
علم الخلية البنيوي وعلم بيولوجيا الخلية
يشيع بين القرّاء الخلط بين علم الخلية البنيوي وعلم بيولوجيا الخلية (المعروف أيضًا باسم "البيولوجيا الخلوية")، فالفرق بينهما دقيق، إذ إن علم الخلية البنيوي هو جزء من علم بيولوجيا الخلية وإن سبقه في الاكتشاف والدراسة، وفي حين يهتم علم الخلية البنيوي بدراسة الخلايا المنفردة، بما في ذلك الجانبان المورفولوجي (الشكلي) والفيزيولوجي (الوظيفي)، وغالبًا ما يُعمد إليه في تشخيص الأمراض عبر فحص عينات الخلايا تحت المجهر[9]، فإن علم بيولوجيا الخلية يدرس بنية الخلايا ووظيفتها بشكل أشمل، ويدرس العضيّات {{العضيات (Organelles): جسيمات خلوية متخصصة محاطة بغشاء - أو أكثر -، مثل النواة (Nucleus) أو الميتوكوندريا (Mitochondria) أو البلاستيدات (Chloroplasts)، توجد داخل الخلايا حقيقية النواة (Eukaryotic cells)، وتؤدي وظائف متخصصة.}} وكيفية تفاعل الخلايا مع بعضها وفي بيئتها[10].
ورغم أن هذين العلمين من العلوم ذات الصلة الوثيقة التي تدرس الخلايا بوصفها كلًّا، فهناك بعض الفروقات المهمة في سياقهما التاريخي وموضوع كل منهما؛ فمن الناحية الاصطلاحية، يُعدّ علم الخلية البنيوي حقلًا فرعيًّا من علم بيولوجيا الخلية يركّز بشكل خاص على دراسة بنية الخلية ووظيفتها، وذلك باعتماد الفحص المجهري للخلايا في أغلب الأحيان، ولذلك اهتمّ علم الخلية البنيوي في البداية باكتشاف الخلايا ووصفها وتصنيفها، وبناءً على ذلك، فإن علم بيولوجيا الخلية أشمل، وقد نشأ خلال القرن العشرين، ويشتمل على دراسة أشكال الخلايا وظائفها، ولكنه يشمل مجموعة واسعة من الموضوعات، إذ يتعمق في الجوانب الأوسع لوظائف الخلية، ويهتم بالعمليات الخلوية والآليات الجزيئية والجينية وفوق الجينية {{الآلية فوق الجينية: دراسة التغيرات في التعبير الجيني ووظيفة الخلايا من حيث تأثرها بالعوامل البيئية والآليات الخلوية المختلفة الأخرى، من دون أن يشمل ذلك دراسة التغييرات في تسلسل الحمض النووي. ومن العوامل فوق الجينية التغيراتُ الجينية المصاحبة للتقدم في العمر.}} (التمثيل الغذائي، نقل الإشارة، تضاعف الحمض النووي، تخليق البروتين، والتفاعلات بين الخلايا داخل الأنسجة، وغيرها)[11]. وبذلك يتشكل علم بيولوجيا الخلية الحديث من تداخل كل من علم الخلية البنيوي، وعلم الوراثة، وعلم الكيمياء الحيوية[12].
أشكال الخلايا
تتكون الكائنات الحية جميعها من خلية واحدة أو أكثر، ويمكن تصنيف هذه الخلايا إلى فئتين رئيستين: خلايا بدائية النواة (Prokaryotes)، وخلايا حقيقية النواة (Eukaryotes). توجد الخلايا بدائية النواة في البكتيريا (Bacteria) والعتائق (الآركيونات، Archaea)، وهي أصغر وأبسط بكثير من الخلايا حقيقية النواة، إذ تفتقر إلى النواة والعضيات الداخلية الأخرى المحاطة بغشاء[13]، كما تتميز الخلايا بدائية النواة بجزيئات الحمض النووي الدائرية. أما الخلايا حقيقية النواة الموجودة في النباتات والحيوانات والفطريات ووحيدات الخلية، فهي غالبًا ما تكون أكبر حجمًا وأكثر تعقيدًا، وفيها أنوية تحتوي على المادة الوراثية التي تكون على شكل كروموسومات (Chromosomes)، وتحتوي - إضافة إلى النواة - على مجموعة متنوعة من العضيّات المحاطة بالغشاء مثل الميتوكوندريا (Mitochondria)، والبلاستيدات الخضراء (Chloroplasts)، والشبكة الإندوبلازمية {{الشبكة الإندوبلازمية (Endoplasmic reticulum, (ER)): هي عُضيّة غشائية موجودة في الخلايا حقيقية النواة، تُعدّ أساسية في عمليات تخليق البروتينات والدهون وتطويعها وتعديلها ونقلها. توجد هذه الشبكة في الخلية بشكلين مختلفين: الشبكة الإندوبلازمية الخشنة التي تكون مغطاة بالريبوسومات وتشارك بشكل أساسي في تخليق البروتينات؛ والشبكة الإندوبلازمية الملساء التي تفتقر إلى الريبوسومات، وهي مسؤولة عن تخليق الدهون، وعمليات إزالة السموم، وبعض عمليات الاستقلاب (الأيض).}}، وجهاز غولجي (Golgi Apparatus)، وغيرها[14].
[الشكل 2]
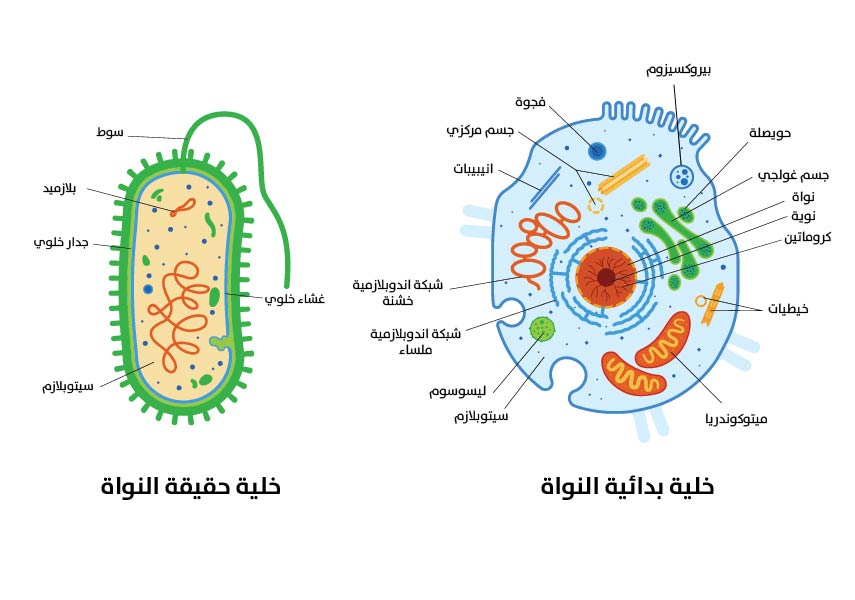 الفرق بين الخلية حقيقية النواة والخلية بدائية النواة
الفرق بين الخلية حقيقية النواة والخلية بدائية النواة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تتكون الخلايا جميعها - بصرف النظر عن نوعها - من ثلاثة أجزاء أساسية: الغشاء البلازمي أو الخلوي (Plasma or cell membrane)، والسيتوبلازم {{السيتوبلازم (Cytoplasm): أو المعروف بالوسط الخلوي، هو ما يوجد داخل الخلية باستثناء النواة في الخلايا حقيقية النوى (Eukaryotic cells)، وكل ما يوجد داخل الخلية في الخلايا غير حقيقية النوى (Prokaryotic cells).}}، والمادة الوراثية (الحمض النووي). أما غشاء البلازما، فيتكون من طبقتين (Bilayer) رقيقتين ومرنتين من الدهن الفسفوري {{الدهون الفسفورية (Phospholipid): أو الفسفوليبيدات، هي دهون أمفيباتية (ذات طبيعة مزدوجة، Amphipathic)، تتكون من رأس فوسفاتي محب للماء وذيلين من الأحماض الدهنية الكارهة للماء. تشكل هذه الدهون القاعدة البنيوية الأساسية لجميع الأغشية الخلوية.}} بينهما بروتينات. يحيط الغشاء بمحتويات الخلية ويفصل داخلَها عن البيئة المحيطة. وأما السيتوبلازم، فهو الوسط المائي داخل الخلية، وفيه تتحرك الجزيئات وتجري معظم التفاعلات البيوكيميائية {{التفاعلات البيوكيميائية: عمليات تتحول فيها المواد (المتفاعلات، Reactants) إلى مواد جديدة (نواتج، Products) عن طريق كسر روابط كيميائية في الكائنات الحية وتكوينها، ويسرّع معظمها الإنزيمات.}} اللازمة لحياة الخلية وموتها أيضًا، ورغم تشابه المادة الوراثية لهذين النوعين من الخلايا، فإنها مختلفة في تشكيلها وطيّها[15].
وظائف الخلايا
تؤدي الخلايا مجموعة واسعة من الوظائف الضرورية للحياة، ومن أهمها إنتاج الطاقة، وهو ضروري للعمليات الخلوية جميعها، وتُولَّد الطاقة عادةً من خلال عملية التنفس الخلوي (Cellular respiration) التي تنطوي على تكسير الغلوكوز {{الغلوكوز: (C₆H₁₂O₆) سكر أحادي سداسي الكربون، وهو المصدر الرئيس للطاقة لمعظم الكائنات الحية، والناتج الرئيس لعملية التمثيل الضوئي (Photosynthesis)، والركيزة الأساسية للتنفس الخلوي (Cellular respiration). يدور في الدم على شكل سكر الدم، ويُخزَّن بشكل غلايكوجين (Glycogen) في الكبد والعضلات لدى الحيوانات، أو بشكل نشا (Starch) في النباتات. يتحلل في الخلية لإنتاج طاقة بوساطة التحلل الغلايكولي (Glycolysis) والفسفرة التأكسدية (Oxidative phosphorylation).}} والجزيئات العضوية الأخرى. إنّ الميتوكوندريا هي مكان إنتاج الطاقة القصوى في الخلية حقيقية النواة، بينما تنتج الطاقة الحيوية في سيتوبلازم بدائيات النوى. وتؤدي الخلايا مجموعة متنوعة من الوظائف الأخرى، مثل تخليق البروتينات والدهون والجزيئات الحيوية الأخرى، كما أنها مسؤولة عن نقل الجزيئات من الخلايا وإليها وبين الخلايا المختلفة.
تؤدي بعض الخلايا – إضافة إلى هذه الوظائف العامة - عمليات متخصصة، مثل انقسام الخلايا (Cell division)، والتمايز {{التمايز (Differentiation): العملية التي تتحول فيها الخلية الأقل تخصصًا (خلية من دون دور محدد) إلى خلية أكثر تخصصًا ذات خصائص ووظائف مميزة خاصة بها.}}، والاستماتة (موت الخلايا المبرمج، Apoptosis)، فعملية تكاثر الخلايا تُسمّى "انقسام الخلية"، وهناك عدة آليات للانقسام؛ فالانقسام المنصف {{الانقسام المنصف: انقسام خلوي متخصص يُقلل عدد الكروموسومات إلى النصف، مُنتجًا أربعة أمشاج أحادية الصيغة الصبغية فريدة وراثيًا للتكاثر الجنسي.}} (الاختزالي أو الميوزي، Meiosis) مهم للخلايا الجنسية {{الخلايا الجنسية: أو الأمشاج، هي خلايا أحادية الصيغة الصبغية (Haploid)، وهي الحيوانات المنوية والبويضات التي تُنتج من خلال الانقسام المنصف، وتحتوي على نصف المادة الوراثية اللازمة للتكاثر الجنسي.}}، والانقسام المتساوي {{الانقسام المتساوي (الميتوزي، Mitosis): عملية انقسام الخلايا في الخلايا حقيقية النواة، تؤدي إلى إنتاج خليتين متماثلتين وراثيًّا، ونسخة من الخلية الأصلية. تتضاعف فيه كروموسومات الخلية الأصلية، ومن ثَمَّ تنقسم بالتساوي في خليتين ناتجتين.}} خاصية مشتركة لمعظم الخلايا. أما التمايز، فهو العملية التي تُصنّف بها الخلايا إلى أنواع مختلفة، مثل الخلايا العضلية أو الخلايا العصبية، وتُنظَّم هذه العملية بوساطة مجموعة متنوعة من مسارات الإشارات التي تتحكم في التعبير الجيني (Gene expression) وتحدد مصير الخلايا، بما في ذلك برمجة بعضها لتموت موتًا محققًا. إن الاستماتة عملية منظمة جدًّا تُبرمج فيها الخلايا لتموت موتًا صامتًا غير مؤذٍ للخلايا المجاورة، وتعتبر هذه العملية ضرورية للتطور الطبيعي والتوازن النسيجي، وكذلك للوقاية من السرطان وعدد من الأمراض الأخرى[16].
التقدم في علم الخلية البنيوي
أدى التقدم التكنولوجي والعلمي طوال العقود القليلة الماضية إلى العديد من الاكتشافات والاختراعات المهمة في علم الخلية البنيوي، فقد سمح تطورُ الأنواع المختلفة من المجاهر برؤيةِ تفاصيل خلوية لم تكن مُدرَكة سابقًا، ومن ذلك ما نتج عن استخدام المجهر الفلوري (Fluorescent microscope) ومشتقاته مع التقنيات البيوكيميائية التي تضيف علامات/ جزيئات فلورية (Fluorescent labeling). أدت هذه التقنيات المتطورة إلى تصوير حركة البروتينات والجزيئات الأخرى داخل الخلايا الحية ودراستها، فيسّر ذلك إدراك تفاصيل العمليات الخلوية، مثل نقل الإشارات وحركة الحويصلات (Vesicle trafficking) وغيرها داخل الخلية. إضافة إلى ذلك، فإن تطوير تقنيات التسلسل العالي الإنتاجية {{تقنيات التسلسل العالي الإنتاجية (High throughput sequencing): (HTS) يشير هذا المصطلح إلى تقنيات متقدمة لفحص تسلسل الحمض النووي الريبي منقوص الأكسجين/ الحمض النووي الريبي (DNA/RNA) (مثل Illumina وPacBio) تُولِّد كميات هائلة من البيانات الجينية بسرعة وبتكاليف منخفضة، وتُستخدم في علم الجينوم، وعلم النسخ، وعلم الميتاجينوم في تطبيقات مثل الكشف عن المتحوّرات (Variants)، وتحليل التعبير الجيني، ومراقبة مسببات الأمراض. وتعزز هذه التقنيات الطب الدقيق والدراسات الجينومية واسعة النطاق.}} قد مكّن الباحثين من كشف تسلسل الجينوم (Genome sequencing) لمجموعة واسعة من الكائنات الحية، ووفرّ رؤًى جديدة حول الأساس الجيني للعمليات الخلوية والأمراض. كما أن التطورات الحديثة في تقنيات تسلسل الخلية الواحدة (Single-Cell sequencing) تسهم في دراسة تنوع الخلايا وعدم تجانسها (Heterogeneity) داخل الأنسجة، رغم أنه كان يُعتقد سابقًا أن كلّ نسيج مكونٌ من خلايا متشابهة النوع.
وفي سياق متصل يندرج تحت علم بيولوجيا الخلية ولكن لا يمكن فصله عن علم الخلية البنيوي، جعلت القفزاتُ النوعية في مجال بيولوجيا الخلايا الجذعية (Stem cells) الدراسات البنيوية للخلية من أكثر المجالات إثارة في الأبحاث البيولوجية، إذ تنفرد الخلايا الجذعية بكونها خلايا متخصصة لديها القدرة على التمايز إلى أنواع الخلايا المختلفة، وتمتلك هذه الخلايا إمكانات هائلة في مجال الطب التجديدي (Regenerative medicine)، إذ يمكن استخدامها لإصلاح الأنسجة والأعضاء التالفة أو استبدالها، وليست التطبيقات الطبية فقط ما تكسب أبحاث الخلايا الجذعية أهمية كبرى، فهي مهمة أيضًا في دراسة العمليات الأساسية، مثل النمو والشيخوخة والسرطان وغير ذلك، وأدت دراسة هذه الخلايا إلى تحديد مجموعة واسعة من مسارات الإشارات والعوامل الوراثية التي تشارك في تنظيم التمايز الخلوي والتجديد الذاتي.
نتج عن التقدم الكبير في أبحاث علم الخلية البنيوي العديد من التطبيقات المهمة في الطب والصناعة والزراعة، إذ تُستخدم تقنيات علم الخلايا في الأغراض التشخيصية والعلاجية[17]، وفي مراقبة فاعلية العلاج، وتطوير علاجات جديدة ولقاحات وأجسام مضادة (Antibodies) وبروتينات علاجية أخرى[18]، كما تُستخدم تقنيات علم الخلية البنيوي في الزراعة لفحص الأدوية الجديدة وتطويرها، ولإنتاج الكائنات المعدلة وراثيًّا[19].
المراجع
Acha, Amelia et al. “Applications of The Oral Scraped (Exfoliative) Cytology in Oral Cancer and Precancer.” Medicina Oral, Patologia Oral y Cirugia Buccal. vol. 10, no. 2 (2005). pp. 95-102.
Alberts, Bruce. Molecular Biology of The Cell. 7th ed. New York: W. W. Norton & Company, 2022.
Anderson, C. T. “Robert Remak and The Multinucleated Cell: Eliminating a Barrier to The Acceptance of Cell Division.” Bulletin of the History of Medicine. vol. 60, no. 4 (1986). pp. 523-543.
Bagot, Catherine N. & Roopen Arya. “Virchow and His Triad: A Question of Attribution.” British Journal of Haematology. vol. 143, no. 2 (2008). pp. 180-190.
Boumann, Henry A. et al. “Biophysical Properties of Membrane Lipids of Anammox Bacteria: I. Ladderane Phospholipids form Highly Organized Fluid Membranes.” Biochimica et Biophysica Acta. vol. 1788, no. 7 (2009). pp. 1444-1451.
Briggs, Elissa & Gary M. Wessel. “In The Beginning… Animal Fertilization and Sea Urchin Development.” Developmental Biology. vol. 300, no. 1 (2006). pp. 15-26.
Coleman, William. “Cell, Nucleus, and Inheritance: An Historical Study.” Proceedings of the American Philosophical Society. vol. 109, no. 3 (1965). pp. 124-158.
Cytology. Collection Development Guidelines of the National Library of Medicine (Internet). Bethesda, MD: National Library of Medicine (US), 2019. at: https://acr.ps/1L9F2Hl
Elgert, Paul A. & Gary W. Gill. “George N. Papanicolaou, MD, PhD: Cytopathology.” Laboratory Medicine. vol. 40, no. 4 (2009). pp. 245-246.
Gest, Howard. “Homage to Robert Hooke (1635-1703): New Insights from The Recently Discovered Hooke Folio.” Perspect Biol Med. vol. 52, no. 3 (Summer 2009). pp. 392-399.
Hand, Carol. Great discoveries in science. New York: Cavendish Square, 2019.
Hardin, Jeff & Gregory Bertoni. Becker's World of the cell. 9th ed. London: Pearson, 2016.
Lane, Nick. “The Unseen World: Reflections on Leeuwenhoek (1677) ‘Concerning Little Animals’.” Philosophical Transactions of The Royal Society B:Biological Sciences. vol. 370, no. 1666 (2015).
Mano, Junichi et al. “Real-Time PCR Array as a Universal Platform for The Detection of Genetically Modified Crops and Its Application in Identifying Unapproved Genetically Modified Crops in Japan.” Journal of Agricultural and Food Chemistry. vol. 57, no. 1 (2009). pp. 26-37.
Nelson, David L., Michael M. Cox & Aaron A. Hoskins. Lehninger Principles of Biochemistry. 8th ed. New York: Macmillan Learning, 2021.
Pantanowitz, Liron et al. Modern Techniques in Cytopathology. Liron Pantanowitz & Marilyn M. Bui (eds.) vol. 25. Basel: Karger, 2020.
Ronald, Pamela & Melinda Kliegman. “CRISPR in Agriculture.” Innovative Genomics Institute. 12/9/2022. at: https://acr.ps/1L9F2Tw
Sutton, Walter S. “The Chromosomes in Heredity.” The Biological Bulletin. vol. 4, no. 5 (1903). pp. 231-250.
[1] Howard Gest, “Homage to Robert Hooke (1635-1703): New Insights from The Recently Discovered Hooke Folio,” Perspect Biol Med, vol. 52, no. 3 (Summer 2009), pp. 392-399.
[2] Nick Lane, “The Unseen World: Reflections on Leeuwenhoek (1677) ‘Concerning Little Animals’,” Philosophical Transactions of The Royal Society B:Biological Sciences, vol. 370, no. 1666 (2015).
[3] Carol Hand, Great discoveries in science (New York: Cavendish Square, 2019).
[4] Catherine N. Bagot & Roopen Arya, “Virchow and His Triad: A Question of Attribution,” British Journal of Haematology, vol. 143, no. 2 (2008), pp. 180-190;
- T. Anderson, “Robert Remak and The Multinucleated Cell: Eliminating a Barrier to The Acceptance of Cell Division,” Bulletin of the History of Medicine, vol. 60, no. 4 (1986), pp. 523-543.
[5] Elissa Briggs & Gary M. Wessel, “In The Beginning… Animal Fertilization and Sea Urchin Development,” Developmental Biology, vol. 300, no. 1 (2006), pp. 15-26.
[6] William Coleman, “Cell, Nucleus, and Inheritance: An Historical Study,” Proceedings of the American Philosophical Society, vol. 109, no. 3 (1965), pp. 124-158.
[7] Walter S. Sutton, “The Chromosomes in Heredity,” The Biological Bulletin, vol. 4, no. 5 (1903), pp. 231-250.
[8] Paul A. Elgert & Gary W. Gill, “George N. Papanicolaou, MD, PhD: Cytopathology,” Laboratory Medicine, vol. 40, no. 4 (2009), pp. 245-246.
[9]Cytology, Collection Development Guidelines of the National Library of Medicine (Internet), (Bethesda, MD: National Library of Medicine (US), 2019), at: https://acr.ps/1L9F2Hl
[10] Jeff Hardin & Gregory Bertoni, Becker's World of the cell, 9th ed. (London: Pearson, 2016).
[11] Bruce Alberts, Molecular Biology of The Cell, 7th ed. (New York: W. W. Norton & Company, 2022).
[12] Hardin & Bertoni.
[13] تجدر الإشارة إلى أن بعض الخلايا بدائية النواة تحوي أغشية داخلية، مثل بكتيريا أناموكس (Anammox Bacteria)، يُنظر:
Henry A. Boumann et al., “Biophysical Properties of Membrane Lipids of Anammox Bacteria: I. Ladderane Phospholipids form Highly Organized Fluid Membranes,” Biochimica et Biophysica Acta, vol. 1788, no. 7 (2009), pp. 1444-1451.
[14] David L. Nelson, Michael M. Cox & Aaron A. Hoskins, Lehninger Principles of Biochemistry, 8th ed. (New York: Macmillan Learning, 2021).
[15] Hardin & Bertoni.
[16] Alberts.
[17] Amelia Acha et al., “Applications of The Oral Scraped (Exfoliative) Cytology in Oral Cancer and Precancer,” Medicina Oral, Patologia Oral y Cirugia Buccal, vol. 10, no. 2 (2005), pp. 95-102.
[18] Liron Pantanowitz et al., Modern Techniques in Cytopathology, Liron Pantanowitz & Marilyn M. Bui (eds.), vol. 25 (Basel: Karger, 2020).
[19] Pamela Ronald & Melinda Kliegman, “CRISPR in Agriculture,” Innovative Genomics Institute. 12/9/2022, accessed on 25/6/2024, at: https://acr.ps/1L9F2Tw;
Junichi Mano et al., “Real-Time PCR Array as a Universal Platform for The Detection of Genetically Modified Crops and Its Application in Identifying Unapproved Genetically Modified Crops in Japan,” Journal of Agricultural and Food Chemistry, vol. 57, no. 1 (2009), pp. 26-37.