الكورتيزول هرمون ستيرويدي يُفرَز من الغدة الكظرية، ويُنظّم استجابة الجسم للتوتر، ويدعم الوظائف الأيضية والمناعية، ويؤثر في مجموعة واسعة من وظائف الجسم، بدءًا من تنظيم الاستقلاب ووصولًا إلى ضبط الاستجابة المناعية والتكيُّف مع التوتر النفسي-الجسدي. ويُعَد التوازن الدقيق لمستوياته ضروريًّا للحفاظ على الصحة الجسدية والنفسية، فارتفاعه أو انخفاضه المزمن قد يؤديان إلى اضطرابات متعددة، مثل متلازمة كوشينغ، ومرض أديسون، ومشكلات التمثيل الغذائي، وأمراض القلب. كذلك فإن فهم نمط الإفراز اليومي للكورتيزول ودوره في استجابات الجسم للإجهاد، يمكن أن يساعد الباحثين والأطباء في تطوير استراتيجيات وقائية وعلاجية أكثر فاعلية. إضافة إلى أن الكورتيزول يظل حجر الزاوية في دراسة وظائف الغدد الصماء، وعلم الأعصاب، والطب الوقائي، ما يُبرز أهميته في العلوم الطبية والحياتية.
[الشكل 1]
 التركيب الكيميائي للهيدروكورتيزون
التركيب الكيميائي للهيدروكورتيزون
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
التعريف والتركيب الكيميائي
الكورتيزول هرمون ستيرويدي يُفرَز من قشرة الغدة الكظرية، وينتمي إلى فئة القشريات السكّرية (الغلوكوكورتيكويدات/ Glucocorticoids)، ويُصنَّع من الكوليسترول في المنطقة الحزمية للغدة الكظرية (Adrenal cortex). يؤدي الكورتيزول دورًا أساسيًّا في كثير من العمليات الفيزيولوجية، مثل تنظيم استجابة الجسم للتوتر، ودعم الوظائف المناعية، والتحكُّم في عمليات الأيض وضغط الدم. ويتميَّز بتأثيره القوي المضاد للالتهابات، ويُستخدم علاجيًّا للتخفيف من حالات متعدّدة، منها: التهابات الجلد، ولدغات الحشرات، والتهاب المفاصل، والتهاب القولون التقرُّحي، واضطرابات الغدة الكظرية[1]. وعند استخدامه دوائيًّا، يُعرف باسم الهيدروكورتيزون (Hydrocortisone).[2]
وظائف الكورتيزول
[الشكل 2]
 وظائف الكورتيزول المختلفة في جسم الإنسان
وظائف الكورتيزول المختلفة في جسم الإنسان
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يؤدي الكورتيزول دورًا محوريًّا في كثير من وظائف الجسم الحيوية، إذ يؤثر في معظم الأعضاء والأنسجة (الشكل 2)، فهو يساعد في تنظيم نشاط الجهاز المناعي والاستجابة الالتهابية، ما يسهم في ضبط الالتهابات ومنع فرط تفاعل المناعة. ويُعَدّ كذلك عنصرًا أساسيًّا في استجابة الجسم للتوتر، إذ يُفرَز بكميات أكبر في أثناء الضغط النفسي أو الجسدي، ضمن آلية "القتال أو الهروب" (الكر أو الفر/ Fight or flight)، لتوفير الطاقة اللازمة للتعامل مع الموقف. فضلًا عن ذلك، يشارك الكورتيزول في تنظيم عمليات الأيض من خلال التحكُّم في توزيع الطاقة واستخدام المُغذّيات، خصوصًا عبر رفع مستوى الغلوكوز في الدم، لضمان تزويد الأنسجة بالطاقة. ويسهم كذلك في الحفاظ على ضغط الدم وتنظيم وظائف القلب والأوعية الدموية، ما يجعله هرمونًا ضروريًّا للتوازن الفيزيولوجي العام في الجسم[3].
تنظيم إفراز الكورتيزول
عند تعرُّض الجسم للإجهاد، يُنشِّط محور ما تحت المهاد -الغدة النخامية- قشرةَ الكظر (Hypothalamic Pituitary Adrenal cortex, HPA)، عبر إشارات عصبية تبدأ في النواة المجاورة للبُطين (Paraventricular Nucleus, PVN) في منطقة المهاد. في هذه الحالة، تُفرِز الخلايا العصبية في النواة المجاورة للبُطين الأيمن (داخل الوطاء/ Hypothalamus) الهرمونَ المطلق لموجِّهة القشرة الكظرية (Corticotropin Releasing Hormone, CRH) نحو شبكة من الأوعية الدموية البابية (Hypophyseal postal vessels) التي تصل مباشرةً إلى الفص الأمامي من الغدة النخامية. تعمل هذه الأوعية بوصفها مسارًا ناقلًا يسمح بانتقال الهرمون بسرعة، ما يؤدي إلى تحفيز الغدة النخامية على إفراز الهرمون الموجّه لقشرة الكظر (Adrenocorticotropic Hormone, ACTH) الذي يُنشّط بدوره الغدة الكظرية لإنتاج الغلوكوكورتيكويدات (مثل الكورتيزول في الإنسان). بعد ذلك، تنتشر هذه الهرمونات في أنسجة الجسم كلها، بما في ذلك الدماغ، إذ تتفاعل مع مستقبلات خاصة لتنظيم استجابات فيزيولوجية متنوعة. كذلك، يعمل الكورتيزول -عند بلوغه مستويات معينة- على تنظيم نشاط المحور نفسه، عبر آليات التغذية الراجعة السلبية التي تُثبّط إفراز CRH وACTH، لمنع الإفراط في النشاط الهرموني[4].
[الشكل 3]
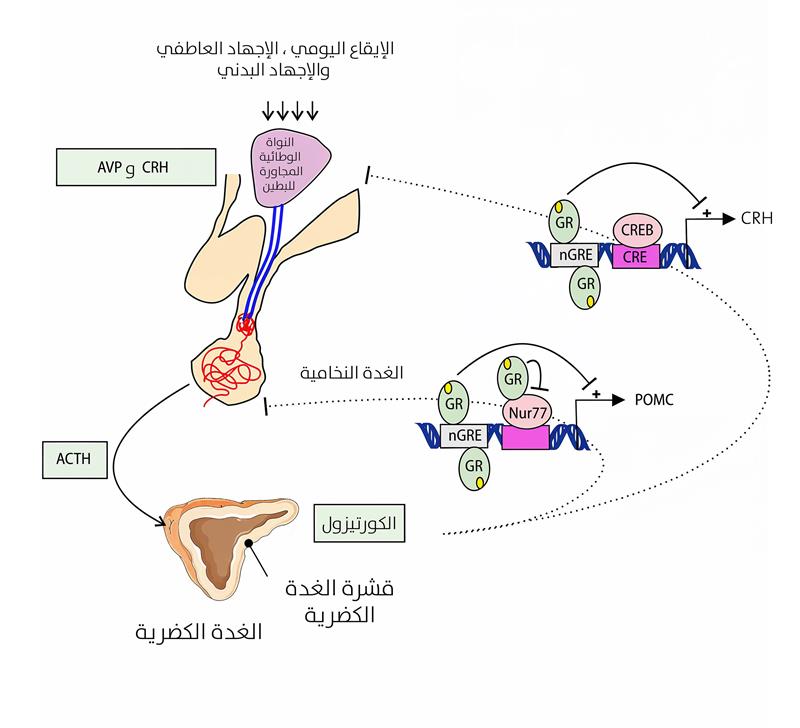 تنظيم محور الوطاء-الغدة النخامية-الغدة الكظرية وإفراز الكورتيزول
تنظيم محور الوطاء-الغدة النخامية-الغدة الكظرية وإفراز الكورتيزول
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يُنظَّم نشاط محور الوطاء في الغدة النخامية-الغدة الكظرية بوساطة الإيقاع اليومي، ويزداد بسبب الضغوط الفيزيولوجية والعاطفية. وعند التنشيط، يُفرَز هرمون مطلق الكورتيكوتروبين (CRH) والفازوبريسين (AVP) من نواة ما حول البطنية في الوطاء، ما يُحفز إفراز هرمون ACTH من الغدة النخامية، في حين أن ACTH يُحفّز إنتاج الكورتيزول في قشرة الغدة الكظرية. يُنظِّم الكورتيزول المحور سلبيًّا عن طريق تثبيط نسخ CRH وPOMC، عبر ارتباطه بعناصر الاستجابة السلبية للغلوكوكورتيكويد (nGRE)، أو عبر التفاعل مع عامل النسخ Nur77، المسؤول عن تعبير POMC (الشكل 3)[5].
يُفرَز الكورتيزول بطريقة إيقاعية يومية (Circadian rhythm)، إذ تكون مستوياته منخفضة نسبيًّا في أثناء النوم، وتبدأ بالارتفاع تدريجيًّا قبل الاستيقاظ مباشرةً في الصباح الباكر (عادةً بين الساعة 6-8 صباحًا)، وهو ما يُعرف بصعود الصباح للكورتيزول (Cortisol awakening response). يساعد هذا الارتفاع الجسم في الاستيقاظ، مع تجهيزه الطاقة المطلوبة للأنشطة اليومية. بعد ذلك، تنخفض مستويات الكورتيزول تدريجيًّا خلال النهار، لتصل إلى أدنى مستوًى لها في المساء قبل النوم، ما يسمح للجسم بالاسترخاء والتحضير للراحة الليلية[6].
هذا النمط اليومي مهم جدًّا للحفاظ على التوازن الفيزيولوجي، إذ يؤثر في ضغط الدم، وسكر الدم، والأداء العقلي، والجهاز المناعي. أي اضطراب في هذا الإيقاع، مثل التعرض المزمن للإجهاد أو النوم غير المنتظم، يمكن أن يؤدي إلى مشكلات صحية متعددة، منها: اضطرابات النوم، وضعف المناعة، وزيادة مخاطر الأمراض القلبية، والتمثيل الغذائي[7].
متوسط مستويات الكورتيزول (±الخطأ المعياري) بعد الاستيقاظ الصباحي لدى ثلاث فئات عمرية: الأطفال (7-14 سنة)، والمراهقين (19-37 سنة)، وكبار السن (59-82 سنة). تختلف استجابة إفراز الكورتيزول باختلاف العمر بعد الاستيقاظ مباشرة (الشكل 4)[8].
[الشكل 4]
 نمط الإفراز
نمط الإفراز
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
طرق قياس الكورتيزول ومستوياته الطبيعية
يمكن قياس الكورتيزول في الدم أو البول أو اللُّعاب لتقييم إنتاجه ووظائفه الفيزيولوجية، وهو يُقاس عادةً في الدم (serum/plasma)، خصوصًا في الصباح بين الساعة 6-8 صباحًا، لمراعاة الارتفاع الصباحي الطبيعي. يمكن كذلك أخذ عيّنات متعددة على مدار اليوم لدراسة النمط اليومي للإفراز، مع استخدام جمع البول مدة 24 ساعة (Urinary Free Cortisol)، لتقدير الكمية الكلية للكورتيزول غير المرتبط بالبروتين. أما قياس الكورتيزول في اللُّعاب، فيُعَدّ وسيلة غير غازية مناسبة لتقييم النمط اليومي والاستجابة للإجهاد[9].
تختلف المستويات الطبيعية للكورتيزول باختلاف الوقت وطريقة القياس؛ ففي الدم، تتراوح المستويات الصباحية عادةً بين 5 و23 ميكروغرامًا/ ديسيلتر، وتصل إلى 3-13 ميكروغرامًا/ ديسيلتر في المساء. ويُقدّر إنتاج الكورتيزول في البول خلال 24 ساعة بين 10 و100 ميكروغرام/ ديسيلتر، بينما تتراوح مستويات اللُّعاب الصباحية بين 0.2 و0.7 ميكروغرام/ ديسيلتر. هذه القِيم تقريبية، وتعتمد على المختبر والطريقة المستخدَمة، ويؤثر النمط اليومي للإفراز بشكل كبير في النتائج.[10]
أظهرت الأبحاث كيفية اختلاف مستويات الكورتيزول بين الأجناس والفئات العمرية المختلفة، فثمة تباينات ملحوظة في نشاط محور الوطاء-النخامية-الكظر (HPA axis) تبعًا للجنس والعمر، كما في النتائج الآتية[11]:
- مرحلة الطفولة المبكرة (أقل من 8 سنوات): يمتلك الأولاد مستويات أعلى من الكورتيزول في اللُّعاب والدم مقارنة بالفتيات.
- في المراحل اللاحقة (من 8 إلى 18 سنة): ينعكس النمط تدريجيًّا، إذ تُظهر الفتيات مستويات أعلى من الكورتيزول الصباحي أو المُقاس في اللُّعاب والدم، ما يُعزى إلى التغيُّرات الهرمونية والتنظيمية التي ترافق النضج الجنسي.
- عند قياس إفراز الكورتيزول في البول مدة 24 ساعة: يظل الأولاد محافظين على مستويات أعلى نسبيًّا مقارنة بالفتيات في مختلف المراحل العمرية، ما يشير إلى وجود فروق في الإيقاع اليومي لإفراز الكورتيزول، أو في استجابة الغدة الكظرية للمحفّزات التنظيمية.
تُبرز هذه النتائج أهمية أخذ الجنس والعمر في الحسبان عند تفسير مستويات الكورتيزول وتقييم وظيفة محور HPA.
تأثيرات إفرازه
التأثيرات المناعية الالتهابية
يُعَدّ الكورتيزول من العوامل المهمة في تنظيم الاستجابة الالتهابية، إذ يمتلك القدرة على تثبيط إنتاج كثير من الوسائط الالتهابية، مع التدخُّل في المسارات الجزيئية المسؤولة عن تنشيط الالتهاب، ما يسهم في الحدّ من شدّة الاستجابة الالتهابية، ومنع تفاقمها في ظروف معينة. ومع ذلك، لا يقتصر تأثيره على التثبيط فقط، إذ يتميّز بنمط تنظيم ثنائي الطور للاستجابة الالتهابية في جسم الإنسان، ويمكن أن يعمل بوصفه مثبّطًا أو محفّزًا تبعًا للسياق الفيزيولوجي والجرعة والتوقيت؛ ففي المستويات القاعدية اليومية، لا يُظهِر عادةً تأثيرًا واضحًا مضادًا للالتهاب، ما يشير إلى غياب علاقة خطيّة مباشرة بين مستوياته والتأثير الالتهابي؛ أما في حالات الإجهاد الحادّ أو بعد العمليات الجراحية، فيؤدي دورًا مثبطًا ضمن نطاقات فيزيولوجية مُحدّدة. وقد أظهرت الدراسات أن إعطاء جرعات متوسطة من الكورتيزول قبل التعرُّض لمحفز التهابي، يمكن أن يؤدي إلى تضخيم الاستجابة الالتهابية اللاحقة، في حين أن الجرعات العالية جدًّا قد لا تُظهر تأثيرًا واضحًا، سواء بالتثبيط أم التحفيز[12].
التأثيرات العصبية والقلبية
يؤدي الكورتيزول دورًا أساسيًّا في تنظيم وظائف الدماغ والقلب والأيض، لكن المستويات المرتفعة منه لأوقات طويلة يمكن أن تؤدي إلى تأثيرات سلبية متعددة. على الصعيد العصبي، أظهرت الدراسات أن الارتفاع المزمن في الكورتيزول، كما يحدث في متلازمة كوشينغ (Cushing’s syndrome/ هو اضطراب ناتج من الإفراط في إنتاج الكورتيزول من الغدة الكظرية) أو خلال أوقات التوتّر الطويلة، يرتبط بانخفاض تدفُّق الدم إلى مناطق الدماغ المسؤولة عن العمليات المعرفية، مثل القشرة الجبهية الأمامية والحُصين. يؤدي ذلك إلى ضعف الاتصال الوظيفي بين هذه المناطق، ما قد ينعكس سلبًا على الذاكرة والانتباه، والقدرة على اتخاذ القرار[13].
أما من الناحية القلبية، فإن المستويات المرتفعة من الكورتيزول ترتبط بزيادة خطر الإصابة بمشكلات القلب والأوعية الدموية. وتشمل هذه التأثيرات: ارتفاع ضغط الدم، وتسارع ضربات القلب، وزيادة القابلية لاضطرابات النظم القلبي. يُعَدّ ارتفاع الكورتيزول المزمن مؤشرًا أيضًا على زيادة احتمالية الإصابة بأمراض القلب في المستقبل، نظرًا لتأثيره في ضغط الدم، والتمثيل الغذائي، ووظائف الأوعية الدموية[14].
علاوة على ذلك، يؤدي الكورتيزول المرتفع إلى تغيُّرات أيضية تُسهم في زيادة تراكُم الدهون، خصوصًا في منطقة البطن، فهو يُعزّز تكسير الدهون في الأنسجة المحيطية (مثل الأطراف)، مع زيادة إعادة توزيعها وتخزينها في منطقة البطن، ويزيد أيضًا من الشهية، ويُحفّز الرغبة في تناول الأطعمة الغنية بالسكريات والدهون. هذه التأثيرات، مع مرور الوقت، تُسهم في زيادة الوزن ومقاومة الإنسولين، وترفع من خطر الإصابة بمتلازمة الأيض وأمراض القلب[15].
الاضطرابات المرتبطة به
تؤدي اختلالات مستويات الكورتيزول إلى مجموعة من الاضطرابات التي تؤثر في الصحة الجسدية والنفسية، من أبرزها متلازمة كوشينغ (Cushing’s syndrome)، التي تنتُج من الارتفاع المزمن في الكورتيزول، سواء بسبب أورام الغدة الكظرية أم الإفراز المفرط لهرمون ACTH من الغدة النخامية. تتميَّز هذه الحالة بزيادة الوزن في منطقتَي البطن والوجه خصوصًا، مع ضعف العضلات، وهشاشة العظام، وارتفاع ضغط الدم، واضطرابات التمثيل الغذائي.[16]
في المقابل، يمكن أن يؤدي نقص الكورتيزول إلى مرض أديسون Addison’s disease))، وهو حالة نادرة تنتُج من قصور الغدة الكظرية في إنتاج الهرمون، وتشمل أعراضها: التعب المزمن، وفقدان الوزن، وانخفاض ضغط الدم، والاضطرابات الأيضية.
علاوة على ذلك، ترتبط اختلالات الكورتيزول المزمنة بمشكلات أخرى، مثل: اضطرابات النوم، والقلق، والاكتئاب، وضعف المناعة، وزيادة خطر الأمراض القلبية، والتمثيل الغذائي. يبرز هذا أهمية التوازن الدقيق لمستويات الكورتيزول للحفاظ على الصحة العامة.[17]
مثلًا، وعند التعرّض للتوتر المزمن، تظل مستويات الكورتيزول مرتفعة مدة طويلة، ما يؤدي إلى اضطراب النمط الطبيعي للإفراز، ويؤثر في وظائف متعددة في الجسم. على الصعيد العصبي، يرتبط ارتفاع الكورتيزول المزمن بتغيُّرات في مناطق الدماغ مثل الحُصين والقشرة الجبهية الأمامية، ما قد يُضعف الذاكرة والتركيز، ويزيد من القلق والاكتئاب[18]. في الجهاز المناعي، يمكن أن يُضعف الكورتيزول المزمن الاستجابة المناعية أو يُخلّ بتوازنها، ما يزيد القابلية للالتهابات والأمراض المزمنة. أما بالنسبة للقلب والأوعية الدموية، فإن التعرض المستمر للكورتيزول المرتفع يرتبط بارتفاع ضغط الدم واضطرابات ضربات القلب، ويزيد من خطر الأمراض القلبية الوعائية على المدى الطويل. كذلك، يمكن أن يؤثر التوتر المزمن في الأيض، مُسبّبًا زيادة مستويات السكر في الدم، ومقاومة الإنسولين، وزيادة تراكم الدهون في منطقة البطن خصوصًا.
بذلك، يُظهر الكورتيزول في سياق التوتر المزمن تأثيرات واسعة في الصحة الجسدية والنفسية، مؤكّدًا دوره -بوصفه هرمونًا رئيسًا- في استجابات الجسم للإجهاد المزمن.[19]
الجوانب السريرية والتشخيص
يرتبط تشخيص اضطرابات الكورتيزول مباشرةً بوظائف الغدة الكظرية والمستويات غير الطبيعية للهرمون في الجسم؛ ففي حالة قصور الغدة الكظرية (مرض أديسون)، تُنتِج الغدة كمية منخفضة من الكورتيزول، ما يؤدي إلى أعراض مثل التعب المزمن، وفقدان الوزن، وانخفاض ضغط الدم. أما متلازمة كوشينغ، فتنتُج من إفراز مفرط للكورتيزول من الغدة الكظرية نفسها، أو نتيجة زيادة إفراز ACTH من الغدة النخامية، وتَظهر سريريًّا بزيادة الوزن في الوجه والجسم الأوسط، مع ضعف العضلات وارتفاع ضغط الدم[20].
يُستخدَم القياس المختبري لمستوى الكورتيزول في الدم أو اللُّعاب أو البول لتحديد وجود خلل؛ ففي مرض أديسون، يظهر انخفاض واضح في مستويات الكورتيزول، بينما في متلازمة كوشينغ يُلحَظ ارتفاع غير طبيعي. ولتحديد مصدر الخلل، يمكن استخدام اختبارات التحفيز أو التثبيط، مثل اختبار ACTH أو اختبار الدكساميثازون (Dexamethasone):
- إذا لم يرتفع الكورتيزول بعد تحفيز ACTH، فهذا يُشير إلى قصور أولي في الغدة الكظرية.
- إذا لم يُثبَّط الكورتيزول بعد تناول الدكساميثازون، فهذا يشير إلى إفراز مفرط من الغدة النخامية أو وجود أورام.
تُستكمَل هذه الفحوصات غالبًا بالتصوير الشعاعي، مثل الموجات المقطعية أو الرنين المغناطيسي للغدة الكظرية أو الغدة النخامية، لتحديد السبب الدقيق للخَلَل، ووضع خطة علاجية مناسبة[21].
علاجه للمناعة الذاتية
يُستخدَم الكورتيزول بجرعاتٍ عالية في علاج كثير من الأمراض الذاتية المناعية، نظرًا لتأثيره القوي في تثبيط نشاط الجهاز المناعي، وتقليل الالتهابات المزمنة الناتجة من مهاجمة الجهاز المناعي لأنسجة الجسم السليمة. تعمل الكورتيكوستيرويدات (Corticosteroids)، وهي الأشكال الدوائية للكورتيزول، على منع إنتاج السيتوكينات الالتهابية (Inflammatory Cytokines)، وتثبيط تكاثر الخلايا اللمفاوية التائية (T Lymphocytes)، ما يؤدي إلى خفض الاستجابة المناعية المفرطة التي تُميّز أمراضًا مثل الذئبة الحمراء (Systemic Lupus Erythematosus, SLE)، والتهاب المفاصل الروماتويدي (Rheumatoid Arthritis). يُستخدَم الكورتيزول كذلك في السيطرة على الأعراض الحادّة مثل الألم والتورم والحُمّى، من خلال تقليل نفاذية الشعيرات الدموية، وتثبيط إفراز المواد الكيميائية الالتهابية[22].
ورغم فاعليته العالية، فإن الاستخدام طويل الأمد للكورتيزول قد يُسبّب آثارًا جانبية خطرة، تشمل: هشاشة العظام، وارتفاع ضغط الدم، وزيادة الوزن، وضعف المناعة، وارتفاع مستويات السكر في الدم. لذلك، يُوصى باستخدامه بجرعات مضبوطة، وتحت إشراف طبي دقيق، لتحقيق التوازن بين فوائده ومخاطره.
المراجع
Björntorp, P. “Do Stress Reactions Cause Abdominal Obesity and Comorbidities?”
Obesity Reviews. vol. 2, issue 2 (2001). pp. 73-140.
Charmandari, E., N. C. Nicolaides & G. P. Chrousos. “Adrenal Insufficiency.”
Lancet. vol. 383, issue 9935 (2014). pp. 2152-2167.
Chrousos, G. P. “Stress and Disorders of the Stress System.”
Nature Reviews Endocrinology. vol. 5 (2009). pp. 374-381.
Clow, A. et al. “The Cortisol Awakening Response: More Than a Measure of HPA Axis Function.”
Neuroscience & Biobehavioral Reviews. vol. 35, no. 1 (2010). pp. 97-103.
Dong, J. et al. “Cortisol Modulates Inflammatory Responses in LPS-Stimulated RAW264.7 Cells via the NF-κB and MAPK Pathways.”
BMC Veterinary Research. vol. 14, no. 30 (2018).
Fries, Eva, Lucia Dettenborn & Clemens Kirschbaum. “The Cortisol Awakening Response (CAR): Facts and Future Directions.”
International Journal of Psychophysiology. vol. 72, issue 1 (2009). pp. 67-73.
Herman, J. P. et al. “Regulation of the Hypothalamic-Pituitary-Adrenocortical Stress Response.”
Comprehensive Physiology. vol. 6, no. 2 (2016). pp. 603-621.
Lillis, Charlotte. “What Is Cortisol? and what is its purpose?”
Medicalnewstoday. 30/10/2024. at:
https://acr.ps/1L9BPSL
Marin, M. F. et al. “Chronic Stress, Cognitive Functioning and Mental Health.” Neurobiology of Learning and Memory. vol. 96, no. 4 (2011). pp. 583–95. doi: 10.1016/j.nlm.2011.02.016
McEwen, B. S. “The Neurobiology of Stress: From Serendipity to Clinical Relevance.”
Brain Research. vol. 886, issue 1-2 (2000). pp. 172-189.
Newell-Price, J. et al. “Cushing’s Syndrome.”
Lancet. vol. 367, no. 9522 (2006). pp. 1605-1617.
Petramala, L. et al. “Autoimmune Diseases in Patients with Cushing's Syndrome.”
International Journal of Endocrinology. vol. 2018 (2018). Article ID 1464967.
Tsigos, C. & G. P. Chrousos. “Hypothalamic–Pituitary–Adrenal Axis, Neuroendocrine Factors and Stress.”
Journal of Psychosomatic Research. vol. 53, issue 4 (2002). pp. 865-871.
Voorn, Bibian van der et al. “Gender-Specific Differences in Hypothalamus–Pituitary–Adrenal Axis Activity During Childhood: A Systematic Review and Meta-Analysis.”
Biology of Sex Differences. vol. 8, no. 3 (2017). pp. 2-9.
Vogelzangs, N. et al. “Urinary Cortisol and Six-Year Risk of All-Cause and Cardiovascular Mortality.”
The Journal of Clinical Endocrinology & Metabolism. vol. 95, issue 11 (2010). pp. 4959-4964.
Wittmann, Miriam. “A General Introduction to Glucocorticoid Biology.”
Frontiers in Immunology. vol. 10 (2019). pp. 1-17. doi:
10.3389/fimmu.2019.01545
[1] Charlotte Lillis, “What Is Cortisol? and what is its purpose?” medicalnewstoday, 30/10/2024, accessed on 18/12/2025, at:
https://acr.ps/1L9BPSL
[2] J. P. Herman et al., “Regulation of the Hypothalamic-Pituitary-Adrenocortical Stress Response,” Comprehensive Physiology, vol. 6, no. 2 (2016), pp. 603–621, doi: 10.1002/cphy.c150015
[3] Ibid.
[4] Ibid.
[5] Miriam Wittmann, “A General Introduction to Glucocorticoid Biology,”
Frontiers in Immunology, vol. 10 (2019), pp. 1-17, doi:
10.3389/fimmu.2019.01545
[6] A. Clow et al., “The Cortisol Awakening Response: More Than a Measure of HPA Axis Function,”
Neuroscience & Biobehavioral Reviews, vol. 35, no. 1 (2010), pp. 97-103.
[7] Eva Fries, Lucia Dettenborn & Clemens Kirschbaum, “The Cortisol Awakening Response (CAR): Facts and Future Directions,”
International Journal of Psychophysiology, vol. 72, issue 1 (2009), pp. 67-73.
[8] Ibid.
[9] J. Newell-Price et al., “Cushing’s Syndrome,”
Lancet, vol. 367, no. 9522 (2006), pp. 1605-1617.
[10] E. Charmandari, N. C. Nicolaides & G. P. Chrousos, “Adrenal Insufficiency,”
Lancet, vol. 383, issue 9935 (2014), pp. 2152-2167.
[11] Bibian van der Voorn et al., “Gender-Specific Differences in Hypothalamus–Pituitary–Adrenal Axis Activity During Childhood: A Systematic Review and Meta-Analysis,”
Biology of Sex Differences, vol. 8, no. 3 (2017), p. 3.
[12] C. Tsigos & G. P. Chrousos, “Hypothalamic–Pituitary–Adrenal Axis, Neuroendocrine Factors and Stress,”
Journal of Psychosomatic Research, vol. 53, issue 4 (2002), pp. 865-871.
[13] M. F. Marin et al., “Chronic Stress, Cognitive Functioning and Mental Health,” Neurobiology of Learning and Memory, vol. 96, no. 4 (2011), pp. 583–95, doi: 10.1016/j.nlm.2011.02.016
[14] N. Vogelzangs et al., “Urinary Cortisol and Six-Year Risk of All-Cause and Cardiovascular Mortality,”
The Journal of Clinical Endocrinology & Metabolism, vol. 95, issue 11 (2010), pp. 4959-4964.
[15] P. Björntorp, “Do Stress Reactions Cause Abdominal Obesity and Comorbidities?”
Obesity Reviews, vol. 2, issue 2 (2001), pp. 73-86.
[16] Tsigos & Chrousos,
op. cit.
[17] J. Dong et al., “Cortisol Modulates Inflammatory Responses in LPS-Stimulated RAW264.7 Cells via the NF-κB and MAPK Pathways,”
BMC Veterinary Research, vol. 14, no. 30 (2018).
[18] G. P. Chrousos, “Stress and Disorders of the Stress System,”
Nature Reviews Endocrinology, vol. 5 (2009), pp. 374-381.
[19] B. S. McEwen, “The Neurobiology of Stress: From Serendipity to Clinical Relevance,”
Brain Research, vol. 886, issue 1-2 (2000), pp. 172-189.
[20] Newell-Price et al.,
op. cit.
[21] Ibid.; Charmandari, Nicolaides & Chrousos,
op.cit.
[22] L. Petramala et al., “Autoimmune Diseases in Patients with Cushing's Syndrome,”
International Journal of Endocrinology, vol. 2018 (2018), Article ID 1464967.