الكيمياء الحيوية (Biochemistry) فرع أساسي من العلوم الدقيقة، يختص في دراسة العناصر والمركبات الكيميائية في الكائنات الحية، من حيث بنيتها وخصائصها والعمليات الحيوية والتفاعلات الكيميائية المرتبطة بها. يجمع هذا العلم بين مبادئ علمَي
الكيمياء والأحياء، ويهدف إلى توضيح الآليات الجزيئية التي تقوم عليها الوظائف الحيوية. بدأ تطوّر علم الكيمياء الحيوية في القرن الثامن عشر، وقد توصّل إلى إنجازات مهمة مثل اكتشاف عمليات
التخمّر (Fermentation) وعمل
الإنزيمات (Enzyme) خلال القرنين الثامن عشر والتاسع عشر، كما اكتُشفت بنية
الحمض النووي (Nucleic acid) في القرن العشرين. تشمل الكيمياء الحيوية مجالات أساسية، مثل
التمثيل الغذائي (الاستقلاب أو الأيض، Metabolism) والعمليات الخلوية والتقنيات التحليلية المختلفة، وتمتد تطبيقاتها إلى مجالات عدة مثل
الطب والصيدلة، من خلال اكتشاف مسببات الأمراض وتشخيصها وعلاجها وتصميم الأدوية الدقيقة، وفي مجال الزراعة وإنتاج المحاصيل وفهم التكوين الجزيئي والخلوي للنباتات، كذلك العلوم البيئية باستخدام المعالجة الحيوية للملوثات الطبيعية والصناعية. ويتقاطع هذا العلم مع علوم أخرى عديدة، وهو مجالٌ يتطوّر باستمرار، مع تطور البحث وتراكم المعرفة والتقدم التقني في مجالات وتخصصات متعددة.
التكامل بين الكيمياء والأحياء
الكيمياء الحيوية (البيوكيمياء أو الكيمياء البيولوجية) فرع من فروع العلوم الدقيقة يهدف إلى دراسة العمليات الحيوية التي تحدث داخل الكائنات الحية وفهمها، بتقاطع علمَي الكيمياء والأحياء. يركّز مجاله بصورة عامة على الآليات الجزيئية والمسارات الحيوية التي تقوم عليها الوظائف البيولوجية للكائنات الحية، من خلال البحث في بُنيات
الجزيئات الحيوية الكبيرة (Macromolecules) الأربع، وخصائصها وتفاعلاتها، وهي
البروتينات (Proteins)، والأحماض النووية، والكربوهيدرات (السكّريّات، Carbohydrates)، والدهون (Lipids)، إضافة إلى البحث في وحدات بنائها الأساسية والجزيئات الصغيرة الأخرى. يهدف علماء الكيمياء الحيوية والباحثين في مجالها إلى اكتشاف المبادئ الأساسية التي تحكم الحياة على المستوى الجزيئي، من خلال دراسة الجزيئات في وسطها الطبيعي في الجسم الحي (in vivo) أو خارجه في المختبر (in vitro) (الشكل 1)، والبحث في كيفية مساهمتها في المسارات البيوكيميائية (Biochemical pathways) والعمليات الخلوية المختلفة. بصورة عامة، فإن دراسات الكيمياء الحيوية تحاول كشف تعقيد الأنظمة البيولوجية وتطبيق هذه المعرفة على التحديات العملية في العديد من التخصصات، مثل الطب والصيدلة والزراعة والعلوم البيئية والعلوم الجنائية وغيرها.
[الشكل 1]
 الدراسات البيوكيميائية في أجسام الحيوانات المخبرية (in vivo) أو خارجها (in vitro)
الدراسات البيوكيميائية في أجسام الحيوانات المخبرية (in vivo) أو خارجها (in vitro)
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
ترتبط الكيمياء الحيوية ارتباطًا وثيقًا بالتخصصين التي انبثقت منهما، الكيمياء والأحياء؛ ففي حين أن الكيمياء تبحث في المبادئ الأساسية للتفاعلات والارتباطات بين الجزيئات وآلياتها، وهي المبادئ الضرورية لتفسير الوظائف الحيوية في الكائنات الحية، يبحث علم الأحياء في معرفة السياق البيولوجي لهذه العمليات، مع التركيز على كيفية مساهمة المسارات البيوكيميائية في العمليات والوظائف الحيوية في الصحة والمرض. لذا فإن الكيمياء الحيوية هي مجال عابر للتخصصات (Interdisciplinary)، ما يسمح لهذا العلم بالتجسير ما بين النظرية الكيميائية والتطبيق البيولوجي، ويتيح التقدم في مجالات تطبيقية مختلفة، مثل تطوير
الأدوية، والهندسة الوراثية، والتحكم بالعمليات الأيضية. تُجسّد الكيمياء الحيوية تكامل المبادئ الكيميائية مع الأنظمة البيولوجية، ما يعزز فهم المجالين.
تاريخ الكيمياء الحيوية
كان النمساوي ڤينسنز كليتزينسكي (1826-1882) أول من أطلق على هذا المجال الكيمياء الحيوية (بالألمانية Biochemie)، في عام 1858، بكتابه
الدليل إلى الكيمياء الحيوية (Compendium der Biochemie)، الذي وصف فيه المكونات الكيميائية للكائنات الحية، وكيفية وصولها إلى الخلايا، والعمليات المحفِّزة التي تخضع لها في مختلف الكائنات[1]. ومع أن الانطلاقة الفعلية لعلم الكيمياء الحيوية بدأت في مطلع القرن العشرين، وهي الفترة التي تميّزت بتراكم الإنجازات التي أتاحت نمو هذا الحقل وتطوره، فإن أصول الاكتشافات هذا العلم بوصفه حقلًا علميًا بذاته تعود إلى أوائل القرن التاسع عشر، وربما قبل ذلك، في محاولات العلماء والأطباء فهم الطبيعة الكيميائية للمواد الحيوية[2].
وقد اختلفت الآراء حول بدايات حقل الكيمياء الحيوية، فالملاحظات التي وضعها أنطوان لاڤوازييه (Antoine Lavoisier، 1743-1794) في القرن الثامن عشر في دراسته عمليتي
التنفس الخلوي (Cellular respiration) والتخمّر[3]، كانت ركنًا أساسيًا لإنشاء هذا العلم. غير أن البداية الفعلية كانت في عام 1828، عندما صنّع العالم الألماني فريدرش ڤولر (1800-1882) مادة اليوريا (Urea) من مركّب غير عضوي[4]، هو
سيانات الأمونيوم (Ammonium cyanate)[5]، النتيجة التي حصل عليها بغير قصد منه[6]، واليوريا مركّب عضوي ينتجه الجسم نتيجة لاستقلاب الجزيئات المحتوية على عنصر نيتروجين. والنتيجة التي حصل عليها ڤولر باكتشافه، كانت لحظة فارقة في علمي الأحياء والكيمياء؛ إذ دحضت التصوّر السائد حينئذ بأن المواد العضوية أو "الحية" لا يمكن تكوينها إلّا بوساطة الكائنات الحية، وأثبتت إمكانية تصنيع المركبات العضوية من مواد غير عضوية. سدّت هذه التجربة الرائدة الفجوة بين
الكيمياء العضوية (Organic chemistry) والأنظمة البيولوجية ومهدت الطريق للدراسات المستقبلية في الأساس الكيميائي للحياة. ومع هذا، يزعُم البعض أن مجال الكيمياء الحيوية بدأ مع اكتشاف العالم الفرنسي أنسيلم باين (Anselme Payen، 1795-1871) أول إنزيم، والمعروف باسم
ألفا أميلاز (Alpha-amylase)، في عام 1833[7]، بينما يعتقد آخرون أن تجارب الكيميائي الألماني إدوارد بوخنر (Eduard Buchner، 1860-1917) في عام 1897، في عملية التخمّر الكحولي (Alcoholic fermentation) في المستخلصات الخالية من الخلايا (Cell-free extracts)، والتي حصل على جائزة نوبل في الكيمياء في عام 1907 بسببها[8]، كانت الانطلاقة الحقيقية للكيمياء الحيوية الحديثة (الصورة 1).
[الصورة 1] - روّاد علم الكيمياء الحيوية
 (من اليمين الى اليسار) : ڤولر، كليتزينسكي، لاڤوازييه، باين، بوخنر
(من اليمين الى اليسار) : ڤولر، كليتزينسكي، لاڤوازييه، باين، بوخنر
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
بعد نشوء الكيمياء الحيوية بوصفه مجالًا علميًا جديدًا، بدأ يتطوّر إلى تخصص علمي منفرد قائم بذاته من خلال إنشاء مؤسسات متخصصة واعتماد برامج أكاديمية معنية بهذا المجال في الجامعات. بدايةً، كان التوجّه بدمج الكيمياء الحيوية ضمن المجالين الأوسع، الكيمياء أو الأحياء، فأنشأت الجامعات أقسام الكيمياء والكيمياء الحيوية، أو الأحياء والكيمياء الحيوية. وفي منتصف القرن العشرين، أُسس بوصفه تخصصًا مستقلًا له منهجياته ومجالاته البحثية. وقد ساهمت المؤسسات المهنية المتخصصة، مثل الجمعية الأميركية للكيمياء الحيوية وعلم الأحياء الجزيئي (American Society for Biochemistry and Molecular Biology, ASBMB) في عام 1906[9]، وإنشاء المجلات المتخصصة أيضًا، في إضفاء الطابع الرسمي على هذا المجال، ومن تلك المجلات
مجلة الكيمياء البيولوجيةJournal of Biological Chemistry التي أُنشئت في عام 1905.
ومنذ ذلك الحين، شهد علم الكيمياء الحيوية تطوّرًا كبيرًا بفضل تطوير تقنيات جديدة ساهمت في تعزيز البحوث البيوكيميائية المتخصصة (الشكل 2)، ما أسفر عن اكتشاف العديد من الجزيئات والعمليات الاستقلابية في الخلايا. من بين هذه التقنيات:
الكروماتوغرافيا (Chromatography)، ودراسة البلورات بالأشعة السينية (X-ray diffraction)، والرنين النووي المغناطيسي (Nuclear magnetic resonance)، والمطيافية (Spectroscopy)، والمجهر الإلكتروني (Electron microscope)، والوسم بالنظائر المشعة (Radiolabelling)، وغيرها من التقنيات العديدة التي أتاحت اكتشاف الجزيئات والمسارات الاستقلابية (Metabolic pathways) المختلفة داخل
الخلية، مثل
تحلل السكّر (أو
التحلل الغلايكولي، Glycolysis)، وحلقة كربس (دورة حمض الستريك،Citric acid cycle ) وغيرها، ما وسّع مفاهيم علم الكيمياء الحيوية على مستوى الجزيئات والمسارات بصورة أعمق وأدق[10].
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
ومع تطوّر علم الكيمياء الحيوية، ساهمت أهم إنجازاته في انبثاق العديد من العلوم الأخرى، منها مثلًا
الأحياء الجزيئية (Molecular biology). ففي عام 1953، استنبط جيمس واتسون (James Watson، 1928-) وفرنسيس كريك (Francis Crick، 1916-2004)[11]، بالاعتماد على إسهامات أساسية من
روزاليند فرانكلين (Rosalind Franklin، 1920-1958) وموريس ويلكنز (Maurice Wilkins، 1916-2004) (الصورة 2)[12]، بنية
الحمض النووي الريبي منقوص الأكسجين (DNA) اللولبي المزدوج (Double helix) (الشكل 3). كان هذا الاكتشاف ثوريًا في مجال الكيمياء الحيوية والمجالات النظيرة، إذ قدّم الأساس الجزيئي لتخزين المعلومات الجينية ونقلها، وأدى إلى الكشف عن ماهية
الشيفرة الوراثية (Genetic code)، وحفّز التقدم السريع في علم الوراثة وعلم الأحياء الجزيئية والطب الشرعي ومجالات أخرى عديدة. كانت الإنجازات في الكشف المتتالي والمتراكم عن أشكال المركبات الحيوية وتفصيل المسارات الاستقلابية محوريةً لتوضيح كيفية توليد الخلايا للطاقة واستخدامها لها، ما أدّى إلى نشوء مجال جديد، هو علم الطاقة الحيوية (Bioenergetics). ومع تطور الحواسيب الآلية، أنشئ علم
المعلوماتية الحيوية (Bioinformatics) المعني باستخدام التقنيات والأدوات الحاسوبية لتحليل وإدارة البيانات البيولوجية وتفسيرها، وخاصة البيانات الجينية والجينومية والبروتينية. كما أتاحت الاكتشافات المتوالية في الكيمياء الحيوية تحسين صحة الإنسان من خلال إدماج مفاهيم الكيمياء الحيوية في العلوم الطبية ودراسة العوامل المُمْرِضة، وعلوم التغذية والحمية، والتمريض والصيدلة، فأصبحت الكيمياء الحيوية جزءًا أساسيًّا من تلك العلوم، وشكلّت دراستها أساسًا لكليات الطب[13].
[الصورة 2] - مكتشفو تحليل شكل الحمض النووي منقوص الأكسجين (DNA)
 (من اليمين إلى اليسار): فرانكلين، ويلكنز، كريك، واتسون
(من اليمين إلى اليسار): فرانكلين، ويلكنز، كريك، واتسون
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل 3]
 الشكل اللولبي المزدوج للحمض النووي الريبي منقوص الأكسجين (DNA)
الشكل اللولبي المزدوج للحمض النووي الريبي منقوص الأكسجين (DNA)
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
استمر علم الكيمياء الحيوية في التطوّر مع بداية القرن الحادي والعشرين، ولا سيّما مع ظهور تقنيات جديدة وأساليب متداخلة التخصصات. وقد أدى دمج
علم الجينوميات (Genomics) وعلم البروتيوميات (Proteomics) وعلم الدهنيات (Lipidomics) وعلم أحياء النُظُم (Systems biology) إلى توسيع نطاق هذا المجال، ما مكّن العلماء من إجراء دراسات شاملة للأنظمة البيولوجية على المستوى الجزيئي. وقد وفّرت ابتكارات مثل
المجهر الإلكتروني المبرَّد أو فائق البرودة {{المجهر الإلكتروني المبرَّد أو فائق البرودة: تقنية تصوير رائدة تكشف عن الهياكل ثلاثية الأبعاد للجزيئات الحيوية بدقة شبه ذريّة. تُجمّد العينات بسرعة للحفاظ على حالتها الأصلية، ثم تُصوّر باستخدام مجهر إلكتروني. وقد ابتكر هذه التقنية جاك دوبوشيه، ويواكيم فرانك، وريتشارد هندرسون، ما منحهم جائزة نوبل في الكيمياء عام 2017. تتجاوز هذه التقنية الحاجة إلى التبلور، ما يتيح دراسة المعقدات البروتينية الكبيرة، والڤيروسات، والآليات الخلوية الأخرى.}} (Cryogenic electron microscope) وأدوات الحوسبة المتقدمة والمعلوماتية الحيوية اكتشافات مهمة في الهياكل والبنيات الجزيئية للمركبات الحيوية، إضافة إلى الوظائف الجزيئية الحيوية في الصحة والمرض.
مفاهيم أساسية في الكيمياء الحيوية
تدرُس الكيمياء الحيوية بشكل أساسي ثلاثة مجالات مرتبطة ببعضها البعض. في المجال الأول تركّز دراسة الكيمياء الحيوية على أشكال الجزيئات الحيوية ووظائفها التي تشكّل اللّبنات الأساسية للحياة. تشمل هذه المركبات العائلات الجزيئية الكبيرة الأربع: الكربوهيدرات والدهون والبروتينات والأحماض النووية (الجدول 1)، إضافة إلى مجموعة متنوّعة من الجزيئات البيولوجية الصغيرة التي تتشكّل في الخلايا، وتكون جزءًا أساسيًا من وظائفها[14].
لكل جزيء حيوي دور أو أدوار مميزة ومهمة في الأنظمة البيولوجية في الخلية وخارجها، فالكربوهيدرات، أولى تلك العائلات الجزيئية، هي مصدر أولي لإنتاج الطاقة في الخلايا، ومنها ما يشكّل بعض المكونات البنيوية في الكائنات الحية، ويمكن تقسيمها حسب بُنيتها أو وظائفها، فمنها الكربوهيدرات البسيطة (Simple carbohydrates)، مثل سكر
الغلوكوز {{الغلوكوز: (C₆H₁₂O₆، Glucose) سكر أحادي سداسي الكربون، وهو المصدر الرئيس للطاقة لمعظم الكائنات الحية، والناتج الرئيس لعملية التمثيل الضوئي (Photosynthesis)، والركيزة الأساسية للتنفس الخلوي (Cellular respiration). يدور في الدم على شكل سكر الدم، ويُخزن على شكل
غلايكوجين {{الغلايكوجين (النشا الحيواني): (Glycogen)جزيء كبير مكون من مبلمرات الغلوكوز المتفرعة، وهو الصورة التي يُخزن فيها الغلوكوز في الجسم. يُخزّن في الكبد والعضلات. وعند نقص مستوى الغلوكوز في الدم فإن الكبد يُكسّر الغلايكوجين للمحافظة على مستوًى ثابتٍ من الغلوكوز، وخصوصًا في حالات الصيام. وبعد تناول وجبة فيها سكريات، يدخل الغلوكوز إلى الدم مسببًا ارتفاع تركيزه، ويدخل إلى خلايا الكبد ومن ثم يُحوّل الغلوكوز إلى غلايكوجين لتخزينه.}} في الكبد والعضلات لدى الحيوانات أو على شكل
نشا (Starch) في النباتات. يتحلل في الخلية لإنتاج طاقة بوساطة التحلل الغلايكولي (Glycolysis) والفسفرة التأكسدية (Oxidative phosphorylation).}} الأحادي أو السكرين الثنائيين: سكر الحليب أو اللاكتوز (Lactose) وسكر المائدة أو السُّكروز (Sucrose)، وجميعها سكريّات مركزية لعمليات الاستقلاب وإنتاج الطاقة الحيوية. في حين تعمل الكربوهيدرات المعقّدة (Complex carbohydrates) منها مخازن احتياطية للطاقة، مثل النشا والغلايكوجين (النشا الحيواني)، أو مواد بنيوية مكوّنة لجدران الخلايا (Cell wall) في الكائنات الحية المختلفة، مثل السليولوز (Cellulose) في النباتات والكايتين (Chitin) في الفطريات والحشرات، والبيبتيدوغلايكان (Peptidoglycan) في
البكتيريا[15].
أما الدهون، ثاني العائلات الجزيئية، فهي جزيئات كارهة للماء (Hydrophobic) تكوّن
أغشية الخلايا (Cell membrane)، وهي ضرورية لتخزين الطاقة وانتقال الإشارات الخلوية (Cell signaling). وتشمل هذه الفئة من الجزيئات الكبيرة
الدهون الفسفورية (Phospholipids)، والزيوت (Oils)، والشحوم (Fats)، والستيرولات (Sterols)، والدهون السفينغولية (Sphingolipids)، إضافة إلى جزيئات أخرى كارهة للماء داخل
الخلايا. تشكّل الدهون الغليسروفسفورية (Glycerophospholipids) على وجه الخصوص الطبقة الدهنية المزدوجة (Lipid bilayer) لأغشية الخلايا، ما يخلق حاجزًا شبه نفّاذ، وهو ضروري لسلامة الخلايا وحياتها ووظائفها. تعتبر الدهون السفينغولية مهمة من الناحية البنيوية من حيث كونها جزيئات ناقلة للإشارات في داخل الخلايا، في حين أن الستيرولات، مثل
الكوليسترول (Cholesterol) لها أدوار بنيوية وهرمونية داخل جسم الكائن الحي وخلاياه[16].
الفئة الثالثة من العائلات الجزيئية الكبيرة هي البروتينات التي تتكوّن من ترابط
الأحماض الأمينية مع بعضها البعض، وهي جزيئات لها أدوار مختلفة في الخلية، منها التحفيز الإنزيمي والدعم البنيوي والاستجابة المناعية (Immune response)، ونقل الإشارات، ونمو الخلية وموت الخلية {{موت الخلية: عملية بيولوجية حيوية ومستمرة تُزال فيها الخلايا التالفة أو المُصابة أو غير الضرورية، ما يُحافظ على توازن الأنسجة ونموها بشكل طبيعي. هناك العديد من المسارات المُنظّمة المؤدية للموت الخلوي، من أبرزها موت الخلايا المُبرمج (Programmed cell death)، أو استماتة الخلايا (Apoptosis)، والنخر (Necrosis)، أي موت الخلايا غير المُتحكّم فيه، والالتهام الذاتي (Autophagy) أي التحلل الذاتي.}}. ففي حين تعمل الإنزيمات، وهي مجموعة فرعية من البروتينات، وظيفة محفزات بيولوجية (Biological catalysts)، وتسرّع التفاعلات الكيميائية المهمة للحياة، تؤدي الناقلات (Transporters) نقل المواد داخل الخلايا وخارجها، وعبر الأغشية. كما تدعم البروتينات الليفية (Fibrous proteins) الهيكل الخلوي (Cytoskeleton) والشبكة النسيجية الخارجية للخلية (المصفوفة خارج الخلية، Extracellular matrix)، وكلاهما يعمل على استقرار الخلايا والأنسجة المحيطة. كما تعمل بروتينات الإشارة على تحويل الإشارات الكيميائية إلى عمل محدد داخل الخلايا[17].
أما الأحماض النووية (DNA وRNA)، الفئة الأخيرة من العائلات الجزيئية الكبيرة، فهي جزيـئات حيوية وأساسية لجميع أشكال الحياة المعروفة على كوكب الأرض، إذ إنها مسؤولة عن الوراثة الجزيئية في الخلية. تعمل الأحماض النووية بوصفها أساسًا جزيئيًا لتخزين المعلومات الوراثية، ونقلها، والتعبير عنها، إذ يشفّر الحمضُ النووي الريبي منقوص الأكسجين الصفاتِ الوراثيةَ، بينما تؤدي
جزيئات الحمض النووي الريبي (RNA) أدوارًا مختلفة، من ضمنها تكوين البروتينات وتنظيم هذه العمليات وغيرها في الخلية[18].
[الجدول 1]
 الجزيئات البيوكيميائية الكبيرة الأساسية
الجزيئات البيوكيميائية الكبيرة الأساسية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يتمحور ثاني مجالات الكيمياء الحيوية حول أبحاث التمثيل الغذائي. تُعرّف عمليات الاستقلاب بالتفاعلات الكيميائية التي تحدث داخل الكائنات الحية للحفاظ على استمرارية الحياة. تنقسم هذه العمليات إلى فئتين رئيستين:
العمليات الهدميّة (Catabolism)، والعمليات البنائيّة (Anabolism) (الشكل 4). في المسارات الهدميّة تتحلّل
الجزيئات الكبيرة المعقدة إلى جزيئات أبسط وتنتج الطاقة الخلوية. على سبيل المثال، يتحلّل جزيء الغلايكوجين المعقّد إلى جزيئات الغلوكوز التي بدورها تتكسّر من خلال عملية
التحلل الغلايكولي وحلقة كربس منتجةً غاز ثاني أكسيد الكربون، ولاحقًا ماء، عن طريق عملية
الفسفرة التأكسدية (Oxidative phosphorylation)، وينتج عن هذه العمليات جزيئات الأدينوسين ثلاثي الفوسفات (Adenosine triphosphate, ATP)، وهي عملية إنتاج الطاقة الخلوية بوساطة
سلسلة نقل الإلكترونات (Electron transport chain)، وهي عملية تتكرر عند تحلل جميع المواد المغذية داخل الخلية. أما العمليات البنائية فهي تخلّق الجزيئات المعقدة الكبيرة من جزيئات أبسط، وهي عمليات تتطلّب استخدام الطاقة الحيوية. فمثلًا من الممكن أن يحدث تجمّع لجزيئات حمض اللاكتيك (Lactic acid) في العضلات، ما يؤدي إلى بناء جزيء غلوكوز في الكبد عن طريق عملية
تخليق الغلوكوز (Gluconeogenesis). وعندما يزيد تركيز جزيئات الغلوكوز في الدم عن المعدل الطبيعي، تتجمّع لتكوّن جزيئات الغلايكوجين المعقدة. تشمل هذه المسارات البنائية أيضًا تخليق البروتينات من الأحماض الأمينية، وتكوين الأحماض النووية من
النوكليوتيدات (Nucleotides)، كما تشمل بناء الدهون وتخزينها في الخلايا خاصة، وفي الجسم عامة. تحدث جميع العمليات الاستقلابية بشكل منظّم، وتترابط شبكتها المعقّدة، كما تشتمل على العديد من الضوابط التي تجعلها أساسية لحياة الخلايا. يضمن هذا التنظيم الأيضي (Metabolic regulation) توازن هذه العمليات بعناية، لتلبية احتياجات الخلية من الطاقة ومن المواد الخام، ويجعلها قادرة على التكيّف مع التغيرات البيئية المحيطة، وأيضًا الحفاظ على توازنها الداخلي (Homeostasis). وعند اختلال تنظيم هذه المسارات، تحدث اضطرابات تؤدي إلى أمراض استقلابية مختلفة[19].
[الشكل 4]
 تفاعلات الهدم تنتج جزيئات الطاقة الخلوية ATP بينما تحتاج تفاعلات البناء إليها
تفاعلات الهدم تنتج جزيئات الطاقة الخلوية ATP بينما تحتاج تفاعلات البناء إليها
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
ثالث مجالات البحث في الكيمياء الحيوية العمليات الخلوية، وهو مجال تتقاطع فيه كل من الكيمياء الحيوية والوراثة (Genetics) وعلم الخلية (Cell biology). تتضمن العمليات الخلوية مجموعة من الأنشطة الديناميكية التي تدعم حياة الخلية على المستويين الجزيئي والخلوي. من أهم هذه العمليات نقل الإشارات الخلوية، إذ تستجيب الخلايا للإشارات الخارجية من خلال مسارات معقّدة، تشتمل على المستقبِلات (Receptors)، والرسل الثواني (Second messengers)، والبروتينات المختلفة داخل الخلايا. تمكّن عملية نقل الإشارات الخلايا من التكيّف مع التغيّرات في بيئتها وتنظيم نموها وتنسيق الاستجابات للمحفّزات في بيئتها[20].
تُعدّ الاتصالات الخلوية (Cellular communications) من العمليات الخلوية المهمة أيضًا، ومنها التصاق الخلايا (Cell adhesion)، والتعرّف الجزيئي (Molecular recognition) الذي يعتبر أساسًا لبدء الاستجابة المناعية، إذ تتفاعل الخلايا وتستجيب لبعضها. كما أن تبادل المواد في الخلية من خلال عمليات
الإدخال الخلوي (Endocytosis) والإخراج الخلوي (Exocytosis) (الشكل 5) يعدّ من أساسيات تعريف الحياة لدى الخلية؛ فلا يمكن للخلية أن تستمر من دون تبادل للغذاء والفضلات مع الوسط الخارجي. كما أن جميع عمليات الاستقلاب هي جزء من العمليات الخلوية، فالتنفس الخلوي يتضمن تحويل الطاقة البيوكيميائية الموجودة في العناصر الغذائية إلى طاقة حيوية، التي تستخدمها الخلية لأداء وظائفها. وتتضمن مسارات التنفس الخلوي عدة عمليات خلوية، مثل الفسفرة التأكسدية التي تحدث في
عضيّات المُتقدّرة (الميتوكوندريا، Mitochondria) في
الخلايا حقيقية النواة. وتشمل العمليات الخلوية الأساسية الأخرى
انقسام الخلايا (Cell division)، فتنمو الخلية وتتكاثر بعد عمليات تضاعف الحمض النووي (DNA replication) وتوزيع
الصبغيّات (الكروموسومات) {{الكروموسومات: هياكل طويلة شبيهة بالخيوط، تتكون من الحمض النووي والبروتينات، تحمل المعلومات الوراثية داخل خلايا الكائنات الحية. تنظَّم الكروموسومات في وحدات مميزة، إذ يمتلك كل نوع من الكائنات الحية عددًا محددًا منها، وهي مسؤولة عن أدوار أساسية في عملية انقسام الخلايا ومضاعفة الحمض النووي وتوزيعه بصورة دقيقة. لدى الإنسان مثلًا 46 كروموسومًا، في 23 زوجًا.}} إلى أطراف الخلايا الجديدة. كذلك تعتبر عمليات
الموت الخلوي المبرمج (Programmed cell death) أيضًا من العمليات الخلوية المهمة التي لها دور في الحفاظ على التوازن الخلوي والتخلّص من الخلايا التالفة مع الحفاظ على الخلايا السليمة. تضمن هذه العمليات الخلوية وغيرها الأداء السليم للخلايا وبقائها على قيد الحياة[21].
[الشكل 5]
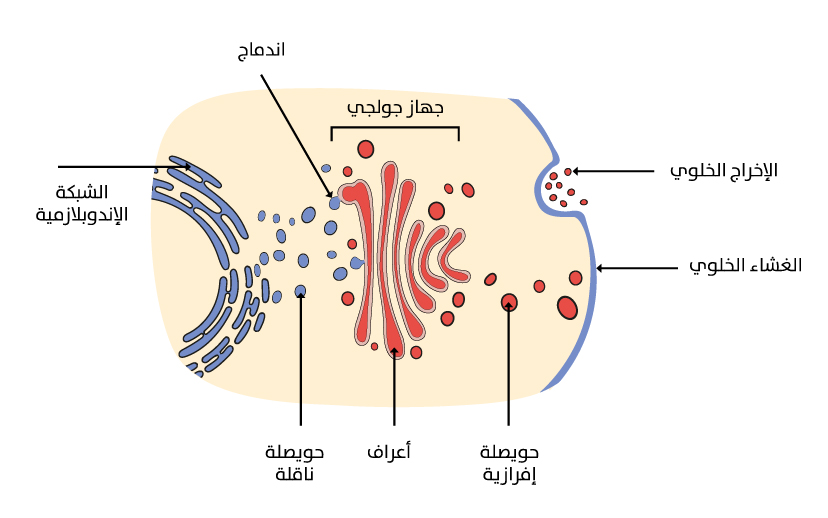 عمليات التبادل الخلوي
عمليات التبادل الخلوي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
التقنيات والأساليب
يستخدم علماء الكيمياء الحيوية ودارسوها مجموعة من التقنيات، منها القديمة ومنها الحديثة، لدراسة الجزيئات والعمليات التي تدعم الحياة. من بين تلك التقنيات والأساليب التحليل الطيفي (المطيافية) الذي يُستخدم فيه الضوء لاستكشاف خصائص العيّنة المفحوصة. على سبيل المثال، تقيس مطيافية الأشعة المرئية وفوق البنفسجية (UV-Vis spectroscopy) مقدار الضوء الذي تمتصه العيّنة المفحوصة، ما يساعد في تحديد تركيز المواد المختلفة فيها، مثل البروتينات أو الأحماض النووية. بينما يوفّر التحليل الطيفي بالرنين المغناطيسي النووي، معلومات مفصّلة حول شكل الجزيئات وبنيتها ككل بتتبّع تصرف أنوية الذرات في المجال المغناطيسي[22]. كذلك يساعد
مطياف الكتلة (Mass spectrometry) في التعرّف على الجزيئات من خلال قياس كتلتها وبنيتها، ما يوفّر معلومات حول تركيبها وتركيزها. لا تُعدّ هذه التقنيات حديثة، غير أنها مكّنت للباحثين من دراسة بنيات الجزيئات البيولوجية ومكوناتها بتفصيل ودقة. وقد شهدت مطيافية الكتلة تحسينات كبيرة في دقة الكشف وتمييز العيّنات، ما أتاح تحليل عيّنات بيولوجية معقّدة تحليلًا تفصيليًا دقيقًا[23].
كما أتاحت التطورات في مجال تقنيات التأيُّن، مثل التفاظ/ تأيين الليزر بمساعدة المصفوفة (Matrix-assisted laser desorption/ionization, MALDI) التحليل المباشر للجزيئات الحيوية. وحسّنت التطورات في مطيافية الكتلة التتابعية (MS/MS) فحص المستقلَبات (Metabolites) والبروتينات المختلفة، ما يجعل هذه التقنية أساسية في أبحاث المكوّن البروتيني (البروتيوم، Proteome) والمكوّن الأيضي أو الأيضيّات (الميتابولوم، (Metabolome والمسارات الاستقلابية[24]. وكان اختراع
المجهر الإلكتروني في ثلاثينيات القرن العشرين، والمجهر الإلكتروني فائق البرودة في عام 1981 حدثين مركزيين، إذ أتاحا للعلماء تصوير الجزيئات البيولوجية المعقّدة بدقة شبه ذرية. تسمح هذه التقنية برؤية المجمّعات البيولوجية الكبيرة في حالتها الأصلية من دون الحاجة إلى تبلورها، بعكس تقنية
دراسة البلورات بالأشعة السينية {{دراسة البلورات بالأشعة السينية: تقنية مخبرية لتحديد البنية الذرية لبلورات المواد البيولوجية، عن طريق تحليل أنماط حيود الأشعة السينية عن البلورات البيولوجية (البروتينات أو الأحماض النووية). يكشف هذا عن الترتيب ثلاثي الأبعاد للجزيئات، ما يُمكّن من تحقيق إنجازات في تصميم الأدوية، وفهم الآليات البيولوجية. كانت روزاليند فرانكلين رائدة هذه التقنية في دراستها للولب الحمض النووي (DNA).}} (X-ray crystallography). وقد أحدثت هذه التقنية المجهرية ثورة في اكتشاف الهياكل الجزيئية المعقدة من خلال توفير صور مفصّلة ثلاثية الأبعاد للعديد من الأجسام، بما في ذلك البروتينات المعقدة والڤيروسات والبكتيريا[25].
أدت التطوّرات الأخيرة في الكواشف والبرمجيات الحاسوبية إلى تحسين دقة المجاهر الإلكترونية فائقة البرودة بشكل كبير أتاح إمكانية دراسة العمليات الديناميكية في التجمّعات الجزيئية الكبيرة. إضافة إلى ذلك، توفّر التطورات في ليزر الإلكترونات الحرة بالأشعة السينية (X-ray free electron lasers, XFELs) للباحثين دراسة التفاعلات الكيميائية والبيوكيميائية السريعة على المستوى الذرّي.
إضافة إلى تلك التقنيات الأقدم نسبيًا، وتحديثاتها، تستدعي دراسة الكيمياء الحيوية استخدام تقنيات حديثة ومتطورة. ومن بين هذه الابتكارات تقنية مسمّاة بـ "تسلسل الحمض النووي الريبي للخلية الواحدة" (Single-cell RNA sequencing, scRNA-seq). توفّر هذه التقنية للباحثين استكشاف التعبير الجيني على مستوى الخلية الواحدة، وتساهم في إيجاد إجابات عن الأسئلة البيوكيميائية المختلفة المتعلقة بآليات الإمراض والاستجابات المناعية ودورة الخلية وغيرها[26]. ومن الجدير ذكره أن التحسينات التي شهدها مطلع القرن الحادي والعشرين في استخدامات هذه التقنية أدت إلى رفع مستوى قدرتها وتحسين دقتها. كما أن الثورة التي أحدثها اكتشاف تقنية
كريسبر-كاس9 (CRISPR-Cas9) لتعديل الجينات ومعالجتها، مطلع القرن العشرين، التي تستخدمها البكتيريا طبيعيًّا آليةً للدفاع ضد الڤيروسات، أتاحت تعديل تسلسلات الحمض النووي بدقة[27]. وقد قطعت هذه التقنية أشواطًا كبيرة حسّنت من دقتها وكفاءتها، إذ مكّنت الباحثين من استهداف جينات معينة ومتعددة في آنٍ، والتعديل عليها، ما يمهد الطريق لدراسات جينية معقدة وتطبيقات علاجية مختلفة، وخاصة في الاضطرابات الوراثية والسرطان. وتستمر هذه الأساليب المتطورة في توسيع حدود الكيمياء الحيوية وجعلها مركزية في العديد من التخصصات المختلفة.
التطبيقات
استفاد الطب بشكل كبير من تطوير مجال الكيمياء الحيوية باستخدام تقنياتها المتعددة في اكتشاف الأدوية والتشخيص وفهم الأمراض. تحدد أساليب الكيمياء الحيوية وتقنياتها اكتشاف الأدوية الجديدة وتصميمها وتطويرها، وإعادة استخدام أدوية أخرى (Drug repurposing)، وتقييم فعاليتها وسلامتها. يستخدم الباحثون الطبيون والصيدلانيون التقنيات البيوكيميائية لدراسة كيفية تفاعل الأدوية مع أهدافها الخلوية على المستوى الجزيئي، ما يتيح تطوير علاجات أكثر فعالية وأكثر تحديدًا[28]. كما ساهمت الكيمياء الحيوية في تطوير تقنيات التشخيص بشكل كبير، وذلك مع تطوير اختبارات مخبرية محددة، وتحديد
الواسمات الحيوية (Biomarkers) التي تسمح بالكشف المبكر عن الأمراض ومتابعتها.
تُستخدم تقنيات بيوكيميائية مثل اختبارات الممتزّ المناعي المرتبط بالإنزيم، أو
الإلايزا (Enzyme-linked immunosorbent assays, ELISA) (الشكل 6) وتفاعل البوليميراز المتسلسل (Polymerase chain reaction, PCR) على نطاق واسع للكشف عن بروتينات أو أحماض نووية محددة مرتبطة بحالات مرضية مختلفة. إضافة إلى ذلك، عززت الكيمياء الحيوية فهم المجتمع الطبي والعلمي للأمراض الوراثية والأيضية والمُعدية من خلال الكشف عن آلياتها الجزيئية وأسباب إمراضها[29]. أدى الكشف عن هذه الآليات الجزيئية إلى تحديد الطفرات الجينية المسؤولة عن اضطرابات مختلفة، مثل التليّف الكيسي (Cystic fibrosis)[30]، ومرض النزف الدموي أو الهيموفيليا (Hemophilia)[31]، وتطوير أدوات تشخيصية جديدة وعلاجات أنجع للأمراض.
[الشكل 6]
 اختبارات الممتزّ المناعي المرتبط بالإنزيم، أو الإلايزا
اختبارات الممتزّ المناعي المرتبط بالإنزيم، أو الإلايزا
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل 7] - الذرة المعدلة وراثيًا المقاومة للأمراض
 إنتاج النباتات المعدلة وراثيًا
إنتاج النباتات المعدلة وراثيًا كيفية قتل الآفات الزراعية
كيفية قتل الآفات الزراعية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
أما في مجالات الزراعة المتنوّعة، فقد أحدثت الكيمياء الحيوية ثورة في إنتاج المحاصيل وإدارة الآفات، من خلال تقنيات الهندسة الوراثية[32] وتطوير المبيدات الحيوية (Biopesticides) والأسمدة الحيوية (Biofertilizers)[33]. تتيح الهندسة الوراثية للعلماء تعديل المحاصيل على المستوى الجيني لتعزيز السِمات المرغوبة، مثل مقاومة الآفات وتحمّل الضغوط البيئية، وتحسين المحتوى الغذائي للمحصول. على سبيل المثال، تُنتج بعض المحاصيل المعدّلة وراثيًا (مثل الذرة المعدّلة وراثيًا التي تحتوي على جين نُقل من بكتيريا
Bacillus thuringiensis) بروتينات سامة لبعض الآفات، ولكنها غير ضارة للإنسان والحيوانات الأخرى[34]. يقلل هذا النهج من الحاجة إلى استعمال المبيدات الحشرية الكيميائية ويزيد من غلّة المحاصيل (الشكل 7)[35]. كما تدعم المبيدات الحيوية والأسمدة الحيوية أساليب الزراعة المستدامة (Sustainable agriculture). تستخدم المبيدات الحيوية الكائنات الحية الدقيقة الطبيعية أو المعدلة وراثيًا للسيطرة على الآفات والأمراض، في حين تعمل الأسمدة الحيوية على تعزيز خصوبة التربة من خلال تعزيز النشاط الميكروبي المفيد. وفي المحصّلة، لا تعمل هذه الابتكارات على تحسين إنتاجية المحاصيل فحسب، بل تقلل أيضًا من التأثير البيئي للمدخلات الكيميائية التقليدية[36].
وفي العلوم البيئية، تساهم الكيمياء الحيوية في حماية النظم البيئية من خلال
المعالجة البيولوجية (أو الإصلاح الحيوي، Bioremediation) ومكافحة التلوث المعتمد على استخدام الإنزيمات[37]. تتضمن المعالجة البيولوجية استخدام
الكائنات الحية الدقيقة أو الإنزيمات لتفكيك الملوّثات وإزالتها من البيئات المتضررة، مثل الملوّثات النفطية أو المعدنية الثقيلة. تستفيد هذه العملية من القدرات الأيضية الطبيعية للميكروبات لإزالة السموم من المواد الضارة، ما يوفر حلولًا فعالة ومستدامةً للحفاظ على البيئة[38]. يُعدّ التحكم في التلوث المعتمِد على استخدام الإنزيمات تطبيقًا آخر، إذ تستخدم إنزيمات محددة لتحلل الملوثات، مثل البلاستيك أو المواد الكيميائية الصناعية. تقدم هذه الأساليب البيوتكنولوجية بدائل للطرق الكيميائية التقليدية، وهي أيضًا بدائل صديقة للبيئة، ما يعزز الاستدامة البيئية ويخفف من تأثير الأنشطة البشرية على كوكب الأرض[39].
للكيمياء الحيوية تطبيقات كثيرة جدًا في مختلف العلوم الأخرى أيضًا، منها علم السموم والصناعات المختلفة، وغيرها من الاتجاهات العلمية والتطبيقية المختلفة.
الشخصيات والمؤسسات الرئيسة
[الصورة 3]
 فريدريش ميشر
فريدريش ميشر
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الصورة 4]
 جينيفر دودنا
جينيفر دودنا
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الصورة 5]
 فرنسيس آرنولد
فرنسيس آرنولد
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
هناك العديد من العلماء والباحثين البارزين في تاريخ الكيمياء الحيوية، وذكرت هذه المقالة إسهامات بعضهم، مثل فرانكلين وواتسون وكريك، ومن قبلهم ڤولر ولاڤوازييه وبوخنر. ومن بين هذه الشخصيات التاريخية، غالبًا ما يُنسب الفضل إلى فريدريش ميشر (Friedrich Miescher، 1844-1895) (الصورة 3) في إرساء الأساس للكيمياء الحيوية الحديثة. ففي عام 1869، اكتشف ميشر الأحماض النووية، التي أطلق عليها في حينها اسم
نوكلين (Nuclein)، بعزل الحمض النووي من أنوية
خلايا الدم البيضاء[40]، ما يُعتبر اكتشافًا أساسيًا في فهم ماهية المادة الوراثية، وقد استغرق وقتًا واستلزم جهدًا من عدة علماء وباحثين للتوصّل إليه. أما
لينوس باولينغ (Linus Pauling، 1901-1994) فيُعتبر أيضًا شخصية أخرى مؤثرة وبارزة في مجالي الكيمياء والكيمياء الحيوية، إذ قدّم إسهامات رائدة في تفسير البنية الجزيئية للبروتينات، ويُعدّ عمله على بنية لولب ألفا (Alpha helix) في البروتينات، الذي فصّله في ورقة بحثية نشرها عام 1951، أساسيًا في تفسير بنية البروتينات ووظائفها[41].
وفي الكيمياء الحيوية المعاصرة، قدّم العديد من العلماء إسهامات فارقة؛ فتُعرف
جينيفر دودنا (Jennifer A. Doudna، 1964-) (الصورة 4) بدورها في تطوير تقنية
كريسبر-كاس9 لتعديل الجينات، التي أحدثت ثورة في الهندسة الوراثية وعلم الأحياء الجزيئية[42]. وقد مكّن عملها من إجراء تعديلات دقيقة على الحمض النووي، وفتح آفاقًا جديدة للبحث والتطبيقات العلاجية، وقد حازت في إثر أعمالها جائزة نوبل في الكيمياء عام 2020[43]. كما تُعدّ فرنسيس آرنولد (Frances Arnold، 1956-) (الصورة 5) شخصية علمية بارزة في المجال، وتُعرف بعملها في مجال التطوّر الموجّه (directed evolution)[44]، الذي ينطوي على تطوير إنزيمات جديدة ذات وظائف محسّنة أو جديدة. وكان لأبحاثها تأثير عميق في
التكنولوجيا الحيوية الصناعية وعلم الأحياء الاصطناعي (Synthetic biology)، فحازت جائزة نوبل في الكيمياء عام 2018[45]. لقد تقدمت كلتا العالمتين المعاصرتين بنتائج علمية رصينة تعزّز الفهم العام للأنظمة البيولوجية، ما يساهم في الدفع بالابتكارات في مختلف التخصصات.
يعدّ المؤسسات البحثية الكبرى المتخصصة في الكيمياء الحيوية مهمة في دراسة الآليات البيولوجية الدقيقة وفهمها لمختلف الوظائف الخلوية في الصحة والمرض، والمساهمة في تطوير علاجات ناجعة للعديد من الأمراض. ومن بين هذه المؤسسات، تبرز المعاهد الوطنية للصحة National Institutes of Health - NIH)) في الولايات المتحدة الأميركية بوصفها كيانًا رائدًا في هذا المجال، فهي واحدة من أبرز منظمات البحث الطبي الحيوي في العالم، فتتألف من 27 معهدًا ومركزًا، يركِّز كل منها على مجالات محددة من الدراسات الحيوية. تتمتع المعاهد الوطنية للصحة بسمعة ممتازة لإنجازات باحثيها في الكيمياء الحيوية، إذ تجري أبحاثًا مكثفة تشمل علم الأحياء الجزيئية وعلم الوراثة وعلم الأدوية، وغيرها الكثير. ويموّل المعهد الوطني للعلوم الطبية العامة (NIGMS)، وهو فرع من المعاهد الوطنية للصحة، جزءًا كبيرًا من أبحاث الكيمياء الحيوية في العالم، كما يدعم دراسات العمليات البيوكيميائية الأساسية وتأثيراتها في الصحة.
وقد أدى التزام المعاهد الوطنية للصحة بدراسة الأمراض على المستوى الجزيئي إلى تحقيق تطورات علمية في مجالات عدة، على سبيل المثال، علاج السرطان والاضطرابات الأيضية والأمراض المعدية. إذ لا تساهم هذه المؤسسات في البحث المعرفة العلميين فحسب، بل تتعاون أيضًا مع شركاء في الصناعة لترجمة نتائج الأبحاث إلى تطبيقات عملية، وتعمل جهودهم الجماعية على تعزيز الابتكارات العلمية والدفع بها للارتقاء بالرعاية الصحية على مستوى العالم.
الكيمياء الحيوية عربيًا
شهدت الكيمياء الحيوية نموًا وتطورًا ملحوظين في العالم العربي، مدفوعة بالتقدم في التعليم والبحث وإسهامات العلماء البارزين. تستثمر المؤسسات في جميع أنحاء المنطقة العربية بشكل متزايد في برامج الكيمياء الحيوية، ما يعكس اهتمامها بالابتكار العلمي وتحسين الرعاية الصحية. تقدّمت العديد من الدول العربية خطوات ملحوظة في توسيع قدراتها البحثية وإنشاء برامجها التعليمية في الكيمياء الحيوية. ويتجلى هذا التقدم بشكل خاص في مؤسسات التعليم العالي ومراكز البحث التي تبنّت الكيمياء الحيوية بشكل متزايد باعتباره مجالًا حاسمًا للتقدم العلمي والطبي، فأنشأت معظم جامعات العالم العربي برامج جيدة في الكيمياء الحيوية.
شهد العالم العربي زيادة في التعاون مع المنظمات الدولية والمشاركة في الشبكات العلمية العالمية، يروم دمج العلماء العرب في المجتمع العلمي العربي والعالمي ويعزز إسهاماتهم. وقد قدّم علماء عرب بارزون إسهامات مهمة في الكيمياء الحيوية على المسرح الدولي. فمثلًا، يُعرف
يوسف عوني حنّون (Yusuf A. Hannun، 1955-) بكونه شخصية علمية بارزة في مجال أبحاث السرطان، نتيجة أبحاثه في مجال الدهون السيفنغولية ودورها في تنظيم الخلايا، إضافة إلى إنجازات كبيرة في دراسة مرض السرطان[46]. فقد ساهمت أبحاثه في فهم آليات السرطان المرضية ومهدت الطريق لاستراتيجيات علاجية جديدة. بدأ حنّون وزوجته الراحلة
لينا ماري عبيد (Lina M. Obeid، 1955-2019) أبحاثهما في مجال الكيمياء الحيوية على الدهون السفينغولية، وقاده سنوات طويلة، ويُعرف كل من حنّون وعبيد بأبحاثهما المؤثرة التي تربط بين الكيمياء الحيوية الأساسية والتطبيقات السريرية.
وعلى الرغم من التطورات المتسارعة في مجالات الكيمياء الحيوية في العالم العربي، فإن التحديات المختلفة لا تزال قائمة، بما في ذلك القيود على التمويل البحثي والحاجة المتعاظمة إلى المزيد من تطوير البنى التحتية في المؤسسات الأكاديمية والبحثية لمواكبة التطورات في الأجهزة والتقنيات على مستوى العالم. ومع ذلك، تبشّر الاستثمارات الجارية في التعليم والبحث العلمي بمستقبل واعد لمجال الكيمياء الحيوية في المنطقة العربية، كما يشير الالتزام بتوسيع القدرات البحثية إلى أن العلماء العرب قادرين على تقديم إسهامات كبيرة في الكيمياء الحيوية العالمية، ما قد يؤدي إلى تحقيق اكتشافات تؤثر في النتائج الصحية على المستويين الإقليمي والعالمي.
المراجع
Aebersold, Ruedi & Matthias Mann. “Mass Spectrometry-Based Proteomics.”
Nature. vol. 422, no. 6928 (2003). pp. 198-207.
________. “Mass-Spectrometric Exploration of Proteome Structure and Function.”
Nature. vol. 537, no. 7620 (2016). pp. 347-355.
Arnold, Frances H. “Directed Evolution: Creating Biocatalysts for the Future.”
Chemical Engineering Science. vol. 51, no. 23 (1996). pp. 5091-5102.
Bhardwaj, Deepak et al. “Biofertilizers Function as Key Player in Sustainable Agriculture by Improving Soil Fertility, Plant Tolerance and Crop Productivity.”
Microbial Cell Factories. vol. 13, article no. 66 (2014).
Chaney, Stephen G., John W. Pelley & William E. Seifert. “The Role and Value of the Basic Sciences in Medical Education (with an Emphasis on Biochemistry).”
Journal of the International Association of Medical Science Educators. vol. 20, no. 3 (2010). pp. 280-283.
Cheng, Yifan. “Single-Particle Cryo-EM at Crystallographic Resolution.”
Cell. vol. 161, no. 3 (2015). pp. 450-457.
Das, Surajit & Hirak R. Dash. “Microbial Bioremediation: A Potential Tool for Restoration of Contaminated Areas.”
Microbial Biodegradation and Bioremediation (2014). pp. 1-21.
Doudna, Jennifer A. & Emmanuelle Charpentier. “The New Frontier of Genome Engineering with CRISPR-Cas9.”
Science. vol. 346, no. 6213 (2014).
“Dr. Yusuf Hannun.”
Stony BrookUniversity. at:
https://acr.ps/1L9F2EW
Drews, Jürgen. “Drug Discovery: A Historical Perspective.”
Science. vol. 287, no. 5460 (2000). pp. 1960-1964.
“Eduard Buchner: Biographical.”
The Noble Prize. at:
https://acr.ps/1L9F2iH
Fauci, Anthony S. & David M. Morens. “The Perpetual Challenge of Infectious Diseases.”
The New England Journal of Medicine. vol. 366, no. 5 (2012). pp. 454-461.
“Frances H. Arnold: Facts.”
TheNobel Prize. at:
https://acr.ps/1L9F34P
“Francis Crick, Rosalind Franklin, James Watson, and Maurice Wilkins.”
Science History Institute. at:
https://acr.ps/1L9F2uJ
Hardin, Jeff, Gregory Bertoni & Lewis J. Kleinsmith.
Becker’s World of the Cell. 8th ed. San Francisco, CA: Pearson International Inc., 2011.
Hargittai, István. “Linus Pauling’s Quest for the Structure of Proteins.”
Structural Chemistry. vol. 21, no. 1 (2010). pp. 1-7.
Hartley, Harold. “Antoine Laurent Lavoisier 26 August 1743--8 May 1794.”
Proceedings of the Royal Society of London. Series B, Biological Sciences. vol. 134, no. 876 (1947). pp. 348-377.
“History of the ASBMB.”
American Society for Biochemistry and Molecular Biology. at:
https://acr.ps/1L9F2S5
Mawcha, Kahsay Tadesse et al. “Recent Advances in Biopesticide Research and Development with a Focus on Microbials.”
F1000Research. vol. 13, no. 1071 (2025).
Kletzinsky, Vincenz.
Compendium der Biochemie. Wien: W. Braumüller, 1858.
Kumar, Kishore R., Mark J. Cowley & Ryan L. Davis. “Next-Generation Sequencing and Emerging Technologies.”
Seminars in Thrombosis and Hemostasis. vol. 45, no. 7 (2019). pp. 661-673.
“Kurt Wüthrich: Nobel Prize Lecture.”
The Nobel Prize. at:
https://acr.ps/1L9F37G
Gierasch, Lila M. “What’s in a Name?”
Journal of Biological Chemistry. vol. 291, no. 35 (2016). pp. 19208-19209.
Malamis, Saimos et al. “Biological Nutrients Removal from the Supernatant Originating from the Anaerobic Digestion of the Organic Fraction of Municipal Solid Waste.”
Critical Reviews in Biotechnology. vol. 34, no. 3 (2014). pp. 244-257.
McIlwain, Henry. “Biochemistry and Neurochemistry in the 1800s: Their Origins in Comparative Animal Chemistry.”
Essays in Biochemistry. vol. 25 (1990). pp. 197-224.
Nelson, David L. & Michael M. Cox.
Lehninger Principles of Biochemistry. 5th ed. New York: W. H. Freeman & Company, 2008.
“Nobel Prize in Chemistry 2020.”
The Nobel Prize. at:
https://acr.ps/1L9F2rT
Dahm, Ralf. “Friedrich Miescher and the Discovery of DNA.”
Developmental Biology. vol. 278, no. 2 (2005). pp. 274-288.
Riordan, John R. et al. “Identification of the Cystic Fibrosis Gene: Cloning and Characterization of Complementary DNA.”
Science. vol. 245, no. 4922 (1989). pp. 1066-1073.
Sanahuja, Georgina et al. “Bacillus Thuringiensis: A Century of Research, Development and Commercial Applications.”
Plant Biotechnology Journal. vol. 9, no.3 (2011). pp. 283-300.
Tang, Fuchou et al. “MRNA-Seq Whole-Transcriptome Analysis of a Single Cell.”
Nature Methods. vol. 6, no. 5 (2009). pp. 377-382.
The Editors of Encyclopaedia Britannica. “Anselme Payen.” Britannica. at:
https://acr.ps/1L9F2x3
Vaeck, Mark et al. “Transgenic Plants Protected from Insect Attack.”
Nature. vol. 328 (1987). pp. 33-37.
Vidali, M. “Bioremediation. An Overview.”
Pure and Applied Chemistry. vol. 73, no. 7 (2001). pp. 1163-1172.
Watson, James D. & Francis H. C. Crick. “Molecular Structure of Nucleic Acids: A Structure for Deoxyribose Nucleic Acid.”
Nature. vol. 171, no. 4356 (1953). pp. 737-738.
Wöhler, Friedrich. “Ueber Künstliche Bildung des Harnstoffs.”
Annalen der Physik. vol. 88, no. 2 (1828). pp. 253-256.
Xudong Ye et al. “Engineering the Provitamin A (β-Carotene) Biosynthetic Pathway into (Carotenoid-Free) Rice Endosperm.”
Science. vol. 287, no. 5451 (2000). pp. 303-305.
[1] Vincenz Kletzinsky,
Compendium der Biochemie (Wien: W. Braumüller, 1858).
[2] Henry McIlwain, “Biochemistry and Neurochemistry in the 1800s: Their Origins in Comparative Animal Chemistry,”
Essays in Biochemistry, vol. 25 (1990), pp. 197-224.
[3] Harold Hartley, “Antoine Laurent Lavoisier 26 August 1743-8 May 1794,”
Proceedings of the Royal Society of London.
Series B, Biological Sciences, vol. 134, no. 876 (1947), pp. 348-377.
[4] في الأوساط العلمية يعتبر تفاعل إنتاج اليوريا الذي اكتشفه ڤولر بداية حقيقية لعلم الكيمياء العضوية (Organic chemistry)، الذي شكّل تمهيدًا لعلم الكيمياء الحيوية، يُنظَر:
Friedrich Wöhler, “Ueber Künstliche Bildung des Harnstoffs,”
Annalen der Physik, vol. 88, no. 2 (1828), pp. 253-256.
[5] درس ڤولر الخصائص غير العضوية لمختلف العناصر، وكان من أوائل العلماء الذين اقترحوا فكرة أن عناصر مختلفة مجتمعة (الجزيئات) يمكن أن تتصرف كأنها كيانات منفردة في التفاعلات الكيميائية. واحد من هذه التفاعلات كان دمج سيانات الرصاص (Lead cyanate,
\(Pb\left(OCN\right)_{2}\)) مع الأمونيا (Ammonia,
\(NH_{3}\))، لينتج منها سيانات الأمونيوم (
\(NH_{4}(OCN)\)) في التفاعل الآتي:
\(Pb\left(OCN\right)_{2}+2NH_{3}+2H_{2}O\rightarrow Pb(OH)_{2}+2NH_{4}(OCN)\).
[6] عند تعريض تفاعل ڤولر للحرارة، يتحلّل مركب سيانات الأمونيوم إلى الأمونيا وحمض السيانيك (Cyanic acid,
\(HOCN\))، اللذين يجتمعان معًا لتكوين مركب اليوريا (
\((NH_{2})_{2}CO\)) بحسب المعادلة الآتية:
\(NH_{4}\left(OCN\right)\underset{\rightarrow}{ةرارح}NH_{3}+HOCN ⇋ (NH_{2})_{2}CO\).
[7] The Editors of Encyclopaedia Britannica, “Anselme Payen,”
Britannica, accessed on 16/7/2025, at:
https://acr.ps/1L9F2x3
[8] “Eduard Buchner: Biographical,”
The Nobel Prize, accessed on 16/7/2025, at:
https://acr.ps/1L9F2iH
[9] “History of the ASBMB,”
American Society for Biochemistry and Molecular Biology, accessed on 16/7/2025, at:
https://acr.ps/1L9F2S5
[10] Lila M. Gierasch, “What’s in a Name?”
Journal of Biological Chemistry, vol. 291, no. 35 (2016), pp. 19208-19209.
[11] James D. Watson & Francis H. C. Crick, “Molecular Structure of Nucleic Acids: A Structure for Deoxyribose Nucleic Acid,”
Nature, vol. 171, no. 4356 (1953), pp. 737-738.
[12] “Francis Crick, Rosalind Franklin, James Watson, and Maurice Wilkins,”
Science History Institute, accessed on 16/7/2025, at:
https://acr.ps/1L9F2uJ
[13] Stephen G. Chaney, John W. Pelley & William E. Seifert, “The Role and Value of the Basic Sciences in Medical Education (with an Emphasis on Biochemistry),”
Journal of the International Association of Medical Science Educators, vol. 20, no. 3 (2010), pp. 280-283.
[14] David L. Nelson & Michael M. Cox,
Lehninger Principles of Biochemistry, 5th ed. (New York: W. H. Freeman & Company, 2008).
[15] Ibid.
[16] Ibid.
[17] Jeff Hardin, Gregory Bertoni & Lewis J. Kleinsmith,
Becker’s World of the Cell, 8th ed. (San Francisco, CA: Pearson International Inc., 2011).
[18] Nelson & Cox,
op. cit.
[19] Ibid.
[20] Hardin, Bertoni & Kleinsmith.
[21] Ibid.
[22] “Kurt Wüthrich: Nobel Prize Lecture,”
The Nobel Prize, accessed on 16/7/2025, at:
https://acr.ps/1L9F37G
[23] Ruedi Aebersold & Matthias Mann, “Mass-Spectrometric Exploration of Proteome Structure and Function,”
Nature, vol. 537, no. 7620 (2016), pp. 347-355.
[24] Ruedi Aebersold & Matthias Mann, “Mass Spectrometry-Based Proteomics,”
Nature, vol. 422, no. 6928 (2003), pp. 198-207.
[25] Yifan Cheng, “Single-Particle Cryo-EM at Crystallographic Resolution,”
Cell, vol. 161, no. 3 (2015), pp. 450-457.
[26] Fuchou Tang et al., “MRNA-Seq Whole-Transcriptome Analysis of a Single Cell,”
Nature Methods, vol. 6, no. 5 (2009), pp. 377-382.
[27] Jennifer A. Doudna & Emmanuelle Charpentier, “The New Frontier of Genome Engineering with CRISPR-Cas9,”
Science, vol. 346, no. 6213 (2014).
[28] Jürgen Drews, “Drug Discovery: A Historical Perspective,”
Science, vol. 287, no. 5460 (2000), pp. 1960-1964.
[29] Anthony S. Fauci & David M. Morens, “The Perpetual Challenge of Infectious Diseases,”
The New England Journal of Medicine, vol. 366, no. 5 (2012), pp. 454-461.
[30] John R. Riordan et al., “Identification of the Cystic Fibrosis Gene: Cloning and Characterization of Complementary DNA,”
Science, vol. 245, no. 4922 (1989), pp. 1066-1073.
[31] Kishore R. Kumar, Mark J. Cowley & Ryan L. Davis, “Next-Generation Sequencing and Emerging Technologies,”
Seminars in Thrombosis and Hemostasis, vol. 45, no. 7 (2019), pp. 661-673.
[32] Xudong Ye et al., “Engineering the Provitamin A (β-Carotene) Biosynthetic Pathway into (Carotenoid-Free) Rice Endosperm,”
Science, vol. 287, no. 5451 (2000), pp. 303-305.
[33] Deepak Bhardwaj et al., “Biofertilizers Function as Key Player in Sustainable Agriculture by Improving Soil Fertility, Plant Tolerance and Crop Productivity,”
Microbial Cell Factories, vol. 13, article no. 66 (2014).
[34] Georgina Sanahuja et al., “Bacillus Thuringiensis: A Century of Research, Development and Commercial Applications,”
Plant Biotechnology Journal, vol. 9, no. 3 (2011), pp. 283-300.
[35] Mark Vaeck et al., “Transgenic Plants Protected from Insect Attack,”
Nature, vol. 328 (1987), pp. 33-37.
[36] Kahsay Tadesse Mawcha et al., “Recent Advances in Biopesticide Research and Development with a Focus on Microbials,”
F1000Research, vol. 13, no. 1071 (2025).
[37] M. Vidali, “Bioremediation. An Overview,”
Pure and Applied Chemistry, vol. 73, no. 7 (2001), pp. 1163-1172.
[38] Surajit Das & Hirak R. Dash, “Microbial Bioremediation: A Potential Tool for Restoration of Contaminated Areas,”
Microbial Biodegradation and Bioremediation (2014), pp. 1-21.
[39] Saimos Malamis et al., “Biological Nutrients Removal from the Supernatant Originating from the Anaerobic Digestion of the Organic Fraction of Municipal Solid Waste,”
Critical Reviews in Biotechnology, vol. 34, no. 3 (2014), pp. 244-257.
[40] Ralf Dahm, “Friedrich Miescher and the Discovery of DNA,”
Developmental Biology, vol. 278, no. 2 (2005), pp. 274-288.
[41] István Hargittai, “Linus Pauling’s Quest for the Structure of Proteins,”
Structural Chemistry, vol. 21, no. 1 (2010), pp. 1-7.
[42] Doudna & Charpentier.
[43] “Nobel Prize in Chemistry 2020,”
The Nobel Prize, accessed on 16/7/2025, at:
https://acr.ps/1L9F2rT
[44] Frances H. Arnold, “Directed Evolution: Creating Biocatalysts for the Future,”
Chemical Engineering Science, vol. 51, no. 23 (1996), pp. 5091-5102.
[45] “Frances H. Arnold: Facts,”
TheNobel Prize, accessed on 16/7/2025, at:
https://acr.ps/1L9F34P
[46] “Dr. Yusuf Hannun,”
Stony BrookUniversity, accessed on 16/7/2025, at:
https://acr.ps/1L9F2EW