الاستماتة (Apoptosis) أو استماتة الخلايا عملية طبيعية في الكائنات الحية متعددة الخلايا، إذ تموت بعض الخلايا بطريقة مبرمجة ومتقنة ومحدّدة. تعدّ هذه العملية، والتي تعرف أيضًا باسم الاستماتة الخلوية أو الانتحار الخلوي أو موت الخلايا المبرمج (Programmed cell death)، من العمليات الأساسية في تطور الأنسجة والأعضاء وتعدّ ضرورية لصيانة الخلايا ولمنع انتشار الخلايا التالفة أو غير الطبيعية.
عندما توسم خلية ما بأنها في طور الاستماتة، تشرع في التقلص حجمًا وتتفتّت إلى أجزاء صغيرة محاطة بغشاء مكونةً أجسام الاستماتة (Apoptotic bodies) التي يمكن إزالتها بسهولة بوساطة جهاز المناعة في الجسم. إن تكوّن أجسام الاستماتة هذا يمنع انفجار
الخلية وإرسال مكوناتها للحيز ما بين الخلايا، ومن ثم لا تحدث التهابات. كذلك تسهم هذه العملية في منع إطلاق المواد الضارة من
الخلية التالفة التي يمكن أن تلحق الضرر بالأنسجة المحيطة.
ثمة كثير من الإشارات الخلوية، الداخلية والخارجية، التي تسهم في بدء برنامج الاستماتة. فقد تخضع الخلايا مثلًا لموت الخلايا المبرمج استجابةً لتلف
الحمض النووي، أو العدوى الڨيروسية، أو التعرض لمواد كيميائية سامة. كذلك يمكن أن يبدأ موت الخلايا المبرمج عن طريق إشارات قادمة من خلايا أخرى في الجسم، مثل
الخلايا المناعية التي تتعرف إلى الخلايا غير الطبيعية أو المصابة وتستهدفها. إن السمة الرئيسة للاستماتة أنها عملية مبرمجة ومتقنة ومنظمة بإحكام. يمكن أن يؤدي الفشل في تنظيم هذه العملية بشكل صحيح إلى نشوء أمراض عدة، مثل
السرطان أو
اضطرابات المناعة الذاتية أو
أمراض القلب أو
ألزهايمر أو غيرها.
تعريفها
موت الخلايا (cell death) هو عملية بيولوجية أساسية وهامّة لتطوير الكائنات متعددة الخلايا جميعها وصيانتها وعملها. في خلايا الثدييات، ثمة عدة آليات متميزة تتحكم في عمليات موت الخلايا، تخدم كل منها أغراضًا محددة وتحدث في ظل ظروف مختلفة. ومع أن موت الخلايا بالطرق المختلفة له ضرورة كبيرة في العمليات الفيزيولوجية الطبيعية، فإن الموت الخلوي يؤدي أيضًا دورًا أساسيًا في الحالات المرضية المختلفة، كالسرطان والأمراض التنكسية العصبية (neurodegenerative diseases) والأمراض المناعية المختلفة. ثمة كثير من الآليات المسؤولة عن الموت الخلوي في
الثدييات. تشكل آليات الاستماتة الخلوية (apoptosis) والنخر (necrosis) الطريقتين الأساسيتين لموت الخلايا في خلايا الثدييات[1]. فالاستماتة، التي يشار إليها غالبًا بموت الخلايا المبرمج، هي عملية منظمة ومحددة ومسيطر عليها بدرجة عالية تحدث استجابةً لإشارات فيزيولوجية مختلفة، مثل
عوامل النمو (growth factors)، أو
تلف الحمض النووي، أو
الإجهاد الخلوي (cellular stress). يتميز
موت الخلايا المبرمج بتغيرات مورفولوجية (شكلية) متميزة في الخلايا مثل انكماش الخلايا، وتكثيف
الكروماتين (chromatin)، وتكوين أجسام الاستماتة[2]. كذلك تتميز الاستماتة بإزالة الخلايا الميتة والتالفة بدقة بوساطة
الخلايا البلعمية (macrophages)، ما يمنع الالتهاب وتلف الأنسجة[3] (الشكل 1).
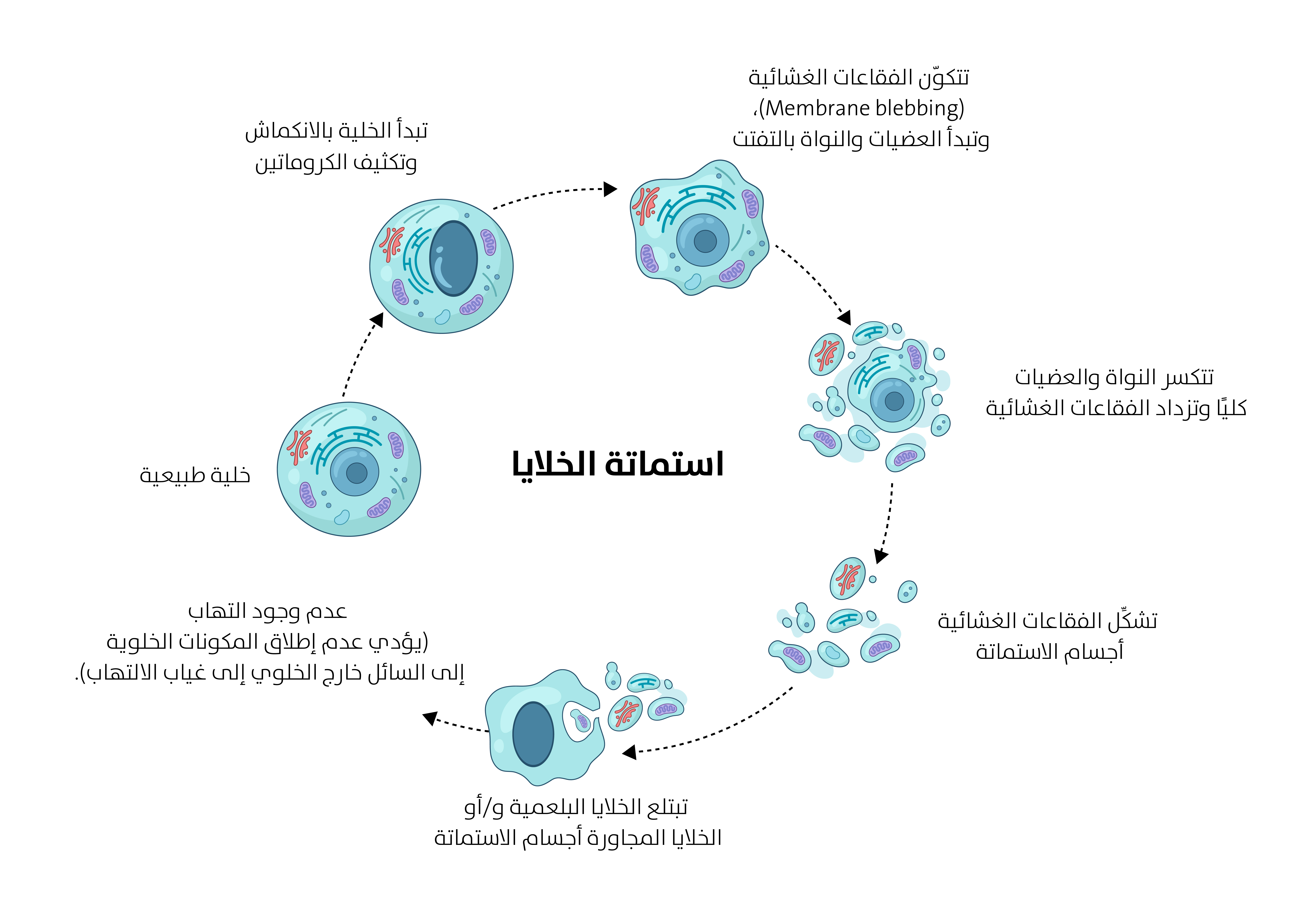 [الشكل 1] مراحل الاستماتة الخلوية المختلفة
[الشكل 1] مراحل الاستماتة الخلوية المختلفة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
من ناحية أخرى، يُعدّ النخر شكلًا من أشكال موت الخلايا غير المنضبط وغالبًا ما يكون التهابيًا وينجم عادةً عن أضرار جسدية أو كيميائية شديدة كالحروق والجروح. تخضع الخلايا النخرية لتورم سريع فتتمزق وتطلق محتوياتها الخلوية، ما يؤدي إلى التهابات وأضرار عدة للأنسجة المجاورة. كشفت الأبحاث في السنوات الأخيرة أن النخر لا يحدث من دون نظام تمامًا كما كان يعتقد سابقًا، وحُدِّدت عدة أنواع فرعية من
النخر المبرمج (programmed cell necrosis, necroptosis)، بما في ذلك
الاستماتة الحديدية (ferroptosis) والموت الحمّي المبرمج (pyroptosis)، ولكل منها مسارات جزيئية متميزة[4]. ويُذكَر أن
الالتهام الذاتي (autophagy) آلية ثالثة يمكن أن تؤدي إلى موت الخلايا تحت ظروف معينة. فالالتهام الذاتي عملية خلوية تتضمن تحلل المكونات والعضيّات الخلوية وإعادة تدويرها للحفاظ على التوازن الخلوي من دون الحاجة إلى قتل
الخلية كليًا. ومع ذلك، ففي حال الإفراط أو عدم تنظيم هذه العملية، يمكن أن تسهم في
موت الخلايا[5].
كما كشفت الأبحاث مؤخرًا عن آليات إضافية لموت الخلايا وهي مشتقة من الآليات الرئيسة، مثل
الميتوفاجي (mitophagy)، والبارثاناتوس (parthanatos)، والكارثة الميتوتية (mitotic catastrophe)، والأنويكيس (anoikis)، ولكل منها محفزات وآليات ونتائج فريدة وكثيرة[6]. تؤكد آليات موت الخلايا المتنوعة هذه على التعقيد الملحوظ لبيولوجيا الكائنات متعددة الخلايا، وتسلط الضوء على الطرق المعقدة التي يمكن للخلايا من خلالها الاستجابة للمؤثرات الداخلية والخارجية.
اكتشافها
أول من سمّى ظاهرة الموت الخلوي المبرمج باستماتة الخلايا (apoptosis) هو العالم الأسترالي جون كير (John Kerr، 1934-2024) عام 1972[7]. والاسم مشتق من اللغة اليونانية (ἀπόπτωσις) بمعنى "تَساقُط" كما يحدث لأوراق الشجر في الخريف. ومع أن المصطلح نفسه صيغ فقط في منتصف القرن العشرين، فإن الأبحاث بشأن هذه الظاهرة بدأت مع اختراع المجهر المركب.
 العالم الأسترالي جون كير
العالم الأسترالي جون كير
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تعود أولى الملاحظات المسجلة عن الموت الخلوي الذي يشبه الاستماتة إلى القرن السابع عشر، حين وثَّق العالم الهولندي أنتوني ڤان ليڤينهوك (Antonie van Leeuwenheok، 1632-1723) وجود "كريات صغيرة" داخل الخلايا، التي يمكن أن تكون أوصافًا مبكرة لأجسام الاستماتة[8]. وخلال القرن التاسع عشر، أجرى العالم كارل فوغت (Carl Vogt، 1817-1895) ملاحظات تتعلق بموت الخلايا والتغيرات النووية[9]، ما مهد الطريق للبحث المستقبلي. بعد تسمية الاستماتة توالت الأبحاث العلمية وأدت إلى تحديد السمات المورفولوجية والبيوكيميائية المحددة لهذه العملية، مثل انكماش الخلايا، وتكثيف الكروماتين، وتكوين أجسام الاستماتة. أسهم علماء مثل ريتشارد لوكشين وزهرة ذاكري في تحديد هذه السمات، ما ساعد على التمييز بين الاستماتة والنخر[10]. وفي أواخر القرن العشرين وأوائل القرن الحادي والعشرين، شرع الباحثون في اكتشاف الآليات الجزيئية للاستماتة، وشمل ذلك اكتشاف البروتينات والمسارات الرئيسة لها. فحُدد أول جين مرتبط بالاستماتة الخلوية، بي سي إل 2 (Bcl-2). ومن ثم اكتُشِفت
بروتينات الكاسباز، وهي عائلة من البروتياز التي لها أدوار مركزية في الاستماتة. ويُذكَر أن جائزة نوبل في الطب لعام 2002 مُنحت إلى كل من سيدني برينر (Sydney Brenner، 1927-2019) وروبرت هورڤيتز (Robert Horvitz، 1947-) وجون سولستون (John Sulston، 1942-2018) لعملهم في تحديد الجينات التي تتحكم في الاستماتة[11].
الحائزون على جائزة نوبل في الطب لعملهم على تحديد الجينات التي تتحكم في الاستماتة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
أهميتها في التطور واستتباب الأنسجة
تؤدي استماتة الخلايا دورًا محوريًا في عمليات النمو المختلفة، بما في ذلك التطور الجنيني وتكوين الأعضاء وإعادة تشكيل الأنسجة. فأثناء التطور الجنيني، يكون موت الخلايا المبرمج أمرًا ضروريًا لنحت الهياكل وتنقيتها، والقضاء على الخلايا الزائدة، وتشكيل الشكل النهائي للأعضاء والأنسجة (نحت الأعضاء، Organ sculpting). يسهم نحت الأعضاء في تشكيل الأعضاء والهياكل عن طريق التخلص من خلايا معينة بشكل انتقائي. ينطوي تكوين أصابع اليدين والقدمين في أجنة الفقاريات على موت الخلايا المبرمج بين الأصابع، والشيء نفسه في إزالة ذنب أبي ذنيبة عند تحوله إلى ضفدع (الشكل 2). وأيضًا، في أثناء تطور الجهاز العصبي تشارك عمليات الاستماتة في إزالة
الخلايا العصبية الزائدة التي لا تُنشئ اتصالات مناسبة، ما يضمن كفاءة الدوائر العصبية (neural circuits). وفي جهاز المناعة، تخضع الخلايا المناعية التي تتعرف إلى
المستضدات الذاتية (self-antigens) لموت الخلايا المبرمج للتخلص من الخلايا الليمفاوية ذاتية التفاعل، ما يضمن التحمل المناعي والوقاية من أمراض المناعة الذاتية.
وفي الأنسجة البالغة، تحافظ آليات الاستماتة المختلفة على توازن الأنسجة عن طريق القضاء على الخلايا غير المرغوب فيها أو التالفة، فتزال الخلايا القديمة أو التالفة ما يفسح المجال لنمو خلايا وظيفية جديدة. هذه الدورة ضرورية بشكل خاص في الأنسجة ذات المعدل المرتفع في تجديد الخلايا، مثل الجلد وبطانة الجهاز الهضمي. كذلك توجد أدوار مهمة للاستماتة في منع الأمراض، ولا سيما
السرطان، إذ تعمل بوصفها آلية دفاعية تتخلّص من الخلايا المصابة بتلف الحمض النووي أو
الطفرات الجينية التي يمكن أن تؤدي إلى نمو غير منضبط وتكوين الأورام[12].
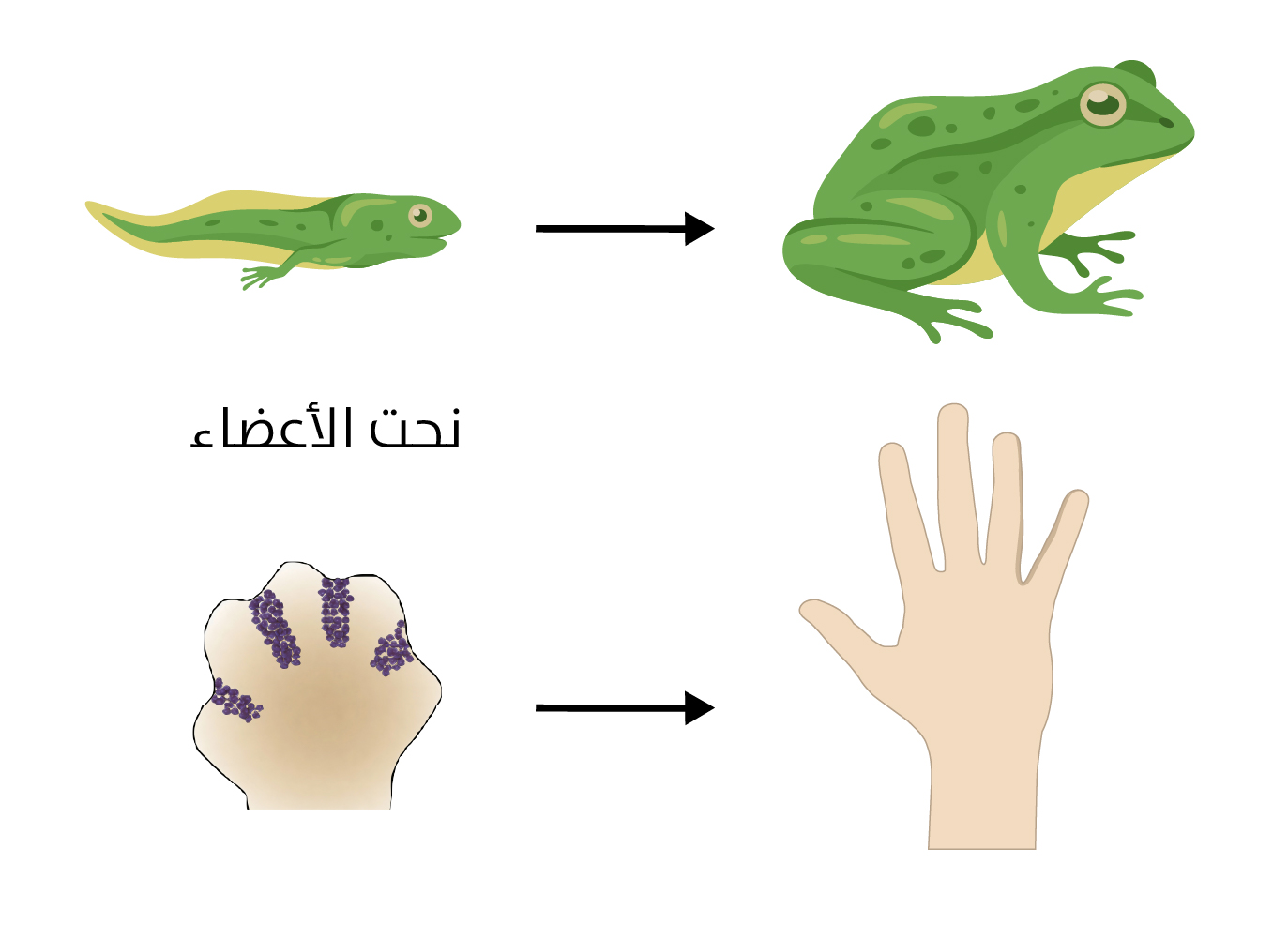 [الشكل 2] الاستماتة في التطور الجنيني
[الشكل 2] الاستماتة في التطور الجنيني
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
آلياتها
تتحكم في استماتة الخلايا شبكة معقدة من الآليات الجزيئية التي تنظم تنشيط موت الخلايا وتنفيذها بطريقة مبرمجة. يعد هذا الشكل المنسّق بدقة من موت الخلايا مهمًا لصيانة الأنسجة والخلايا في الكائنات الحية المعقدة متعددة الخلايا وتنظيمها[13]. إن دراسة الآليات الجزيئية للاستماتة لها آثار كبيرة في المسارات الأيضية الخلوية في الصحة والمرض، فقد أدت إلى كثير من الاكتشافات الرائدة في علاج السرطان، والأمراض التنكسيّة العصبية، وأمراض القلب والجهاز المناعي وغيرها[14]. تُحفَّز عملية الاستماتة من خلال مسارين رئيسين: المسار الخارجي (extrinsic pathway)، الذي تبدؤه مستقبلات الموت (death receptors)، والمسار الداخلي (intrinsic pathway)، الذي تنظمه في المقام الأول صحة
الميتوكوندريا والحمض النووي DNA داخل الخلية. إن انطلاق الاستماتة عملية معقدة ومنظمة تمر بها الخلية لتحديد ما إذا كانت ستخضع لبرنامج الاستماتة الكامل أم لا.
المسار الخارجي
يعد المسار الخارجي للاستماتة، المعروف أيضًا باسم "مسار مستقبلات الموت"، آلية لبدء عملية مبرمجة لموت الخلايا تُنشَّط عن طريق إشارات من خارج الخلية. وتحديدًا، فإن ارتباط أي من رُبَيْطات الموت (death ligands) بمستقبِلات الموت المقابلة لها على سطح
الخلية تستهلّ هذا المسار الخلوي. تاليًا نستعرض الأحداث الجزيئية التفصيلية الرئيسة لهذا المسار:
- ارتباط ربيطات الموت: يبدأ المسار الخارجي عن طريق ربط ربيطات موت محددة، مثل
عامل نخر الورم (Tumor necrosis factor - TNF) ورُبَيْطة فاس (Fas ligand, FasL)، بمستقبلات الموت المقابلة لها الموجودة على سطح الخلية متجهة إلى البيئة خارج الخلية. فيرتبط عامل نخر الورم بمستقبِله (Tumor necrosis factor receptor 1 - TNFR1)، في حين يكون ارتباط
ربيطة فاس بمستقبِل فاس المعروف أيضًا باسم CD95.
- تجمّع مستقبلات الموت: يؤدي الارتباط على مستقبلات الموت إلى تجميع هذه المستقبلات وتكاثفها معًا على سطح
الخلية، ما يؤدي إلى انتقال إشارات الموت إلى داخل الخلية.
- تركيب مجمع الإشارات المسبب للموت (ديسك) (death-inducing signaling complex - DISC): يشير تجمّع مستقبلات الموت على السطح إلى استقطاب
بروتينات مساندة تحتوي على مناطق في هيكلها تسمى مجالات الموت (death domains). على سبيل المثال، يعمل بروتين مجال الموت المرتبط بفاس (Fas-associated death domain - FADD) على تسهيل تجميع مجمع الإشارات المسبب للموت مباشرة، في حين أن بروتين مجال الموت المرتبط بـمستقبِل عامل نخر الورم (TNFR1-associated death domain - TRADD) يسهم بارتباط FADD أولًا للمستقبِل وبعده يجري تشكيل ديسك.
- تنشيط
الكاسباز البادئ (initiator caspase): بعد تكوين ديسك، يستقطب ويرتبط بالكاسباز البادئ (caspase-8 وفي بعض الحالات caspase-10). يرتبط جزيئان من كاسباز-8 بالديسك وينشطان بعضهما بوساطة إزالة جزء من كل بروتين (انشقاق تحفيزي ذاتي، autocatalytic cleavage). إن تنشيط
الكاسباز البادئ أساسي للبدء بتتالي الكاسباز (caspase cascade) التي تؤدي إلى استهلال برنامج الاستماتة.
- بدء
تتالي الكاسباز: إن تحفيز كاسباز-8 أو كاسباز-10 يؤدي إلى تنشيط
الكاسبازات المنفذة (executioner caspases) بوساطة الانشقاق التحفيزي لكل منها. وعند تنشيط كل
كاسباز منفذ، مثل كاسباز-3 وكاسباز-7، يسهم بتحفيز جزيئات بروتينية كاسبازية أخرى وهكذا دواليك (فتنشيط جزيء بادئ يسهم بتنشيط الآلاف من المنفذين، وهذا هو
تتالي الكاسباز)[15].
- تنفيذ الاستماتة:
الكاسبازات المنفذة، وخاصة كاسباز-3، مسؤولة عن تكسير كثير من الجزيئات الخلوية مثل البروتينات الهيكلية، ما يؤدي إلى التغيرات المورفولوجية والبيوكيميائية المميزة المصاحبة لمسار الاستماتة، وهذا يشمل تكثيف الكروماتين في النواة، وتجزئة الحمض النووي، وانكماش الخلايا، وتكوين أجسام الاستماتة من
الغشاء الخلوي.
يعمل المسار الخارجي بوصفه آلية تنظيمية تسمح للخلية بالاستجابة للإشارات أو التهديدات الخارجية. وبما أن تنشيط المسار الخارجي له علاقة بكثير من العمليات الخلوية،
الاستجابة المناعية مثلًا، فإن أي خلل في تنظيم هذا المسار له آثار كبيرة في أمراض مختلفة مثل
اضطرابات المناعة الذاتية وبعض أنواع
السرطان[16].
المسار الداخلي
أما في مسار الاستماتة الداخلي، المعروف أيضًا باسم "مسار
الميتوكوندريا"، فتخضع
الخلية لعدد من الإشارات الداخلية التي تؤدي إلى زيادة نفاذية غشاء
الميتوكوندريا الخارجي للبروتينات. فتُطلق
بروتينات مؤازرة للاستماتة (pro-apoptotic proteins) من
الميتوكوندريا إلى
سيتوبلازم (cytoplasm)
الخلية، لتبدأ بتنفيذ برنامج الاستماتة. يُنظَّم هذا المسار بإحكام ويكون جزءًا أساسيًا في معظم عمليات النمو، وتوازن الأنسجة، والقضاء على الخلايا التالفة أو غير المرغوب فيها[17]. أما تفاصيل هذا المسار فهي:
- تفعيل المسار وبدؤه: يُنشَّط المسار الداخلي عن طريق كثير من الضغوط الخلوية الداخلية، كتلف الحمض النووي، أو إجهاد
الشبكة الإندوبلازمية (ER stress)، أو فقدان إشارات البقاء (survival signals). تؤدي هذه الضغوط إلى تفعيل المسارات الداخلية المؤدية لموت
الخلية المبرمج.
- تنشيط أفراد عائلة بي سي إل 2 المؤازرين للاستماتة (pro-apoptotic Bcl-2 family proteins) ودور
السيراميد (ceramide): تضم عائلة
بروتيناتبي سي إل 2 كثيرًا من الأفراد، قسم منهم مؤازرون وآخرون مانعون للاستماتة (anti-apoptotic). فالبروتينات المؤازرة للاستماتة مثل مجموعة بي إتش 3 (BH3) وبروتينَي باكس (Bax) وباك (Bak) تتنشط وتتجمع وتتمركز في غشاء
الميتوكوندريا الخارجي وتسهم في زيادة نفاذيته بتكوينها لقنوات كبيرة. وعلاوة على البروتينات، ثمة دور أساسي تؤديه
الدهون السفينغولية وبالتحديد
السيراميد[18] في بداية العملية وزيادة نفاذية الغشاء الخارجي[19]. فيتكوّن
السيراميد استجابةً لإشارات الإجهاد من خلال التخليق المجدَّد "دي نوڤو" (de novo synthesis) باستخدام
الحمض الأمينيسيرين (serine) والحمض الدهني بالميتويل مُرافِق الإنزيم أ (palmitoyl-CoA)[20]. وعند تراكم
السيراميد في الغشاء الخارجي يتشكل في قنوات دهنية كبيرة تسهم في خروج البروتينات إلى السيتوبلازم لاستكمال المسار[21]. يُذكَر أن أفراد عائلة بي سي إل 2 المؤازرة للاستماتة
والسيراميد يتعاونون معًا لقتل
الخلية، في حين يمنع أفراد عائلة بي سي إل 2 المانعين للاستماتة
السيراميد من تكوين قنواته، ومن ثم يمنعون الاستماتة[22].
- نفاذية الغشاء الخارجي للميتوكوندريا (mitochondrial outer membrane permeabilization - MOMP) وإطلاق عوامل الاستماتة: يفصل غشاء
الميتوكوندريا الخارجي الحيز ما بين الغشاءين (inter membrane space) في
الميتوكوندريا عن
السيتوبلازم، وهو منفِّذ للجزيئات الصغيرة في الوضع الطبيعي. أما
البروتينات فهي كبيرة ولا تمر منه. فعند زيادة النفاذية بوساطة قنوات باكس أو باك أو
السيراميد أو غيرها، تستطيع هاته البروتينات الانطلاق من الحيز للسيتوبلازم. ثمة كثير من البروتينات الموجودة في الحيز ما بين الغشاءين في الوضع الطبيعي تخرج عند البدء بالمسار الداخلي للاستماتة. أهم بروتين يُطلق هو سيتوكروم سي (cytochrome c) وهو بروتين مهم للغاية ودوره أساسي في تفاعلات إنتاج الطاقة في
الميتوكوندريا من مكانه في الحيز بين الغشاءين. ينقل هذا البروتين الإلكترونات من المعقّد الثالث (complex III) إلى المعقّد الرابع (complex IV) في سلسلة نقل الإلكترونات التي تسبق الفسفرة التأكسدية (oxidative phosphorylation) وإنتاج الطاقة الحيوية على شكل الأدينوسين ثلاثي الفوسفات (adenosine triphosphate, ATP). عند إطلاقه إلى السيتوبلازم يرتبط هذا البروتين مع
بروتينات أخرى، ليشكّل جسيم الاستماتة (apoptosome). أما بروتين سماك (SMAC، اختصار للاسم: المنشِّط الثاني للكاسباز المشتق من
الميتوكوندريا second mitochondria-derived activator of caspases) فيحفز الكاسبازات المنفذة بالمشاركة مع بروتين آخر يدعى ديابلو (DIABLO). يعمل انطلاق سماك/ ديابلو من
الميتوكوندريا على منع مثبط
بروتينات الاستماتة 3 (XIAP)، ما يؤدي إلى تحفيز الكاسباز[23].
- تكوين جسيم الاستماتة وتنشيط كاسباز-9: في السيتوبلازم، يرتبط السيتوكروم سي بعامل تنشيط بروتياز الاستماتة 1 (أباف-1) (apoptotic protease-activating factor 1 - APAF-1) مشكلًا وحدة واحدة بمساعدة جزيئات الأدينوسين ثلاثي الفوسفات. ترتبط 7 وحدات (سيتوكروم سي وأباف-1) معًا لتكوين الشكل الكامل لجسيم الاستماتة[24]. يستقطب هذا الجسيم الكاسباز-9 ويفعّل تتالي الكاسباز. يُنشط جسيم الاستماتة
إنزيم كاسباز-9 من خلال الانشقاق التحللي له مكونًا
إنزيم كاسباز-9 النشِط.
- بدء تتالي الكاسباز: إن الكاسباز-9 المنشَّط هو الكاسباز البادئ الذي يبدأ تتالي الكاسباز في المسار الداخلي. وكما الكاسبازات البادئة في المسار الخارجي يعمل كاسباز-9 على تحفيز الكاسبازات المنفذة (كاسباز-3 وكاسباز-7) بوساطة قطعهم.
- تنفيذ الاستماتة: تُنفَّذ الاستماتة الآن بطريقة المسار الخارجي نفسها لأن المسارين يلتقيان في هذه الخطوة فتكسر الكاسبازات المنفذة البروتينات الهيكلية والحمض النووي، وتؤدي إلى موت
الخلية، وهذه النتيجة هي التي تميز الاستماتة من حيث الصفات الشكلية.
وكما المسار الخارجي، فإن مسار الاستماتة الداخلي منظم بدقة تسمح للخلايا بالاستجابة للضغوطات الداخلية. لذا فإن اختلال هذا المسار يؤثر في ظهور أمراض عدة كالسرطان والاضطرابات التنكسية العصبية وغيرها[25].
تقاطع المسارين
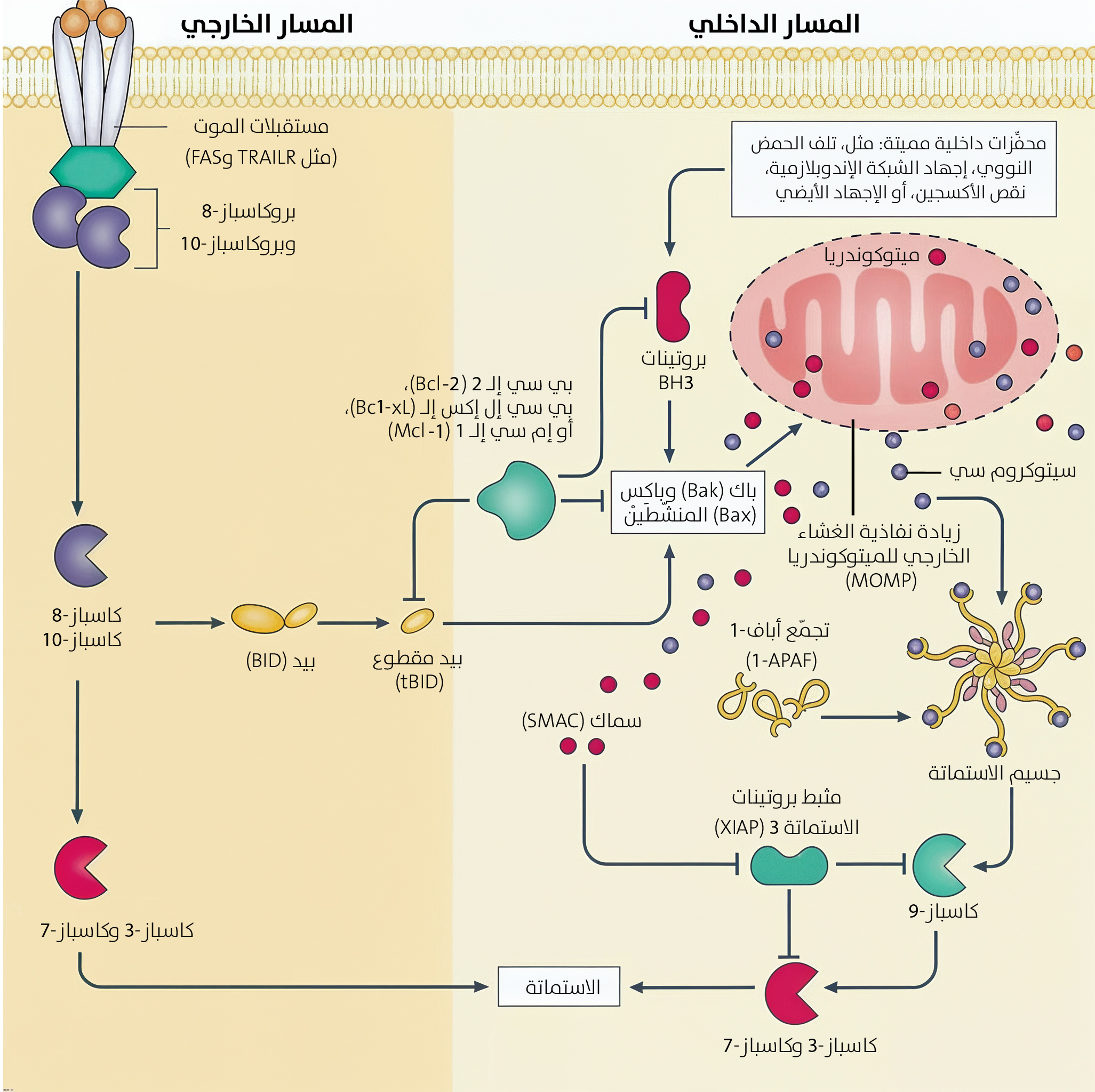 [الشكل 3] مسارا الاستماتة الخلوية
[الشكل 3] مسارا الاستماتة الخلوية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
مثل كثير من المسارات في
الخلية، يتشارك المساران الخارجي والداخلي في بعض الأحيان ويكونان مترابطين، ويُنظَّمان على نطاق واسع من خلال آليات متعددة. يمكن أن يؤدي تحفيز كاسباز-8 في المسار الخارجي إلى تفعيل أعضاء عائلة بي سي إل 2 المؤازرة للاستماتة (باكس وبيد)، الذي يؤدي لاحقًا إلى بدء المسار الداخلي من خلال زيادة نفاذية الغشاء الخارجي للميتوكوندريا[26]. وعلى النقيض، يمكن للمسار الداخلي تضخيم أثر المسار الخارجي من خلال إطلاق بعض البروتينات من
الميتوكوندريا. يضمن تداخل الإشارات ثنائي الاتجاه هذا ضبط إشارات الاستماتة وتنسيقها[27].
بعد تنفيذ الاستماتة عبر أي من المسارين، تعد التصفية الفعالة للخلايا الميتة أمرًا ضروريًا لمنع الالتهاب والحفاظ على استتباب الأنسجة المحيطة وأمانها. تُنفَّذ عملية ابتلاع أجسام الاستماتة وإزالتها عن طريق
البلعمة (phagocytosis)، بوساطة الخلايا المناعية أو الأنسجة المحيطة. تُسهَّل عملية
البلعمة عن طريق التعرف إلى جزيئات محددة على سطح أجسام الاستماتة والخلايا المحتضرة، بما في ذلك
الدهن الفسفوري (phospholipid) الفوسفاتيديل سيرين (phosphatidylserine) الذي يجري إخراجه على الطبقة الخارجية لأغشية الخلايا المحتضرة. تحتوي
الخلايا البلعمية على مستقبلات الفوسفاتيديل سيرين فتتعرف إلى الخلايا المحتضرة وترتبط بها وتبتلعها[28].
إنزيمات الكاسباز وتتالي الكاسباز
إنزيمات الكاسباز (وهي اختصار لـ "بروتياز السيستين-حمض الأسبارتيكcysteine-aspartic acid protease ") عائلة من
إنزيمات البروتياز المهمة في تنظيم عمليات موت الخلايا المختلفة وفي الالتهابات أيضًا. في الإنسان، تعد الكاسبازات مكونات أساسية للتوازن الخلوي، حيث تشارك في بدء الاستماتة وتنظيمها وتنفيذها (راجع 1.4 و2.4) والموت الحُمّي المبرمج، وهو شكل من موت الخلايا الالتهابية[29]. من مزايا هذه العائلة اعتمادها على الحمض الأميني سيستين في الموقع النشط الذي يسهم في عملية قطع الروابط الببتيدية بعد حمض الأسبارتيك فقط في البروتين المستهدف. في الإنسان هناك 12 عضوًا في عائلة الكاسباز[30]. تصنف هذه
الإنزيمات إلى ثلاث مجموعات رئيسة: الكاسبازات الالتهابية، والكاسبازات البادئة، والكاسبازات المنفذة. فالكاسبازات الالتهابية (كاسباز-1، -4، -5، و-12) لهم أدوار مهمة في تفعيل
بروتينات الالتهاب كإنترلوكين 1-بيتا (Interleukin 1b). أما البادئة التي تشمل كاسباز-8، -9، و-10، علاوة على -2 و-12، فمسؤولة عن بدء تتالي الكاسباز وتُنشَّط عادةً استجابةً لإشارات محددة، مثل تفعيل المستقبلات على الغشاء البلازمي (المسار الخارجي) أو تلف
الميتوكوندريا (المسار الداخلي). وآخر مجموعة هي الكاسبازات المنفذة (كاسباز-3، -6، و-7) التي تؤدي العمل النهائي بشق كثير من الجزيئات الخلوية ومؤدية إلى تحلل
الخلية الكامل بوساطة عملية الاستماتة. يُذكَر أن كاسباز-2، -12، و-14 يصعب وضعهم في أي من المجموعات الثلاث لاختلافهم عن البقية بتعقيدات مهماتهم ما يجعلهم مميزين. كاسباز-14 على سبيل المثال عضو مميز من عائلة الكاسبازات. ففي حين توجد البروتينات الأخرى في كثير من الخلايا والأنسجة، يوجد كاسباز-14 في أماكن محددة بالذات في النسيج الجلدي. وأن هذا البروتين أيضًا لا يؤثر في عملية الاستماتة وإنما ينظم شكلًا آخر من أشكال موت الخلايا الذي يدعى التقرّن (cornification)، وهي آلية خلوية متخصصة في نسيج البشرة[31].
تعدّ الاستماتة من أهم العمليات التي تجريها الكاسبازات، وفيها يتجلى دور تتالي الكاسباز. يتكون تتالي الكاسباز من سلسلة من الخطوات المنظمة للغاية تهدف بالنهاية لقتل
الخلية، بغض النظر عن مسار ابتداء الاستماتة. وهذه هي الخطوات العامة المتضمنة في هذا التتالي:
- تنشيط الكاسباز البادئ: في المسار الخارجي، واستجابة لإشارات معينة من خارج
الخلية، يتحفز كاسباز-8 أو -10 بوساطة استقطابهم في ديسك وانشقاقهم التحللي. وفي المسار الداخلي، يتحفز كاسباز-9 داخل جسيم الاستماتة.
- تحفيز الكاسبازات المنفذة: يعمل الكاسباز البادئ المحفَّز بوصفه آليات لتكسير وتحفيز البروتينات التالية (الكاسبازات المنفذة). فمن خلال قطع أجزاء من الكاسبازات المنفذة بوساطة البادئة، يُنشَّط التنفيذ. فينقسم كل من كاسباز-3، -6، و-7 ويصبحون جاهزين لتحليل مجموعة واسعة من المركبات الخلوية وتكسيرها بما في ذلك البروتينات الهيكلية، وإنزيمات إصلاح
الحمض النووي، ومكونات الهيكل الخلوي (cytoskeleton).
- تنفيذ الاستماتة: عند تحفيز الكاسبازات المنفذة، تصبح
الخلية تحت التكسير من الداخل، فيتكثف الكروماتين ويتجزأ الحمض النووي وتنكمش الخلايا وتتشكل جسيمات الاستماتة ويُجَهز على
الخلية.
يُنظَّم تتالي الكاسباز بإحكام لمنع موت الخلايا العرضي ولضمان حدوث موت الخلايا المبرمج فقط، استجابة لإشارات محددة. فيتضمن هذا التنظيم آليات مختلفة، بما في ذلك وجود
بروتينات مضادة للاستماتة مثل بي سي إل 2 وبي سي إل إكس إل (Bcl-xL) وغيرها التي تمنع عمل البروتينات المؤازرة للاستماتة، ومثبطات
بروتينات الاستماتة (Inhibitor of Apoptosis Proteins, IAPs) التي تمنع نشاط الكاسبازات. إن عدم تنظيم تتالي الكاسباز له آثار مهمة في الأمراض المختلفة. فعلى سبيل المثال، يرتبط تحفيز الكاسباز المفرط بالاضطرابات التنكسية العصبية وأمراض القلب، في حين أن المشكلات في تنشيط الكاسباز يمكن أن تسهم في تطور
السرطان[32].
الاستماتة المستقلة عن الكاسباز
الاستماتة المستقلة عن الكاسباز (caspase-independent apoptosis) شكل من أشكال موت الخلايا المبرمج الذي يحدث من دون تدخل مباشر من
إنزيمات الكاسباز. فعلى عكس الاستماتة المعتمدة على الكاسباز هناك مجموعة بديلة من الأحداث والآليات الجزيئية التي تؤدي إلى الاستماتة المستقلة عن الكاسباز وتنبع عنها. فتبدأ هذه العملية عن طريق محفزات مختلفة (تختلف غالبًا عن تلك الخاصة بالمسار المعتمد على الكاسباز)[33]. تتضمن بعض المحفزات الشائعة ما يلي:
- اختلال الميتوكوندريا: يمكن أن يؤدي تلف
الميتوكوندريا إلى إطلاق عوامل مؤازرة لموت الخلايا المبرمج، مثل العامل المسبب للاستماتة (apoptosis-inducing factor - AIF) والإندونوكلياز جي (endonuclease G) من
الميتوكوندريا وتنتقل إلى النواة. يحفز العامل المسبب للاستماتة تكثيف الكروماتين وتجزئة الحمض النووي على نطاق واسع، وهي سمة من سمات الاستماتة المستقلة عن الكاسباز. وعلى غرار العامل المسبب لاستماتة يجزِّئ الإندونوكلياز جي في النواة الحمض النووي بقطع أجزاء داخلية منه[34].
- إجهاد الشبكة الإندوبلازمية: يمكن أن يؤدي إجهاد
الشبكة الإندوبلازمية المطول إلى تنشيط عوامل مثل كينازات JNK (c-Jun N-terminal kinases). يؤدي تنشيط كينازات JNK إلى تحفيز كثير من البروتينات الخلوية والإشارات من خلال مسارات إشارات متعددة التي تؤدي بالنهاية إلى الاستماتة المستقلة عن الكاسباز[35].
- مركبات الأكسجين التفاعلية (reactive oxygen species - ROS): تؤدي مركبات الأكسجين التفاعلية إلى الإجهاد التأكسدي (oxidative stress)، وهو مرتبط بعدة مسارات خلوية من ضمنها الاستماتة المستقلة عن الكاسباز[36].
- زيادة نفاذية الليسوسومات: زيادة نفاذية الغشاء الليسوسومي يؤدي إلى إطلاق
بروتينات الكاثيبسين (cathepsin) ولا سيما الكاثيبسين ب (Cathepsin B) الذي يعمل في بدء برنامج الاستماتة[37].
وعلاوة على الجزيئات الخلوية، ثبت أن كثيرًا من المركبات الطبيعية والاصطناعية والجزيئات غير العضوية والأدوية المعاد استخدامها تسبب هذا الشكل من موت الخلايا المبرمج[38].
مقارنة بين موت الاستماتة والنخر
الاستماتة والنخر نوعان مختلفان من موت الخلايا ويختلفان في عدة طرق رئيسة (الشكل 4).
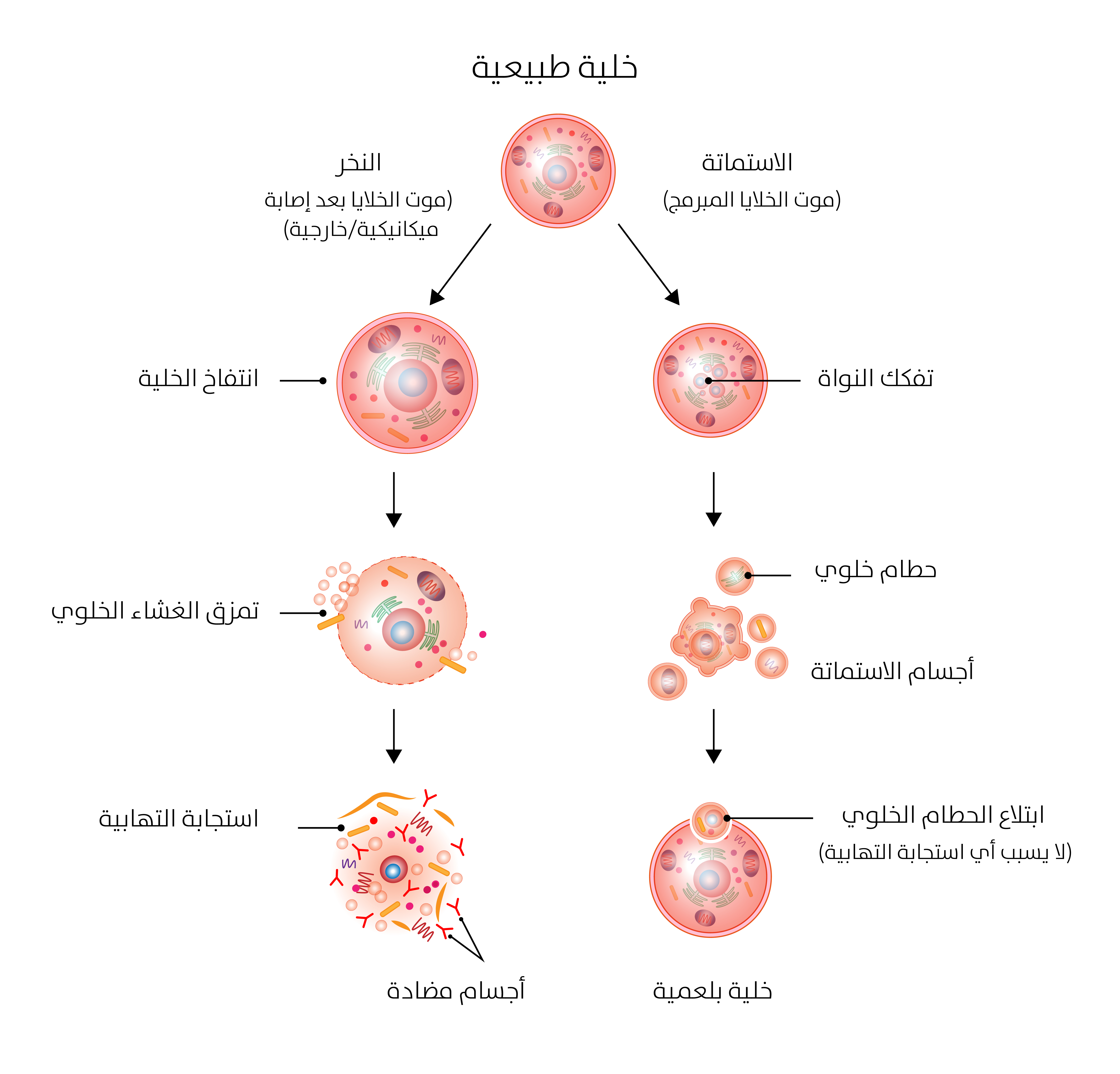 [الشكل 4] مقارنة شكلية بين النخر والاستماتة
[الشكل 4] مقارنة شكلية بين النخر والاستماتة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
أولًا: الاستماتة عملية مبرمجة تموت فيها الخلايا من دون أذية للخلايا المحيطة، في حين أن النخر (إجمالًا) عملية غير خاضعة للسيطرة. وفي حين تحدث الاستماتة نتيجة لمسار إشارات معقد يؤدي إلى تنشيط
إنزيمات (وجينات) معينة، يحدث النخر بسبب الضرر المادي أو الكيميائي الحاصل على
الخلية ما يؤدي إلى عدم قدرة
الخلية على الحفاظ على هيكلها ووظيفتها فتنفجر.
ثانيًا: تختلف الاستجابة الخلوية للاستماتة والنخر. ففي حالة الاستماتة، تخضع
الخلية المحتضرة لسلسلة من التغييرات تؤدي إلى تفتيت
الخلية إلى قطع صغيرة تُزال بسهولة بوساطة الجهاز المناعي من دون التسبب في حدوث التهاب. ومن ناحية أخرى، يتسبب النخر في تمزق
الخلية وإطلاق محتوياتها للخارج إلى الأنسجة المحيطة، ما يؤدي إلى استجابة التهابية يمكن أن تلحق الضرر بالخلايا السليمة القريبة.
ثالثًا: تختلف نتائج العمليتين. فالاستماتة عملية فيزيولوجية طبيعية ضرورية للتطور السليم للأنسجة وصيانتها، تساعد أيضًا في منع انتشار الخلايا التالفة أو غير الطبيعية، ولا تسبب عادةً ضررًا للأنسجة المحيطة. وفي المقابل، يرتبط
النخر عمومًا بتلف الأنسجة والالتهابات، ويمكن أن يؤدي إلى إطلاق مواد ضارة يمكن أن تلحق الضرر بالأنسجة السليمة المجاورة. وفي حين تخضع الاستماتة للرقابة المحكمة وتحدث بوصفها جزءًا من العمليات الفيزيولوجية الطبيعية، لا يخضع النخر للرقابة ويؤدي إلى تلف نسيجي عام[39].
المراجع
Abou-Ghali, Majdouline & Johnny Stiban. “Regulation of Ceramide Channel Formation and Disassembly: Insights on the Initiation of Apoptosis.” Saudi Journal of Biological Sciences. vol. 22, no. 6 (2015). pp. 760-772.
Bertheloot, Damien, Eicke Latz & Bernardo S. Franklin. “Necroptosis, Pyroptosis and Apoptosis: An Intricate Game of Cell Death.” Cellular & Molecular Immunology. vol. 18, no. 5 (2011). pp. 1106- 1121.
Bhadra, Kakali. “A Mini Review on Molecules Inducing Caspase-Independent Cell Death: A New Route to Cancer Therapy.” Molecules. vol. 27, no. 19 (2022).
Caroppi, P. et al. “Apoptosis and Human Diseases: Mitochondrion Damage and Lethal Role of Released Cytochrome C as Proapoptotic Protein.” Current Medicinal Chemistry. vol. 16, no. 31 (2009). pp. 4058-4065.
Colombini, M. “Ceramide Channels and Mitochondrial Outer Membrane Permeability.” Journal of Bioenergetics and Biomembranes. vol. 49, no. 1 (2017). pp. 57-64.
Colombini, M. Advances in Experimental Medicine and Biology. vol. 1159 (2019).
Dijkstra, C. D. “[Nobel Prize for Physiology or Medicine 2002 Is Awarded for Research into the Genetic Regulation of Organ Development and Programmed Cell Death].”
Nederlands Tijdschrift voor Geneeskunde. vol. 146, no. 51 (2002). pp. 2525 2527.
Duque-Parra, Jorge Eduardo. “Note on the Origin and History of the Term 'Apoptosis'.” Anatomical Record Part B: The New Anatomist. vol. 283B, no. 1 (2005). pp. 2-4.
Elmore, Susan. “Apoptosis: A Review of Programmed Cell Death.” Toxicologic Pathology. vol. 35, no. 4 (2007). pp. 456-516.
- Cecconi & M. D'Amelio (ed.).
Apoptosome: An up-and-coming Therapeutical Tool. Dordrecht: Springer Netherlands, 2010.
Ganesan, Vidyaramanan & Marco Colombini. “Regulation of Ceramide Channels by Bcl-2 Family Proteins.” FEBS Letters. vol. 584, no. 10 (2010). pp. 2128-2134.
Ganesan, Vidyaramanan et al. “Ceramide and Activated Bax Act Synergistically to Permeabilize the Mitochondrial Outer Membrane.” Apoptosis. vol. 15, no. 5 (2010). pp. 553-562.
Green, D. R. “Nonapoptotic Cell Death Pathways.” Cold Spring Harbor Perspectives in Biology. vol. 14, no. 6 (2022).
Hannun Yusuf A. & Lina M. Obeid. “Ceramide: An Intracellular Signal for Apoptosis.” Trends in Biochemical Sciences. vol. 20, no. 2 (1995). pp. 73-77.
Issleny, Batoul M. et al. The Enzymes. London: Academic Press, 2023.
Julien, Olivier & James A Wells. “Caspases and Their Substrates.” Cell Death & Differentiation. vol. 24, no. 8 (2017), pp. 1380-1389.
Kerr, J., A. Wyllie, & A. Currie. “Apoptosis: A Basic Biological Phenomenon with Wide-Ranging Implications in Tissue Kinetics.” British Journal of Cancer. vol. 26, no. 4 (1972). pp. 239-257.
Kesavardhana, Sannula, R.K. Subbarao Malireddi & Thirumala-Devi Kanneganti, “Caspases in Cell Death, Inflammation, and Pyroptosis,” Annual Review of Immunology. vol. 38 (2020). pp. 567-595.
Kiechle Frederick L. & Zhang Xinbo. “Apoptosis: Biochemical Aspects and Clinical Implications.” Clinica Chimica Acta. vol. 326, no. 1-2 (2002), pp. 27-45.
Kroemer, Guido & Seamus J Martin. “Caspase-Independent Cell Death.” Nature Medicine. vol. 11, no. 7 (2005). pp. 725-730.
Lane, Nick. “The Unseen World: Reflections on Leeuwenhoek (1677) 'Concerning Little Animals'.” Philosophical Transactions of the Royal Society B: Biological Sciences. vol. 370, no. 1666 (2015).
Lockshin, R. A. & Z. Zakeri )eds.(. When Cells Die II: A Comprehensive Evaluation of Apoptosis and Programmed Cell Death. Hoboken: Wiley-Liss, 2004.
Markiewicz, Agnieszka et al. “Caspase-14-From Biomolecular Basics to Clinical Approach. A Review of Available Data.” International Journal of Molecular Sciences. vol. 22, no. 11 (2021).
Martinez-Ruiz, Gustavo et al. “Role of Smac/DIABLO in Cancer Progression.” Journal of Experimental & Clinical Cancer Research. vol. 27, no. 1 (2008).
McIlwain, David R., Thorsten Berger & Tak W. Mak, “Caspase Functions in Cell Death and Disease.” Cold Spring Harbor Perspectives in Biology. vol. 5, no. 4 (2013).
Nagata, S. “Apoptosis and Clearance of Apoptotic Cells.” Annual Review of Immunology. vol. 36 (2018). pp. 489-517.
Nigam, M. et al. “Centchroman Mediated Apoptosis Involves Cross-Talk between Extrinsic/Intrinsic Pathways and Oxidative Regulation.” Life Sciences. vol. 87, no. 23-24 (2010). pp. 750-758.
Nikoletopoulou, Vassiliki. et al., “Crosstalk between Apoptosis, Necrosis and Autophagy.” Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. vol. 1833, no. 12 (2013). pp. 3448- 3459.
Qing Gu et al. “Activation of the Caspase-8/Bid and Bax Pathways in Aspirin-Induced Apoptosis in Gastric Cancer.” Carcinogenesis. vol. 26, no. 3 (2005). pp. 541-546.
Samanta, Soumya et al. “Visualization of Ceramide Channels by Transmission Electron Microscopy.” Biochimica et Biophysica Acta (BBA) - Biomembranes, vol. 1808, no. 4 (2011). pp. 1196-1201.
Slee, E. A., C. Adrain & S. J. Martin. “Serial Killers: Ordering Caspase Activation Events in Apoptosis.” Cell Death & Differentiation. vol. 6, no. 11 (1999). pp. 1067-1074.
- Sun & Z. L. Peng. “Programmed Cell Death and Cancer.”Postgraduate Medical Jounal. vol 85, no. 1001 (2009).
Zheng-Hong Qin (ed.). Autophagy: Biology and Diseases. Singapore: Springer, 2019.
[1] Vassiliki Nikoletopoulou et al., “Crosstalk between Apoptosis, Necrosis and Autophagy,” Biochimica et Biophysica Acta (BBA) - Molecular Cell Research, vol. 1833, no. 12 (2013), pp. 3448- 3459.
[2] Susan Elmore, “Apoptosis: A Review of Programmed Cell Death,” Toxicologic Pathology, vol. 35, no. 4 (2007), p. 495.
[3]Majdouline Abou-Ghali & Johnny Stiban, “Regulation of Ceramide Channel Formation and Disassembly: Insights on the Initiation of Apoptosis,” Saudi Journal of Biological Sciences, vol. 22, no. 6 (2015), p. 760.
[4] Damien Bertheloot, Eicke Latz & Bernardo S. Franklin, “Necroptosis, Pyroptosis and Apoptosis: An Intricate Game of Cell Death,” Cellular & Molecular Immunology, vol. 18, no. 5 (2011), p. 1106.
[5] Li-Fang Hu, “Epigenetic Regulation of Autophagy,” in: Zheng-Hong Qin (ed.), Autophagy: Biology and Diseases (Singapore: Springer, 2019), p. 221.
[6] D. R. Green, “Nonapoptotic Cell Death Pathways,” Cold Spring Harbor Perspectives in Biology, vol. 14, no. 6 (2022).
[7] J. Kerr, A. Wyllie, & A. Currie, “Apoptosis: A Basic Biological Phenomenon with Wide-Ranging Implications in Tissue Kinetics,” British Journal of Cancer, vol. 26, no. 4 (1972), p. 239.
[8] Nick Lane, “The Unseen World: Reflections on Leeuwenhoek (1677) 'Concerning Little Animals',” Philosophical Transactions of the Royal Society B: Biological Sciences, vol. 370, no. 1666 (2015).
[9] Jorge Eduardo Duque-Parra, “Note on the Origin and History of the Term 'Apoptosis',” Anatomical Record Part B: The New Anatomist, vol. 283B, no. 1 (2005), p. 2.
[10] R. A. Lockshin & Z. Zakeri )eds.(, When Cells Die II: A Comprehensive Evaluation of Apoptosis and Programmed Cell Death (Hoboken: Wiley-Liss, 2004).
[11] C. D. Dijkstra, “[Nobel Prize for Physiology or Medicine 2002 Is Awarded for Research into the Genetic Regulation of Organ Development and Programmed Cell Death],”
Nederlands Tijdschrift voor Geneeskunde, vol. 146, no. 51 (2002), p. 2525.
[12] Frederick L. Kiechle & Zhang Xinbo, “Apoptosis: Biochemical Aspects and Clinical Implications,” Clinica Chimica Acta, vol. 326, no. 1-2 (2002), p. 27.
[13] Y. Sun & Z. L. Peng, “Programmed Cell Death and Cancer,” Postgraduate Medical Journal, vol 85, no. 1001 (2009), p. 134.
[14] P. Caroppi et al., “Apoptosis and Human Diseases: Mitochondrion Damage and Lethal Role of Released Cytochrome C as Proapoptotic Protein,” Current Medicinal Chemistry, vol. 16, no. 31 (2009), p. 4058.
[15] E. A. Slee, C. Adrain & S. J. Martin, “Serial Killers: Ordering Caspase Activation Events in Apoptosis,” Cell Death & Differentiation, vol. 6, no. 11 (1999), p. 1067.
[16] David R. McIlwain, Thorsten Berger & Tak W. Mak, “Caspase Functions in Cell Death and Disease,” Cold Spring Harbor Perspectives in Biology, vol. 5, no. 4 (2013).
[17] Kiechle & Zhang.
[18] Yusuf A. Hannun & Lina M. Obeid, “Ceramide: An Intracellular Signal for Apoptosis,” Trends in Biochemical Sciences, vol. 20, no. 2 (1995), p. 73.
[19] M. Colombini, “Ceramide Channels,” in: Advances in Experimental Medicine and Biology, vol. 1159 (2019), p. 33; M. Colombini, “Ceramide Channels and Mitochondrial Outer Membrane Permeability,” Journal of Bioenergetics and Biomembranes, vol. 49, no. 1 (2017), p. 57.
[20] Batoul M. Issleny et al., “Sphingolipids: From Structural Components to Signaling Hubs,” in The Enzymes (London: Academic Press, 2023).
[21] Soumya Samanta et al., “Visualization of Ceramide Channels by Transmission Electron Microscopy,” Biochimica et Biophysica Acta (BBA) - Biomembranes, vol. 1808, no. 4 (2011), p. 1196.
[22] Vidyaramanan Ganesan et al., “Ceramide and Activated Bax Act Synergistically to Permeabilize the Mitochondrial Outer Membrane,” Apoptosis, vol. 15, no. 5 (2010), p. 553; Vidyaramanan Ganesan & Marco Colombini, “Regulation of Ceramide Channels by Bcl-2 Family Proteins,” FEBS Letters, vol. 584, no. 10 (2010), p. 2128.
[23] Gustavo Martinez-Ruiz et al., “Role of Smac/DIABLO in Cancer Progression,” Journal of Experimental & Clinical Cancer Research, vol. 27, no. 1 (2008), p. 48.
[24] E. Ferraro et al., “Mitochondrial Granules and the Control of Apoptosis,” in: F. Cecconi & M. D'Amelio (ed.)
Apoptosome: An up-and-coming Therapeutical Tool (Dordrecht: Springer Netherlands, 2010), p. 27.
[25] Kiechle & Zhang.
[26] Qing Gu et al., “Activation of the Caspase-8/Bid and Bax Pathways in Aspirin-Induced Apoptosis in Gastric Cancer,” Carcinogenesis, vol. 26, no. 3 (2005), p. 541.
[27] M. Nigam et al., “Centchroman Mediated Apoptosis Involves Cross-Talk between Extrinsic/Intrinsic Pathways and Oxidative Regulation,” Life Sciences, vol. 87, no. 23-24 (2010), p. 750.
[28] S. Nagata, “Apoptosis and Clearance of Apoptotic Cells,” Annual Review of Immunology, vol. 36 (2018), p. 489.
[29] Sannula Kesavardhana, R.K. Subbarao Malireddi & Thirumala-Devi Kanneganti, “Caspases in Cell Death, Inflammation, and Pyroptosis,” Annual Review of Immunology, vol. 38 (2020), p. 567.
[30] Olivier Julien & James A Wells, “Caspases and Their Substrates,” Cell Death & Differentiation, vol. 24, no. 8 (2017), p. 1380.
[31] Agnieszka Markiewicz et al., “Caspase-14-From Biomolecular Basics to Clinical Approach. A Review of Available Data,” International Journal of Molecular Sciences, vol. 22, no. 11 (2021), p. 5575.
[32] McIlwain et al.
[33] Guido Kroemer & Seamus J Martin, “Caspase-Independent Cell Death,” Nature Medicine, vol. 11, no. 7 (2005), p. 725.
[34] Kakali Bhadra, “A Mini Review on Molecules Inducing Caspase-Independent Cell Death: A New Route to Cancer Therapy,” Molecules, vol. 27, no. 19 (2022), p. 6401.
[35] Ibid.
[36] Ibid.
[37] Ibid.
[38] Ibid.
[39] Bertheloot et al.