الناسور الشرجي (Anal fistula)، هو قناة غير طبيعية تصل بين الجلد المحيط بفتحة الشرج وبطانة قناة الشرج، وأحيانًا - في حالات نادرة - مع بطانة المستقيم. وقد يمر الناسور عبر العضلة العاصرة الشرجية، مكوِّنًا أنواعًا مختلفة بحسب مساره، وتشمل: الناسور بين جزأَي العضلة العاصرة، والناسور العابر للعضلة العاصرة، والناسور فوق العضلة العاصرة، علاوة على الناسور خارج العضلة العاصرة. تُشخَّص أكثر من 90 في المئة من حالات الناسور الشرجي اعتمادًا على السيرة المرضية والفحص السريري، من دون الحاجة إلى تصوير طبي. وتتمثل الأهداف العلاجية الأساسية في السيطرة على الالتهاب، وعلاج الناسور جراحيًا بصورة شافية تمنع تكراره، مع الحفاظ على وظيفة العضلة العاصرة، وضمان التحكم الطبيعي بعملية الإخراج.
في النواسير البسيطة، يُعد بضع الناسور الخيار العلاجي الأمثل. أما في النواسير المعقدة، فيُفضَّل اللجوء إلى تقنيات حافظة للعضلة العاصرة، لتجنّب حدوث مضاعفات مثل السلس البرازي. ومن بين هذه الإجراءات: عملية الخُزامة، والسديلة المستقيمية الانزلاقية، وربط الناسور في المسافة بين جزأَي العضلة العاصرة. وتُستخدم كذلك خيارات علاجية إضافية، مثل الحقن بغراء الفيبرين، ووضع سدادة في مسار الناسور. أما التقنيات المستحدثة فتشمل: إغلاق الناسور بالليزر، والعلاج باستخدام التسجيل المرئي، وبضع الناسور مع إصلاح العضلة العاصرة بعد قطعه، علاوة على العلاج بالخلايا الجذعية، أو الإغلاق بالمشبك عبر منظار القولون.
تعريفه
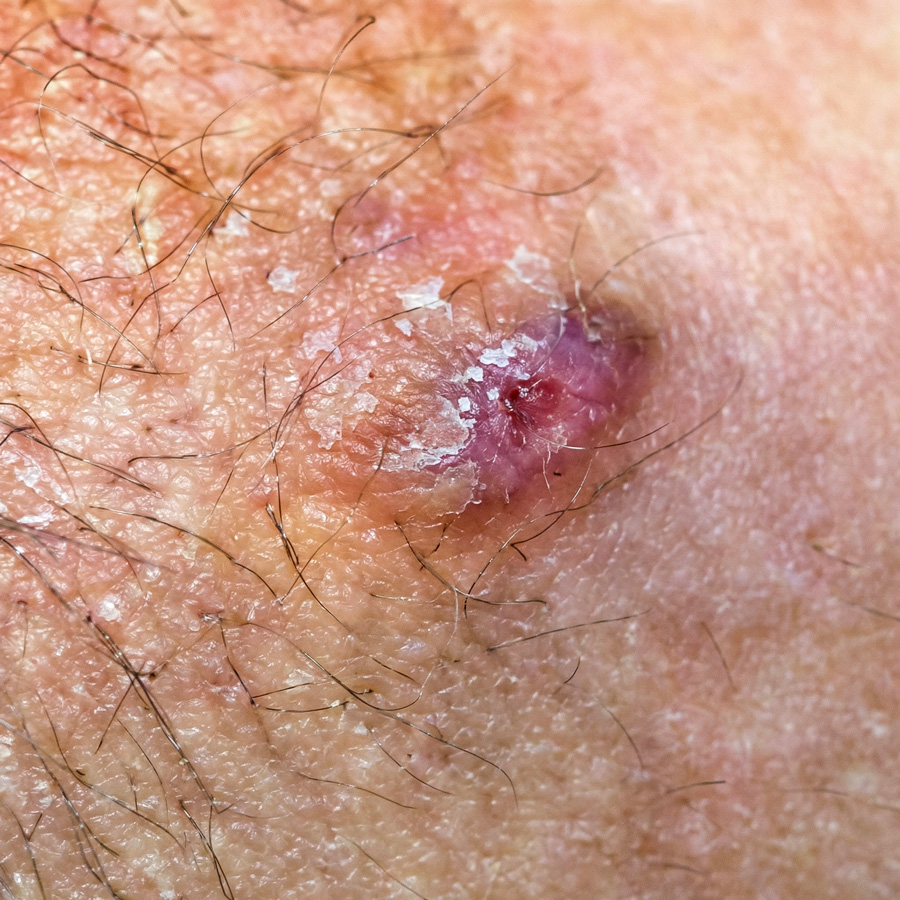
يُعرف الناسور (Fistula) على العموم بأنه قناة اتصال بين سطحَيْن من الجسم مبطنَيْن بالأنسجة الطلائية أو الظهارية (tissues Epithelial). والسطحان المقصودان في حالة الناسور الشرجي، هما الجلد المحيط بفتحة الشرج (Perianal skin)، وبطانة قناة الشرج (Anal canal)، وفي حالات قليلة بطانة المستقيم (Rectum). ويترتّب على هذا الاتصال مرور ذلك الناسور من خلال العضلة العاصرة الشرجية، أو مصرة الشرج (Anal sphincter) (الشكل 1).
[الشكل1] - الفتحة الخارجية لناسور شرجي على بعد 3 سنتيمترات إلى اليسار من فتحة الشرج
 المصدر : من مجموعة المؤلف
المصدر : من مجموعة المؤلف
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
آلية حدوثه
ثمة عدة نظريات تُفسّر ظهور الناسور الشرجي، من أبرزها[1]:
أولًا: النظرية الجرابية الغُدِّية (Cryptoglandular theory)، التي تُفسر تَكوّن نحو 90 في المئة من النواسير الشرجية. تشير هذه النظرية إلى أنَّ النواسير تتبع الخراجات الشرجية المستقيمية (Anorectal abscesses) في 30-35 في المئة من الحالات، عقب تصريف محتواها من الصديد {{الصديد: (Pus) سائل كثيف أصفر أو أخضر، يتكوّن من خلايا دم بيضاء ميتة، وبكتيريا، ونواتج التهابية أخرى. ويشير عادة إلى وجود عدوى بكتيرية نشطة في الأنسجة.}}. وتشير أيضًا إلى أن بداية الالتهاب تحدث في أحد الجرابات أو الخبايا (Crypt) الموجودة في الغشاء المبطن لقناة الشرج، وتحديدًا في منتصف قناة الشرج، على الخط المسنن (Dentate line). يبدأ الالتهاب في إحدى الغدد الشرجية (Anal glands) الموجودة بين عضلات العضلة العاصرة الشرجية، التي تنتهي فتحاتها في تلك الجرابات، نتيجة انسداد إحدى تلك الفتحات بالبكتيريا أو البراز أو غير ذلك، فيتجمع الصديد في تلك الغدة، مكوّنًا خراجًا بين جزأي العضلة العاصرة الشرجية (Intersphincteric abscess).
ثانيًا: من الممكن أن يجد الصديد طريقه إلى الأسفل، مكوّنًا خراجًا حول الشرج (Perianal abscess)، أو مخترقًا العضلة العاصرة الشرجية إلى خارجها، مكوّنًا الخراج الإسكي المستقيمي (Ischiorectal abscess)، أو إلى الأعلى مكوّنًا خراجًا فوق العضلة الرافعة الشرجية (Supralevator abscess). وفي حالات قليلة، يلتفّ الصديد حول قناة الشرج، مكوّنًا خراجًا على شكل حذوة الحصان (Horse shoe abscess). إنَّ مآل الخراجات الشرجية المستقيمية هو حدوث تصريف لمحتواها الصديدي، إما جراحيًا عن طريق البضع (أي الفتح) والنزح (التصريف/ Incision and drainage)، وإما عن طريق النزح أو التصريف الذاتي (Spontaneous drainage)، ليعقب ذلك تكوّن الناسور الشرجي في 30-35 في المئة من الحالات. ويُتوقَّع أيضًا أن يكون نوع الناسور الشرجي متناسبًا مع مسار الغدة الشرجية المصابة بالالتهاب أصلًا، أو المسار الذي اتخذته البكتيريا المسببة للالتهاب.
ثالثًا: ثمة نسبة من النواسير الشرجية تتبع الخراجات المرتفعة، من نوع الخراجات فوق الرافعة الشرجية، التي يكون مصدرها امتدادًا لخراجات في الحوض، ناتجة من التهابات في أعضاء البطن، مثل التهاب الزائدة الدودية (Acute appendicitis)، وداء الرتوج (Diverticular disease)، والتهابات المبيض وقناة فالوب (Tubo-ovarian infections)، والأورام السرطانية (Colorectal cancer)، وغيرها. إنَّ تشخيص هذا النوع من الخراجات والنواسير مهم، نظرًا لاختلاف عرضه السريري، والفحوصات المطلوبة للتشخيص، وطريقة العلاج.
كذلك تنتج بعض هذه النواسير من وجود أمراض أخرى تصيب منطقة الشرج، مثل إصابات الولادة، ومرض كرون (Crohn’s disease)، ومرض السل (Tuberculosis)، ومرض الساركويد (الغرناوية) {{مرض الساركويد أو الغرناوية: (Sarcoidosis) اضطراب التهابي مزمن، يتميز بتكوين حبيبات متناهية الصغر (Granulomas) في الأنسجة، غالبًا في الرئتين والعقد اللمفاوية، ما يعيق وظائف الأعضاء المصابة. ويحتاج إلى تشخيص دقيق وعلاج مناعي عند الضرورة.}}، ومرض نقص المناعة المكتسبة (HIV)، ونقص المناعة الناتج من سرطانات الدم وعلاجاتها وغير ذلك. وتوجد بعض أنواع النواسير، تكون جزءًا من سرطانات القناة الشرجية (Anal cancer).
تصنيفاته
- الناسور السطحي أو الظاهري (Subcutaneous or submucosal): يكون مساره محدودًا تحت الجلد أو المخاطية، ولا يشمل أي جزء من العضلة العاصرة الشرجية.
- الناسور بين جزأي العضلة العاصرة الشرجية (Intersphincteric): يمتد عبر التلم الواقع بين جزأي العضلة العاصرة الشرجية، والعضلة العاصرة الشرجية الداخلية (Internal anal sphincter)، والعضلة العاصرة الشرجية الخارجية (External anal sphincter).
- الناسور العابر للعضلة العاصرة الشرجية (Transsphincteric): يخترق الجزأين الداخلي والخارجي للعضلة العاصرة الشرجية، ويمتد إلى الحفرة الإسكية الشرجية (Ischiorectal fossa) قبل وصوله إلى الجلد. ويُصنَّف هذا النوع إلى: منخفض، ويشمل أقل من 30 في المئة من الجزء الخارجي للعضلة العاصرة الشرجية؛ ومرتفع، ويشمل أكثر من 30 في المئة من الجزء الخارجي للعضلة العاصرة الشرجية.
- الناسور فوق العضلة العاصرة الشرجية: يتجه مساره صعودًا، مخترقًا العضلة الرافعة للشرج.
- الناسور خارج العضلة العاصرة الشرجية (Extrasphincteric): لا ينشأ وفقًا للنظرية الجرابية الغدية (Cryptoglandular theory)، وإنما ينتج عادة من خراجات بطنية، أو أمراض مصاحبة، أو بوصفه من المضاعفات العلاجية لعمليات تصريف الخراج الشرجي المستقيمي، من النوع فوق الرافعة الشرجية (الشكل 2)[2].
[الشكل 2]
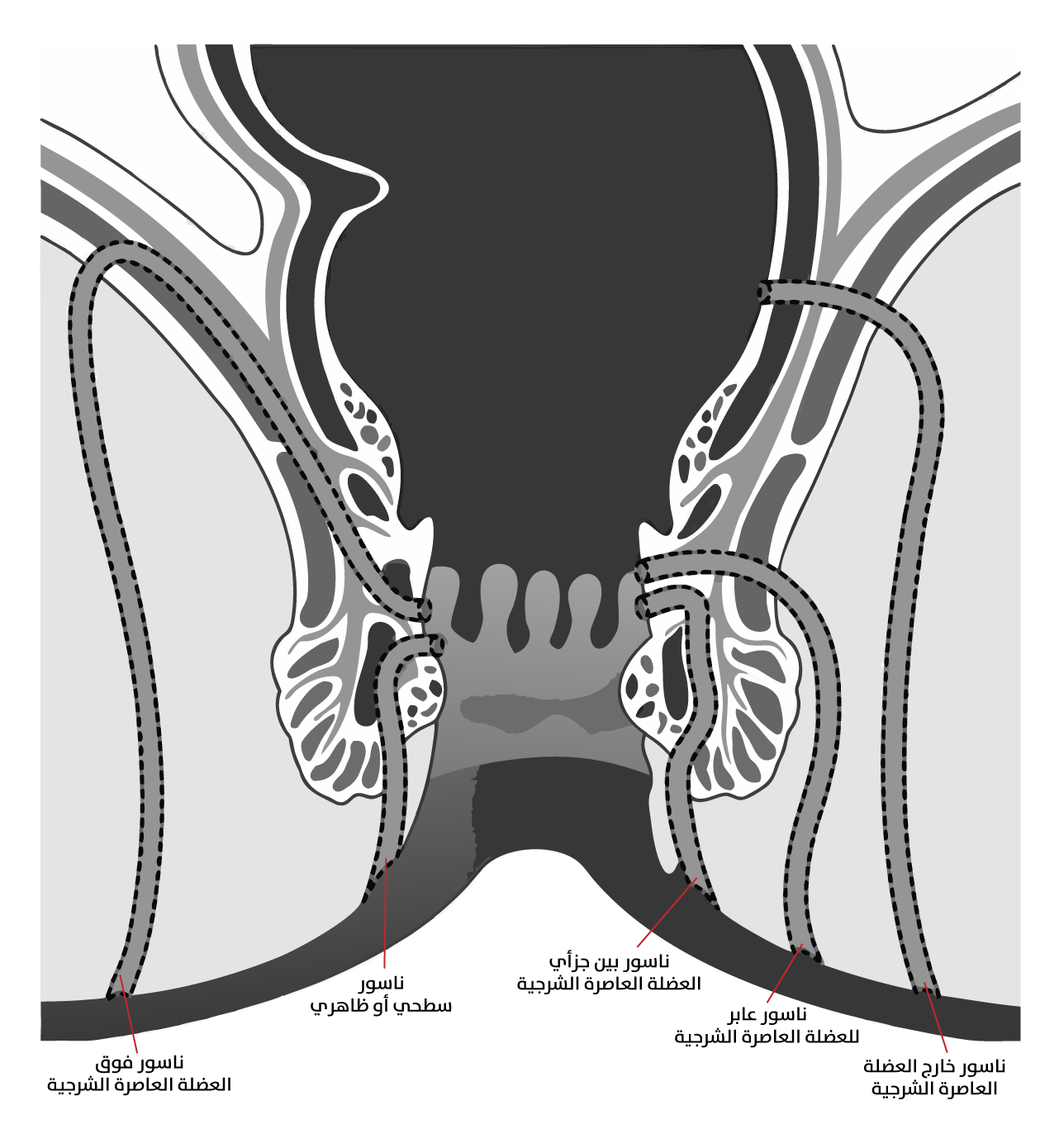 تصنيف النواسير الشرجية
تصنيف النواسير الشرجية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
كذلك تُعَد بعض النواسير الشرجية من النوع المعقد، نظرًا لارتباطها بعوامل تزيد من صعوبة علاجها ومضاعفاتها، وتشمل: الناسور العابر للعضلة العاصرة الشرجية، عندما يمتد لأكثر من 30 في المئة من سماكة العضلة العاصرة؛ والناسور فوق العضلة العاصرة الشرجية؛ والناسور خارج العضلة العاصرة الشرجية؛ علاوة على النواسير الأمامية لدى النساء (Anterior fistulas in females). كذلك تُعَدّ النواسير متعددة المسارات (Multiple tracts) والمتكررة (Recurrent fistulas) من الأنواع المعقدة، وكذلك تلك المرتبطة بأمراض أخرى مثل داء كرون، أو الناتجة من العلاج الشعاعي لمنطقة الشرج (Irradiation therapy)، فضلًا عن النواسير المصاحبة لوجود سلس برازي (Fecal incontinence).
أعراضه السريرية
من أبرز الأعراض السريرية المصاحبة للناسور الشرجي: الخروج المستمر للصديد، الذي قد يكون ممزوجًا بالدم أحيانًا، وما يترتب على ذلك من رائحة وصعوبة في الحفاظ على النظافة الشخصية؛ وحدوث ألم متكرر في منطقة الشرج وحولها، يتبعه تكوّن انتفاخ أو ورم. وتنتهي الأعراض بتصريف ذاتي لمحتوى ذلك الانتفاخ، على شكل مادة صديدية، والإحساس بندبة أو كتلة صغيرة في منطقة ما حول الشرج، والشعور بالهيجان والحكة في منطقة الشرج وما حولها[3].
فحصه سريريًّا
قد تُشاهَد فتحة خارجية (External opening) أو نتوء (Bump) أو عقدة صغيرة (Nodule) على الجلد المحيط بفتحة الشرج، بقربها أو بعيدًا عنها. وتُمثّل هذه الفتحة الخارجية بداية مسار الناسور. ويُلحَظ أيضًا أحيانًا وجود علامات التهاب متفاوتة الشدة في الجلد المحيط بفتحة الشرج، مثل الاحمرار، والتورم، والألم عند الجس (Tenderness)، علاوة على سخونة الجلد. في حالات النواسير المنخفضة (Low fistulas)، يمكن تحسس مسار الناسور من خلال الفحص المزدوج: فحص الجلد المحيط بقناة الشرج، مع إجراء الفحص الشرجي الإصبعي (Digital rectal examination) من الداخل.
تشخيصه
الغالبية العظمى من حالات الناسور الشرجي (أكثر من 90 في المئة) تُشخَّص من خلال السيرة المرضية والفحص السريري، من دون الحاجة إلى إجراء تصوير طبي (Medical imaging).
لا يمكن الاعتماد على موقع الفتحة الخارجية للناسور، أو على نوع الخراج السابق للناسور، في تحديد المقدار الذي يشتمل عليه الناسور من عضلة الشرج (Sphincteric involvement)، ولكن يمكن الاستفادة من موقع الفتحة الخارجية في تحديد موقع الفتحة الداخلية الموجودة على الخط المسنن.
وتوجد كثير من الإجراءات التي ييتخذها الجراح لتحقيق غايات الفحص تحت البنج سابقة الذكر، مثل الفحص اليدوي بالإصبع، واستخدام منظار الشرج (Anoscope)، وحقن مواد ملونة أو مواد تُصدر فقاعات هوائية، مثل مادة الهيدروجين بيروكسايد (Hydrogen peroxide)، وإدخال مسبار في الناسور الشرجي من الفتحة الخارجية لغاية الفتحة الداخلية.
ويمكن اللجوء إلى التصوير الطبي في حالات خاصة، مثل: الناسور المتكرر أو الناكس بعد الجراحة (Recurrent disease)، والنواسير المصاحبة لأمراض أخرى مثل مرض كرون، والنواسير من النوع خارج العضلة العاصرة الشرجية (Extra-sphincteric)، والناسور الذي لم يتمكن الجرّاح من تحديد تفاصيله في الفحص تحت البنج (Examination under anesthesia).
ومن أهم أنواع التصوير الطبي التي تُستخدم في هذا المجال: التصوير بالرنين المغناطيسي (Magnetic resonance imaging, MRI)، والتصوير الطبقي المحوري (Computed tomography)، والتصوير بالأمواج فوق الصوتية من داخل قناة الشرج (Endoanal ultrasound)، وتصوير الناسور بالأشعة السينية بعد حقن الناسور بمادة ملونة (Fistulography)[4].
يُحدّد الجرّاح بعد ذلك نوع الناسور، بسيطًا كان أو معقدًا. ويجري التفريق بين النوعَيْن بناءً على احتمالية حدوث سلس برازي {{سلس برازي: فقدان السيطرة على عملية التبرز، نتيجة ضعف العضلات أو الأعصاب في المستقيم أو فتحة الشرج، ما يؤدي إلى تسرب البراز بشكل لا إرادي، ويؤثر في جودة الحياة اليومية.}} إذا أُجرِيت عملية جراحية للناسور تتطلب قطعًا في العضلة العاصرة الشرجية. ومن ثَم، يترتب على هذا التصنيف نوع الإجراء الجراحي الأمثل للمريض، وتجنب حدوث السلس البرازي.
علاجه
تتمثل أهداف العلاج الرئيسة في السيطرة على الالتهاب (Control of sepsis)، وعلاج الناسور جراحيًا بطريقة شافية، لا تؤدي إلى تكرار المرض أو عودته (Sustained cure)، والمحافظة على التحكم (Maintenance of continence) بعملية إخراج البراز والغازات.
ويشار إلى أن المضادات الحيوية وحدها لا تكفي لعلاج النواسير الشرجية، ويمكن اللجوء إليها بوصفها وسيلة مساعدة في حالات خاصة فقط، للسيطرة على الالتهاب، وليس لشفاء الناسور، وذلك في المرضى ذوي عوامل الاختطار الشديدة، الذين يعانون من أعراض خفيفة تتعلق بالناسور.
تتطلب الخطوة الأولى من العلاج الفحص تحت البنج بأحد أنواعه المختلفة، إذ يجري من خلال هذا الفحص تحديد درجة الالتهاب في منطقة الشرج وما حولها، وتحديد مسار الناسور من الفتحة الخارجية في الجلد المحيط بالشرج ولغاية الفتحة الداخلية، ونوع الناسور والوضع التشريحي، ولا سيما علاقة الناسور بعضلة الشرج، واستثناء الأمراض المصاحبة أو أمراض أخرى[5].
أنواع التداخلات الجراحية
[الشكل 3]
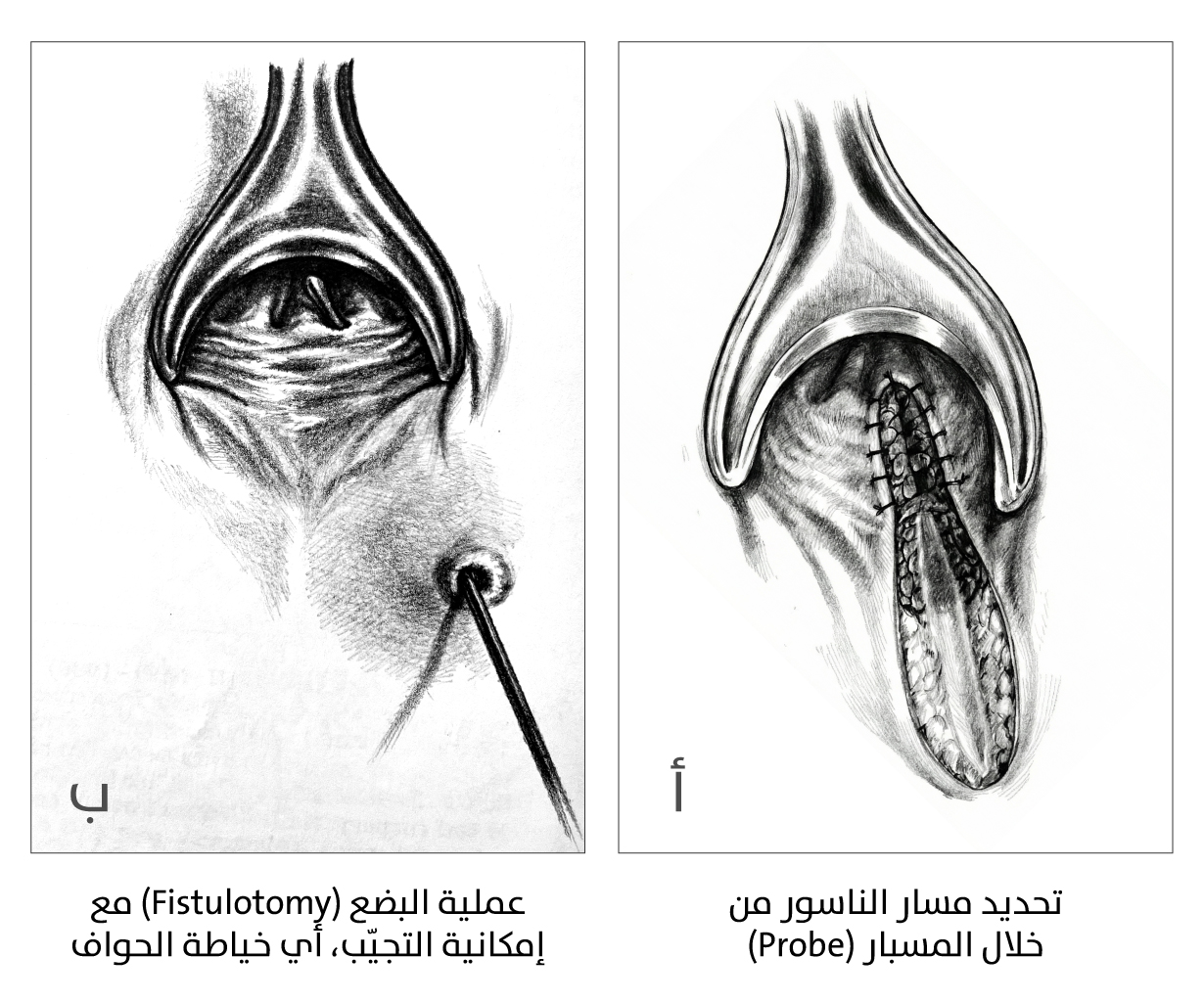 عملية بضع الناسور
عملية بضع الناسور
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
إنَّ الحُكم على نجاعة أي تداخل جراحي لعلاج الناسور، يكون من خلال المؤشرات التالية: نسبة الشفاء أي الالتئام (Healing rate)، ونسبة عودة الناسور وتكراره (Recurrence rate)، ونسبة الحفاظ على الإخراج أو فقدان التحكم به (Incontinence rate).
أما الخيارات المتاحة للعلاج فمتعددة، وتتباين بينها في نتائجها حسب المؤشرات السابقة. كذلك تتباين باختلاف الدراسات المنشورة تباينًا كبيرًا، وهذا يعني عدم وجود علاج مثالي حتى اللحظة، وإنما خيارات متعددة، ما يترك هامشًا لاختيار الجرّاح، بحسب الحالة والخبرة وتوفّر الإمكانات، ومن ثم، لا بُدَّ من إطْلاع المريض على الخيارات، والفروقات بينها، والنتائج المتوقعة قبل الإجراء.
في حالات النواسير البسيطة، فإنَّ الخيار الأفضل للعلاج هو عملية بضع الناسور (Fistulotomy)، التي تُعَد من العمليات الآمنة إذا اختير المريض المناسب لها، وتمتاز بنسبة شفاء مرتفعة، ونسبة مقبولة من تكرار الناسور أو سلس البراز. تشمل العملية فتح الناسور على طوله بين الفتحة الخارجية والداخلية، ومن ثم فهي تشمل فتح الجلد وبطانة قناة الشرج التي تُغطي الناسور، وكذلك ذلك الجزء من عضلة الشرج الذي يشتمل عليه الناسور. كذلك تشمل كشط تجويف الناسور (Fistula tract curettage)، وأحيانًا يُضافُ التجيب أو خياطة الحواف (Marsupialization)، لِما لذلك من فائدة في اختصار مدة الالتئام وتقليل النزف. من أهم المضاعفات لهذه العملية حدوث السلس البرازي، لذلك، لا بد من حُسن التقييم قبل الإجراء (الشكل 3).
[الشكل 4]
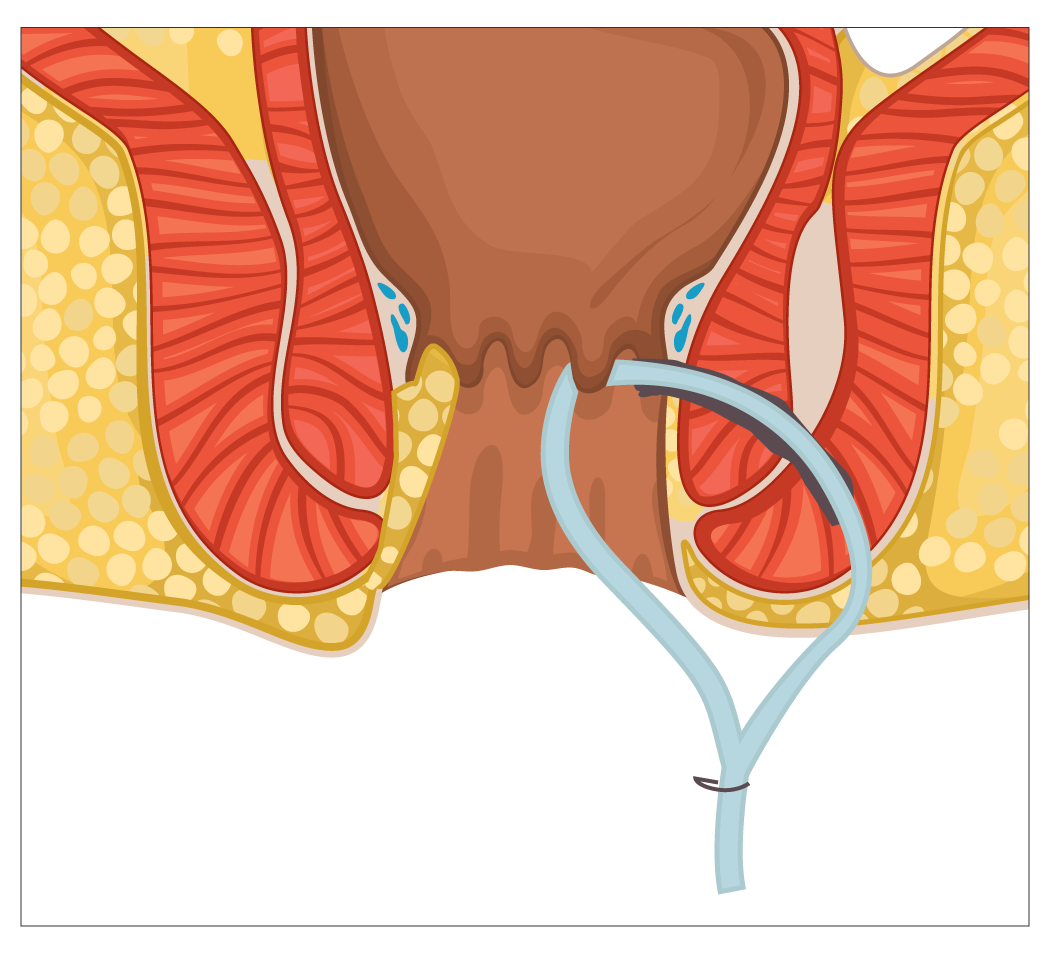 رسم توضيحي لمكان تركيب الخزامة
رسم توضيحي لمكان تركيب الخزامة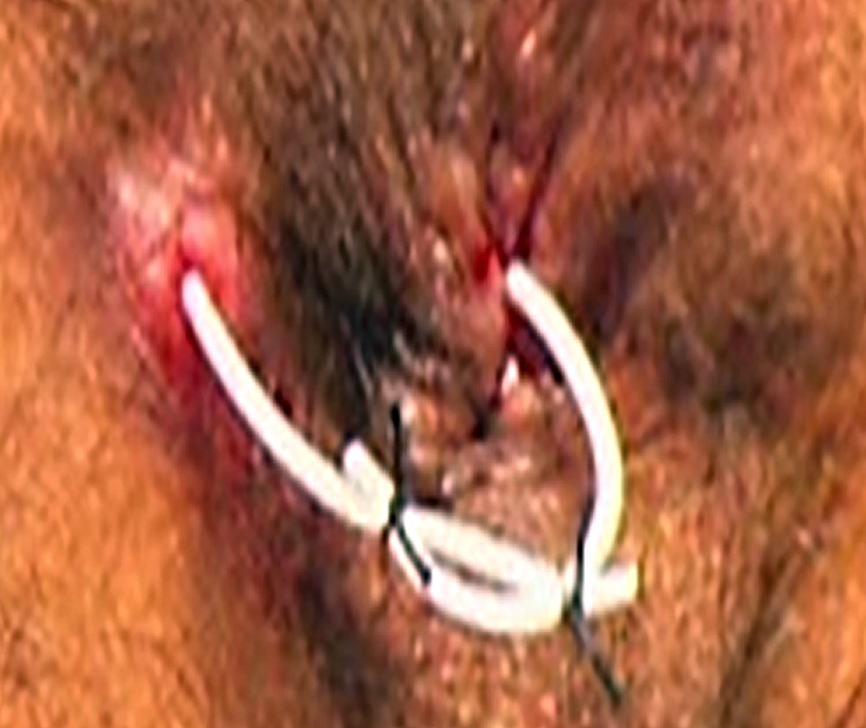 صورة لخزامة مشدودة في مكانها
صورة لخزامة مشدودة في مكانها
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل 5]
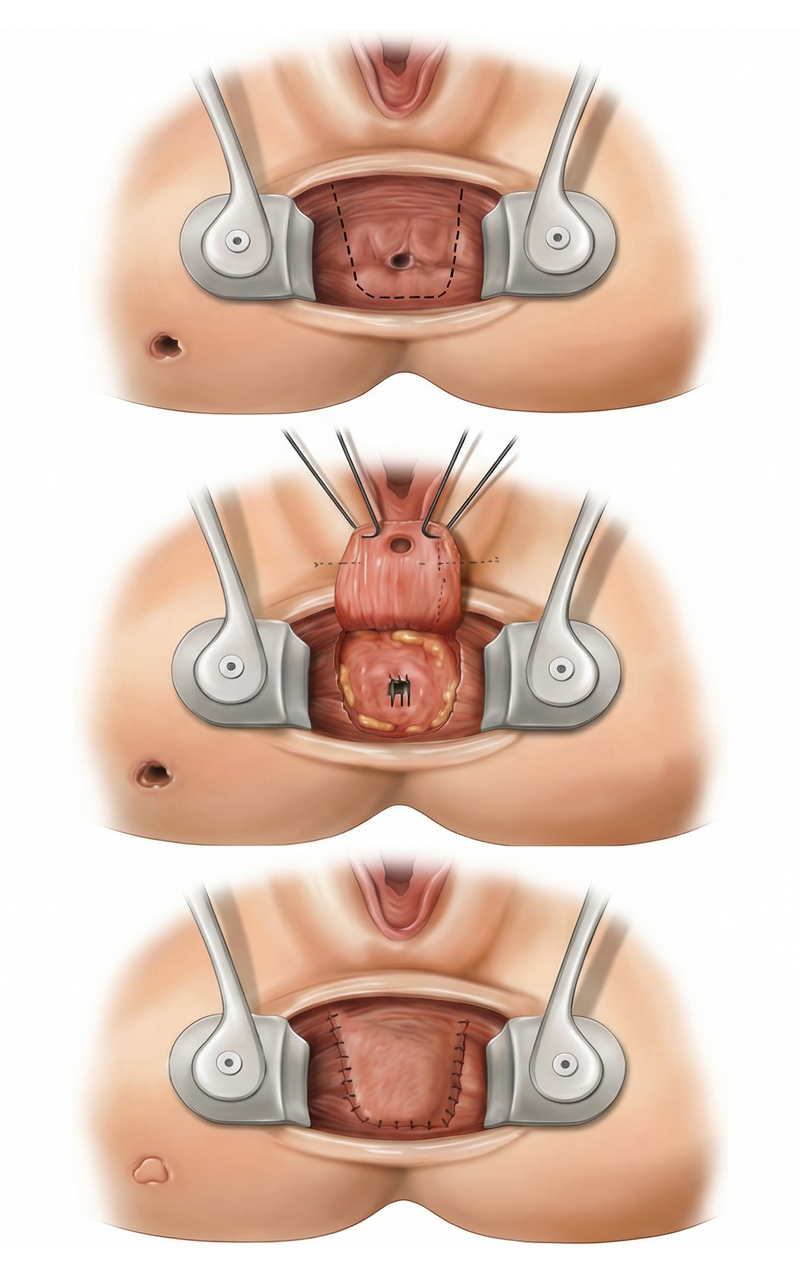 سديلة المستقيم الانزلاقية
سديلة المستقيم الانزلاقية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل 6]
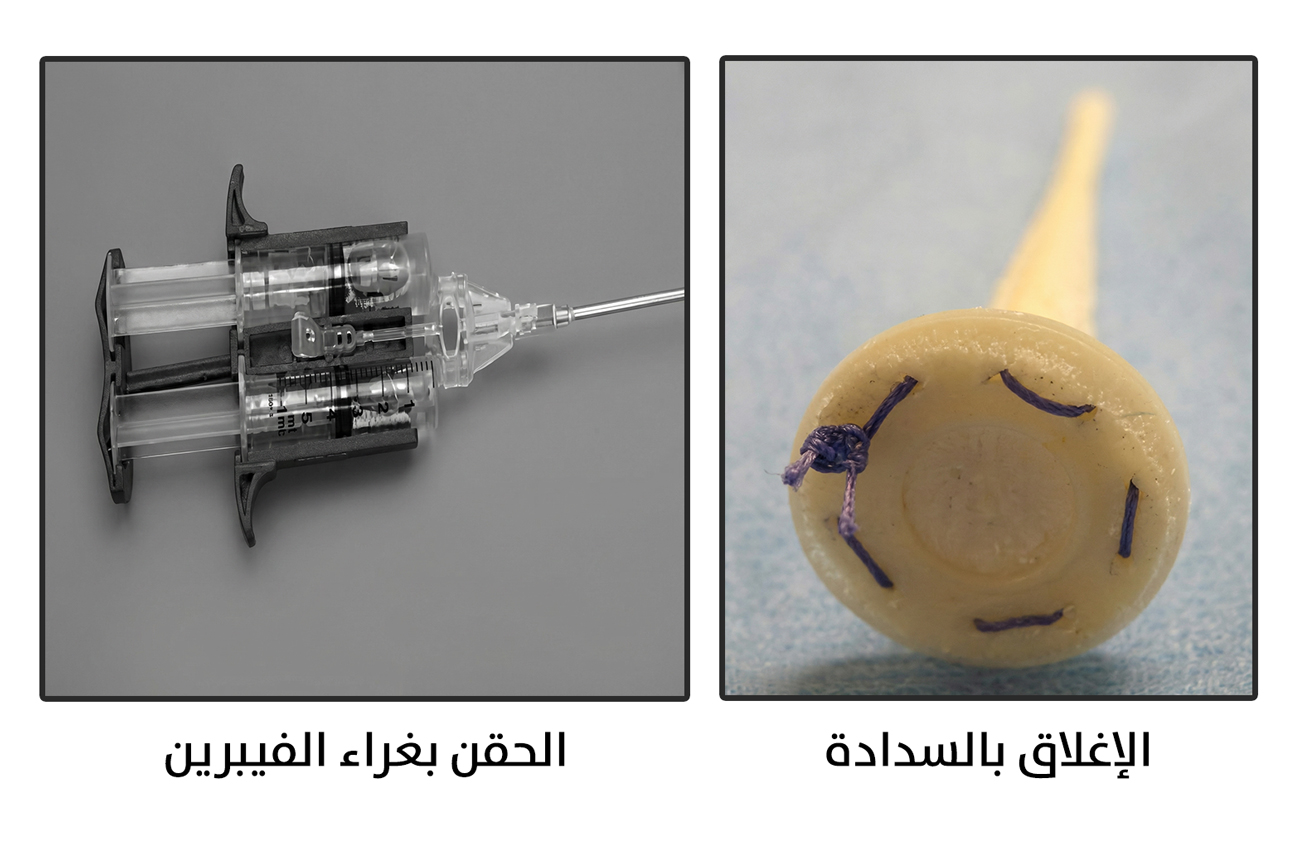 طرائق أخرى أقل فاعلية للعمليات الحافظة للعضلة العاصرة الشرجية
طرائق أخرى أقل فاعلية للعمليات الحافظة للعضلة العاصرة الشرجية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل 7]
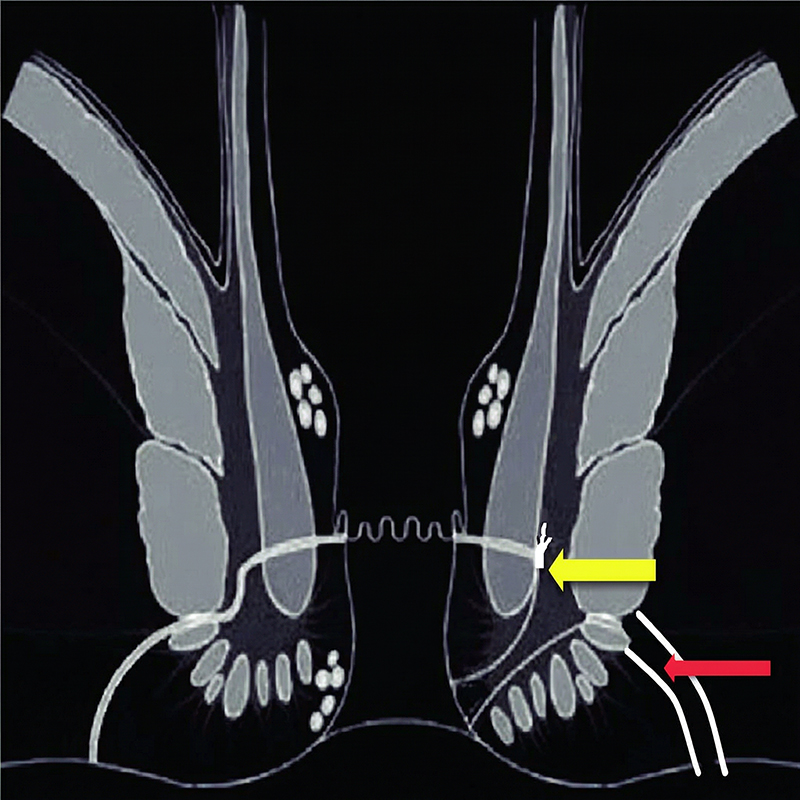 عملية ربط الناسور في الأخدود الواقع بين جزأي العضلة العاصرة الشرجية
عملية ربط الناسور في الأخدود الواقع بين جزأي العضلة العاصرة الشرجية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
في حالات النواسير المعقدة، لا بُدَّ من اللجوء إلى عمليات حافظة للعضلة العاصرة الشرجية (Sphincter preserving operations)، تجنبًا لحدوث المضاعفات، ومن أهمها ضعف العضلة، ما يؤدي إلى السلس البرازي.
يمكن اللجوء ابتداءً إلى عملية الخُزامة (Seton procedure)، عبر تمرير خيط داخل الناسور من الفتحة الخارجية إلى الداخلية، ثم إخراجه من قناة الشرج، وربط طرفَيْه ليشكل حلقة، ويمكن استخدام خيوط جراحية من أنواع مختلفة لهذه الغاية. وتُقسم الخزامة إلى نوعَيْن، بحسب الغاية منها (الشكل 4): النوع الأول يُسمّى الخزامة النَّزَّاحة (Loose seton)، التي تُستخدم للتصريف ومنع تجمع الصديد داخل الناسور (Draining seton)؛ والآخر هو الخزامة القاطعة (Cutting seton)، وتُستخدَم لقص الناسور، أو تمريره تدريجيًا عبر العضلة العاصرة لإغلاقه، مع الحفاظ على وظيفة العضلة.
في النوع الأول، تكون الخزامة رخوة (Loose)، لا تُمارس أي شدّ على العضلة العاصرة الشرجية، ويهدف استخدامها إلى تسريع تصريف الصديد والسيطرة على الالتهاب، علاوة على إتمام نضج الناسور (Maturation)، تمهيدًا (Bridge) لإجراء عملية لاحقة في ظروف أفضل. كذلك يمكن استخدام هذا النوع من الخزامة بوصفه علاجًا نهائيًا (Definitive treatment) في بعض الحالات[6].
أما في النوع الثاني، فتُربَط الخزامة بشكل ضاغط (Tight)، بحيث تُجرى عملية قطع والتئام تدريجية للعضلة، ويمكن إجراء عمليات شد متكرر بين مدة وأخرى لتسريع عملية القطع والالتئام. كذلك يمكن إضافة عملية قطع إلى الجزء الداخلي من العضلة العاصرة الشرجية، وذلك لزيادة احتمالية الشفاء، ولكن على حساب زيادة نسبة السلس البرازي، إذ تُعَدّ نسبته مرتفعة لدرجة لا تجعل من هذا النوع من العمليات خيارًا مفضلًا[7].
أما عمليات الخيار الأول، فهي العمليات الحافظة للعضلة العاصرة الشرجية (Sphincter -preserving operations)، وتشمل كلًّا من: سديلة المستقيم الانزلاقية (Endorectal advancement flap)، وربط الناسور في الأخدود الواقع بين جزأي العضلة العاصرة الشرجية (Intersphincteric ligation). وعلى الرغم من اختلاف تفاصيل الإجراء بين العمليتين، فإنهما تتشابهان في تحقيق نسبة نجاح معقولة، تتجاوز 50 في المئة، مع معدل منخفض للمضاعفات. وقد أدى ذلك إلى عدّهما الخيارَيْن الأولَيْن بين العمليات الحافظة للعضلة العاصرة، نظرًا لاجتيازهما مدة تجربة طويلة (Passed the test of time)، ودعمهما من خلال دراسات متعددة ونتائج قابلة للتكرار (Reproducible results) (الشكل 5)[8]. أما عمليات الخيار الثاني فتشمل: الحقن بغراء الفيبرين (Fibrin glue)، ووضع السدادة في الناسور (Fistula plug). يتميّز هذان النوعان من العلاج بنسبة مضاعفات منخفضة، ولكن بنسبة شفاء متباينة جدًا بين الدراسات المختلفة (الشكل 6)[9].
أما العمليات المستحدثة، فتشمل: إغلاق الناسور بالليزر (Fistula tract laser closure “FiLaC™”)[10]، والعلاج باستخدام التسجيل المرئي (Video-assisted anal fistula treatment - VAAFT)[11]، وبَضْع الناسور مع إصلاح العضلة العاصرة الشرجية بعد قطعها (Fistulotomy with sphincter repair)[12]، والعلاج باستخدام الخلايا الجذعية {{الخلايا الجذعية: (Stem cell therapy) خلايا غير متمايزة، قادرة على التحول إلى أنواع مختلفة من الخلايا، تُستخدم في العلاجات التجديدية لإصلاح الأنسجة المتضررة، واستعادة وظائف الأعضاء المصابة.}}[13]، والإغلاق باستخدام المشبك من خلال منظار القولون (Over the Scope Clip - OTSC)[14]. هذه الخيارات الجراحية المستحدثة جميعها، ما زالت قيد التقييم من حيث الفاعلية (نسب الشفاء ونسب المضاعفات)، للتباين الكبير في النتائج الأولية لتطبيقها، والدراسات عليها قائمة قبل الخروج بتوصيات يُعتمَد عليها (الشكل 7).
المراجع
Amor, I. B. et al. “Treatment of Complex Recurrent Fistula-in-Ano by Surgery Combined to Autologous Bone Marrow-Derived Mesenchymal Stroma Cells and Platelet-Rich Plasma Injection.” International Journal of Colorectal Disease. vol. 34, no. 10 (2019). pp. 1795-1799.
Balciscueta, Z. et al. “Rectal Advancement Flap for the Treatment of Complex Cryptoglandular Anal Fistulas: A Systematic Review and Meta-Analysis.” International Journal of Colorectal Disease. vol. 32, no. 5 (2017). pp. 599-609.
Bleier, J. I. & H. Moloo. “Current Management of Cryptoglandular Fistula-in-Ano.” World Journal of Gastroenterology. vol. 17, no. 28 (2011). pp. 3286-3291.
Brillantino, A. et al. “Preoperative Assessment of Simple and Complex Anorectal Fistulas: Tridimensional Endoanal Ultrasound? Magnetic Resonance? Both?” Radiologia Medica. vol. 124, no. 5 (2019). pp. 339-349.
Daodu, O. O., J. O’Keefe & J. A. Heine. “Draining Setons as Definitive Management of Fistula-in-Ano.” Diseases of the Colon & Rectum. vol. 61, no. 4 (2018). pp. 499-503.
Emile, S. H. et al. “A Systematic Review and Meta-Analysis of the Efficacy and Safety of Video-Assisted Anal Fistula Treatment (VAAFT).” Surgical Endoscopy. vol. 32, no. 4 (2018). pp. 2084-2093.
Gonzalez-Ruiz, C. et al. “Intraoperative Physical Diagnosis in the Management of Anal Fistula.” American Surgeon. vol. 72, no. 1 (2006). pp. 11-15.
Hall, J. F. et al. “Outcomes after Operations for Anal Fistula: Results of a Prospective, Multicenter, Regional Study.” Diseases of the Colon & Rectum. vol. 57, no. 11 (2014). pp. 1304-1308.
Halligan, S. “Magnetic Resonance Imaging of Fistula-in-Ano.” Magnetic Resonance Imaging Clinics of North America. vol. 28, no. 1 (2020). pp. 141-151.
Hamadani, A. et al. “Who Is at Risk for Developing Chronic Anal Fistula or Recurrent Anal Sepsis after Initial Perianal Abscess?” Diseases of the Colon & Rectum. vol. 52, no. 2 (2009). pp. 217-221.
Johnson, Eric K. & Greta Bernier. “The American Society of Colon and Rectal Surgeons Clinical Practice Guidelines for the Management of Cryptoglandular Abscess and Fistula.” Diseases of the Colon & Rectum. vol. 66, no. 2 (2023). pp. 253-270.
Johnson, Eric K., J. U. Gaw & D. N. Armstrong. “Efficacy of Anal Fistula Plug vs. Fibrin Glue in Closure of Anorectal Fistulas.” Diseases of the Colon & Rectum. vol. 49, no. 3 (2006). pp. 371-376.
Kamrava, A. & J. C. Collins. “A Decade of Selective Use of Adjustable Cutting Seton Combined with Fistulotomy for Anal Fistula.” American Surgeon. vol. 77, no. 10 (2011). pp. 1377-1380.
Kelly, M. E. et al. “The Role of Loose Seton in the Management of Anal Fistula: A Multicenter Study of 200 Patients.” Techniques in Coloproctology. vol. 18, no. 10 (2014). pp. 915-919.
Liang, C. et al. “CT Imaging with Fistulography for Perianal Fistula: Does It Really Help the Surgeon?” Clinical Imaging. vol. 37, no. 6 (2013). pp. 1069-1076.
Limura, E. & P. Giordano. “Modern Management of Anal Fistula.” World Journal of Gastroenterology. vol. 21, no. 1 (2015). pp. 12-20.
Litta, F. et al. “Fistulotomy and Primary Sphincteroplasty for Anal Fistula: Long-Term Data on Continence and Patient Satisfaction.” Techniques in Coloproctology. vol. 23, no. 10 (2019). pp. 993-1001.
Madbouly, K. M. et al. “Ligation of Intersphincteric Fistula Tract versus Mucosal Advancement Flap in Patients with High Transsphincteric Fistula-in-Ano: A Prospective Randomized Trial.” Diseases of the Colon & Rectum. vol. 57, no. 10 (2014). pp. 1202-1208.
Malakorn, S. et al. “Ligation of Intersphincteric Fistula Tract for Fistula in Ano: Lessons Learned from a Decade of Experience.” Diseases of the Colon & Rectum. vol. 60, no. 10 (2017). pp. 1065-1070.
Mascagni, D. et al. “OTSC® Proctology vs. Fistulectomy and Primary Sphincter Reconstruction as a Treatment for Low Trans-Sphincteric Anal Fistula in a Randomized Controlled Pilot Trial.” Minerva Chirurgica. vol. 74, no. 1 (2019). pp. 1-6.
Parks, A. G., P. H. Gordon & J. D. Hardcastle. “A Classification of Fistula-in-Ano.” British Journal of Surgery. vol. 63, no. 1 (1976). pp. 1-12.
Soker, G. et al. “The Comparison of CT Fistulography and MR Imaging of Perianal Fistulae with Surgical Findings: A Case-Control Study.” Abdominal Radiology. vol. 41, no. 8 (2016). pp. 1474-1483.
Van Tets, W. F. & H. C. Kuijpers. “Continence Disorders after Anal Fistulotomy.” Diseases of the Colon & Rectum. vol. 37, no. 12 (1994). pp. 1194-1197.
Wilhelm, A., A. Fiebig & M. Krawczak. “Five Years of Experience with the FiLaC™ Laser for Fistula-in-Ano Management: Long-Term Follow-up from a Single Institution.” Techniques in Coloproctology. vol. 21, no. 4 (2017). pp. 269-276.
[1] Eric K. Johnson & Greta Bernier, “The American Society of Colon and Rectal Surgeons Clinical Practice Guidelines for the Management of Cryptoglandular Abscess and Fistula,” Diseases of the Colon & Rectum, vol. 66, no. 2 (2023), pp. 253-270.
[2] Ibid.; A. Hamadani et al., “Who Is at Risk for Developing Chronic Anal Fistula or Recurrent Anal Sepsis after Initial Perianal Abscess?” Diseases of the Colon & Rectum, vol. 52, no. 2 (2009), pp. 217-221; C. Gonzalez-Ruiz et al., “Intraoperative Physical Diagnosis in the Management of Anal Fistula,” American Surgeon, vol. 72, no. 1 (2006), pp. 11-15.
[3] Johnson & Bernier, op. cit.; Hamadani et al., op. cit.; Gonzalez-Ruiz et al., op. cit.; A. G. Parks, P. H. Gordon & J. D. Hardcastle, “A Classification of Fistula-in-Ano,” British Journal of Surgery, vol. 63, no. 1 (1976), pp. 1-12.
[4] Johnson & Bernier, op. cit.; C. Liang et al., “CT Imaging with Fistulography for Perianal Fistula: Does It Really Help the Surgeon?” Clinical Imaging, vol. 37, no. 6 (2013), pp. 1069-76; G. Soker et al., “The Comparison of CT Fistulography and MR Imaging of Perianal Fistulae with Surgical Findings: A Case-Control Study,” Abdominal Radiology, vol. 41, no. 8 (2016), pp. 1474-1483; S. Halligan, “Magnetic Resonance Imaging of Fistula-in-Ano,” Magnetic Resonance Imaging Clinics of North America, vol. 28, no. 1 (2020), pp. 141-151; A. Brillantino et al., “Preoperative Assessment of Simple and Complex Anorectal Fistulas: Tridimensional Endoanal Ultrasound? Magnetic Resonance? Both?” Radiologia Medica, vol. 124, no. 5 (2019), pp. 339-349.
[5] Johnson & Bernier, op. cit.; Hamadani et al., op. cit.; Gonzalez-Ruiz et al., op. cit.; W. F. Van Tets & H. C. Kuijpers, “Continence Disorders after Anal Fistulotomy,” Diseases of the Colon & Rectum, vol. 37, no. 12 (1994), pp. 1194-1197; J. I. Bleier & H. Moloo, “Current Management of Cryptoglandular Fistula-in-Ano,” World Journal of Gastroenterology, vol. 17, no. 28 (2011), pp. 3286-3291; E. Limura & P. Giordano, “Modern Management of Anal Fistula,” World Journal of Gastroenterology, vol. 21, no. 1 (2015), pp. 12-20; J. F. Hall et al., “Outcomes after Operations for Anal Fistula: Results of a Prospective, Multicenter, Regional Study,” Diseases of the Colon & Rectum, vol. 57, no. 11 (2014), pp. 1304-1308.
[6] O. O. Daodu, J. O’Keefe & J. A. Heine, “Draining Setons as Definitive Management of Fistula-in-Ano,” Diseases of the Colon & Rectum, vol. 61, no. 4 (2018), pp. 499-503; M. E. Kelly et al., “The Role of Loose Seton in the Management of Anal Fistula: A Multicenter Study of 200 Patients,” Techniques in Coloproctology, vol. 18, no. 10 (2014), pp. 915-919.
[7] A. Kamrava & J. C. Collins, “A Decade of Selective Use of Adjustable Cutting Seton Combined with Fistulotomy for Anal Fistula,” American Surgeon, vol. 77, no. 10 (2011), pp. 1377-1380.
[8] Z. Balciscueta et al., “Rectal Advancement Flap for the Treatment of Complex Cryptoglandular Anal Fistulas: A Systematic Review and Meta-Analysis,” International Journal of Colorectal Disease, vol. 32, no. 5 (2017), pp. 599-609; S. Malakorn et al., “Ligation of Intersphincteric Fistula Tract for Fistula in Ano: Lessons Learned from a Decade of Experience,” Diseases of the Colon & Rectum, vol. 60, no. 10 (2017), pp. 1065-1070; K. M. Madbouly et al., “Ligation of Intersphincteric Fistula Tract versus Mucosal Advancement Flap in Patients with High Transsphincteric Fistula-in-Ano: A Prospective Randomized Trial,” Diseases of the Colon & Rectum, vol. 57, no. 10 (2014), pp. 1202-1208.
[9] Eric K. Johnson, J. U. Gaw & D. N. Armstrong, “Efficacy of Anal Fistula Plug vs. Fibrin Glue in Closure of Anorectal Fistulas,” Diseases of the Colon & Rectum, vol. 49, no. 3 (2006), pp. 371-376.
[10] A. Wilhelm, A. Fiebig & M. Krawczak, “Five Years of Experience with the FiLaC™ Laser for Fistula-in-Ano Management: Long-Term Follow-up from a Single Institution,” Techniques in Coloproctology, vol. 21, no. 4 (2017), pp. 269-276.
[11] S. H. Emile et al., “A Systematic Review and Meta-Analysis of the Efficacy and Safety of Video-Assisted Anal Fistula Treatment (VAAFT),” Surgical Endoscopy, vol. 32, no. 4 (2018), pp. 2084-2093.
[12] F. Litta et al., “Fistulotomy and Primary Sphincteroplasty for Anal Fistula: Long-Term Data on Continence and Patient Satisfaction,” Techniques in Coloproctology, vol. 23, no. 10 (2019), pp. 993-1001.
[13] I. B. Amor et al., “Treatment of Complex Recurrent Fistula-in-Ano by Surgery Combined to Autologous Bone Marrow-Derived Mesenchymal Stroma Cells and Platelet-Rich Plasma Injection,” International Journal of Colorectal Disease, vol. 34, no. 10 (2019), pp. 1795-1799.
[14] D. Mascagni et al., “OTSC® Proctology vs. Fistulectomy and Primary Sphincter Reconstruction as a Treatment for Low Trans-Sphincteric Anal Fistula in a Randomized Controlled Pilot Trial,” Minerva Chirurgica, vol. 74, no. 1 (2019), pp. 1-6.