نقص ڤيتامين ب12 هو حالة مرضية تنشأ عندما تنخفض مستوياته في الجسم عن المعدل الطبيعي، ويحدث ذلك عادةً نتيجة سوء امتصاص في الجهاز الهضمي، أو قلة تناول الأطعمة الغنية به، أو بسبب بعض الأمراض المزمنة. يؤدي نقص ڤيتامين ب12 إلى مشكلات صحية خطِرة، تشمل: فقر الدم ضخم الأرومات (Megaloblastic anemia)، واعتلال الأعصاب، واضطرابات معرفية ونفسية، علاوة على أعراض مثل التعب وضعف التركيز والتنميل وفقر الدم.
ڤيتامين ب12 المعروف أيضًا باسم كوبالامين (Cobalamin)، هو عنصر غذائي أساسي، يؤدي دورًا مهمًا في وظائف الجهاز العصبي وتكوين خلايا الدم، ويُستمَدّ بشكل رئيس من المصادر الحيوانية. يُعدّ التشخيص الدقيق لنقص ڤيتامين ب12 تحديًا، بسبب تعدد أعراضه وتشابهها مع حالات أخرى، مثل نقص حمض الفوليك أو اعتلال الأعصاب المحيطية، لذلك، يعتمد التشخيص الفعّال على الجمع بين الأعراض السريرية والفحوصات المخبرية المتخصصة. يعتمد علاج نقص ڤيتامين ب12 على تعويض النقص من خلال إعطاء الڤيتامين، مع اختلاف طريقة العلاج ومدته حسب السبب الكامن وراء النقص. وفي حالة التأخر في التشخيص أو عدم العلاج المناسب، قد تؤدي الحالة إلى مضاعفات خطرة تؤثر في عدة أجهزة في الجسم.
تعريفه
نقص ڤيتامين ب12 هو حالة مرضية تنجم عن انخفاض مستوى ڤيتامين ب12 في الجسم عن الحد الطبيعي، ما يؤثر في تكوين كريات الدم الحمراء ووظائف الجهاز العصبي. ويؤدي هذا النقص إلى ظهور أعراض مثل الإرهاق، وضعف التركيز، والتنميل، وفقر الدم.
ڤيتامين ب12
ڤيتامين ب12، المعروف أيضًا باسم الكوبالامين، هو أحد الڤيتامينات الأساسية القابلة للذوبان في الماء، ويتكوّن من حلقة كورين تحتوي في مركزها على ذرة كوبالت، ترتبط بها قاعدة نكليوتيدية (Nucleotide base) (الشكل 1). وتختلف أنواعه بحسب المجموعة المرتبطة بذرة الكوبالت، وتشمل: السيانيد (Cyanide)، والهيدروكسيل (Hydroxyl)، والميثيل (Methyl)، والديوكسي أدينوسيل (Deoxyadenosyl). الشكل النشط بيولوجيًا هو ديوكسي أدينوسيل كوبالامين (Deoxyadenosyl cobalamin)، وهو الشكل الرئيس المُخزّن في الكبد. يُستمَدّ ڤيتامين ب12 بشكل رئيس من المنتجات الحيوانية، مثل اللحوم الحمراء والبيض والحليب، ويمكن الحصول عليه من بعض الأطعمة المدعّمة[1].
 يتكوّن من حلقة كورين تحتوي في مركزها على ذرة كوبالت، ترتبط بها قاعدة نكليوتيدية (Nucleotide base)
يتكوّن من حلقة كورين تحتوي في مركزها على ذرة كوبالت، ترتبط بها قاعدة نكليوتيدية (Nucleotide base)
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
امتصاصه ودوره الأيضي
تُعَدّ آلية امتصاص ڤيتامين ب12 وفهم دوره الأيضي الحيوي من الأساسيات الضرورية لفهم أسباب نقصه وتأثيراته السريرية. في الوضع الطبيعي، وعند تناول الأغذية الغنية بڤيتامين ب12، يرتبط الڤيتامين ببروتين يُعرَف باسم العامل R R factor))، ويعرف أيضًا باسم الهابتوكورين (Haptocorrin)، وهو بروتين يُفرَز من الغدد اللعابية في الفم. وعند وصول هذا المركّب إلى الأمعاء الدقيقة، تفصله الإنزيمات البنكرياسية عن العامل (R)، ما يسمح للڤيتامين بالارتباط بالعامل الداخلي (Intrinsic factor, IF)، وهو بروتين سكري يُفرَز بوساطة خلايا المعدة الجدارية. وبعد تكوّن مركّب ڤيتامين ب12 مع العامل الداخلي، ينتقل هذا المركب إلى
اللفائفيالطرفي {{اللفائفي الطرفي: (Terminal
ileum) الجزء الأخير من الأمعاء الدقيقة، ويمتد من نهاية الصائم (Jejunum) حتى بداية الأعور (Cecum) في الأمعاء الغليظة.}}، إذ يرتبط بمستقبلات خاصة على السطح الداخلي للخلايا المعوية، ما يتيح امتصاص الڤيتامين بفاعلية. وبعد الامتصاص، يُشارك ڤيتامين ب12 في كثير من المسارات الأيضية الأساسية، التي تُعنى بوظائف الجهاز العصبي والجهاز الدموي[2].
الدور الإنزيمي والبيوكيميائي
يعمل ڤيتامين ب12 بوصفه عاملًا مساعدًا لإنزيم ميثيونين سينثاز (Methionine synthase)، الذي يُحوّل
الهوموسيستئين {{الهوموسيستئين: ((Homocysteine مركب كبريتي غير بروتيني، ينتج من عملية التمثيل الغذائي للأحماض الأمينية، ولا سيما من تحلل الميثيونين. وارتفاع مستوياته في الدم يرتبط بزيادة خطر الإصابة بأمراض القلب والأوعية الدموية، والسكتات الدماغية، وبعض الاضطرابات العصبية.}} إلى ميثيونين ((Methionine. خلال هذه العملية، يتحوّل الميثيل – تتراهيدروفولات (Methyl-tetrahydrofolate, THF) إلى تتراهيدروفولات (Tetrahydrofolate, THF)، الذي يُستخدَم في تكوين القواعد البيريميدينية اللازمة لتصنيع
الحمض النووي
منقوص الأكسجين (Deoxyribonucleic Acid, DNA) وبنائها، وفي حالة حدوث نقص ڤيتامين ب12، لا يجري هذا التحويل الحيوي، ما يؤدي إلى تراكم الهوموسيستئين وتعطّل تكوين قواعد البيريميدينة، وتثبيط تصنيع الحمض النووي، وظهور فقر الدم ضخم الأرومات. كذلك يتأثر نشوء
الخلايا الدموية متعددة النوى {{الخلايا الدموية متعددة النوى: (Polymorphonuclear cells,
PMNs) خلايا دم بيضاء مناعية، تحتوي على نواة مقسّمة إلى فصوص متعددة، وظيفتها الدفاع عن الجسم عبر مهاجمة البكتيريا والڨيروسات.}}، وتظهر تحت المجهر بصفة تعدد
الفصوصالنووية {{الفصوص النووية: (HypersegmentedNeutrophils) أجزاء النواة المنفصلة جزئيًا في بعض الخلايا، مثل الخلايا الدموية متعددة النوى، تساعد في مرونة النواة وحركتها داخل الأنسجة.}}، وهي علامة دالة على نقص الكوبالامين[3].
الدور العصبي
يُستخدَم ڤيتامين ب12 بوصفه عاملًا مساعدًا لإنزيم ميثيل مالونيل–كوA ميوتاز (Methylmalonyl-CoA mutase)، الذي يحوّل ميثيل مالونيل–كوA (Methylmalonyl-CoA) إلى سكسينيل-كوA Succinyl-CoA)). وفي حالة نقص مستوى ڤيتامين ب12، يتراكم حمض الميثيل مالونيك (Methylmalonic acid, MMA) في الدم، لعدم تحوّله إلى سكسينيل-كوA (Succinyl-CoA). وتشير الأدلة إلى أن ارتفاع الميثيل مالونيك والهوموسيستئين، يسهم في إصابة غمد الميالين العصبي (Myelin sheath)، ما يؤدي إلى اعتلال الأعصاب الطرفية، واختلال التوازن الحركي، وقد يتطور الأمر إلى الضمور النخاعي المشترك تحت الحاد (Subacute Combined Degeneration, SCD)[4].
أسبابه
يُعزى نقص ڤيتامين ب12 إلى مجموعة متنوعة من الأسباب، تتداخل فيها العوامل الغذائية والمناعية والهضمية والدوائية والوراثية. ونظرًا لتعدد المراحل التي يمر بها الڤيتامين منذ دخوله الجسم وحتى امتصاصه واستعماله، فإن الخلل في أيّ مرحلة من هذه المراحل قد يؤدي إلى نقصه.
ورغم أن بعض الحالات تنجم عن نقص المدخول الغذائي (Inadequate dietary intake)، ولا سيما لدى النباتيّين أو كبار السن، فإن النسبة الأكبر من الحالات تعود إلى اضطرابات في الامتصاص المعوي أو إنتاج العامل الداخلي. كذلك فإن بعض الأدوية الشائعة، مثل مثبطات مضخة البروتون (Proton Pump Inhibitors, PPIs) والميتفورمين (Metformin)، باتت تُشكّل أسبابًا متزايدة الانتشار لهذا النقص.
فقر الدم الخبيث
يُعَدّ فقر الدم الخبيث (Pernicious Anemia) الشكل الكلاسيكي لنقص ڤيتامين ب12، وهو مرض مركّب ينتج من تدمير مناعي ذاتي للخلايا الجدارية في المعدة، ما يؤدي إلى نقص في إفراز العامل الداخلي. تمنع الأجسام المضادة في هذا المرض ارتباط الڤيتامين ب12 بالعامل الداخلي IF، ما يحول دون تكوّن المركب اللازم لامتصاص الڤيتامين عبر جدار الأمعاء الدقيقة.
وُجِد أن فقر الدم الخبيث يُشخَّص لدى نسبة تصل إلى 25 في المئة من المرضى المصابين بالتهاب المعدة المناعي الذاتي (Autoimmune gastritis)، وهو حالة تصيب قاع المعدة وجسمها، باستثناء منطقة الغار (الأنتروم/ Antrum)، وتتميز بوجود أجسام مضادة موجّهة ضد الخلايا الجدارية، تؤدي إلى تدميرها ضمن الغشاء المخاطي الأوكسنتي (Oxyntic mucosa)، المسؤول عن إفراز الحمض المعدي والعامل الداخلي. ويؤدي غياب حمض المعدة إلى ضعف في قدرة الجسم على تحرير ڤيتامين ب12 المرتبط بالبروتينات الغذائية، إلى جانب نقص إنتاج العامل الداخلي، ما يُفاقم من ضعف الامتصاص (الشكل 2 والشكل 3)[5].
 الشكل 2 - فقر الدم الخبيث
الشكل 2 - فقر الدم الخبيث الشكل 3 - فقر الدم الخبيث
الشكل 3 - فقر الدم الخبيث
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
سوءالامتصاص
يُعزى سوء الامتصاص إلى مشكلات في الجهاز الهضمي، منها
قصورالبنكرياس {{قصورالبنكرياس: (pancreatic insufficiency) حالة يفقد فيها البنكرياس القدرة على إفراز ما يكفي من الإنزيمات الهاضمة، ما يؤدي إلى سوء امتصاص الطعام ونقص العناصر الغذائية. ومن أسبابه التليّف الكيسي، والتهاب البنكرياس المزمن. تظهر الأعراض في إسهال دهني وفقدان وزن، ويشمل العلاج تعويض الإنزيمات ودعم التغذية.}}، إذ يقل إفراز البنكرياس للإنزيمات المهمة التي تسهم في فصل ڤيتامين ب12 عن العامل R، ما يُضعف ارتباط الڤيتامين بالعامل الداخلي (IF) الضروري لامتصاصه. كذلك فإن الالتهابات المعوية، مثل العدوى البكتيرية والتهاب الداء الزلاقي (Celiac disease)، قد تؤثر سلبًا في عملية الامتصاص.
وتُعَدّ الإجراءات الجراحية، مثل الاستئصال الجزئي أو الكلي للمعدة أو الأمعاء، كما في حالات داء كرون (Crohn’s Disease)، من الأسباب المباشرة لنقص الامتصاص، نتيجة فقدان الأجزاء المسؤولة عن إفراز العامل الداخلي أو امتصاص ڤيتامين ب12[6].
النقص الغذائي
قد يؤدي سوء التغذية إلى حدوث نقص في ڤيتامين ب12، ولا سيما لدى كبار السن أو مدمني الكحول، إذ ينخفض استهلاكهم اليومي للأطعمة الحيوانية الغنية بالكوبالامين. ونظرًا إلى أن المصادر الطبيعية لڤيتامين ب12 هي حصريًا من أصل حيواني، مثل اللحوم الحمراء والبيض والحليب، فإن النباتيّين الصارمين (Vegan or Strict vegetarians)، الذين لا يستهلكون اللحوم إطلاقًا، يُعَدّون الأكثر عُرضة للإصابة بنقصه.
ويُشار إلى أن نقص ڤيتامين ب12 لأسباب غذائية يتطور ببطء شديد، نظرًا لقدرة الجسم على تخزين كميات كبيرة منه في الكبد، لذلك، قد تمر عدة سنوات قبل ظهور الأعراض السريرية الواضحة.
وقد وُثّقت كثيرٌ من الدراسات حالات سريرية لهذا النقص، ولا سيما بين الرضّع الذين يُولدون لأمهات نباتيات صارمات يُرضِعن طبيعيًا. كذلك ظهرت أدلة حديثة تُبيّن أن النباتيّين اللاكتو-أوفو (Lacto-ovo vegetarians)، الذين يستهلكون الحليب والبيض ويتجنّبون اللحوم، مُعرَّضون أيضًا لخطر نقص الكوبالامين، ولكن بدرجة أقل من النباتيّين الصارمين[7].
الأدوية والسموم
تؤثر بعض الأدوية مباشرةً في امتصاص الڤيتامينات، ولا سيما تلك التي تُثبّط إفراز حمض المعدة وإنزيمالببسين {{إنزيم الببسين: (Pepsin) إنزيم هضمي يُفرَز في المعدة، يكسر البروتينات إلى سلاسل أقصر من الأحماض الأمينية.}}، ما يُضعف عملية تحرير ڤيتامين ب12 من البروتينات الغذائية. من أبرز هذه الأدوية شائعة الاستخدام، أدوية علاج
قرحةالمعدة {{قرحة المعدة: (Gastriculcer) تآكل أو جرح في بطانة المعدة، ينتج غالبًا من زيادة إفراز الحمض أو الإصابة بجرثومة المعدة (المَلَوِيَّة البوابية الحلزونية/ (Helicobacter pylori. تتسبّب قرحة المعدة بألم في الجزء العلوي من البطن، وقد تترافق مع حرقة أو غثيان، ويشمل علاجها الأدوية المثبطة للحمض، والمضادات الحيوية عند وجود عدوى.}} والارتجاع المعدي المريئي (Gastroesophageal reflux disease, GERD)، ومضادات مستقبلات الهيستامين-2 (H2 receptor antagonists) مثل السيميتيدين (Cimetidine)، ومثبطات مضخة البروتون (PPIs)، مثل الأوميبرازول (Omeprazole) واللانسوبرازول (Lansoprazole).
كذلك أثبتت الأدلة أن دواء الميتفورمين (Metformin)، المستخدم على نطاق واسع في علاج داء السكري من النوع الثاني، مرتبط بانخفاض كبير في مستويات ڤيتامين ب12 في الدم، ولا سيما عند الاستخدام المزمن.
علاوة على ذلك، فإن التعرض لغاز أكسيد النيتروز (Nitrous Oxide)، قد يؤدي إلى تثبيط نشاط ڤيتامين ب12، وظهور أعراض عصبية واضحة[8].
أعراضه وعلاماته السريرية
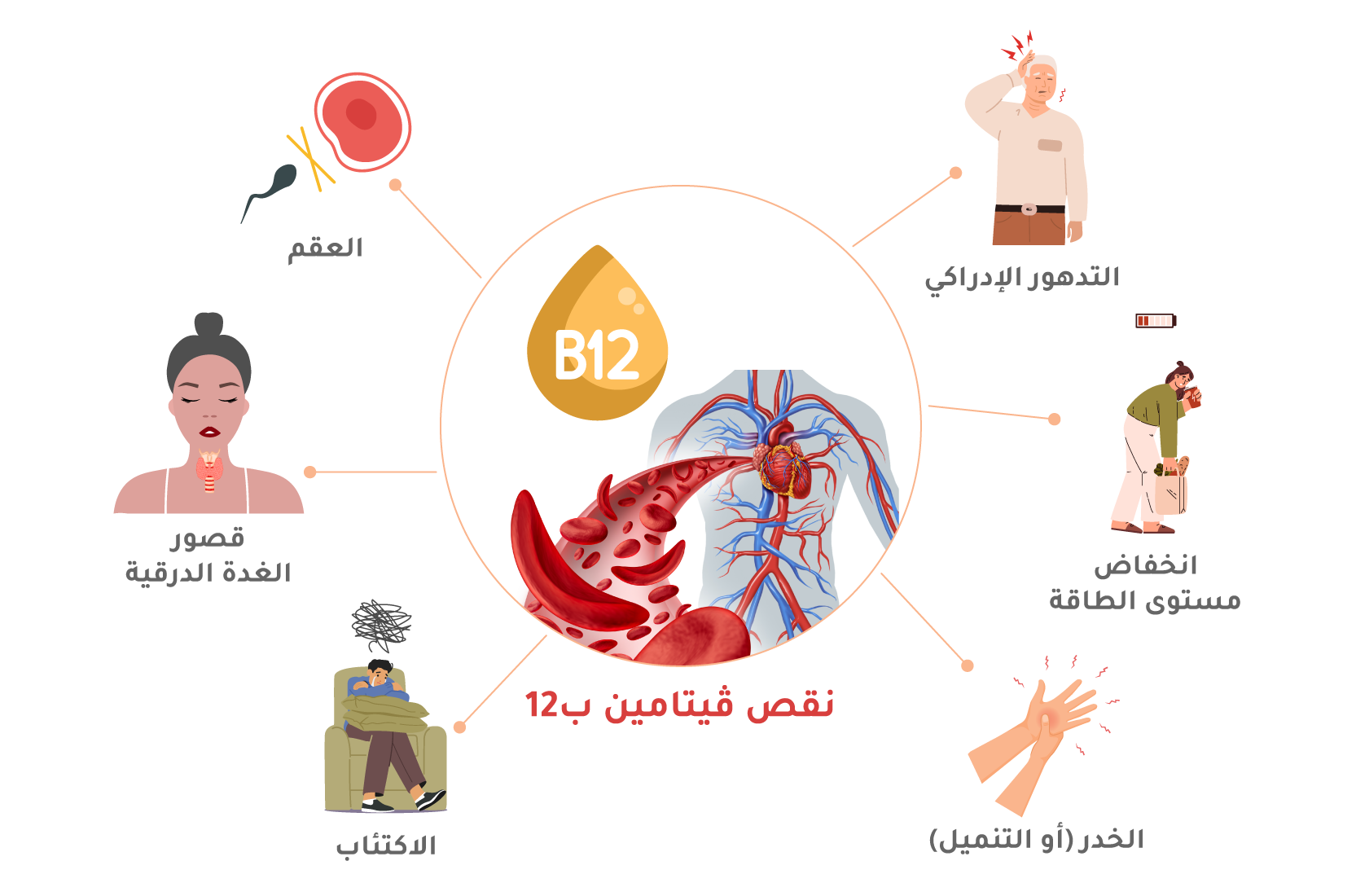 بعض من الأعراض الجسدية والعقلية لنقص ڤيتامين ب12
بعض من الأعراض الجسدية والعقلية لنقص ڤيتامين ب12
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
يتطلب تقييم نقص ڤيتامين ب12 أخذ التاريخ المرضي وإجراء فحص سريري شامل، مع التركيز خصوصًا على الجهازَيْن الهضمي والعصبي، نظرًا لارتباط نقص الڤيتامين بهما بشكل مباشر.
الأعراض الدموية
قد يظهر نقص ڤيتامين ب12 على هيئة فقر الدم ضخم الأرومات (Megaloblastic anemia)، نتيجة تثبّط تخليق الحمض النووي في خلايا نخاع العظم، ما يؤدي إلى أعراض فقر الدم، المتمثلة في الإرهاق العام والضعف والخمول، وشحوب الجلد، وضيق النفس عند الجهد وخفقان القلب، علاوة على انخفاض تركيز الهيموغلوبين، وارتفاع متوسط حجم الكريات الحمراء (Macrocytosis)، وتعدد فصوص العدلات (Hypersegmented Neutrophils) في فحص الدم المحيطي، ونقص الكريات الشامل في الحالات المتقدمة[9].
الأعراض العصبية
يُعَدّ ڤيتامين ب12 أساسيًا لصحة الجهاز العصبي المركزي والطرفي، ويدخل في تكوين غمد المايلين الذي يحيط بالألياف العصبية، ويؤدي نقصه إلى أعراض تظهر على شكل خدر وتنميل في الأطراف، وضعف الإحساس بالاهتزاز أو الوضعية، واختلال التوازن والصداع، وضعف المشي أو التردد الحركي، واعتلال الأعصاب الطرفية، علاوة على ضمور الحبل الشوكي المشترك تحت الحاد (Subacute Combined Degeneration)، الذي يصيب عادةً الأعمدة الظهرية، والمسالك القشرية الشوكية الجانبية، والمسالك الشوكية المخيخية. وقد تظهر الأعراض العصبية من دون أي علامات دموية، ما يزيد من احتمالية تأخر التشخيص[10].
في المقابل، فإن نقص حمض الفوليك {{نقصحمضالفوليك: حالة تنجم عن انخفاض مستوى ڤيتامين B9 الضروري لتكوين خلايا الدم الحمراء وتكاثر الخلايا. يؤدي النقص إلى فقر الدم، وتأثيرات سلبية في النمو الخلوي، ولا سيما خلال الحمل، إذ يزيد من خطر التشوهات الخلقية، مثل عيوب الأنبوب العصبي (Neural tube defects).}} يؤدي إلى أعراض دموية متشابهة، مثل فقر الدم ضخم الأرومات والتعب والشحوب، ولكنه لا يُسبّب أعراضًا عصبية، لأن الفولات لا تشارك في استقلاب الميالين أو حماية الألياف العصبية، لذا، فإن وجود أعراض عصبية مصاحبة لفقر الدم، يُعَدّ مؤشرًا مميزًا يُرجّح كفة نقص ڤيتامين ب12 على نقص الفولات.
الأعراض النفسية والعقلية
قد يظهر نقص ڤيتامين ب12 بمظاهر نفسية - عصبية من دون وجود فقر دم واضح، وتشمل: التهيج، والتوتر، والاكتئاب، والتقلبات العاطفية، والتغيرات في الشخصية، والذهان أو الهذيان، وتراجع الذاكرة، والخرف الذي قد يُشابه مرض الزهايمر في الحالات المتقدمة[11].
الأعراض الهضمية
على الرغم من أن الأعراض الهضمية أقل شيوعًا، فقد تظهر بعض الأعراض مثل: فقدان الشهية، وفقدان الوزن، والتهاب اللسان، إذ يبدو اللسان أملس وأحمر مع نقصان حاسة التذوق أو فقدانها، والإسهال أو الإمساك[12].
نقصه لدى الأمهات والرضّع
قد يؤدي نقص ڤيتامين ب12 لدى الأم خلال الحمل أو الرضاعة الطبيعية، إلى عواقب صحية خطِرة على الطفل، منها:
عيوبالأنبوبالعصبي {{عيوبالأنبوبالعصبي: (NeuralTubeDefects,
NTDs) تشوهات خلقية تحدث في أثناء تطوّر الجنين، إذ يفشل الأنبوب العصبي في الانغلاق بشكل كامل، ما يؤدي إلى مشكلات في الدماغ أو الحبل الشوكي، مثل السنسنة المشقوقة (Spina bifida) أو انعدام الدماغ (Anencephaly).}}، وتأخر النمو والتطور، وفشل النمو، ونقص التوتر العضلي {{نقصالتوترالعضلي: حالة تتميز بانخفاض غير طبيعي في قوة توتر العضلات، ما يؤدي إلى ضعف العضلات، ومشكلات في الحركة، وتأخر في تحقيق المهارات الحركية لدى الأطفال. وقد يكون وراثيًا أو مرتبطًا بحالات عصبية أخرى.}}، واختلال التوازن الحركي، وفقر الدم[13].
تشخيصه المخبري والسريري
يُعَدّ التشخيص الدقيق لنقص ڤيتامين ب12 أمرًا معقّدًا، نظرًا لتنوّع مظاهره السريرية وتشابهه مع حالات أخرى، مثل نقص حمض الفوليك أو اعتلال الأعصاب المحيطية. وبناءً عليه، يتطلب التشخيص الناجح دمجًا بين المعطيات السريرية والفحوص المخبرية النوعية.
التقييم السريري الأولي
يبدأ التشخيص بأخذ التاريخ المرضي الشامل، مع التركيز على العوامل المساعدة مثل: التاريخ الغذائي (ولا سيما النظام النباتي الصارم)، والعمليات الجراحية (استئصال المعدة أو اللفائفي)، وأمراض الجهاز الهضمي (الداء الزلاقي، وداء كرون)، والأدوية المستخدَمة (الميتفورمين، ومثبطات مضخة البروتون)، والأعراض العصبية أو النفسية، مثل ضعف التركيز والاكتئاب واضطرابات المشي. يُرافق ذلك فحص سريري دقيق، قد يكشف عن شحوب الجلد، والتهاب اللسان، واختلال الحس العميق والتوازن، وتراجع المنعكسات أو غيابها (Decreased or absent reflexes) ولا سيما منعكس الكاحل، علاوة على الأعراض النفسية مثل الاكتئاب أو الهذيان[14].
التحاليل المخبرية الأولية
تشمل الفحوص المبدئية: تعداد الدم الكامل (Complete Blood Count, CBC)، الذي يُظهِر غالبًا فقر دم كبير الحجم (Macrocytic anemia)، ويكون متوسط حجم الكرية الحمراء (Mean Corpuscular Volume, MCV) أكبر من 100 فيمتوليتر، مع انخفاض في الهيموغلوبين (Hemoglobin) والهيماتوكريت (Hematocrit)؛ وفحص لطاخة الدم المحيطية (Peripheral blood smear examination)، الذي يُظهر وجود نوى متعدّدة الفصوص في العدلات (Hypersegmented Neutrophils)، وخلايا حمراء بيضاوية كبيرة الحجم؛ علاوة على فحص مستوى ڤيتامين ب12 في المصل، إذ إن تركيز أقل من 200 بيكومول/ لتر يشير إلى نقص في ڤيتامين ب12.
في المقابل، تُعَدّ القيم بين 200 و300 بيكومول/ لتر من ڤيتامين ب12 نتيجة مشكوكًا فيها، ولا يمكن تأكيد النقص أو استبعاده بشكل قاطع. وفي هذه الحالات، يُنصَح بإجراء فحوص إضافية، مثل قياس مستوى حمض الفوليك (ڤيتامين ب9)، لتحديد السبب بدقة، لأن نقص حمض الفوليك أيضًا يسبب فقر دم كبير الحجم (Macrocytic anemia)، ويشترك مع نقص ڤيتامين ب12 في بعض الأعراض والمعطيات المخبرية. يُجرى أيضًا فحص الحديد والفريتين، لتقييم التوازي أو التداخل مع فقر الدم الناجم عن نقص الحديد، ولا سيما في التهابات المعدة المزمنة[15].
الفحوص التأكيدية عند الاشتباه أو الغموض
عند عدم وضوح التشخيص، تُجرى الفحوص التالية: فحص حمض الميثيل مالونيك ((Methylmalonic acid, MMA، الذي يرتفع بشكل نوعي عند نقص ڤيتامين ب12؛ وفحص الهوموسيستئين، إذ يرتفع عند نقص كلٍّ من ڤيتامين ب12 والفولات، لكن ارتفاعه مع حمض الميثيل مالونيك MMA يُرجّح نقص ب12؛ والهولوترانس - كوبالامين (Holotranscobalamin)، الذي يُمثّل الشكل النشط من ڤيتامين ب12 في الدم، وقد يُستخدَم بوصفه مؤشرًا أكثر دقة لحالة الامتصاص[16].
الفحوص المناعية لتشخيص فقر الدم الخبيث
للتمييز بين فقر الدم الخبيث وغيره من أسباب النقص، يُنصَح بإجراء فحوصات لمضادات العامل الداخلي (Anti-IF antibodies)، ومضادات الخلايا الجدارية (Anti-parietal cell antibodies)، بوصفها اختبارات مساعدة في تشخيص فقر الدم الخبيث[17].
علاجه
يعتمد علاج نقص ڤيتامين ب12 على تعويض النقص من خلال إعطاء الڤيتامين، غير أن طبيعة العلاج ومدته وطريقته تختلف تبعًا لسبب النقص، ففي الحالات الناتجة من نظام غذائي نباتي صارم، يُعَدّ التعويض الفموي لڤيتامين ب12 كافيًا وفعّالًا؛ أما في الحالات التي ينقص فيها العامل الداخلي، مثل فقر الدم الخبيث، أو بعد جراحة تحويل مسار المعدة، فيُوصى بإعطاء الڤيتامين عن طريق الحقن العضلي أو الوريدي، إذ لا يُمتَصّ الڤيتامين فمويًا بشكل كافٍ في ظل غياب العامل الداخلي[18].
كذلك يُوصى في هذه الحالات بإعطاء جرعة مقدارها 1000 ميكروغرام من ڤيتامين ب12، عن طريق الحقن العضلي مرة واحدة شهريًا. وعند تشخيص الحالة حديثًا، يُعطى 1000 ميكروغرام عضليًا أسبوعيًا مدة أربعة أسابيع، لتعبِئة المخازن أولًا، ثم يُحوَّل المريض بعد ذلك إلى جرعات شهرية دائمة[19].
أظهرت الدراسات أن تناول جرعات فموية عالية من ڤيتامين ب12، يمكن أن يكون كافيًا لإشباع مستقبلات الامتصاص في الأمعاء، وقد يظل فعّالًا حتى في حالات غياب العامل الداخلي، رغم أن الامتصاص يكون محدودًا. كذلك يُنصَح بمراقبة مستويات ڤيتامين ب12 بشكل دوري لدى الفئات المعرّضة لخطر النقص، مثل مرضى داء كرون والداء الزلاقي، وإذا لُوحِظ انخفاض تدريجي في المستويات، يبدأ العلاج فورًا[20].
مضاعفاته المحتملة
عند التأخّر في تشخيص نقص ڤيتامين ب12 أو عدم معالجته بالشكل المناسب، قد تترتب عليه مضاعفات خطِرة تؤثر في أجهزة متعددة من الجسم، منها: قصور القلب نتيجة فقر الدم المزمن، إذ يؤدي انخفاض الهيموغلوبين إلى إجهاد عضلة القلب، نتيجة زيادة الحمل لتعويض نقص الأكسجين؛ واضطرابات عصبية شديدة قد تكون غير قابلة للعكس، مثل فقدان الإحساس، والاختلال الحركي، والضعف العضلي، والاعتلالات الدماغية. كذلك يزيد النقص من خطر الإصابة بسرطان المعدة، ولا سيما لدى مرضى فقر الدم الخبيث، المرتبط بالتهاب المعدة الضموري المناعي الذاتي، إذ تصبح لديهم قابلية أعلى للإصابة بأمراض مناعية ذاتية، مثل داء السكري من النوع الأول، وداءهاشيموتو {{داءهاشيموتو: (Hashimoto’sdisease) اضطراب مناعي ذاتي يصيب الغدة الدرقية، إذ يُهاجم الجهاز المناعي خلايا الغدة، ما يؤدي إلى التهاب مزمن وضعف في وظيفتها. يُسبّب قصور الغدة الدرقية أعراضًا، مثل التعب، وزيادة الوزن، وبرودة الجلد.}}، والتهاب المفاصل الروماتويدي، والوهن العضلي الشديد (Myasthenia Gravis)، نتيجة الارتباط الوثيق بين فقر الدم الخبيث واضطراب المناعة الذاتية، لذا، فإن الكشف المبكّر والتدخل العلاجي المناسب، أمران حاسمان لتجنّب هذه المضاعفات الخطِرة[21].
المراجع
Allen, Lindsay H. “Causes of Vitamin B12 and Folate Deficiency.”
Food and Nutrition Bulletin. vol. 29, no. 2, supp. l1 (2008). pp. S20-S34.
Ankar, Alex & Anil Kumar. “Vitamin B12 Deficiency.” in:
StatPearls. Treasure Island, FL: StatPearls Publishing, 2025. at: https://www.ncbi.nlm.nih.gov/books/NBK441923/
Jajoo, Sakshi S., Udit M. Zamwar & Prachee Nagrale. “Etiology, Clinical Manifestations, Diagnosis, and Treatment of Cobalamin (Vitamin B12) Deficiency.”
Cureus. vol. 16, no. 1, article no. e52153 (2024).
Kräutler, Bernhard. “Vitamin B12: Chemistry and Biochemistry.”
Biochemical Society Transactions. vol. 33, no. 4 (2005). pp. 806-810.
Shipton, Michael J. & Jecko Thachil. “Vitamin B12 Deficiency – A 21st Century Perspective.”
Clinical Medicine. vol. 15, no. 2 (2015). pp. 145-150.
Vaqar, Sarosh & Karen B. Shackelford. “Pernicious Anemia.” in:
StatPearls. Treasure Island, FL: StatPearls Publishing, 2025. at: https://www.ncbi.nlm.nih.gov/books/NBK540989/
[1] Michael J. Shipton & Jecko Thachil, “Vitamin B12 Deficiency – A 21st Century Perspective,”
Clinical Medicine, vol. 15, no. 2 (2015), pp. 145-150; Bernhard Kräutler, “Vitamin B12: Chemistry and Biochemistry,”
Biochemical Society Transactions, vol. 33, no. 4 (2005), pp. 806-810.
[2] Alex Ankar & Anil Kumar, “Vitamin B12 Deficiency,” in:
StatPearls (Treasure Island, FL: StatPearls Publishing, 2025), accessed on 21/9/2025, at: https://www.ncbi.nlm.nih.gov/books/NBK441923/; Sakshi S. Jajoo, Udit M. Zamwar & Prachee Nagrale, “Etiology, Clinical Manifestations, Diagnosis, and Treatment of Cobalamin (Vitamin B12) Deficiency,”
Cureus, vol. 16, no. 1, article no. e52153 (2024).
[3] Ibid.
[4] Ibid.
[5] Sarosh Vaqar & Karen B. Shackelford, “Pernicious Anemia,” in:
StatPearls (Treasure Island, FL: StatPearls Publishing, 2025), accessed on 21/9/2025, at: https://www.ncbi.nlm.nih.gov/books/NBK540989/
[6] Lindsay H. Allen, “Causes of Vitamin B12 and Folate Deficiency,”
Food and Nutrition Bulletin, vol. 29, no. 2, supp. l1 (2008), pp. S20-S34.
[7] Ibid.
[8] Ibid.
[9] Ibid.
[10] Ibid.
[11] Ibid.
[12] Ibid.
[13] Ibid.
[14] Ibid.
[15] Ibid.
[16] Ibid.
[17] Ibid.
[18] Ibid.
[19] Ibid.
[20] Ibid.
[21] Ibid.