البروتين جزيئات حيوية أساسية كبيرة الحجم ومعقدة التركيب، توجد في الكائنات الحية جميعها، وهي ضرورية لمعظم العمليات البيولوجية لديها، إن لم يكن جميعها، وتتكون من سلاسل طويلة من
الأحماض الأمينية (Amino acids) المرتبطة ببعضها بروابط ببتيدية، لتشكيل سلاسل طويلة تتثنى في هياكل ثلاثية الأبعاد تختلف باختلاف أنواعها، ما يُمكّنها من أداء مجموعة متنوعة من الوظائف. يُحدد التسلسل المحدد للأحماض الأمينية في البروتين هيكله ووظيفته، ويمكن للتغييرات الطفيفة في التسلسل أن تكون لها تأثيرات كبيرة في شكل البروتين وثباته ونشاطه. وتعد بنية البروتين أمرًا بالغ الأهمية لوظيفته، إذ تتيح الهياكل المختلفة وظائف متنوعة. تؤدي البروتينات مجموعة واسعة من الوظائف داخل الكائن الحي، بما في ذلك: تحفيز التفاعلات البيوكيميائية الخلوية (الإنزيمات، Enzymes)، وتوفير الدعم الهيكلي للخلايا (البروتينات، الليفيةFibrous proteins)، ونقل الجزيئات عبر
أغشية الخلايا (النواقل،Transporters)، ومضاعفة
الحمض النووي (البوليميراز،Polymerase)، وتنظيم العمليات الخلوية (البروتينات الناظمة،Regulatory proteins)، وغيرها من الوظائف والعمليات الخلوية. وتشارك البروتينات كذلك في كل جانب من جوانب علم الأحياء تقريبًا، بدءًا من الحفاظ على الوظائف الخلوية الأساسية، وحتى العمليات الفيزيولوجية المعقدة، مثل الاستجابة المناعية، وتقلص العضلات، وكيمياء الدماغ، والإدراك.
تُصنَّع البروتينات من خلال عملية معقدة تتضمن نسخ الجين المشفِّر للبروتين إلى جزيئات
الحمض النووي الريبي المرسال (Messenger RNA, mRNA)، التي تُعدَّل ثم تُستخدَم لترجمة الرسالة (تسلسل وحدات النيوكليوتيدات، Nucleotides) إلى بروتين (تسلسل أحماض أمينية) على
الريبوسوم (Ribosome). وبعد ذلك، يخضع البروتين الناشئ لكثير من التعديلات اللاحقة للترجمة (Post-translational modifications)، للوصول إلى الهيكل الملائم للبروتين النشط. تعد عملية طيّ البروتينات في هياكلها الوظيفية ثلاثية الأبعاد خطوة حاسمة في عملية التكوين، لذا فإن هذه العمليات تحتاج إلى التسهيل بوساطة البروتينات المرافقة (Chaperones)، التي تمنع سوء تشكيل البروتينات الناشئة وتجميعها بصورة خاطئة. بعد التصنيع على
الريبوسوم، تُعدَّل البروتينات في معظم الحالات من خلال عمليات مثل إضافة الفوسفات (الفسفرة)، أو
السكريات (الغلكزة)، أو اليوبيكويتين (الوبكنة)، وغيرها من التعديلات. ويمكن لهذه التعديلات اللاحقة للترجمة أن تغير هيكل البروتين ووظيفته، وهي ضرورية لتنظيم نشاطه وتفاعلاته مع الجزيئات الأخرى في
الخلية.
يُعدّ فهم بنية البروتينات وتركيبها ووظيفتها أمرًا ضروريًّا لفهم كثير من العمليات البيولوجية الأساسية، وكذلك لتطوير علاجات مناسبة للأمراض المختلفة. وقد أدى التقدم التكنولوجي إلى فهم أفضل لبنية البروتين ووظيفته، ومكَّن ذلك الفهم الباحثين من تصميم عقاقير وعلاجات جديدة، تستهدف بروتينات معينة تشارك في العمليات المرضية، فعلى سبيل المثال، أظهرت علاجات السرطان التي تستهدف بروتينات معينة تُشارك في نموّ الورم، نتائجَ واعدةً في التجارب السريرية، كذلك فإن الأدوية التي تستهدف اختلال البروتين المرتبط بالأمراض التنكسية العصبية (Neurodegenerative diseases) مثل مرض ألزهايمر ومرض باركنسون قيد التطوير.
نبذة تاريخية
تعدّ البروتينات مكوّنًا أساسيًّا للحياة، ووظائفها المتنوعة وتركيباتها المعقدة تجعلها موضوعًا مهمًا للدراسة في كثير من المجالات. ومما يُذكَر أن علم
الكيمياء الحيوية (Biochemistry) قد بدأ بدراسة البروتينات؛ ففي القرن الثامن عشر، درس عالم الكيمياء الفرنسي أنطوان فوركروي (Antoine Fourcroy، 1755-1809) الألبومين (Albumin) والغلوتين (Gluten)[1]، قبل أن يكتشف العالم الهولندي خيريت يان مولدر (Gerrit Jan Mulder، 1802-1880) تكوينهما الجزيئي، يُسمّيهما العالم السويدي البارون يونس ياكوب بيرزيليوس (Baron Jöns Jacob Berzelius، 1779-1848) بالبروتين عام 1838[2]. انطلقت دراسة البروتينات مع بدايات القرن التاسع عشر، إذ عرف الكيميائيون أن البروتينات مواد عضوية مميزة. أما تركيبتها وطبيعتها المبلمرة فقد اكتُشِفتا من العالمَيْن فرانز هوفمايستر (Franz Hofmeister، 1850-1922) وإميل فيشر (Emil Fischer، 1852-1919) عام 1902، وقد اقترحا بشكل مستقل أن البروتينات تتكوّن من سلاسل خطية من
الأحماض الأمينية مرتبطة ببعضها عبر روابط ببتيدية[3]. وفي عام 1926، اكتشف الأميركي جيمس سَمْنِر (James Sumner، 1887-1955) أن
إنزيم اليورياز (Urease) هو بروتين نقي، ما أكّد أن من وظائف البروتينات تحفيز التفاعلات الحيوية[4]، وقد حاز على جائزة نوبل في الكيمياء عام 1946 نظير هذا الاكتشاف، الذي نقض الاعتقاد السائد بأن النشاط الإنزيمي يتطلب مكونات غير بروتينية، وأرسى الدور المركزي للبروتينات في التفاعلات البيوكيميائية. تقدّمت دراسة البنية البروتينية بشكل كبير بفضل أبحاث ويليام أستبري (William Astbury، 1898-1961)، التي أشارت إلى وجود أنماط متكررة في تركيب البروتينات، وهي الأبحاث التي بنى عليها الأميركي لينوس باولينغ (Linus Pauling، 1901-1994)، وتنبّأ بشكل صحيح بوجود اللولب ألفا (α-helix) والصفيحة بيتا (β-sheet) عام 1951، مقدّمًا مفهوم البنية الثانوية المدعّمة بروابط هيدروجينية[5].
أما البريطاني فريدريك سانغر (Frederick Sanger، 1918-2013)، فقد نجح في كشف التسلسل الكامل للأحماض الأمينية لهرمون
الإنسولين عام 1949، وهو أول بروتين كُشِف تسلسله، فكان الإنجاز كبيرًا، ما أهّله للحصول على جائزة نوبل في الكيمياء عام 1958، فقد أثبت أن البروتينات هي مبلمرات خطية وليست متفرعة أو حلقية[6]. وأضاف كريستيان أنفينسن (Christian Anfinsen، 1916-1995) الحاصل على جائزة نوبل عام 1972، بسبب أبحاثه عن طيّ البروتينات من خلال تجاربه على
إنزيم ريبونيوكلياز أ (Ribonuclease A) في الستينيات من القرن العشرين؛ فالبروتين عندما يفقد شكله بسبب تأثيرات خارجية، يمكنه أن يعيد طيَّ نفسه تلقائيًّا إلى هيئته الوظيفية بزوال المؤثر الخارجي. وقد أدت هذه التجارب إلى الفرضية الديناميكية الحرارية لطيّ البروتين، التي تنص على أن البنية الطبيعية للبروتين تُمثل حالته ذات الطاقة الحرة الأقل[7].
شكلت هذه الاكتشافات مجتمعةً الإطار العام للكيمياء الحيوية البروتينية الحديثة، وأثّرت في مجالات مثل
البيولوجيا الجزيئية، وتصميم الأدوية، والتكنولوجيا الحيوية، والطب التشخيصي والعلاجي. وقد سمحت التطورات اللاحقة في علم البلورات والأشعة السينية (X-ray crystallography) والرنين المغناطيسي النووي (Nuclear magnetic resonance) والمجهر الإلكتروني فائق البرودة (Cryogenic electron microscope)، بتحليل بنية البروتينات بدقة غير مسبوقة، وما تزال الدراسة المستمرة عن البروتينات ودورها في
الخلية وصحة الإنسان، مجالًا لبحث نَشِط متعدّد الأوجه.
الأحماض الأمينية
[الشكل1]
 التركيب الكيميائي للحمض الأميني
التركيب الكيميائي للحمض الأميني
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
الأحماض الأمينية هي مركبات عضوية تحتوي على مجموعتَيْن وظيفيتَيْن أساسيتَيْن (حمضَي كربوكسيلي وأمين) موجودتَيْن في
الأحماض الأمينية كلها، ومجموعة إضافية متغيرة بحسب
الحمض الأميني. وتحتوي
الأحماض الأمينية جميعها على ذرة كربون مركزية، تُعرَف باسم كربون ألفا، وتكون مرتبطة بأربع مجموعات: مجموعة أمين (-NH2)، ومجموعة حمض الكربوكسيل (-COOH)، وذرة الهيدروجين، وسلسلة جانبية تُعرف أيضًا بمجموعة R (الشكل 1)، وتُشكّل الجزء المختلف بين
الأحماض الأمينية التي تُحدّد خصائصها الكيميائية والفيزيائية[8].
[الشكل2]
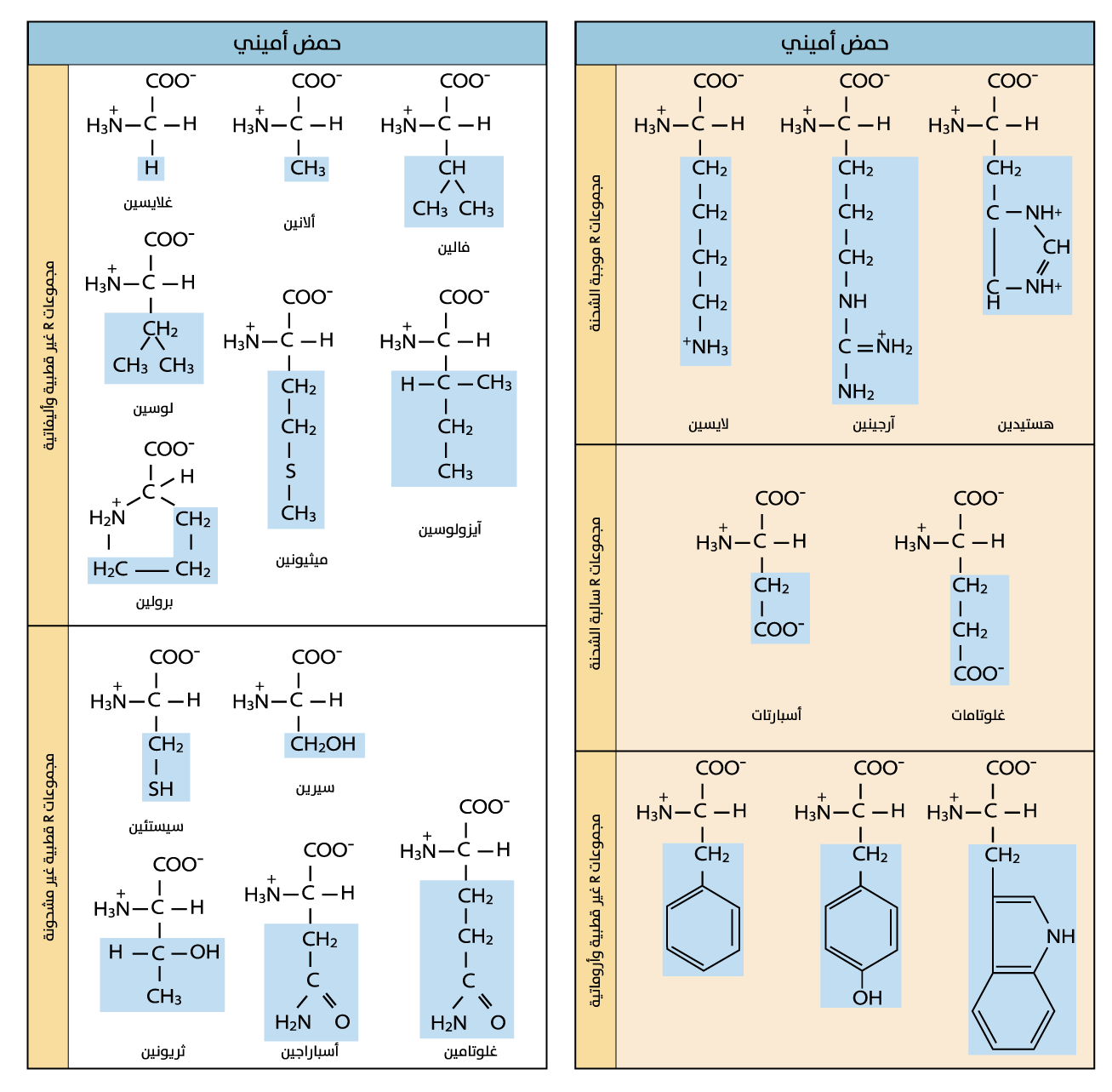 الأحماض الأمينية
الأحماض الأمينية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
إن كلًا من المجموعة الأمينية ومجموعة الكربوكسيل الموجودتين على الكربون ألْفا قطبيتان، ما يعني أنهما تذوبان بسهولة في الماء، ففي الظروف الفيزيولوجية، تكون شحنة المجموعة الأمينية موجبةً بسبب اكتسابها بروتونًا، في حين أن شحنة الكربوكسيل تكون سالبة، فقد فقدت بروتونًا. هذا يجعل
الأحماض الأمينية قابلة للذوبان في الماء، وقادرة على المشاركة في بناء روابط هيدروجينية بين بعضها وبين جزيئات الماء، أما الخصائص الكيميائية للسلسلة الجانبية، فتحدد الخصائصَ العامةَ للحمض الأميني. ومن الممكن أن تكون السلسلة الجانبية قطبية متعادلة الشحنة (في خمسة
أحماض أمينية)، أو قطبية مشحونة (في خمسة
أحماض أمينية)، أو غير قطبية (في 10
أحماض أمينية). ويكمُن سبب الاختلاف الجوهري بين هذه المجموعات المختلفة، في أن السلاسل الجانبية القطبية تحتوي على
مجموعات وظيفية مثل الهيدروكسيل (-OH) أو الأمين (-NH2)، وهي قادرة على تكوين روابط هيدروجينية مع الجزيئات القطبية الأخرى. من ناحية أخرى، تعد السلاسل الجانبية غير القطبية كارهةً للماء، وعند وجودها داخل البروتين تميل إلى أن تكون مدفونة داخله بعيدًا عن الماء. ويمكن أن تكون
الأحماض الأمينية الكارهة للماء أليفاتية (سبعة
أحماض أمينية)، أو أروماتية (ثلاثة
أحماض أمينية)، أما
الأحماض الأمينية المشحونة، فتكون إما قاعدية موجبة الشحنة (في ثلاثة
أحماض أمينية)، وإما حامضية سالبة الشحنة (في اثنين من
الأحماض الأمينية) (الشكل 2)، وتُمكّنها هذه الشحنات من المشاركة في الروابط الأيونية مع الجزيئات المشحونة الأخرى[9].
تحدد خصائص السلاسل الجانبية كيفية تفاعل
الأحماض الأمينية مع بعضها ومع الجزيئات الأخرى في
الخلية. على سبيل المثال، من المرجح أن توجد
الأحماض الأمينية ذات السلاسل الجانبية القطبية المحبة للماء على سطح البروتين، إذ يمكن أن تتفاعل مع الجزيئات القطبية الأخرى، مثل الماء أو البروتينات القطبية الأخرى. ومن المرجح أن توجد
الأحماض الأمينية غير القطبية في الجزء الداخلي من البروتين بعيدًا عن الماء، إذ يمكن أن تشكّل تجاذبات كارهة للماء مع
الأحماض الأمينية غير القطبية الأخرى. كذلك يمكن للأحماض الأمينية المشحونة، المشاركة في التفاعلات الكهروستاتيكية مع الجزيئات المشحونة الأخرى، ما يسهم في التفاعلات بين البروتينات[10].
تتكوّن بروتينات الثديات جميعها في هذه المجموعة من العشرين نوعًا من
الأحماض الأمينية المختلفة، فالشيفرة الوراثية تُحدّد أي
حمض أميني يُضاف، وفي أي مكان. ولا تدخل سوى هذه
الأحماض الأمينية في تركيب البروتين، ولكن مما يلزم ذكره أن ثمة بعض
الأحماض الأمينية الإضافية التي يمكن دمجها استثناءً في بعض البروتينات، مثل سيلينوسيستئين (Selenocysteine)، وهو
حمض أميني يحتوي على عنصر السيلينيوم عوضًا عن الكبريت الموجود في السيستئين. وثمة أيضًا كثير من
الأحماض الأمينية التي لا يمكن دمجها في البروتينات، ولكن لها وظائف مهمة أخرى في استقلاب (Metabolism)
الأحماض الأمينية الأخرى، والمركبات التي تحتوي على النيتروجين في
الخلية، مثل أورنيثين (Ornithine) وسيترولين (Citrulline)[11]. وعلاوة على دورها بوصفها عناصر بناء للبروتينات أو استقلاب لها، فإن للأحماض الأمينية وظائف مهمة أخرى في
الخلية، إذ تشارك بعضها - على سبيل المثال - في تكوين جزيئات مهمة مثل
الناقلات العصبية (Neurotransmitters) والنيوكليوتيدات. كذلك يمكن أن تستخدم
الخليةالأحماض الأمينية بوصفها مصدرًا للطاقة حين تشحّ، إما من خلال عملية استحداث السكر (Gluconeogenesis)، وإما عبر إنتاج مركب أسيتيل مرافق الإنزيم أ (Acetyl coenzyme A) من خلال عملية تكسير
الحمض الأميني[12].
[الشكل3]
 لإنتاج رابطة ببتيدية بين حمضَيْن أمينيَّيْن/___تفاعل-إزالة-الماء.png) تفاعل إزالة الماء (تفاعل التكثيف) لإنتاج رابطة ببتيدية بين حمضَيْن أمينيَّيْن
تفاعل إزالة الماء (تفاعل التكثيف) لإنتاج رابطة ببتيدية بين حمضَيْن أمينيَّيْن
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تعد
الأحماض الأمينية اللبنات الأساسية للبروتينات، وتؤدي هياكلها الفريدة وخصائصها الكيميائية دورًا مهمًا في تحديد بنية البروتينات ووظيفتها. ولتكوين البروتين، تتجمّع
الأحماض الأمينية معًا بطريقة معينة تُحددها الشيفرة الوراثية، في تفاعل تكثيف (Condensation reaction) يؤدي إلى إزالة جزيء الماء، لذا يُسمّى هذا التفاعل التكثيفي تفاعل إزالة الماء (Dehydration reaction). تتكثف
الأحماض الأمينية معًا على سطح
الريبوسوم، لتشكيل رابطة بين نيتروجين المجموعة الأمينية وكربون مجموعة الكربوكسيل لحمض أميني آخر، ويُزال جزيء الماء في العملية (الشكل 3). تُسمّى الرابطة بين
الحمضَيْن الأمينيَّيْن الأول والثاني بالرابطة الببتيدية (Peptide bond)، وهي الرابطة بين الكربون والنيتروجين (O=C – NH)، ويستمرّ هذا التفاعل بإضافة مزيد من
الأحماض الأمينية إلى سلسلة الببتيد المتنامية، لتخليق مُتعدّد الببتيد (Polypeptide) أو البروتين[13].
بنية البروتينات
[الشكل4]
 مستويات أشكال البروتين الأربعة
مستويات أشكال البروتين الأربعة
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
ترتبط وظيفة البروتين كثيرًا ببنيته الهيكلية، إذ إن الأشكال المختلفة للبروتينات تُنتِج بطبيعة الحال بروتينات بوظائف مختلفة. وتُستمَد معرفة بنية البروتين من الهياكل المحلولة والمرفوعة على بنك بيانات البروتين[14] (Protein data bank). ويُعرَف تسلسل
الأحماض الأمينية للبروتينات من قواعد بيانات التسلسلات الموجودة لدى المركز الوطني الأميركي لمعلومات التكنولوجيا الحيوية[15] (NCBI). أما الوظيفة، فتُكتشَف من خلال مجموعة الدراسات البيوكيميائية الحيوية المخبرية[16]. وفي الآونة الأخيرة، وتحديدًا في الربع الأول من القرن الحادي والعشرين، ومع ظهور الذكاء الاصطناعي وتمدّده، وظهور أدوات فائقة التطور مثل برمجية
ألفا فولد[17]، أصبح التنبؤ ببنية البروتينات من خلال فحص تسلسلات
الأحماض الأمينية أسهل بكثير. تركيبيًّا، يمكن تقسيم البروتينات إلى أربعة مستويات من التركيب: الابتدائي (Primary structure)، والثانوي (Secondary structure)، والثلاثي (Tertiary structure)، والرباعي (Quaternary structure) (الشكل 4).
يُوصَف التركيب الابتدائي بأنه الهيكل الأساسي للبروتين القائم على تسلسل
الأحماض الأمينية التي يتكوّن منها البروتين، ويتحدّد التسلسل الدقيق للأحماض الأمينية لأي بروتين بناءً على تسلسل
الحمض النووي للجين الذي يشفّر هذا البروتين، ويرتبط كل
حمض أميني في السلسلة المذكورة بالحمض الأميني الذي يليه بوساطة الرابطة الببتيدية، التي تتكوّن بين المجموعة الأمينية للحمض الأميني الأول ومجموعة الكربوكسيل للحمض الأميني الذي يليه[18]. في المقابل، يشير التركيب الثانوي للبروتين إلى أنماط الطيّ المنتظمة والمتكررة الموجودة في سلسلة البروتين.
[الشكل5]
 لولب ألفا وصفائح بيتا
لولب ألفا وصفائح بيتا
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تختلف أنواع التركيب الثانوي وأشكاله وأعداده باختلاف البروتين، ويُعدّ لولب ألفا (Alpha helix) وصفائح بيتا المُتَثَنِّية (Beta pleated sheets) النوعَيْن الأكثر شيوعًا للهياكل الثانوية. أما لولب ألفا، فهو مقاطع صغيرة في شكل البروتين، تكون ملفوفة بإحكام بشكل لولبي حلزوني، إذ تلتفّ السلسلة حول نفسها على النحو الذي تُكوّن فيه كلُّ دورة كاملة فيها تقريبًا 3.6 أحماض أمينية، وبارتفاع مقداره 0.54 نانومتر. وتُشكّل الروابط الهيدروجينية أساسًا متينًا لهذا الشكل، إذ يكون هناك ارتباط بين
الحمض الأميني الأول والحمض الرابع الذي يليه في السلسلة (والثاني والخامس وهكذا دواليك) بشكل مستمر (الشكل 5)، لذا، فإن عدد الروابط الهيدروجينية يَطّرد مع طول اللولب. أما السلاسل الجانبية، فتخرج عموديًّا من اللولب، بينما تُشكّل صفائح بيتا المتثنية هياكل أكثر امتدادًا من لولب ألفا، إذ تُطوى السلسلة البروتينية ذهابًا وإيابًا على نفسها لتشكيل بنية مسطحة تشبه الصفيحة[19].
يتكوّن البروتين الكامل من مجموعة من التركيبات الثانوية، التي تُشكِّل معًا التركيب الثلاثي الفراغي للبروتين، الذي يشير بدوره إلى الشكل العام ثلاثي الأبعاد للبروتين، ويتحدّد هذا الهيكل من خلال التفاعلات بين السلاسل الجانبية للأحماض الأمينية داخل البروتين. وتؤدي الارتباطات الكارهة للماء بين
الأحماض الأمينية غير القطبية إلى تجمّعها معًا في الجزء الداخلي من البروتين، بينما توجد
الأحماض الأمينية القطبية المشحونة على سطحه، حيث يمكن أن تترابط مع الماء والجزيئات القطبية الأخرى. وتشمل الارتباطات الأخرى التي تسهم في البنية الثلاثية للبروتينات: الرابطة الهيدروجينية، والروابط الكهروستاتيكية، وروابط ثنائي الكبريتيد (Disulfide bonds). وتحتوي البروتينات جميعها
البروتينات غير المرتبة جوهريًّا (Intrinsically disordered proteins) على بنى من المستوى الثلاثي. من جهة أخرى، تحتوي البروتينات التي تتكوّن من أكثر من سلسلة ببتيدية واحدة على مكوّن هيكلي إضافي وهو التركيب الرباعي، لذا، فإن التركيب الرباعي للبروتين يشير إلى الطريقة التي تتجمّع بها سلاسل البروتين المتعددة معًا، لتشكيل شكل بروتيني كبير ذي وظيفة فعّالة، بينما تحدد التفاعلات بين هذه السلاسل الهيكل العام ووظيفة مُجمَّع البروتين[20].
ومع أن البروتين يميل إلى اتخاذ الشكل (أو الأشكال) الذي تكون لديه أقل طاقة حيوية ممكنة، فإن أشكال البروتين قابلة للتعديل، فيمكن أن تخضع البروتينات لتغييرات شكلية استجابةً للمتغيرات في بيئتها، أو بسبب التفاعلات مع جزيئات أخرى، وبإمكان هذه التحولات تغيير بنية البروتين ووظيفته وتعديلهما، وهي ضرورية لكثير من العمليات البيولوجية، مثل تحفيز التفاعلات البيوكيميائية، ونقل الإشارات الخلوية، وتفاعلات البروتينات بعضها مع بعض[21].
[الشكل6]
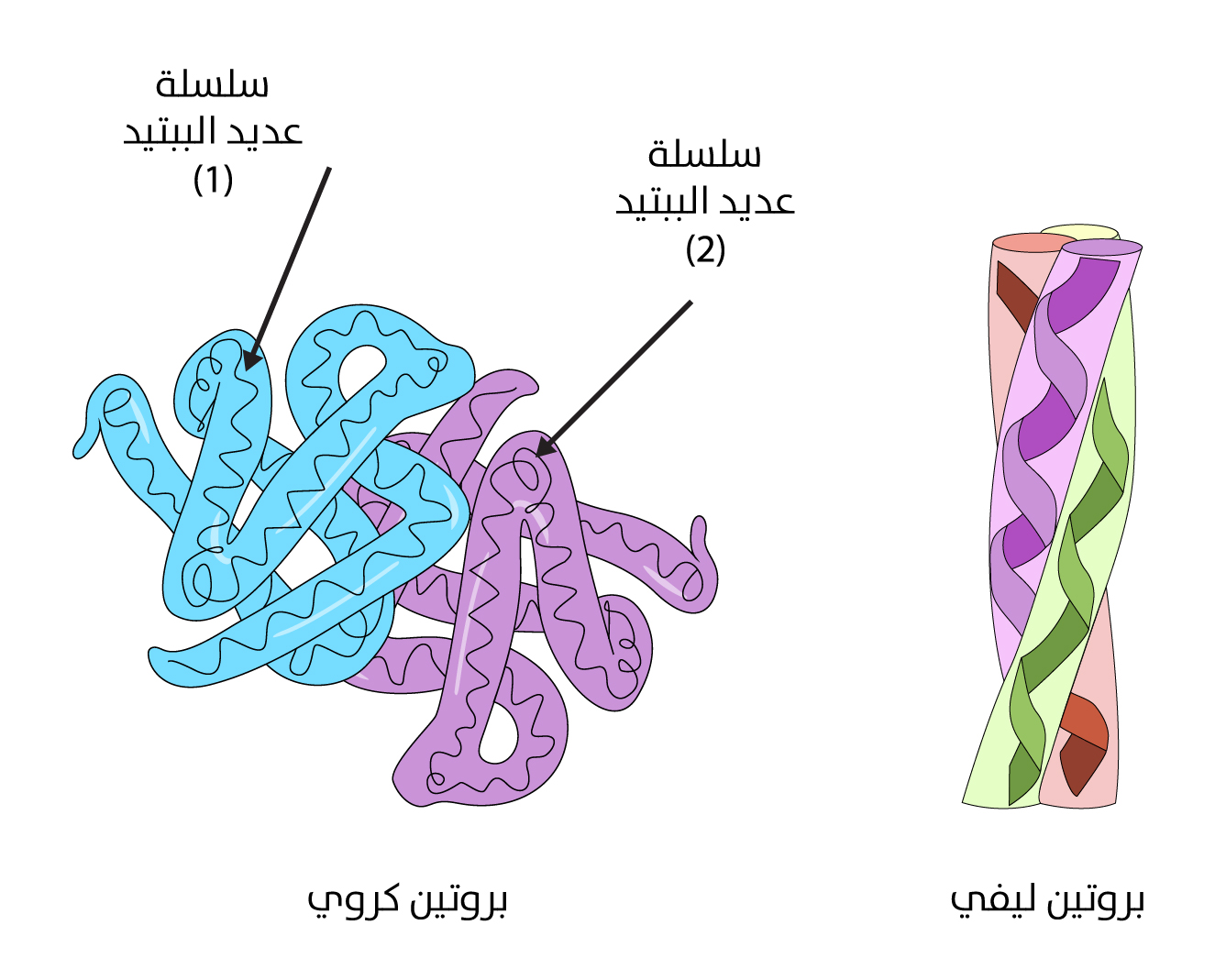 بروتين ليفي وبروتين كروي
بروتين ليفي وبروتين كروي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
[الشكل7]
 مقارنة بين خصائص البروتينات الليفية والبروتينات الكروية
مقارنة بين خصائص البروتينات الليفية والبروتينات الكروية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تُقسّم البروتينات حسب شكلها ثلاثي الأبعاد أساسًا، إلى بروتينات خيطية (Fibrous proteins) وبروتينات كروية (Globular proteins)، وتختلف أشكالها وارتباطاتها ووظائفها. أما الاختلاف الجوهري في البنية بين البروتينات الليفية والبروتينات الكرويّة، فتُحدّده وظائفها المميزة (الشكل 6). عادةً ما تُطوى البروتينات الكروية إلى أشكال كروية مُتراصّة، وغالبًا ما تكون ذات أسطح مُحبّة للماء، ما يجعلها قابلة للذوبان في الماء، ومناسبةً لأدوار ديناميكية مثل التحفيز الإنزيمي والنقل والإشارات والتنظيم. في المقابل، تحافظ البروتينات الليفية على شكلها المُستطيل الشبيه بالخيوط، وهو شكل مُحسّن لتكوين ألياف طويلة ومترابطة وقوية ومرنة، تعمل بوصفها دعامات هيكلية للخلايا، وهذا التحسين الهيكلي للأدوار الميكانيكية يعني أنها تُضحي بقابلية الذوبان في الماء من أجل الاستقرار وقوة الشدّ. تُؤدي تسلسلات
الأحماض الأمينية المتكررة في البروتينات الليفية إلى تجمعات جزيئية عالية التنظيم والاستقرار، وهي ضرورية للحفاظ على الشكل والمرونة والقوة لشدّ أنسجة مثل الجلد والأوتار والعظام والشعر، وهذا الاختلاف الهيكلي يجعلها فريدة من نوعها من حيث إسهاماتها البيولوجية[22].
ثمة تباين بصري بين الخصائص الرئيسة للبروتينات الليفية والبروتينات الكروية، ويُبرِز تفوق البروتينات الليفية في مجالات مثل القوة الميكانيكية، والاستقرار الهيكلي، ومقاومة الشد، مع انخفاض قابليتها للذوبان في الماء. في المقابل، تتميز البروتينات الكروية بقابليتها للذوبان في الماء بشكل كبير، لكنها تفتقر إلى مستوى الصلابة الهيكلية نفسه (الشكل 7).
البروتينات الليفية
البروتينات الليفية، وتُسمّى أيضًا البروتينات الخيطية، فئة متخصصة من البروتينات، تتميز بتكويناتها الخيطية الطويلة ومرونتها الميكانيكية. وهذه البروتينات غنية بهياكل ثانوية متكررة، فعلى سبيل المثال، ثمة تكرار للولب ألفا في بروتين ألفا-كيراتين (a-keratin)، وتكرار آخر لصفائح بيتا في بروتين فيبروين الحرير (Silk fibroin)، وهذه الخيوط تتبلمر لتشكّل أليافًا عالية القوة الشدّية[23]. وهذه البروتينات غنية أيضًا بالأحماض الأمينية الكارهة للماء الموجودة حتى على سطح البروتين، وتمتاز بوجود كثير من
الروابط التساهمية المقطعية داخلها (مثل روابط ثنائي الكبريتيد في الكيراتين، أو روابط لايسين- هيدروكسي لايسين في بروتين الكولاجين (Collagen)[24]، ما يجعلها غير قابلة للذوبان في الماء، وملائمة لتصبح لها أدوار هيكلية في الخلية[25]. وبخلاف البروتينات الكروية، تفتقر البروتينات الليفية إلى الطيّ المضغوط في أشكال كروية، بل تُشكّل بدلًا من ذلك مصفوفات ممتدة تقاوم قوى الشد[26].
تُعرَف البروتينات الليفية بأنها العناصر الهيكلية الأساسية في الكائنات متعددة
الخلايا، إذ تسهم في سلامة الأنسجة ووظائفها الحيوية. ويُشكّل الكولاجين، وهو البروتين الحيواني الأكثر وفرةً، لُيَيْفات تُعزز الأنسجة الضامّة، بينما يُوفر بروتين الإيلاستين (Elastin) مرونة للأوعية الدموية والجلد. وفي الهيكل الخلوي، تحافظ خيوط الأكتين (الخييطيات، Microfilaments) والخيوط المتوسطة (Intermediate filaments) (مثل بروتين ڨيمنتين Vimentin) على شكل
الخلية، وتُمكِّن من الحركة[27].
تُصنَّف البروتينات الليفية حسب بنيتها الثانوية وتنظيمها فوق الجزيئي، وتُشكّل بروتينات ألفا الحلزونية، مثل الكيراتين والميوسين (Myosin) ثنائيات لولبية (Coiled-coils) مُثبّتة بتفاعلات كارهة للماء، بينما يُحقق لولب الكولاجين الثلاثي (Collagen triple helix) قوة كبيرة، ويحتوي الكولاجين على تكرار من
الأحماض الأمينية الثلاثية غلايسين-برولين-هيدروكسي برولين (Gly-X-Y)، ويكون شكله الثلاثي مليئًا بالروابط التساهمية القوية بين اللايسين والهيدروكسي لايسين، ما يمنحه استقرارًا غير عادي[28]. يستعرض الجدول الآتي أهم السمات المميزة والوظائف البيولوجية لبعض البروتينات الليفية البارزة.
الصفة
| كولاجين
| كيراتين | إيلاستين |
|---|
الشكل الابتدائي | غني بالغلايسين والبرولين والهيدروكسي برولين | غني بالسيتئين (وروابط ثنائي الكبريتيد) | غني بالغلايسين والبرولين واللايسين والهيدروكسي لايسين والروابط التساهمية بين الألياف |
الشكل الثانوي | لولب ثلاثي مكون من 3 خيوط من الكولاجين ملتفة على بعضها | لولبا ألفا ملتفان على بعضهما في ثنائيات لولبية | صفائح بيتا وعدد من المناطق غير المرتبة جوهريًّا |
الشكل ثلاثي الأبعاد | خيط طويل قوي يشبه الحبال | خيط طويل ملتف وغير ذائب في الماء | ألياف مرنة ملتفة بعشوائية |
الذائبية في الماء | شبه منعدمة |
الوظيفة الأساسية | قوة شد عالية وبنية قوية لحماية الأوتار والعظام | حاجز وقائي ذو صلابة عالية في الأظفار والحوافر والشعر | مرونة وارتداد يسمحان بتدفق دم سلس في الأوعية الدموية |
أمثلة على أماكن وجوده | الأوتار، الأربطة، العظام، الجلد، الغضاريف | الشعر، الأظفار، الطبقة الخارجية للجلد، الصوف، القرون | الجلد، الأوعية الدموية، الرئتان، الأربطة |
البروتينات الكروية
البروتينات الكروية فئة متنوعة من البروتينات القابلة للذوبان في الماء، تتميز ببنيتها الثلاثية الكروية المضغوطة. وعلى عكس البروتينات الليفية، فإنها تتثنّى في أشكال مضغوطة، فيها أسطح محبّة للماء، وداخلها كاره للماء، ما يُمكّنها من الذوبان في البيئات المائية. وتستقر بنيتها بفضل مزيج من الروابط الهيدروجينية والتفاعلات الأيونية وروابط ثنائي الكبريتيد، وغالبًا ما تتميز ببنًى ثانوية مختلطة بعكس البروتينات الليفية، ما يُضفي عليها تنوعًا وظيفيًّا[29]. ومن الأمثلة على ذلك:
الإنزيمات، والأجسام المضادة، وبروتينات النقل، التي تعتمد جميعها على الطي الدقيق في أشكال كروية لنشاطها البيولوجي[30].
تشارك البروتينات الكروية في العمليات الخلوية جميعها تقريبًا، من التحفيز إلى الإشارة، وتُسرِّع
إنزيمات مثل الهيكسوكيناز (Hexokinase) التفاعلات الاستقلابية عبر مواقع نشطة مُحددة بدقة في شكل البروتين، في حين أن البروتينات المناعية تتعرّف إلى مُسببات الأمراض بدقة عالية بسبب شكلها الكروي. كذلك تسمح بنية بعض البروتينات الكروية المتحركة بالتنظيم التفارغي (Allosteric regulation)، فعلى سبيل المثال، عند ارتباط جزيء أكسجين بمكان على بروتين الهيموغلوبين، يتغير شكل الهيموغلوبين قليلًا لتحفيز ارتباط جزيء أكسجين آخر[31]. ويخضع طيّ البروتينات الكروية لمبدأ الديناميكا الحرارية، المتمثل في اكتساب البروتين الشكل الذي يأخذ الحد الأدنى من الطاقة الحرة، والذي غالبًا ما يتطلب وجود بروتينات مساندة، مثل بروتين الصدمة الحرارية 70 (HSP70) لمنع تكتل البروتين عند طيّه[32]. ويعتمد ثبات البروتينات الكروية واستقرارها في
الخلية على الرقم الهيدروجيني، ودرجة الحرارة، ووجود عوامل بيوكيميائية أخرى تُعطّل فقدان شكلها ووظيفتها. وتتنبَّأ الأدوات الحاسوبية الحديثة والذكاء الاصطناعي مثل برمجية
ألفا فولد الآن، بالهياكل الكروية بدقة ذرية[33].
[الشكل8]
 تصنيف البروتينات في الإنسان حسب وظائفها
تصنيف البروتينات في الإنسان حسب وظائفها
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
وظائفها
تتنوع البروتينات بشكل كبير في تركيبها، ومن ثم فهي تؤدي مجموعة واسعة من الوظائف المختلفة في
الخلية، إذ تتوسط الحياةَ الخلوية بوصفها جزيئات تؤدي معظم العمل في
الخلية، وتشمل هذه الوظائف: الارتباط مع الجزيئات الحيوية الأخرى، وتحفيز التفاعلات البيوكيميائية، ونقل الجزيئات عبر
أغشية الخلايا، وتوفير الدعم الهيكلي، ونقل الإشارات، وتنظيم التكشّف الجيني، وغير ذلك من الوظائف الخلوية المهمة الأخرى (الشكل 8)[34].
التحفيز
يُعدّ التحفيز الكيميائي من أهم وظائف البروتينات، ويتمّ عن طريق
الإنزيمات. وعمومًا، فإن
الإنزيمات هي بروتينات متخصصة، مع بعض الاستثناءات النادرة، قادرة على تسريع التفاعلات الكيميائية الحيوية في
الخلية بشكل هائل، إذ إن كثيرًا من التفاعلات البيوكيميائية الخلوية لا يمكن أن تحدث من دونها، فالإنزيمات مسؤولة عن التفاعلات الأيضية كلها في
الخلية، بما في ذلك تكسير جزيئات الطعام، وتكوين جزيئات معقدة جديدة، وتحويل الطاقة من صورة إلى أخرى. وتعمل
الإنزيمات من خلال الارتباط بجزيئات معينة، ثم تُغيِّر تركيبها الكيميائي بطريقة تسمح بحدوث التفاعل بسرعة أكبر، وتتراوح أمثلتها من اليورياز الذي يُكسِّر جزيء اليوريا، إلى الهيكسوكيناز الذي يُفسْفِر
الغلوكوز، وصولًا إلى بوليميراز الحمض النووي (DNA polymerase) الذي يُصنِّع
الحمض النووي الريبي منقوص الأكسجين.
توجد سبع فئات يمكن أن يوضع فيها كل
إنزيم معروف[35]. توجد
الإنزيمات التي تحفز تفاعلات الأكسدة والاختزال في الفئة الأولى، وهي الأوكسيدوردكتاز (Oxidoreductase)؛ أما
الإنزيمات التي تنقل المجموعات الوظيفية بين الجزيئات فتشكِّل الفئة الثانية، الترانسفيراز (Transferase)؛ ونجد في الفئة الثالثة الهيدرولاز (Hydrolase)، وهي
إنزيمات تسرِّع التفاعلات التي تكسِّر الروابط الكيميائية باستخدام جزيئات الماء؛ أما المجموعة الرابعة، وهي اللاياز (Lyase)، فتتضمّن تفاعلات تكوين
الروابط التساهمية المزدوجة أو تكسيرها؛ وتشكِّل الآيزوميراز (Isomerase) المجموعة الخامسة من
الإنزيمات المهيِّئة لتحفيز التغييرات داخل الجزيئات لتكوين آيزومرات مختلفة من الجزيء المتفاعل؛ وفي المجموعة السادسة، يتكوّن الليغاز (ligase) من
إنزيمات تُكوِّن
الروابط الكربونية التساهمية باستخدام الطاقة من تحليل الـنيوكليوسيد ثلاثي الفوسفات (NTP)؛ وأخيرًا، تأتي المجموعة السابعة المُكوَّنة من الترانسلوكاز (translocase)، وهي بروتينات ناقلة تساعد الجزيئات في عبور
الأغشية البيولوجية.
قائمة بفئات الإنزيمات
|
|---|
الفئة
| اسم عائلة الإنزيم المنقحرة
| اسم عائلة الإنزيم باللغة العربية | التفاعل الذي تحفزه |
1 | أوكسيدوردكتاز | إنزيمات الأكسدة والاختزال | نقل إلكترونات (أكسدة واختزال) |
2 | ترانسفيراز | إنزيمات النقل
| نقل المجموعات الوظيفية |
3 | هيدرولاز | إنزيمات التحلل المائي | تكسير الروابط الكيميائية بوساطة الماء |
4 | لاياز | إنزيمات الفصل | نزع مجموعة وظيفية دون استخدام الماء وإنشاء رابطة مزدوجة |
5 | آيزوميراز | إنزيمات التشكُّل | التحويل بين المتصاوغات (الآيزوميرات) |
6 | ليغاز | إنزيمات الربط | إنشاء رابطة جديدة بين مركبين باستخدام طاقة الـATP |
7 | ترانسلوكاز | إنزيمات النقل عبر الغشاء | نقل المركبات والجزيئات عبر الأغشية الحيوية |
النقل
تُمثّل المجموعة السابعة المذكورة أعلاه، البروتينات التي تشارك في نقل الجزيئات عبر
أغشية الخلايا، وتشمل هذه الناقلات القنوات (Channels) والمضخات (Pumps) التي تنقل الجزيئات عبر
الغشاء، استجابةً لتدرجات
التركيز أو الشحنة الكهربائية. وتتضمن أمثلة الناقلات: مضخة الصوديوم والبوتاسيوم (sodium potassium pump) التي تحافظ على
تركيز الأيونات في
الخلية؛ وناقل الغلوكوز (GLUT) الذي يسمح للغلوكوز بالدخول إلى الخلايا.
وثمة أيضًا بروتينات تنقل الجزيئات في الدم أو داخل
الخلايا، فالهيموغلوبين (Hemoglobin) بروتين ينقل الأكسجين من الرئتين إلى أنسجة الجسم عبر الدورة الدموية؛ والترانسفيرين (Transferrin) هو البروتين الناقل لأيونات الحديد في الدم؛ بينما ينقل الألبومين (Albumin)
الأحماض الدهنية؛ أما الغلوبيولين المرتبط بالهرمونات الجنسية (Sex hormone-binding globulin)، فينقل هذه الهرمونات من أماكن تصنيعها إلى أماكن عملها في الجسم، وتعد قائمة الأمثلة على البروتينات الناقلة طويلة. أما داخل
الخلايا، فتساعد البروتينات الحركية في نقل
الحويصلات (Vesicles) من
الشبكة الإندوبلازمية (Endoplasmic reticulum) وإليها، عبر نظام الغشاء الداخلي (Endomembrane system). وتُعد بروتينات أخرى مثل كينيسين (Kinesin) وداينين (Dynein)، ناقلات خلوية مهمة للحويصلات من داخل
الخلية إلى خارجها وبالعكس[36].
الدعم الهيكلي
تشارك البروتينات أيضًا في توفير الدعم الهيكلي للخلايا والأنسجة. وتشمل البروتيناتُ الهيكلية الكولاجين الذي يُشكِّل النسيج الضامّ في الجسم؛ والأكتين (Actin) والميوسين (Myosin) المسؤولَيْن عن انقباض العضلات. وتشمل الأمثلة الأخرى للبروتينات الهيكلية: الكيراتين (keratin) الموجود في الشعر والأظفار؛ والإيلاستين (Elastin) الذي يسمح للأنسجة بالتمدد والارتداد؛ أما الإنتغرينات (Integrins) فهي المستقبِلات الرئيسة التي تستخدمها
الخلايا الحيوانية لربطها بالمصفوفة خارج الخلية (Extracellular matrix). وتعمل هذه البروتينات الهيكلية بوصفها وصلات بين
المصفوفة خارج الخلية والهيكل الخلوي الأكتيني[37]. ويُذكَر أيضًا وجود كثير من البروتينات المختلفة المشاركة في بنية
الخلايا.
التصاق الخلية والتواصل بين الخلايا
تشارك البروتينات في التصاق
الخلايا والتواصل بينها، وتؤدي دورًا مهمًا في تكوين الأنسجة والأعضاء وصيانتها. وتتوسّط البروتينات مثل الإنتغرينات والكادهيرينات (Cadherins) في التصاق الخلية بالخلايا المجاورة، في حين أن بروتينات أخرى مثل عوامل النمو (Growth factors) والسيتوكينات (Cytokines)، تُمكّن
الخلايا من التواصل والاستجابة بينها[38].
التنظيم الفيزيولوجي ونقل الإشارة الحيوية
تشارك البروتينات أيضًا في تنظيم العمليات الفيزيولوجية في الخلية، وتُعد الهرمونات مثل
الإنسولين وهرمون النمو (Growth hormone) بروتينات تُطلَق في مجرى الدم من مكان إنتاجها، لترتبط بـمستقبلات معينة في
الخلايا البعيدة، ما يؤدي إلى استجابة معينة. فالإنسولين على سبيل المثال، يُنظِّم امتصاص
الغلوكوز واستقلابه، في حين أن
هرمون النمو يُحفّز نمو
الخلايا وإصلاحها، لتستقبل بدورها الإشارات من بيئتها وتستجيب لها عبر نقل الإشارة الخلوية. وتُعد بروتينات الإشارات، مثل المستقبِلات والكينازات (Kinases)، مسؤولة عن نقل الإشارات من خارج بيئة
الخلية إلى داخلها، ما يؤدي إلى استجابات معينة. وتتضمن أمثلة بروتينات الإشارة: مستقبلات الغلوكاغون (Glucagon) الذي يؤدي إلى رفع نسبة
الغلوكوز في الدم، عكس تأثير
الإنسولين؛ وسلسلة ماب كيناز (MAP kinase)، التي تشارك في نمو
الخلايا وتمايزها[39].
الاستشعار والاستجابة للمنبهات
للبروتينات أيضًا وظائف في الاستشعار والاستجابة لمحفزات معينة، مثل الضوء والحرارة والضغط الميكانيكي، فمثلًا، يوجد بروتين رودوبسين (Rhodopsin) في شبكيّة العين، وهو مسؤول عن الاستجابة للضوء وبدء عملية الرؤية. من ناحية أخرى، تستجيب بروتينات الصدمة الحرارية (Heat shock proteins) لارتفاع درجات الحرارة، وتُسهم في حماية
الخلايا من التلف[40].
جهاز المناعة
تُعد
الأجسام المضادة - وهي بروتينات متخصصة - التي تفرزها
الخلايا اللمفية البائية استجابةً لغزو خارجي من عوامل مُمْرِضة مثل
الفيروسات والبكتيريا، ضروريةً لجهاز المناعة، إذ ترتبط هذه
الأجسام بهذه الجزيئات الخارجية وتميّزها للتدمير بوساطة جهاز المناعة. وتشمل البروتينات الأخرى المشاركة في الجهاز المناعي:
السيتوكينات (Cytokines)، وهي
جزيئات إشارة تُنسّق الاستجابة المناعية؛ والبروتينات المكمّلة (Complement proteins) التي تساعد في تدمير المواد الغريبة[41].
التكشّف الجيني
تُنظِّم البروتينات عملية التعبير الجيني، وفي هذا السياق، تُعد عوامل النسخ بروتينات ترتبط بالحمض النووي، وتنظّم نسخ
الجينات إلى
الحمض النووي الريبي، ومن ثم تسهم في عملية تحويل الرسالة من
الجين إلى البروتين. وتؤدي هذه البروتينات دورًا مهمًا في تحديد
الجينات التي تُشغَّل أو يُوقَف تشغيلها في خلية معينة، وتشارك في كثير من العمليات الفيزيولوجية، بما في ذلك التطور والتمايز والاستجابة للإجهاد[42].
التخزين
يمكن أن تعمل البروتينات أيضًا بوصفها آلية تخزين للجزيئات الأساسية، مثل
الأحماض الأمينية، والمعادن، والأيونات، والغلوكوز، وغيرها، فعلى سبيل المثال، يُخزّن بروتين فيريتين (Ferritin) الحديد، ويُخزّن الكازين (Casein) أيونات الكالسيوم في الحليب. علاوة على ذلك، فإن بعض البروتينات الموجودة في بذور النباتات كالبقوليات، تُخزِّن
الأحماض الأمينية التي تُستخدَم من أجل النمو عند إنبات البذور[43].
الحركة
تتحكم البروتينات أيضًا في الحركتَيْن الخلوية والعضوية، إذ تستخدِم الطلائعياتُ وحيدةُ
الخليةِ وبعضُ
الخلايا الحيوانية الأهدابَ أو الأسواطَ للحركة، لذا فإن الأهداب والأسواط مسؤولة عن الحركة الخلوية. تتكوّن الأهداب والأسواط من الأنيبيبات (Microtubules) والبروتينات الحركية مثل الداينين والكينيسين، في حين أن الميوسين والأكتين والبروتينات الأخرى تشارك في انقباض العضلات، ما يُمكّن الكائنات الحية من الحركة وأداء الأنشطة البدنية[44].
تنظيم التمثيل الغذائي والاستقلاب
توجد البروتينات المنظِّمة في
المسارات الأيضية الخلوية كلها، وتتحكّم في بدئها واستمرارها، ومن الأمثلة على ذلك تنظيم
استقلابالغلوكوز والدهون، فالهرمونات مثل
الإنسولين والغلوكاغون واللبتين (leptin)، هي بروتينات ناظمة لعمليات أيض
الغلوكوز والدهون، ولها أدوار حيوية في الحفاظ على
التوازن الخلوي (Homeostasis)[45].
إصلاح الحمض النووي
تشارك البروتينات في إصلاح
الحمض النووي التالف لمنع
الطفرات وحصول الأمراض مثل السرطان، وتُعدّ
الإنزيمات مثل بوليميراز الحمض النووي، وليغاز الحمض النووي، وإندونيوكلياز (Endonuclease)، وإكزونيوكلياز (Exonuclease)، مسؤولةً عن إصلاح الحمض النووي التالف، بينما تؤدي البروتينات مثل بي 53 (p53) دورًا مهمًا في مراقبة سلامة
الحمض النووي، وبدء عملية الإصلاح عند اكتشاف خلل ما[46].
الهضم
تتطلب التغذيةُ القائمةُ على نظام غذائي بروتيني وجودَ
إنزيمات تُحلل البروتين، على النحو الذي تتكسَّر فيه البروتينات المبْتَلَعَة إلى
الأحماض الأمينية المكوّنة لها ليجري امتصاصها بعد ذلك، لاستخدامها في النمو والإصلاح في
الخلايا. إن
الإنزيمات مثل البيبسين (Pepsin)، والتريبسين (Trypsin)، والكيموتريبسين (Chymotrypsin)، والأمينوببتيداز (Aminopeptidase)، والكاربوكسيببتيداز (Carboxypeptidase)، مسؤولة عن تكسير البروتينات إلى ببتيدات وأحماض أمينية أصغر، ويُعدّ هذا التكسير شرطًا لامتصاص
الأحماض الأمينية في خلايا الأمعاء[47].
إنتاج الطاقة
تُستخدَم البروتينات مصدرًا للطاقة، إذ يمكن تكسيرها إلى
الأحماض الأمينية المكوّنة لها واستخدامها وقودًا في
الخلايا في حالات معينة، ففي أوقات الجوع أو في حالة
مرض السكري غير المعالَج على سبيل المثال، يُفكِّك الجسم بعض الأنسجة العضلية، ويستخدم
الأحماض الأمينية لإنتاج الطاقة[48].
تكوينها وإنتاجها
تُعرَف العملية التي تُستخدَم من خلالها المعلومات الجينية المخزّنة في
الحمض النووي لإنتاج البروتينات، باسم تخليق البروتين (Protein synthesis)، وتعني تكوين البروتين داخل
الخلية، بحسب الجين الذي يشفّره. وتحدث هذه العملية على مرحلتَيْن رئيستَيْن: النسخ (Transcription)، والترجمة (Translation)[49]. في المرحلة الأولى، مرحلة النسخ، يُنسَخ جزء من
الحمض النووي الذي يحتوي على الشفرة الجينية لبروتين معيّن، إلى جزيء من
الحمض النووي الريبي المرسال (mRNA)، ويُفَكّ اللولب المزدوج للحمض النووي (DNA double helix) في أثناء النسخ، مع استخدام أحد الخيطَيْن المُكوّنَيْن له قالبًا لتصنيع جزيء
الحمض النووي الريبي المرسال. وتُنفّذ هذه العملية بوساطة
إنزيم يُسمى RNA بوليميراز، وهو يقرأ الـحمض النووي ويصنع شريطًا مكمِّلًا من
الحمض النووي الريبي المرسال. وعند الانتهاء من النسخ، يُعدّل جزيء الحمض النووي الريبي بإضافة قبعة 5’ (5’ cap) وذيل عديد الأدينين (Poly A tail)، ما يُساعد على استقرار الجزيء المرسال وحمايته من التكسير. وبمجرد تصنيع الجزيء، ينتقل عن طريق الثقوب النووية إلى
السيتوبلازم، حيث تحدث المرحلة الأخرى من تخليق البروتين، مرحلة الترجمة[50].
[الشكل9]
 الشفرة الوراثية
الشفرة الوراثية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
في أثناء الترجمة، تقرأ
الريبوسومات جُزيء
الحمض النووي الريبي المرسال وعندما يتحرك
الريبوسوم على طول جزيء ذلك
الحمض، فإنه يقرأ الشفرة الجينية في مجموعات من ثلاثة نيوكليوتيدات، تُعرَف باسم الكودون (Codon). يُحدِّد كلُّ كودون
حمضًا أمينيًّا مُعينًا (الشكل 9) من أجل تجميع البروتين، وينقل الحمضُ النووي الريبي الناقِل (tRNA)
الأحماض الأمينية المناسبة إلى
الريبوسوم، إذ تُربَط معًا لتشكيل سلسلة ببتيدية، عن طريق تصنيع روابط ببتيدية بين
الأحماض الأمينية المتتالية، ثم يستمر
الريبوسوم على طول جزيء
الحمض النووي الريبي المرسال، بإضافة
الأحماض الأمينية إلى السلسلة النامية، حتى يصل إلى شفرة التوقف، وعند هذه النقطة، يُطلَق البروتين المركّب حديثًا من
الريبوسوم، ويُطوى في هيكله النهائي ثلاثي الأبعاد، وهو أمر بالغ الأهمية لوظيفته المناسبة[51].
تُنظَّم عملية تكوين البروتين على عدّة مستويات، بدءًا من النسخ ووصولًا إلى الطي النهائي للبروتين، ومع ذلك، فهي عملية لا تخلو من الأخطاء، إذ يمكن أن تحدث الأخطاء في مراحل مختلفة من تكوين البروتين، ما قد يؤدي إلى إنتاج بروتينات غير وظيفية أو ضارّة. ويُعدّ فهم عملية تكوين البروتين أمرًا بالغ الأهمية لمجموعة واسعة من المجالات الحيوية المختلفة، مثل
الأحياء الجزيئية، والتكنولوجيا الحيوية، والطب، والصيدلة. ومما يُذكر، أن الأبحاث العلمية في مجالات الكيمياء الحيوية تعتمد كثيرًا على هذه العملية، إذ إنه بالإمكان التلاعب بالشفرة الجينية وعملية الترجمة، لإنتاج بروتينات ذات خصائص ووظائف محددة لغرض البحث العلمي، ولفتح مجالات جديدة لتطوير الأدوية وتطبيقات التكنولوجيا الحيوية.
تعديلات بعد الترجمة
بعد تصنيع سلسلة البروتين، يخضع البروتين عادةً لمزيد من التعديلات، ليصبح بروتينًا نشطًا وظيفيًّا[52].
الطيّ
طيّ البروتين (Protein folding) هو عملية تخضع فيها السلسلة الببتيدية المركَّبة حديثًا لمجموعة من التغييرات الهيكلية، التي تؤدي إلى تشكيل هيكلها النهائي ثلاثي الأبعاد. ويُعدّ الطي المناسب للبروتين أمرًا بالغ الأهمية لكي يؤدي وظيفته، وأي خطأ أو اضطراب في هذه العملية يمكن أن يؤدي إلى مرض أو أعطال خلوية وظيفية. عمومًا، يمكن أن يحدث طيّ البروتين تلقائيًّا من خلال ارتباطات وتفاعلات كثيرة معقَّدة بين الخصائص الفيزيائية والكيميائية للبروتين والبيئة المحيطة به، وتجري عملية الطي باستخدام كثير من القوى الفيزيائية، مثل: الروابط الهيدروجينية، وروابط فان دير فال، والارتباطات الكارهة للماء، والتفاعلات الكهروستاتيكية، وغيرها. ومع أن العملية في المجمل يمكن أن تكون شبه تلقائية، فثمة بروتينات مُسانِدة يمكن استعمالها لمساعدة البروتينات الأخرى على الطيّ بشكل صحيح، مثل بروتينات الصدمة الحرارية والشابيرونين (Chaperonin).
يمكن تقسيم عملية طيّ البروتين إلى عدة مراحل، تتضمن المرحلة الأولى تكوين عناصر بنيوية ثانوية، مثل لولب ألفا وصفائح بيتا المُتثَنِّية، أي تلك التي تُثبَّت عن طريق عدة روابط هيدروجينية بين ذرات العمود الفقري للسلسلة الببتيدية. وتتضمّن المرحلة التالية تكوين الشكل الثلاثي، عبر طيّ البروتين ليأخذ شكله النهائي ثلاثي الأبعاد، وتُحفَّز العمليات في هذه المرحلة بوساطة مزيج من الارتباطات الكارهة للماء، التي تجمع
الأحماض الأمينية غير القطبية معًا لتشكيل قلبٍ بروتينيٍّ كارهٍ للماء؛ والتفاعلات الكهروستاتيكية، التي تسعى إلى استقرار الهيكل المطوي النهائي. وفي بعض الحالات، قد تخضع البروتينات أيضًا لمرحلة نهائية من الطي تُعرَف بالبنية الرباعية، إذ تتجمّع وحدات فرعية بروتينية متعددة في مجمّع بروتيني أكبر، منتجةً البروتين الفعّال[53].
أخطاء في الطيّ
يُعدّ طي البروتين عملية معقدة، وليست دائمًا مباشرة وبسيطة، وبناء على ذلك، يمكن أن تتأثر بمجموعة متنوعة من العوامل، فعلى سبيل المثال، يمكن أن يتداخل وجود بروتينات أو مركبات كيميائية أخرى في
الخلية مع عملية الطيّ، ويؤدي ذلك إلى بروتينات غير مطوية أو مطوية بشكل خاطئ[54].
الأمراض الناتجة من الخطأ في الطي
يُعدّ اختلال البروتين آلية أساسية شائعة في كثير من الأمراض، ويمكن أن يؤدي تراكم البروتينات المشوهة إلى تعطيل الوظيفة الخلوية الطبيعية، والإسهام في نشوء مجموعة واسعة من الأعراض والأمراض. يحدث الاختلال في تشكيل البروتين وطيّه، عندما تفشل البروتينات في الانطواء في هياكلها الأصلية ثلاثية الأبعاد، ما يؤدي إلى تكوين بروتينات مشوّهة، ويمكن أن يحدث هذا بسبب مجموعة من العوامل، بما في ذلك
الطفرات الجينية، والاعتلالات في البيئة، والتغيرات المرتبطة بالعمر. ويمكن أن تتراكم البروتينات غير المطوية جيدًا في
الخلايا، ما يؤدي إلى تكوين تجمعات البروتين، التي يمكن أن تُسبّب تلفًا خلويًّا، وتسهم في تطور مجموعة متنوعة من الأمراض. وتؤدي
الطفرات الجينية إلى تغييرات في تسلسل
الأحماض الأمينية للبروتين، ما قد يؤدي إلى تعطل عملية الطي، أو إنتاج بروتينات غير مطويّة بشكل جيد أو غير فعالة وظيفيًّا. وترتبط هذه البروتينات خاطئة الطيّ بمجموعة واسعة من الأمراض، مثل مرض آلزهايمر، ومرض هنتنغتون، والتليف الكيسي[55].
يُعدّ مرض الزهايمر من الأمراض المرتبطة بسوء تكوين البروتين وتشكيله، فهو يترتّب نتيجة أخطاء في تشكيل بروتين أميلويد بيتا (Amyloid β)، ما يؤدي إلى تجمع جزيئات كثيرة منه معًا، مكونةً لويحات أميلويد في الدماغ. تُظهر نتائج البحوث أن تعطل هذه اللويحات الوظيفية الخلوية الطبيعية، يسهم في التدهور المعرفي التدريجي الذي يميّز هذا المرض المرتبط بالعمر[56]. أما مرض باركنسون، فهو مرض آخر يرتبط بخلل في شكل البروتين، إذ يؤدي الخطأ في تجمّع بروتين ألفا سينوكلين (α-synuclein) إلى تراكم أجسام ليوي (Lewy bodies) في الدماغ، التي تُعطّل الوظيفة الخلوية الطبيعية للدماغ، ويُعتقَد أنها تُسهم في الأعراض الحركية المميزة لمرض باركنسون[57]. أما مرض التليف الكيسي، فهو مرض وراثي يرتبط بخلل في بروتين CFTR، وهي قناة أيونية، تؤدي إلى نقل أيوني غير طبيعي عبر
أغشية الخلايا، ما يُعطّل الوظيفة الخلوية الطبيعية، ويُسبب عددًا من الأعراض، بما في ذلك مشكلات الجهازَيْن التنفسي والهضمي[58]. وأخيرًا، يُعدّ مرض هنتنغتون مرضًا وراثيًّا آخر يرتبط بسوء تشكيل البروتين وطيّه، وفي هذا المرض، لا يتشكل بروتين هنتنغتين (Huntingtin) بصورة جيدة، إذ يتجمع ويُكوّن أجسامًا غريبة داخل
الخلايا تعطل الوظيفة الخلوية الطبيعية. ويمكن أن يؤدي هذا المرض إلى الخلل الوظيفي الحركي والتدهور الإدراكي[59]. أما أمراض البريون، فهي أمراض تُسببها بروتينات غير مطوية جيدًا تسمى البريونات (Prions). تتسبّب البريونات غير المطوية في اختلال البروتينات الطبيعية، ما يؤدي إلى تكوين تجمعات البروتين في الدماغ، ويمكن أن يؤدي هذا إلى الخرف والضعف الحركي وأعراض عصبية أخرى[60].
الانشقاق
تنشَط كثير من البروتينات عن طريق الانشقاق التحللي (Proteolytic cleavage)، وتحدث هذه العملية بشكل شائع في عمليات تنشيط
الإنزيمات والهرمونات وجزيئات الإشارة الأخرى. ويتصنَّع البروتين أولًا في شكل غير نشط، ومن ثم ينشَط عند قطعه في أماكن معينة محددة بوساطة
إنزيمات البروتياز القاطعة، التي تشق البروتين المراد تنشيطه، مكونةً بروتينًا نشطًا بيولوجيًّا. ويتعرّف
إنزيم البروتياز إلى روابط ببتيدية معينة داخل البروتين، ويقطعها مُكوّنًا قطعتَيْن من البروتين. وفي بعض الحالات، يزيل حدث الانشقاق جزءًا مثبطًا من البروتين، ما يسمح له بأن ينشط[61].
ومن الأمثلة المعروفة لانشقاق البروتين، تنشيط
إنزيم التربسين الهضمي، إذ يُصنَع التربسين بوصفه جزيئًا أوليًّا يُسمّى التربسينوجين (Trypsinogen)، وهو غير فعّال حتى يُقطَع بوساطة الإنزيم الآخر المُسمّى إنتيروببتيداز (Enteropeptidase)، الذي يشق التربسينوجين في موقع معين كاشفًا الموقع النشط للتربسين، ما يسمح له بالبدء في أداء وظيفته، بوصفه هاضمًا للبروتينات في الأمعاء الدقيقة[62].
يُعدّ هرمون الإنسولين مثالًا آخر على انشقاق البروتين المنشط، فالإنسولين يُصنَع على أنه جزيء أولي يُسمّى بروإنسولين (Proinsulin)، وهو بروتين يحتوي على سلسلة ببتيد داخلية تُسمّى ببتيد سي (C-peptide). يُشَق البروإنسولين بوساطة
إنزيم بروتياز يُدعى بروهرمون كونفرتاز (Prohormone convertase)، يزيل الببتيد سي ويُصنّع الإنسولين الناضج النشط. ويُعدّ حَدَثُ الانقسام هذا أمرًا بالغ الأهمية للنشاط البيولوجي للإنسولين الذي يُنظم استقلاب الغلوكوز في الجسم[63].
من الأمثلة الأخرى المهمة، تحفيز الكاسبيز (Caspase)، وتُعدّ عائلة الكاسبيز من
إنزيمات البروتينات التي تؤدي دورًا أساسيًّا في عملية
الاستماتة الخلوية أو
موت الخلايا المبرمج (Apoptosis). إن تنشيط الكاسبيزات خطوة أولية لا غنى عنها في بدء
موت الخلايا المبرمج وتنفيذه، وتوجد الكاسبيزات في
الخلية بصورة غير نشطة تُعرَف باسم بروكاسبيز (Procaspase)، ويحتاج تنشيطها إلى سلسلة من الأحداث التي تؤدي إلى انشقاق البروكاسبيز. تبدأ هذه العملية عن طريق إشارات داخلية أو خارجية تؤدي إلى انشقاق الكاسبيزات البادئة وتنشيطها، مثل بروكاسبيز-8 وبروكاسبيز-9 وبروكاسبيز-10، ومن ثم تَشقّ هذه الكاسبيزاتُ المحفَّزةُ الكاسبيزاتِ المنفّذةَ مثل كاسبيز-3 وكاسبيز-6 وكاسبيز-7 وتُنشّطها. ويؤدي تحفيز الكاسبيزات المنفذة إلى عمليات تحليل بروتينات
الخلية الأخرى وتقسيمها، ما يؤدي إلى تفكيك
الخلية[64].
الفسفرة
الفسفرة في البروتينات هي إضافة مجموعة فوسفات إلى جزيء بروتيني بغرض تنظيم نشاطه، ويمكن أن يُغير هذا التعديل نشاط البروتين ومكان عمله وتفاعلاته مع البروتينات الأخرى[65]. وثمة ثلاثة أنواع رئيسة من
الإنزيمات التي تُحفّز
الفسفرة، تُصنَّف بحسب
الحمض الأميني الذي تُضاف إليه مجموعة الفوسفات إلى: كيناز السيرين/ ثريونين، وكيناز التيروسين، وكيناز الهيستيدين[66].
كينازات السيرين/ ثريونين
كينازات السيرين/ ثريونين، عائلة كبيرة من
الإنزيمات التي لديها القدرة على
فسفرةالأحماض الأمينية لسيرين وثريونين الموجودة في البروتينات المستهدفة. تؤدي هذه الكينازات أدوارًا رئيسة في تنظيم كثير من العمليات الخلوية، مثل انقسام الخلايا، والتمايز، والاستماتة، والتمثيل الغذائي. ومن الأمثلة على كينازات السيرين/ ثريونين: بروتين كيناز أ (PKA)، وبروتين كيناز ب(PKB/Akt) ، وغلايكوجين سينثاز كيناز (GSK3)[67].
كينازات التيروسين
تهدف كينازات التيروسين إلى
فسفرةالحمض الأميني تيروسين الموجود في البروتين المستهدف، وتُعدّ هذه
الإنزيمات مهمة لتنظيم مسارات الإشارة في
الخلية، وتشارك كذلك في نمو الخلايا والتمايز والبقاء على قيد الحياة. ويمكن أن يؤدي عدم انتظام كينازات التيروسين إلى تطور كثير من الأمراض مثل السرطان. وتتضمن أمثلة كينازات التيروسين: مستقبل عامل نمو النسيج الطلائي (EGFR)، ومستقبل عامل النمو المشتق من الصفائح الدموية (PDGFR)، ومستقبل الإنسولين[68] .
كينازات الهستيدين
تُشكِّل كينازات الهستيدين عائلة أصغر من سابقتَيْها، بسبب قلة انتشارها مقارنة بهما، فالحمض الأميني هستيدين في البروتينات المستهدفة، هو هدف هذه
الإنزيمات التي تضيف إليه مجموعة الفوسفات. وتوجد هذه الكينازات في البكتيريا والفطريات والنباتات، وتؤدي أدوارًا مهمة في الاستشعار والاستجابة للإشارات البيئية، وعادةً ما تشارك في مسارات مكوّنة من عنصرَيْن أساسيين مكوّنَيْن من كيناز الهستيدين، وهو مستشعر وبروتين منظم للاستجابة. يكتشف المستشعر الإشارة البيئية ويفسفر نفسه على الهستيدين، ثم تُنقَل مجموعة الفوسفات إلى بروتين منظم الاستجابة، الذي يبدأ باستجابة خلوية[69] .
تُنظَّم عملية
فسفرة البروتين من خلال شبكة معقدة من مسارات الإشارات الخلوية، التي تضم كثيرًا من البروتينات وجزيئات الإشارة المختلفة. ويمكن أن تكون للفسفرة عدة تأثيرات على وظيفة البروتين، بما في ذلك تغيير نشاطه الإنزيمي وتوطينه وتفاعله مع البروتينات الأخرى. ويمكن أن تؤدي
الفسفرة أيضًا إلى إنشاء مواقع ربط للبروتينات الأخرى. وقد ارتبط الاختلال في
فسفرة البروتين بكثير من الأمراض، بما في ذلك السرطان، ومرض آلزهايمر، والسكري، لذا يُعدّ فهم آليات
فسفرة البروتين ودورها في الأمراض مجالًا نشطًا للبحث، بهدف تطوير علاجات جديدة لهذه الحالات[70].
الارتباط بالغليكوزيل
يُعدّ ارتباط الغليكوزيل بالبروتين أو الغلكزة تعديلًا مهمًا في بعض البروتينات يحصل بعد الترجمة، ويرتبط فيه جزيء سكريّ واحد أو أكثر بالبروتين. إن عمليات الغلكزة تبدأ في
الشبكة الإندوبلازمية، وتكتمل في
جهاز غولجي (Golgi apparatus) في
الخلية. في
الفسفرة كذلك، يمكن لهذا الارتباط أن يغير نشاط البروتين واستقراره وتوطينه. ويُذكَر أن الغلكزة تسهم في كثير من العمليات الخلوية، بما في ذلك التصاق
الخلية، وانتقال الإشارات، والمناعة. ويمكن أن يحمي الارتباط بالغليكوزيل البروتين من التحلل بوساطة بعض
الإنزيمات الخلوية[71].
ثمة نوعان رئيسان من الغلكزة: الغلكزة المرتبطة بالنيتروجين، والغلكزة المرتبطة بالأكسجين. يرتبط جزيء السكر على البروتين بوساطة ذرة نيتروجين من
الحمض الأميني أسباراجين في الغلكزة المرتبطة بالنيتروجين، بينما يرتبط السكر بذرة أكسجين من سيرين أو ثريونين في الغلكزة المرتبطة بالأكسجين. وتختلف وظائف البروتين باختلاف نوع الغلكزة واختلاف عدد
السكريات المُضافة. أما تنظيم العملية، فيتطلب شبكة معقدة من
الإنزيمات والناقلات (الدهنية والبروتينية)، التي تُنسّق تكوين جزيئات السكر ونقلها وارتباطها بالبروتينات المستهدفة. وعادةً ما تُستخدَم جزيئات السكر من
المسارات الأيضية المختلفة في
الخلية، وبالإمكان تعديلها قبل إضافتها على البروتين المستهدف أو بعدها[72].
يرتبط اختلال نظام الغلكزة بكثير من الأمراض، مثل السرطان، واضطرابات المناعة الذاتية، وأمراض التحلل العصبي. فعلى سبيل المثال، يمكن أن تؤثر التغييرات في الغلكزة في قدرة بروتينات سطح
الخلية على الالتصاق بالخلايا المجاورة، ما يؤدي إلى انسلاخ هذه
الخلية وهجرتها في مجرى الدم إلى أماكن أخرى، وهذه عملية أساسية في الأورام السرطانية الخبيثة تُسمّى عملية
الانبثاث (Metastasis). مثال آخر على أهمية الغلكزة يحصل في
الأجسام المضادة: إن
الأجسام المضادة هي بروتينات ينتجها الجهاز المناعي لتحديد العوامل المُمرِضة وتحييدها، مثل
الفيروسات والبكتيريا، ومن الممكن أن تؤثر إضافة جزيئات السكر إلى
الأجسام المضادة في قدرتها على الارتباط بأهدافها، ما قد يؤثر في فاعلية الاستجابة المناعية. يدرس الباحثون أدوار ارتباط الغليكوزيل بالأجسام المضادة في عدة أمراض، بهدف تطوير علاجات مناعية جديدة تُسخّر قدرة الجهاز المناعي للتعرف على الخلايا السرطانية ومهاجمتها[73].
تعديل اليوبيكويتين
تعديل اليوبيكويتين أو الوبكنة، هو تعديل إضافي لاحق للترجمة يُطبّق على بعض البروتينات، ويجري فيه ربط بروتين صغير يُسمّى يوبيكويتين بالبروتين المستهدف. ويشارك هذا التعديل في كثير من العمليات الخلوية المهمة، مثل
انتقال الإشارة الخلوية، ونقل البروتين داخل
الخلية، وهضم البروتين وتكسيره. وتتضمن عملية الوبكنة سلسلة من التفاعلات الإنزيمية المتتالية، التي تؤدي إلى ربط جزيء اليوبيكويتين بالحمض الأميني لايسين على البروتين المستهدف. أما
الإنزيمات المحفزة لهذه العملية التي تعمل بتتابع تامّ، فإنها تُسمى اختصارًا
إنزيمات E1 وE2 وE3. يُنشّط
إنزيم E1 (وهو الإنزيم المحفز لليوبيكويتين Ubiquitin-activating enzyme) اليوبيكويتين، ثم ينقله إلى
إنزيم E2 (وهو الإنزيم الرابط مع اليوبيكويتين Ubiquitin-conjugating enzyme)، الذي ينقله بدوره إلى
إنزيم E3. أما
إنزيم E3 (لايغاز اليوبيكويتين Ubiquitin ligase)، فيتعرّف بعد ذلك إلى البروتين المستهدف ويرتبط به، ناقلًا اليوبيكويتين إلى اللايسين الموجود في البروتين المستهدف[74].
ويمكن أن تكون لإضافة اليوبيكويتين إلى البروتين تأثيرات كثيرة في وظيفة البروتين، من أكثرها شيوعًا استهداف البروتين للتحلّل بوساطة البروتيزوم (Proteasome)، وهو مركب بروتيني كبير يُحلِّل البروتينات إلى ببتيدات أصغر، للتخلص منها وإعادة استعمال مكوّناتها. إن وسم البروتين للتحلّل عن طريق إضافة اليوبيكويتين، يكون بوساطة إضافة سلسلة من جزيئات اليوبيكويتين إلى البروتين المستهدف (الوبكنة المتعددة، Polyubiquitinylation)، فتتكوّن سلسلة من اليوبيكويتين على لايسين واحد في البروتين المستهدف، وبعد إضافة جزيء يوبيكويتين الأول إلى اللايسين، يمكن إضافة مزيد من جزيئات اليوبيكويتين إليه، ما يُنتِج سلسلة من اليوبيكويتين. عادةً، تُميَّز البروتينات المستهدفة للتحلّل عن طريق وجود سلسلة من أربعة أو أكثر من جزيئات اليوبيكويتين عليها، وهذه السلسلة هي التي يُتعرَّف إليها بوساطة البروتيزوم، للإشارة إلى البدء في عملية تحلل البروتين[75].
أما إضافة جزيء يوبيكويتين واحد (الوبكنة الأحادية، Monoubiquitinylation) أو جزيئات يوبيكويتين متعددة، إلى أحماض أمينية مختلفة في البروتين المستهدف (الوبكنة الأحادية المتعددة، Multi-monoubiquitination)، فلها وظائف أخرى غير تحليل البروتين المستهدف وتكسيره، مثل تنظيم نشاط البروتين (تحفيزه أو تثبيطه)، ونقله في
الخلية، وانتقال الإشارات الخلوية، والإدخال الخلوي (Endocytosis). على سبيل المثال، يمكن أن تؤدي إضافة جزيء يوبيكويتين واحد إلى البروتين، إلى تغيير نشاطه أو توطينه داخل
الخلية. علاوة على ذلك، يمكن أن تكون الوبكنة الأحادية بمنزلة إشارة إلى بروتينات أخرى للارتباط بالبروتين المعدل، ما يؤدي إلى تكوين مجمّعات البروتين، وبدء مسارات إشارة خلوية متعددة
[76].
وكما هي الحال في العمليات الأخرى، فإن اختلال عمليات الوبكنة مرتبط بمجموعة واسعة من الأمراض، مثل السرطان، وأمراض التنكس العصبي، والاضطرابات الالتهابية، فثمة ارتباط وثيق بين
الطفرات في الجينات التي تُنظم عمليات الوبكنة مع ظهور أنواع معينة من السرطانات.
الاستتباب وتكسير البروتينات
يُعدّ تكسير البروتين عملية بيولوجية تؤدي دورًا رئيسًا في تنظيم مستويات البروتينات في
الخلايا، ويُحقّق الاستتباب البروتيني أو التوازن البروتيني (proteostasis) توازنًا بين تكوين البروتين وطيّه وتكسيره في
الخلية، ويُعدّ الحفاظ عليه أمرًا بالغ الأهمية لإتمام الوظيفة الخلوية على أكمل وجه، لأنه يمنع تراكم البروتينات المشوهة أو التالفة، التي في أغلب الأحيان تكون ضارّة للخلية، ويضمن وجود التراكيز الملائمة للبروتينات الوظيفية جيدة التكوين[77].
تشمل مسارات تحلل البروتين نظام يوبيكويتين-بروتيزوم، والتحلل الليسوسومي، والتحلل المرتبط بالشبكة الإندوبلازمية (ER associated degradation, ERAD)، وتعمل هذه المسارات معًا لضمان تنظيم البروتينات بشكل صحيح، وإزالة البروتينات المشوهة أو التالفة من
الخلية[78].
شبكة الاستتباب البروتيني
يتضمّن تكوين البروتينات وتكسيرها في
الخلايا حقيقية النوى، شبكة معقدة من المسارات الجزيئية تحتوي على كثير من البروتينات الكبيرة الناظمة، التي تنسق التوازن بين تكوين البروتين وطيّه وتحلّله. وتُنظَّم هذه العملية المعقدة من خلال مجموعة متنوعة من مسارات
انتقال الإشارات الخلوية وآليات الاستجابة للضغط، التي تؤدي إلى تعديلات مهمة في السرعة والكمية لتكوين البروتين وتحلله. ومن الأمثلة الشائعة على الآليات الموجودة خلويًا: استجابة الصدمة الحرارية (Heat shock response)، إذ تُنشَّط هذه العملية استجابةً للإجهاد الخلوي مثل الصدمة الحرارية (التغيير المفاجئ في درجات الحرارة) أو الإجهاد التأكسدي (Oxidative stress) على سبيل المثال. وتؤدي استجابة الصدمة الحرارية إلى زيادة إنتاج البروتينات الناظمة، مثل البروتينات المساعدة التي تسهّل عملية طيّ البروتين والبروتياز، أي
الإنزيمات المسؤولة عن تحلل البروتينات. وتعد هذه
الإنزيمات ضرورية للحفاظ على عملية الاستتباب البروتيني في ظل الظروف المجهِدة للخلية. وتشمل مسارات الإشارات الأخرى التي تُنظم الاستتباب البروتيني: استجابةَ البروتينات غير المطوية (Unfolded protein response, UPR)، والاستجابة المتكاملة للإجهاد (Integrated stress response, ISR)[79].
تُنشَّط استجابة البروتينات غير المطوية استجابةً لتراكم البروتينات غير المطوية جيدًا، أو ذات الخلل في عملية الطيّ في
الشبكة الإندوبلازمية، ما يؤدي إلى زيادة في إنتاج الشابيرونين وبروتينات التحلل المرتبط بالشبكة الإندوبلازمية (ERAD proteins) وتنشيطهما، وذلك لتقليل إجهاد
الشبكة الإندوبلازمية (ER stress). إن التحلل المرتبط بالشبكة الإندوبلازمية مسؤول عن هدم البروتينات غير المجمعة بشكل سليم، أو المتراكمة بشكل خاطئ في
الشبكة الإندوبلازمية. ويجري التعرف إلى هذه البروتينات بوساطة البروتينات المرافقة، ثم تُوجَّه إلى التحلل بوساطة البروتيزوم أو
الليسوسوم[80].
أما الاستجابة المتكاملة للإجهاد، فتُنشَّط عند العجز عن الحصول الكافي على المغذيات، أو استجابةً لعوامل إجهاد أخرى. وتؤدي هذه الاستجابة إلى تقليل عمليات تكوين البروتين، وفي الوقت نفسه تُحفّز عمليات
الالتهام الذاتي (Autophagy)، للحفاظ على التوازن البروتيني خصوصًا، والتوازن الخلوي عمومًا. وتؤدي كثير من البروتينات المعقدة أيضًا أدوارًا حاسمة في الاستتباب البروتيني[81].
البروتينات المرافقة لعمليات الطيّ
مع أن عمليات طيّ البروتينات بعد ترجمتها يمكن أن تحدث تلقائيًّا دون الحاجة إلى مساعدة، فإن طيَّ كثير من البروتينات يتطلب مساعدة من البروتينات المرافقة، التي تسهل طيَّ البروتينات المصنعة حديثًا، وتمنع تراكمها إن كانت معتلّة. تساعد هذه البروتينات المرافقة أيضًا في إعادة طيّ البروتينات التي أصبحت غير متوازنة بسبب الإجهاد الخلوي. وتُصنَّف البروتينات المرافقة إلى عدة عائلات، بناءً على هيكلها ووظيفتها[82].
توجد عدة مركبات بروتينية مثل الشابيرونين تُساعد كذلك في طيّ البروتينات، وخصوصًا بروتينات الهيكل الخلوي وبروتينات الحويصلات الخلوية، إذ تُوفر لهما بيئة معزولة عن بيئة
الخلية لتساعدهما في عمليات الطيّ، لأنهما تتشكلان بوصفهما برميلَيْن لديهما غطاء يُدخِل البروتين غير المطوي ويُخرجه مطويًا. وتُعد بروتينات الصدمة الحرارية (HSPs) أكثر هذه البروتينات المرافقة شهرة، وتُصنَّف إلى عدة عائلات بناءً على وزنها الجزيئي، ويُرمَز إلى وزنها في اسمها، مثل بروتين الصدمة الحرارية 60 (HSP60)، وبروتين الصدمة الحرارية 70 (HSP70)، وبروتين الصدمة الحرارية 90 (HSP90). أما بروتين الصدمة الحرارية 90، فهو البروتين المرافق الأكثر انتشارًا، ويؤدي دورًا مهمًا في منع تراكم البروتين، وتعزيز إعادة تشكيل البروتينات غير المطوية، فهو يهدف إلى استقرار البروتينات وطيّها، ولا سيما بروتينات الإشارة. كذلك يشارك بروتين الصدمة الحرارية 70 في علميات طيّ البروتينات أو تحليلها إن لم تُطوَ بشكل ملائم عن طريق البروتيزوم[83].
تحلّل البروتين والبروتيزوم
علاوة على طيّ البروتين، يُعدّ تحلل البروتين أيضًا مكونًا أساسيًا لعملية توازن البروتين في
الخلية، فالمسار الأساسي لتدهور البروتين في الخلايا حقيقية النواة يتضمّن الارتباط التساهمي لليوبيكويتين بالحمض الأميني لايسين على البروتينات المستهدفة، ما يؤدي إلى تحللها بوساطة البروتيزوم. إن البروتيزوم مركب بروتيني كبير يتكوّن على شكل برميل من سلسلة 20S وسلسلتين منظمتين 19S تُشكّلان غطاءه[84]. يتعرّف 19S إلى البروتين متعدد اليوبيكويتين، ويزيل اليوبيكويتين، ما يسمح بنقل البروتين عبر سلسلة 20S الأساسية، إذ يتحلل إلى ببتيدات صغيرة. إن للبروتيزوم أدوارًا مهمة في الحفاظ على التوازن الخلوي من خلال تنظيم مستويات البروتينات الرئيسة، مثل عوامل النسخ، والبروتينات الناظمة لدورة حياة الخلية. كذلك، يزيل البروتيزوم البروتينات غير المطويّة جيدًا أو التالفة، ما يمنع تراكمها داخل
الخلية[85].
الالتهام الذاتي والاستتباب البروتيني
في حين أن نظام اليوبيكويتين-بروتيزوم هو المسار الأساسي لتكسير البروتينات في الخلايا حقيقية النوى، فإن مسار
الالتهام الذاتي عن طريق
الليسوسوم (Autophagy lysosomal pathway) لديه عدة وظائف في
الخلية، ومنها إزالة البروتينات والعضيّات التالفة، أو تلك التي لا يمكنها أن تتحلل بوساطة نظام اليوبيكويتين-بروتيزوم. كذلك فإن التحلل الليسوسومي مسار مهم آخر لتكسير البروتينات، ويتضمن ابتلاع البروتينات بوساطة
الجسيمات الحالَّة (الليسوسومات)، وهي عضيّات محاطة بغشاء، وتحتوي على مجموعة متنوعة من
الإنزيمات المحلِّلة للمواد الخلوية الكبيرة، مثل
الدهون والسكريات والبروتينات. وعادةً ما تكون البروتينات المستهدفة للتحلّل الليسوسومي، أكبر وأكثر تعقيدًا من تلك التي تكسّر بوساطة نظام اليوبيكويتين-بروتيزوم. في
الليسوسوم، تُفكّك
الإنزيمات المحلّلة البروتينات إلى أحماض أمينية يمكن للخلية إعادة تدويرها بشكل فعّال[86].
وينشط مسار
الالتهام الذاتي استجابةً لكثير من المؤثرات، مثل الإجهاد الخلوي والحرمان من المغذيات، فتتكوّن الحويصلة مزدوجة الغشاء التي تُعرَف باسم جسيم الالتهام الذاتي (Autophagosome)، ومن ثم تُبتلَع المادة السيتوبلازمية وتُحلَّل أوليًّا، وتصل إلى
الليسوسوم لتحليلها كليًا. إن
الالتهام الذاتي للميتوكوندريا من خلال عملية تُسمى ميتوفاجي (Mitophagy)، يضمن المحافظة على وجود
ميتوكوندريا نشطة وظيفيًّا وغير تالفة بعد التخلص من تلك التالفة، ويمكن أن يؤدي تراكم
الميتوكوندريا التالفة إلى كثير من التأثيرات السلبية في
الخلايا، وأهمها
موت الخلية[87].
تنظيم عمليات هدم البروتينات
يتّسم تنظيم عملية هدم البروتينات وتحليلها بالتعقيد، إذ إنها عملية تنطوي على مستويات متعددة من التحكم، فعلى مستوى النسخ، يمكن تنظيم التكشّف الجيني للبروتينات الهادمة التي تعمل في مسارات التحلل، استجابةً لإشارات خلوية مختلفة، إذ يؤدي حرمان
الخلايا من المغذيات أو تعرضها للإجهاد التأكسدي مثلًا، إلى زيادة التكشّف الجيني للجينات المرتبطة بالالتهام الذاتي، من خلال تنشيط عوامل النسخ المختلفة. أما على مستوى ما بعد الترجمة، فيمكن تنظيم تحلل البروتين من خلال تعديلات مختلفة مثل
الفسفرة، والأستلة (Acetylation)، والوبكنة.
كذلك يمكن تعديل نشاط مسارات التحلل، من خلال تحفيز مسارات الإشارة المختلفة مثل مسار mTOR، والمسارات سابقة الذكر مثل استجابة البروتينات غير المطوية واستجابة الصدمة الحرارية. ويمكن أن يُعزز تحفيز هذه المسارات تحلل البروتين أو يمنعه، استجابةً للظروف الخلوية المختلفة. ويُعدّ تنظيم مراقبة جودة البروتين من الآليات المهمة لضمان التعرف إلى البروتينات غير المطويّة أو التالفة وإزالتها ومنع تراكمها؛ لذا، فإن تنظيم عمليات هدم البروتينات ضروري في المجمل، لمنع تراكم البروتينات الضارة التي يمكن أن تؤدي إلى اختلالات خلوية مُمرِضة[88].
المراجع
Alberts, B. et al.
Molecular Biology of the Cell. 4th ed. New York: Garland Science, 2002.
AlphaFold Server – About Page. Alpha fold server. at:
https://acr.ps/1L9F2ut
Anfinsen, C. B. "Principles That Govern the Folding of Protein Chains." Science. vol. 181, no. 4096 (1973).
Ardito, F. et al. "The Crucial Role of Protein Phosphorylation in Cell Signaling and Its Use as Targeted Therapy." International Journal of Molecular Medicine. vol. 40, no. 2 (2017).
Becker, W. M., L. J. Kleinsmith & J. Hardin.
The World of the Cell. 6th ed. San Francisco: Pearson/Benjamin Cummings, 2006.
Beyersmann, D. "Regulation of Mammalian Gene Expression." Experientia Supplementum. vol. 89 (2000).
Brodsky, Barbara & Anton V. Persikov. "Molecular Structure of the Collagen Triple Helix."
Advances in Protein Chemistry. vol. 70 (2005).
Chen, G. F. et al., "Amyloid Beta: Structure, Biology and Structure-Based Therapeutic Development." Acta Pharmacologica Sinica. vol.38 (2017).
"Conformation of Proteins in Interfaces." Encyclopaedia Britannica. at:
https://acr.ps/1L9F2TY
Dikic, I. & Z. Elazar. "Mechanism and Medical Implications of Mammalian Autophagy." Nature Reviews Molecular Cell Biology. vol. 19 (2018).
Ehlinger, Aaron & Kylie J. Walters. "Structural Insights into Proteasome Activation by the 19S Regulatory Particle." Biochemistry. vol. 52, no. 21 (2013).
Fraser, R. D. B. & D. A. D. Parry. "Molecular Packing in the Feather Keratin Filament."
Journal of Structural Biology. vol. 162, no. 1 (2008).
Friedman, M. (ed.).
Protein Crosslinking. Boston: Springer, 1977.
Finkbeiner, S. "The Autophagy Lysosomal Pathway and Neurodegeneration." Cold Spring Harbor Perspectives in Biology. vol. 12, no. 3 (2020).
Glickman, Michael H. & Aaron Ciechanover. "The Ubiquitin-Proteasome Proteolytic Pathway: Destruction for the Sake of Construction." Physiological Reviews. vol. 82, no. 2 (2002).
Hartl, F. Ulrich & Manajit Hayer-Hartl. "Converging Concepts of Protein Folding in Vitro and in Vivo." Nature Structural & Molecular Biology. vol. 16 (2009).
Hartl, F., A. Bracher & M. Hayer-Hartl. "Molecular Chaperones in Protein Folding and Proteostasis." Nature. vol. 475 (2011).
Hartley, H. "Origin of the Word 'Protein'."
Nature. vol. 168 (1951).
Hershko, Avram & Aaron Ciechanover. "The Ubiquitin System." Annual Review of Biochemistry. vol. 67 (1998).
Julien, O. & J. A. Wells. "Caspases and Their Substrates." Cell Death & Differentiation. vol. 24 (2017).
Jumper, J. et al. "Highly Accurate Protein Structure Prediction with AlphaFold." Nature. vol.596 (2021).
- Pakos-Zebrucka et al., "The Integrated Stress Response,"EMBO Reports,vol. 17, no. 10 (2016).
Lee, T. I. & R. A. Young. "Transcription of Eukaryotic Protein-Coding Genes." Annual Review of Genetics. vol. 34 (2000).
“Lewy Body Dementia.” Mayo Clinic. at:
https://acr.ps/1L9F2RL
Maloy, Stanley & Kelly Hughes Brenner's (ed.).
Encyclopedia of Genetics. 2nd ed. San Diego: Academic Press, 2013.
Manning, G. et al. "The Protein Kinase Complement of the Human Genome." Science. vol. 298, no. 5600 (2002).
Manning, Brendan D. & Alex Toker. "AKT/PKB Signaling: Navigating the Network." Cell. vol. 169, no. 3 (2017).
Martinez-Fonts, Kirby et al. "The Proteasome 19S Cap and Its Ubiquitin Receptors Provide a Versatile Recognition Platform for Substrates." Nature Communications. vol. 11, no. 1 (2020).
McDonald, A. G. & K. F. Tipton. "Enzyme Nomenclature and Classification: The State of the Art." FEBS Journal. vol. 290 (2023).
McDonald, E. F., J. Meiler & L. Plate. "CFTR Folding: From Structure and Proteostasis to Cystic Fibrosis Personalized Medicine." ACS Chemical Biology. vol. 18, no. 10 (2023).
Mizushima, N. et al. "Autophagy Fights Disease through Cellular Self-Digestion." Nature. vol. 451 (2008).
Morris, Rhiannon, Katrina A. Black, & Elliott J. Stollar. "Uncovering Protein Function: From Classification to Complexes." Essays in Biochemistry. vol. 66, no. 3 (2022).
Mukhopadhyay, Debdyuti & Howard Riezman. "Proteasome-Independent Functions of Ubiquitin in Endocytosis and Signaling." Science. vol. 315, no. 5809 (2007).
National Center for Biotechnology Information (NCBI). U.S. National Library of Medicine (NLM). at:
https://acr.ps/1L9F2sq
Nelson, D. L. & M. M. Cox.
Lehninger's Principles of Biochemistry. 8th ed. New York: W. H. Freeman, 2021.
Paul, Manash K. & Anup K. Mukhopadhyay. "Tyrosine Kinase - Role and Significance in Cancer." International Journal of Medical Sciences. vol. 1, no. 2 (2004).
Pauling, L. & R. B. Corey. "Atomic Coordinates and Structure Factors for Two Helical Configurations of Polypeptide Chains."
Proceedings of the National Academy ofSciences. vol. 37, no. 5 (1951).
Perutz, M. "Stereochemistry of Cooperative Effects in Haemoglobin: Haem–Haem Interaction and the Problem of Allostery." Nature. vol. 228 (1970).
Pinho, S. & C. Reis. "Glycosylation in Cancer: Mechanisms and Clinical Implications." Nature Reviews Cancer. vol. 15 (2015).
RCSB Protein Data Bank (PDB) Website/ Database.
Research Collaboratory for Structural Bioinformatics (RCSB). at:
https://acr.ps/1L9F3do
Reynolds, J. A. & C. Tanford.
Nature's Robots: A History of Proteins. New York: Oxford University Press, 2003.
Richards, Frederic M. "The 1972 Nobel Prize for Chemistry."
Science. vol. 178, no. 4060 (1972).
Robinson, V. L. et al. "A Tale of Two Components: A Novel Kinase and a Regulatory Switch." Nature Structural Biology. vol. 7, no. 8 (2000).
Sanger, Frederick. "Nobel Lecture."
NobelPrize.org. at:
https://acr.ps/1L9F2uU
Seidah, Nabil G. et al. "The Multifaceted Proprotein Convertases: Their Unique, Redundant, Complementary, and Opposite Functions." Journal of Biological Chemistry. vol. 288, no. 30 (2013).
Shacham, T., N. Sharma & G. Z. Lederkremer. "Protein Misfolding and ER Stress in Huntington's Disease." Frontiers in Molecular Biosciences. vol. 6 (2019).
Schjoldager, K. T. et al. "Global View of Human Protein Glycosylation Pathways and Functions." Nature Reviews Molecular Cell Biology. vol. 21 (2020).
Shoulders, Matthew D. & Ronald T. Raines. "Collagen Structure and Stability." Annual Review of Biochemistry. vol. 78 (2009).
Siltberg-Liberles, J. J., A. Grahnen & D. A. Liberles. "The Evolution of Protein Structures and Structural Ensembles under Functional Constraint."
Genes. vol. 2, no. 4 (2011).
Sumner, James B. "The Isolation and Crystallization of the Enzyme Urease: Preliminary Paper."
Journal of Biological Chemistry. vol. 69, no. 2 (1926).
Urry, Lisa A. et al.
Campbell Biology. 11th ed. New York: Pearson Education, 2017.
Varki, Ajit. "Biological Roles of Glycans." Glycobiology. vol. 27, no. 1 (2017).
Walter, Peter & David Ron. "The Unfolded Protein Response: From Stress Pathway to Homeostatic Regulation." Science. vol. 334, no. 6059 (2011).
[1] J. A. Reynolds & C. Tanford,
Nature's Robots: A History of Proteins (New York: Oxford University Press, 2003), p. 15.
[2] H. Hartley, "Origin of the Word 'Protein',"
Nature, vol. 168 (1951), p. 244.
[3] "Conformation of Proteins in Interfaces," Encyclopaedia Britannica, accessed on 14/8/2025, at:
https://acr.ps/1L9F2TY
[4] James B. Sumner, "The Isolation and Crystallization of the Enzyme Urease: Preliminary Paper,"
Journal of Biological Chemistry, vol. 69, no. 2 (1926), p. 435.
[5] L. Pauling & R. B. Corey, "Atomic Coordinates and Structure Factors for Two Helical Configurations of Polypeptide Chains,"
Proceedings of the National Academy ofSciences, vol. 37, no. 5 (1951), p. 235.
[6] Frederick Sanger, "Nobel Lecture,"
NobelPrize.org, accessed on 13/8/2025, at:
https://acr.ps/1L9F2uU
[7] Frederic M. Richards, "The 1972 Nobel Prize for Chemistry,"
Science, vol. 178, no. 4060 (1972), p. 492.
[8] D. L. Nelson & M. M. Cox,
Lehninger's Principles of Biochemistry, 8th ed. (New York: W. H. Freeman, 2021).
[9] Ibid.
[10] Lisa A. Urry et al.,
Campbell Biology, 11th ed. (New York: Pearson Education, 2017).
[11] Nelson & Cox.
[12] W. M. Becker, L. J. Kleinsmith & J. Hardin,
The World of the Cell, 6th ed. (San Francisco: Pearson/Benjamin Cummings, 2006).
[13] Urry et al.
[14] RCSB Protein Data Bank (PDB) Website/ Database,
Research Collaboratory for Structural Bioinformatics (RCSB), accessed on 13/8/2025, at:
https://acr.ps/1L9F3do
[15] National Center for Biotechnology Information (NCBI), U.S. National Library of Medicine (NLM), accessed on 13/8/2025, at:
https://acr.ps/1L9F2sq
[16] J. Siltberg-Liberles, J. A. Grahnen & D. A. Liberles, "The Evolution of Protein Structures and Structural Ensembles under Functional Constraint,"
Genes, vol. 2, no. 4 (2011), p. 748.
[17] AlphaFold Server – About Page, Alpha fold server, accessed on 17/8/2025, at:
https://acr.ps/1L9F2ut
[18] B. Alberts et al.,
Molecular Biology of the Cell, 4th ed. (New York: Garland Science, 2002).
[19] Nelson & Cox.
[20] Alberts et al.
[21] Nelson & Cox.
[22] R. M. Schultz, "Proteins and Protein Structure," in: Stanley Maloy & Kelly Hughes Brenner's (ed.),
Encyclopedia of Genetics, 2nd ed. (San Diego: Academic Press, 2013), p. 496.
[23] R. D. B. Fraser & D. A. D. Parry, "Molecular Packing in the Feather Keratin Filament,"
Journal of Structural Biology, vol. 162, no. 1 (2008), p. 1.
[24] N. P. Stimler & M. L. Tanzer, "Location of the Intermolecular Crosslinking Sites in Collagen," in: M. Friedman (ed.),
Protein Crosslinking (Boston: Springer, 1977).
[25] Matthew D. Shoulders & Ronald T. Raines, "Collagen Structure and Stability," Annual Review of Biochemistry, vol. 78 (2009), p. 929.
[26] Barbara Brodsky & Anton V. Persikov, "Molecular Structure of the Collagen Triple Helix,"
Advances in Protein Chemistry, vol. 70 (2005), p. 301.
[27] Becker, Kleinsmith & Hardin.
[28] Brodsky & Persikov.
[29] Nelson & Cox.
[30] C. B. Anfinsen, "Principles That Govern the Folding of Protein Chains," Science, vol. 181, no. 4096 (1973), p. 223.
[31] M. Perutz, "Stereochemistry of Cooperative Effects in Haemoglobin: Haem–Haem Interaction and the Problem of Allostery," Nature, vol. 228 (1970), p. 726.
[32] F. Ulrich Hartl & Manajit Hayer-Hartl, "Converging Concepts of Protein Folding in Vitro and in Vivo," Nature Structural & Molecular Biology, vol. 16 (2009), p. 574.
[33] J. Jumper et al., "Highly Accurate Protein Structure Prediction with AlphaFold," Nature, vol.596 (2021), p. 583.
[34] Rhiannon Morris, Katrina A. Black, & Elliott J. Stollar, "Uncovering Protein Function: From Classification to Complexes," Essays in Biochemistry, vol. 66, no. 3 (2022), p. 255.
[35] A. G. McDonald & K. F. Tipton, "Enzyme Nomenclature and Classification: The State of the Art," FEBS Journal, vol. 290 (2023), p. 2214.
[36] Becker, Kleinsmith & Hardin.
[37] Ibid.
[38] Ibid.
[39] Nelson & Cox.
[40] Becker, Kleinsmith & Hardin.
[41] Urry et al.
[42] Becker, Kleinsmith & Hardin.
[43] Nelson & Cox.
[44] Becker, Kleinsmith & Hardin.
[45] Nelson & Cox.
[46] Becker, Kleinsmith & Hardin.
[47] Nelson & Cox.
[48] Ibid.
[49] T. I. Lee & R. A. Young, "Transcription of Eukaryotic Protein-Coding Genes," Annual Review of Genetics, vol. 34 (2000), p. 77.
[50] D. Beyersmann, "Regulation of Mammalian Gene Expression," Experientia Supplementum, vol. 89 (2000), p. 11.
[51] Ibid.
[52] Morris, Black & Stollar, p. 255.
[53] Nelson & Cox.
[54] Ibid.
[55] Ibid.
[56] G. F. Chen et al., "Amyloid Beta: Structure, Biology and Structure-Based Therapeutic Development," Acta Pharmacologica Sinica, vol.38 (2017), p. 1205.
[57] “Lewy Body Dementia,” Mayo Clinic, accessed on: 15/8/2025, at:
https://acr.ps/1L9F2RL
[58] E. F. McDonald, J. Meiler & L. Plate, "CFTR Folding: From Structure and Proteostasis to Cystic Fibrosis Personalized Medicine," ACS Chemical Biology, vol. 18, no. 10 (2023), p. 2128.
[59] T. Shacham, N. Sharma & G. Z. Lederkremer, "Protein Misfolding and ER Stress in Huntington's Disease," Frontiers in Molecular Biosciences, vol. 6 (2019), p. 20.
[60] Nelson & Cox.
[61] Ibid.
[62] Ibid.
[63] Nabil G. Seidah et al., "The Multifaceted Proprotein Convertases: Their Unique, Redundant, Complementary, and Opposite Functions," Journal of Biological Chemistry, vol. 288, no. 30 (2013), p. 21473.
[64] O. Julien & J. A. Wells, "Caspases and Their Substrates," Cell Death & Differentiation, vol. 24 (2017), p. 1380.
[65] F. Ardito et al., "The Crucial Role of Protein Phosphorylation in Cell Signaling and Its Use as Targeted Therapy," International Journal of Molecular Medicine, vol. 40, no. 2 (2017), p. 271.
[66] V. L. Robinson et al., "A Tale of Two Components: A Novel Kinase and a Regulatory Switch," Nature Structural Biology, vol. 7, no. 8 (2000), p. 626.
[67] Brendan D. Manning & Alex Toker, "AKT/PKB Signaling: Navigating the Network," Cell, vol. 169, no. 3 (2017), p. 381.
[68] Manash K. Paul & Anup K. Mukhopadhyay, "Tyrosine Kinase - Role and Significance in Cancer," International Journal of Medical Sciences, vol. 1, no. 2 (2004), p. 101.
[69] Robinson et al., p. 626.
[70] G. Manning et al., "The Protein Kinase Complement of the Human Genome," Science, vol. 298, no. 5600 (2002), p. 1912.
[71] Ajit Varki, "Biological Roles of Glycans," Glycobiology, vol. 27, no. 1 (2017), p. 3.
[72] K. T. Schjoldager et al., "Global View of Human Protein Glycosylation Pathways and Functions," Nature Reviews Molecular Cell Biology, vol. 21 (2020), p. 729.
[73] S. Pinho & C. Reis, "Glycosylation in Cancer: Mechanisms and Clinical Implications," Nature Reviews Cancer, vol. 15 (2015), p. 540.
[74] Avram Hershko & Aaron Ciechanover, "The Ubiquitin System," Annual Review of Biochemistry, vol. 67 (1998), p. 425.
[75] Michael H. Glickman & Aaron Ciechanover, "The Ubiquitin-Proteasome Proteolytic Pathway: Destruction for the Sake of Construction," Physiological Reviews, vol. 82, no. 2 (2002), p. 373.
[76] Debdyuti Mukhopadhyay & Howard Riezman, "Proteasome-Independent Functions of Ubiquitin in Endocytosis and Signaling," Science, vol. 315, no. 5809 (2007), p. 201.
[77] Nelson & Cox.
[78] Becker, Kleinsmith & Hardin.
[79] F. Hartl, A. Bracher & M. Hayer-Hartl, "Molecular Chaperones in Protein Folding and Proteostasis," Nature, vol. 475 (2011), p. 324.
[80] Peter Walter & David Ron, "The Unfolded Protein Response: From Stress Pathway to Homeostatic Regulation," Science, vol. 334, no. 6059 (2011), p. 1081.
[81] K. Pakos-Zebrucka et al., "The Integrated Stress Response," EMBO Reports,vol. 17, no. 10 (2016), p. 1374.
[82] Nelson & Cox.
[83] Hartl, Bracher & Hayer-Hartl, p. 324.
[84] Kirby Martinez-Fonts et al., "The Proteasome 19S Cap and Its Ubiquitin Receptors Provide a Versatile Recognition Platform for Substrates," Nature Communications, vol. 11, no. 1 (2020), p. 477.
[85] Aaron Ehlinger & Kylie J. Walters, "Structural Insights into Proteasome Activation by the 19S Regulatory Particle," Biochemistry, vol. 52, no. 21 (2013), p. 3618.
[86] S. Finkbeiner, "The Autophagy Lysosomal Pathway and Neurodegeneration," Cold Spring Harbor Perspectives in Biology, vol. 12, no. 3 (2020).
[87] N. Mizushima et al., "Autophagy Fights Disease through Cellular Self-Digestion," Nature, vol. 451 (2008), p. 1069.
[88] I. Dikic & Z. Elazar, "Mechanism and Medical Implications of Mammalian Autophagy," Nature Reviews Molecular Cell Biology, vol. 19 (2018), p. 349.