مضادات الصرع هي علاجات تنظم النشاط الكهربائي غير الطبيعي في الدماغ، ما يساعد في الحد من تكرار النوبات الصرع وشدتها. يعدّ الصرع من الاضطرابات العصبية المزمنة، إذ تتسبب النوبات المتكررة بتحديات جسدية ونفسية واجتماعية، قد تؤثر بشكل مباشر في جودة حياة المرضى. تعمل هذه العلاجات من خلال تقليل النشاط العصبي المفرط، وذلك عبر عدة آليات، مثل التأثير في النواقل العصبية والقنوات الأيونية، ويعتمد اختيار العلاج بناءً على نوع الصرع، وعلى الحالة السريرية للمريض.
أصبحت العلاجات الدوائية، وعلى رأسها مضادات الصرع، الخيار الأساسي لإدارة هذا المرض، وتؤدي دورًا أساسيًّا في تقليل تواتر النوبات وحدتها، ما يتيح للمرضى فرصة حياة أكثر استقرارًا وأمانًا. ومع ذلك، فإن التحديات التي يواجهها المرضى لا تقتصر على الأعراض فحسب، بل تشمل أيضًا الآثار الجانبية للأدوية، وتفاعلها مع العلاجات أخرى، علاوة على استجابة المرضى المتفاوتة، وتأثير العوامل الوراثية والبيئية في فعالية الأدوية؛ لذا، فإن تطوير نهج علاجي أكثر تكيفًا مع طبيعة كل مريض، بات ضرورة ملحّة في المسار العلاجي للصرع، كذلك فإن التقنيات الحديثة مثل التطبيب عن بُعد، والتطبيقات الذكية، قد فتحت آفاقًا جديدة في متابعة المرضى ورصد الاستجابة الدوائية، وتقليل أخطار النوبات المفاجئة، ما عزز من التزامهم بالعلاج، وأسهم في تحسين جودة حياتهم.
تعريفها
مضادات الصرع (Antiepileptics)، وتُعرف أيضًا باسم مضادات الاختلاج (Anticonvulsants)، أو الأدوية المضادة للنوبات (Anti-seizure medications)، وهي فئة من الأدوية تُستخدم للوقاية من نوبات الصرع أو علاجها، وذلك من خلال التحكم في النشاط الكهربائي غير الطبيعي في الدماغ. تعمل هذه الأدوية عن طريق تعديل مستويات بعض النواقل العصبية في الدماغ، ما يساعد في منع حدوث النوبات. علاوة على علاج الصرع، تُستخدم مضادات الصرع في علاج اضطرابات متعددة، بما في ذلك
اضطراب ثنائي القطب (Bipolar disorder)، وآلام الأعصاب،
والصداع النصفي (Migraines)،
والألم العضلي الليفي (Fibromyalgia)،
ومتلازمة تململ الساقين (Restless legs syndrome)[1].
مرض الصرع
الصرع (Epilepsy) هو مجموعة من الاضطرابات العصبية غير المعدية، تتميز بنوبات صرعية متكررة، وفي معظم الحالات يكون السبب غير معروف، في حين أن في بعض الحالات، يحدث الصرع نتيجة إصابات دماغية، أو سكتات دماغية، أو أورام، أو عدوى دماغية، أو عيوب خلقية، أو التهابات الجهاز العصبي المركزي، أو الاستعداد الوراثي، وقد تكون الطفرات الجينية مرتبطة بنسبة صغيرة من الحالات.
قُدِّر عدد المصابين بالصرع نحو 51 مليون شخص، مع وقوع 80 في المئة من الحالات في الدول النامية. سُجلت الوفيات المرتبطة بالصرع ارتفاعًا كبيرًا ووصلت إلى 140,000 حالة في عام 2021 (الشكل 1).
 صورة توضيحية للنوبة الصرعية
صورة توضيحية للنوبة الصرعية
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تعدّ النوبة الصرعية (Epileptic seizure) تفريغًا كهربائيًّا غير طبيعي ومفرط ومتزامن في الخلايا العصبية في قشرة الدماغ، ويمكن ملاحظته من خلال مخطط كهربية الدماغ (Electroncephalogram, EEG). يمكن أن تتراوح النوبات من نوبات غير قابلة للاكتشاف ذات فترات قصيرة تقريبًا، إلى نوبات طويلة أو قوية تسبب فقدان الوعي، أو تسبب إصابات جسدية مباشرة وخطرة مثل كسور العظام. كذلك فإن المرضى قد لا يدركون حدوث نوباتهم، ما يشكل مشكلة كبيرة، ولا سيما إذا وقعت النوبة في الأماكن العامة أو في أثناء العمل، ما قد يُسبب أضرارًا نفسية قوية للمريض[2] (الشكل 2).
يُصنّف الصرع بشكل رئيس إلى فئتين رئيستين: الصرع العام (Generalized Epilepsy)، إذ تبدأ النوبات في أنحاء الدماغ جميعها في الوقت نفسه، وتشمل النوبات التوترية الرمعية العامة (Generalized Tonic-Clonic Seizures)، والنوبات الغيابية (Absence Seizures)، والنوبات التوترية (Tonic Seizures)، والنوبات الرمعية (Clonic Seizures)، والنوبات الارتخائية (Atonic Seizures)، والنوبات الرمعية العضلية (Myoclonic Seizures)، في حين تنشأ النوبات في الصرع البؤري (Focal Epilepsy) أو الصرع الجزئي (Partial Epilepsy) من منطقة محددة من الدماغ، ويمكن أن تظل محصورة في تلك المنطقة أو تنتشر إلى مناطق أخرى[3] (الشكل 2).
![الشكل [2]](https://arabica.dohainstitute.org/EncyclopediaGalleries/الشكل [2]/الشكل [2].png) صورة توضيحية تُفرق بين الصرع العام والصرع الجزئي
صورة توضيحية تُفرق بين الصرع العام والصرع الجزئي
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تشخيصه
يتطلب تشخيص الصرع استبعاد الحالات الأخرى التي قد تسبب أعراضًا مشابهة، مثل الإغماء أو انسحاب الكحول، أو اضطرابات القلب، ويكون ذلك عن طريق تصوير الدماغ، وإجراء فحوصات الدم، أو باستخدام مخطط كهربية الدماغ، مع العلم أن قراءة مخطط كهربية الدماغ الطبيعية لا تستبعد الصرع تمامًا.
يعتمد تشخيص الصرع على وجود نوبتين أو أكثر غير مبررتين، تفصل بينهما أكثر من 24 ساعة، أو نوبة واحدة غير مبررة، مع احتمالية عالية لحدوث نوبات أخرى مشابهة، وبناءً على التشخيص الدقيق، يُحدَّد العلاج ونوعه. يسهم التشخيص السليم والعلاج المناسب في تحسين حياة المرضى، وتقليل تأثيرات الصرع في حياتهم اليومية.[4]
علاجه
قبل البدء في علاج الصرع، يجب التأكد من التشخيص الدقيق لحالة المريض، ويمكن لنحو ثلثي مرضى الصرع السيطرة على نوباتهم إذا شُخِّصوا وعولجوا بشكل صحيح. وثمة جدل فيما أكان يجب إعطاء الدواء بعد نوبة صرع واحدة، أو الاعتماد على خطر تكرار النوبات. ويعدّ العلاج الفوري غير ضروري، ولا سيما إذا كان سبب النوبة قابلًا للعلاج.
تتطلب الحالة الصرعية عناية خاصة، فهي حالة طوارئ عصبية تتّسم بنوبات طويلة الأمد، ويبدأ العلاج عندما تستمر النوبات التوترية الرمعية العامة (Generalized Tonic-Clonic Seizures) أكثر من 5 دقائق، أو النوبات البؤرية (Focal Seizures) أكثر من 10 دقائق. تتمثل استراتيجية العلاج الأولية في العلاج الأحادي (Monotherapy)، إذ يحقق نحو نصف مرضى الصرع الذين شُخِّصوا حديثًا، تحسنًا كاملًا بعد تناول أول دواء مضاد للصرع. ولتقليل الآثار الجانبية، يُوصى بالبدء بجرعة منخفضة، وزيادتها تدريجيًّا حتى الوصول إلى الجرعة المستهدفة.[5]
تطور مضادات الصرع
مع التقدم العلمي في القرن التاسع عشر، تعمق العلماء في دراسة الصرع، ما أدى إلى تطوير العلاجات الدوائية الأولى. وفي عام 1857، اكتُشف أن البروميدات (Bromides) يمكنها تقليل حدة النوبات الصرعية، وكانت هذه من أولى المحاولات الجادة لاستخدام الأدوية الكيميائية لعلاج الصرع[6].
في عام 1912، اكتُشف الفينوباربيتال (Phenobarbital) بوصفه أول دواء فعال في تقليل تكرار النوبات، لكنه سبب آثارًا جانبية مثل النعاس والتخدير، ما قيد من استخدامه. لاحقًا، في ثلاثينيات القرن العشرين، طُوّر الفينيتوين (Phenytoin)، الذي كان أقل تسببًا للنعاس وأكثر فاعلية في السيطرة على النوبات، ما جعله ركيزة أساسية في علاج الصرع لسنوات طويلة، وقد شكّل هذا الاكتشاف نقطة تحول، إذ ساعد في تقليل معدلات حدوث النوبات وتحسين جودة حياة المرضى[7].
حتى عام 2025، ضمت العلاجات الدوائية للصرع أكثر من 30 دواء (الجدول 1)، وتختلف هذه الأدوية في حركيتها الدوائية وفعاليتها وآثارها الجانبية، ما يتيح خيارات علاجية متنوعة تناسب احتياجات المرضى. ومنذ عام 1985، ظهر جيل جديد من الأدوية يُعرف بالجيل الثاني (Second generation)، الذي يتميز بسلامة أعلى مقارنة بالعقاقير القديمة، لكنه لم يؤدِّ إلى زيادة كبيرة في عدد المرضى الذين يحققون تحكمًا كاملًا في النوبات.
مع تقدم البحث العلمي، يُعمَل على تطوير أدوية تعتمد على الطب الشخصي (Personalized medicine)، الذي يعتمد على تحليل التكوين الجيني لكل مريض لاختيار الدواء الأنسب له. كذلك يجري استكشاف تقنيات مثل تحفيز العصب المبهم (Vagus nerve stimulation)، والعلاج الجيني (Gene therapy) لعلاج الصرع المقاوم للأدوية.[8]
يُتوقع أن يشهد علاج الصرع نقلة نوعية مع التقدم المستمر في علوم الأدوية والجينوميات العصبية، ومن أبرز هذه التطورات، تطوير أدوية تستهدف الآليات الجزيئية المرتبطة بالصرع بشكل أكثر دقة، ما قد يسهم في تحسين الاستجابة العلاجية وتقليل الأعراض الجانبية، كذلك فإن اكتشاف المؤشرات الحيوية قد يُحدث تحولًا كبيرًا في كيفية اختيار العلاج الأمثل لكل مريض، ما يعزز من فرص السيطرة على المرض بفاعلية أكبر. إلى جانب ذلك، فإن الأبحاث المستمرة في العلاجات الجينية والخلايا الجذعية، قد تفتح المجال أمام علاجات جديدة تهدف إلى تعديل مسار المرض ذاته، بدلًا من مجرد السيطرة على أعراضه، ما يبعث الأمل في إمكانية الوصول إلى علاجات قد تؤدي إلى التعافي التام لبعض المرضى مستقبلًا.
اختيارها
يمكن السيطرة على نوبات الصرع باستخدام الأدوية في نحو 69 في المئة من الحالات، كذلك أصبح من الممكن تحسين النتائج من خلال تعديل الجرعات بعناية، ومراقبة مستويات الدواء في الدم عند الحاجة.
يتطلب اختيار الدواء المناسب مراعاة عدة عوامل، ومنها تصنيف الصرع ونوع النوبات، وفعالية الدواء، والتفاعلات الدوائية {{التفاعلات الدوائية: (Drug interactions) ظاهرة بيولوجية تنجم عن تفاعل بين دوائين أو أكثر، ما يؤدي إلى تغيرات في فعالية أحد الأدوية المتفاعلة أو جميعها أو سميتها. تتجلى هذه التغييرات في صورة زيادة في التأثير العلاجي أو نقصانها، أو في شكل آثار جانبية جديدة غير متوقعة.}}، وطبيعة حالة المريض، مثل العمر والجنس ونمط الحياة، ومدى تحمله للعلاج وتكلفته، بما يتناسب مع الوضع المالي للمريض، فبعض الأدوية فعالة لنوع معين من النوبات فقط، على سبيل المثال، قد يؤدي الكاربامازيبين ((Carbamazepine والڤيغاباترين (Vigabatrin)، إلى تفاقم النوبات الرمعية العضلية (Myoclonic seizures)، في حين يُوصى بالإيثوسكسيميد (Ethosuximide) وحمض الڤالبرويك (Valproic Acid) للنوبات الغيابية (Absence seizures). كذلك يجب تقييم الآثار الجانبية المحتملة والأمراض المصاحبة، مثل الاكتئاب والخرف ومشاكل الكبد والكلى، ما يسهم في تحسين الاستجابة السريرية.
إلى جانب ذلك، تقدِّم الفهم للتداخلات الدوائية، وأهمية الاختيار بين العلاج الأحادي والعلاج المركب، علاوة على تطور المعرفة بتاريخ متلازمات الصرع، والعوامل التي تؤثر في تكرار النوبات، يساعد في تحديد التوقيت المناسب لإيقاف العلاج بعد تحقيق السيطرة على النوبات لفترة معينة. وبالنسبة للمرضى الذين لا يستجيبون للعلاج الدوائي، ينبغي النظر في الجراحة، أو العلاجات البديلة، أو تحفيز العصب المبهم، أو العلاج الغذائي في وقت مبكر[9].
آلية عملها
تعمل مضادات الصرع من خلال تقليل النشاط العصبي المفرط، وذلك عبر عدة آليات، وتشمل التأثير في النواقل العصبية والقنوات الأيونية، علاوة على آليات متعددة. يعتمد اختيار العلاج بناءً على نوع الصرع والحالة السريرية للمريض.[10]
التأثير في النواقل العصبية
تُنقَل الإشارات العصبية في الدماغ من خلال النواقل الكيميائية، ويُعدّ الغلوتامات (Glutamate) من أهم النواقل العصبية المؤثرة في الصرع، وهو ناقل محفز يزيد من النشاط العصبي، وكذلك يُعدّ حمض الغاما-أمينوبيوتيريك (Gamma-aminobutyric acid, GABA) ناقلًا عصبيًّا مثبطًا يحدّ من النشاط الكهربائي المفرط.
تعمل مضادات الصرع من خلال تعزيز نشاط مستقبلات حمض الغاما-أمينوبيوتيريك (GABA) لزيادة التثبيط العصبي، ومن الأمثلة عليها: الفينوباربيتال (Phenobarbital)، والبنزوديازيبينات مثل ديازيبام (Diazepam) ولورازيبام (Lorazepam)، والڤيغاباترين. في حين تعمل بعض مضادات الصرع من خلال تقليل تحفيز مستقبلات الجلوتامات للحد من الإفراط في الإشارات العصبية، ومن الأمثلة عليها: التوبيرامات (Topiramate) والفيلبامات (Felbamate)، والبيرامبانيل (Perampanel)[11].
التأثير في القنوات الأيونية
تؤدي القنوات الأيونية دورًا أساسيًّا في تنظيم تدفق الأيونات داخل الخلايا العصبية وخارجها، فتعمل مضادات الصرع من خلال التأثير في النواقل العصبية، وذلك بتثبيط قنوات الصوديوم والكالسيوم، فينجم عن ذلك تقليل فرط النشاط العصبي. يمنع كل من الفينيتوين (Phenytoin)، والكاربامازيبين (Carbamazepine)، ولاموتريجين (Lamotrigine)، والأُكسكاربازيبين (Oxcarbazepine) تدفقَ الصوديوم، في حين يؤثر الإيثوسكسيميد (Ethosuximide)، والغابابنتين (Gabapentin)، والبريغابالين (Pregabalin) في قنوات الكالسيوم لتقليل النشاط الكهربائي المفرط[12].
تأثيرات متعددة
لتحقيق تأثير أكثر شمولًا في السيطرة على النوبات، تعمل بعض الأدوية بآليات متعددة، على سبيل المثال، يؤثر حمض الڤالبرويك (Valproic acid) في حمض الغاما-أمينوبيوتيريك وقنوات الصوديوم والكالسيوم معًا، وكذلك يعمل زونيساميد (Zonisamide) عبر تثبيط قنوات الصوديوم والكالسيوم، مع تأثيرات إضافية في حمض الغاما-أمينوبيوتيريك والغلوتامات[13].
أنواع مضادات الصرع
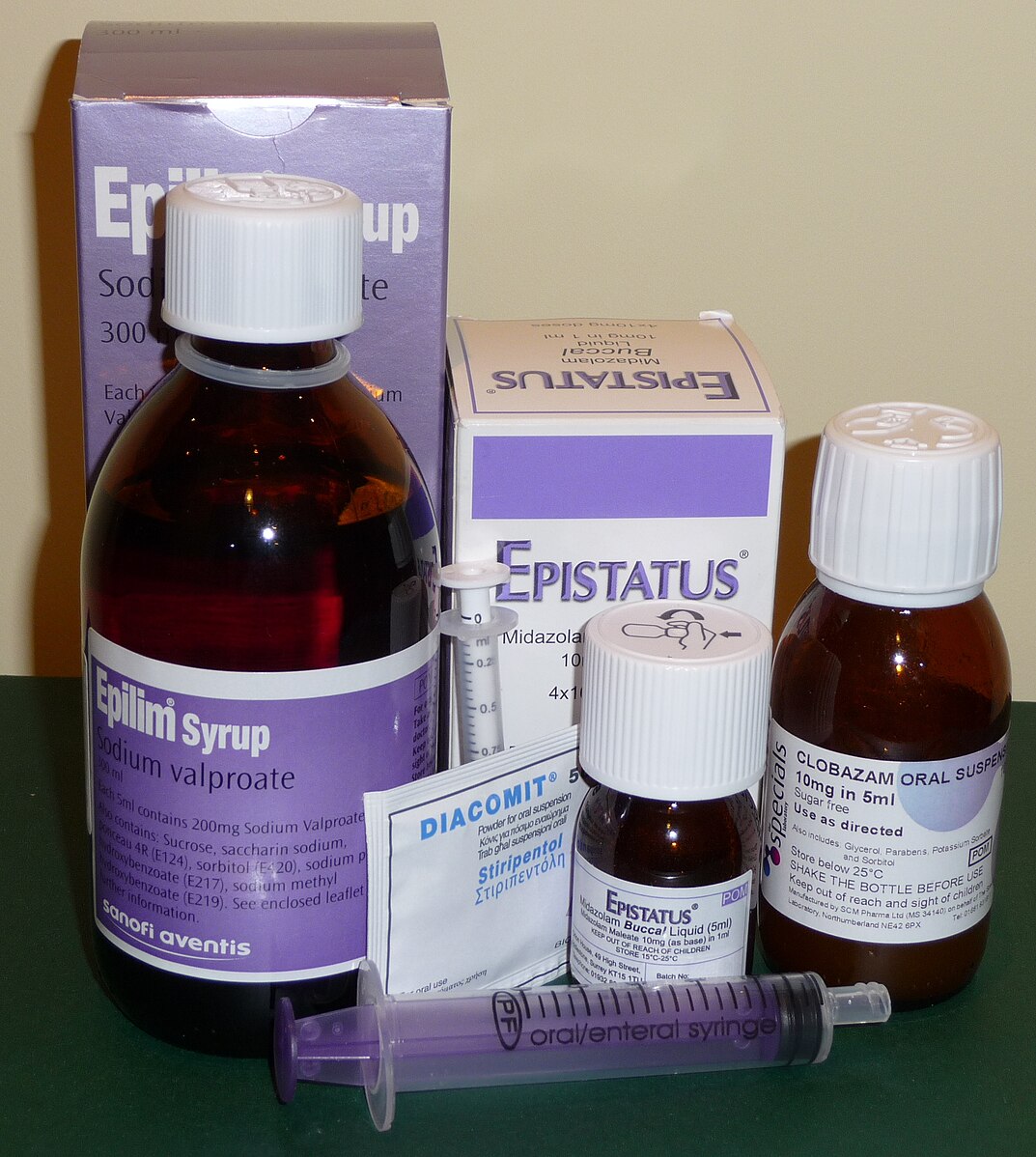 فالبروات الصوديوم، ستيريبنتول، كلوبازام، وميدازولام
فالبروات الصوديوم، ستيريبنتول، كلوبازام، وميدازولام
حذف الصورة؟
سيؤدي هذا إلى نقل الصورة إلى سلة المهملات.
تُعدّ مضادات الصرع من العلاجات الأساسية للصرع، وتُستخدم لعلاج أنواع مختلفة من نوبات الصرع، علاوة على بعض الحالات الأخرى، مثل الألم العصبي واضطراب ثنائي القطب، يُختَار الدواء المناسب بناءً على نوع النوبات، والاستجابة الفردية للعلاج، والتأثيرات الجانبية المحتملة. وتختلف هذه الأدوية في آليات عملها، وخصائصها الدوائية والجرعات المستخدمة[14]، وتتضمن ما يأتي:
1. الكاربامازيبين
يُستخدم الكاربامازيبين (Carbamazepine) في علاج الصرع الجزئي (Partial epilepsy)، والنوبات التوترية الرمعية، والألم العصبي، واضطراب ثنائي القطب، وتبلغ جرعته الموصى بها للبالغين من 200 إلى 400 ملّيغرام مرتين يوميًّا، ويمكن زيادتها إلى 800 حتى 1600ملّيغرام يوميًّا، في حين تكون الجرعة للأطفال 20-10 ملّيغرامًا/ كيلوجرام/ يوم، وتعتمد فترة العلاج على استجابة المريض، وقد يستمر العلاج سنوات. من الأعراض الجانبية للعلاج بالكاربامازيبين: الصداع والدوار والغثيان، والطفح الجلدي، واضطرابات في نظم القلب.
2. الإيثوسكسيميد
الإيثوسكسيميد (Ethosuximide) هو دواء مضاد للاختلاج، يُستخدم بشكل أساسي لعلاج نوبات الغياب (Absence Seizures)، وهو نوع من الصرع يتميز بفقدان وجيز للوعي من دون حركات تشنجية واضحة. ينتمي إلى فئة السكسينيميدات (Succinimides)، ويعمل عن طريق تثبيط قنوات الكالسيوم من النوع T في الدماغ، ما يقلل النشاط الكهربائي غير الطبيعي. يُعدّ الإيثوسكسيميد العلاج الأول لنوبات الغياب، نظرًا لفعاليته العالية وآثاره الجانبية المحدودة مقارنة بالأدوية الأخرى، ويتوفر في شكل كبسولات أو
معلق فموي {{معلق فموي: (Oral suspension) شكل صيدلاني سائل يتضمن جسيمات صلبة غير مذابة ومعلّقة في وسط سائل، ويُستخدم لتسهيل تعاطي الأدوية التي لا تتمتع بقابلية جيدة للذوبان، إذ يُتناول عبر الفم لتعزيز الامتصاص والفعالية العلاجية.}}، وتبدأ الجرعة عادةً بـ500 ملّيغرام يوميًّا للبالغين والأطفال فوق 6 سنوات، مع إمكانية زيادتها تدريجيًّا حتى 1500 ملّيغرام يوميًّا. تشمل آثاره الجانبية الشائعة الدوخة والنعاس، والصداع والغثيان، في حين قد تحدث أعراض أكثر خطورة، مثل تغيرات في المزاج أو ردود فعل تحسسية.
3. الغابابنتين
يُستخدم الغابابنتين (Gabapentin) لعلاج الصرع الجزئي والألم العصبي الناتج من السكري أو
الحزام الناري {{الحزام الناري: (Shingles) عدوى فيروسية تنتج عن إعادة تنشيط فيروس الحماق النطاقي (Varicella-Zoster Virus, VZV) الكامن. يتميز هذا المرض بظهور طفح جلدي مؤلم يأخذ نمط التوزيع العصبي وغالبًا ما يظهر على جانب واحد فقط من الجسم، مترافقًا مع إحساس بعدم الراحة العصبية.}}. إذ ينظم النشاط الكهربائي في الدماغ، عن طريق تقليل إشارات الألم العصبي، يبدأ مفعوله خلال 2-3 ساعات، لكنه قد يستغرق أسبوعين أو أكثر للوصول إلى أقصى فعالية. تتفاوت جرعاته حسب العمر، فتبدأ عند البالغين بـ300 ملّيغرام يوميًّا، وتزداد تدريجيًّا حتى الجرعة القصوى 600 ملّيغرام 3 مرات يوميًّا، وقد يسبب آثارًا جانبية مثل النعاس والدوخة والغثيان وزيادة الوزن.
4. لاكوساميد
لاكوساميد (Lacosamide) هو دواء مضاد للاختلاج، يُستخدم لعلاج النوبات الجزئية والنوبات التوترية الرمعية المعممة لدى البالغين، والأطفال من عمر 4 سنوات فما فوق، إذ يقلل النشاط الكهربائي غير الطبيعي في الدماغ. الجرعة المعتادة لعلاج الصرع عند البالغين، تبدأ بـ 100ملّيغرام مرتين يوميًّا، ويمكن زيادتها تدريجيًا حتى تصل إلى 200-150 ملّيغرام مرتين يوميًّا، ويجب استخدامه بحذر عند المرضى الذين يعانون من أمراض القلب والكبد، أو اضطرابات المزاج.
5.لاموتريجين
يعدّ لاموتريجين ((Lamotrigine من مضادات الصرع الحديثة التي تقلل من تكرار النوبات، ويستخدم لعلاج نوبات الصرع الجزئية والمعممة، واضطراب ثنائي القطب. تبدأ الجرعة بـ50 ملّيغرامًا يوميًّا، وتزداد تدريجيًّا إلى أن تصل إلى 200 حتى 400 ملّيغرام يوميًّا، وقد يستمر العلاج طويل الأمد حسب استجابة المريض. ومن الأعراض الجانبية له الطفح الجلدي والدوار والغثيان واضطرابات النوم.
6. ليفِتيراسيتام
ليڤيتيراسيتام (Levetiracetam)، هو دواء مضاد للصرع، يقلل تكرار النوبات دون علاجها نهائيًّا، ويستخدم لعلاج النوبات الجزئية والتوترية الرمعية. تتراوح جرعته بين 1500 و500 ملّيغرام مرتين يوميًّا للبالغين، في حين تُحدد للأطفال بناءً على الوزن. قد يسبب آثارًا جانبية مثل النعاس والدوار والصداع والتعب وتقلبات المزاج، وفي حالات نادرة، قد يؤدي إلى ميول انتحارية أو إلى التهاب الكبد والبنكرياس، ويجب استخدامه بحذر لدى مرضى الكلى والنساء الحوامل.
7. الأوكسكاربازيبين
الأوكسكاربازيبين (Oxcarbazepine) هو دواء مضاد للاختلاج، يُستخدم لعلاج النوبات الجزئية لدى البالغين والأطفال، ويعمل عبر تقليل النشاط الكهربائي غير الطبيعي في الدماغ. تشمل الجرعة المعتادة للبالغين في العلاج الأحادي 300 ملّيغرام مرتين يوميًّا، مع إمكانية زيادتها تدريجيًّا حتى 1200 ملّيغرام مرتين يوميًّا في حد أقصى، وقد يسبب الدواء آثارًا جانبية، مثل الغثيان والدوخة والنعاس والتعب والرعشة والرؤية المزدوجة والطفح الجلدي واضطرابات التوازن، لذا، يُنصح بتوخي الحذر عند الاستخدام، ولا سيما لدى المرضى الذين يعانون من أمراض الكبد أو الكلى، واضطرابات المزاج، أو خلال فترة الحمل والرضاعة.
8. الفينيتوين
يُعدّ فينيتوين الصوديوم (Phenytoin Sodium) دواءً مضادًا للصرع، يُستخدم أساسًا للسيطرة على النوبات التوترية الرمعية والنوبات الجزئية، كذلك يُستخدم في بعض حالات عدم انتظام ضربات القلب وآلام الأعصاب، ويعمل عن طريق تثبيط قنوات الصوديوم، ما يساعد في تقليل استثارة الخلايا العصبية. تتراوح جرعته العلاجية بين 10-20 ميكروغرامًا/ مللليتر، ومن آثاره الجانبية الشائعة: تضخم اللثة، وفرط نمو الشعر، والترنح (Ataxia)، والرأرأة {{الرأرأة: (Nystagmus) حركات سريعة وغير إرادية للعينين قد تكون أفقية، أو رأسية، أو دائرية. تُعدّ هذه الظاهرة إشارة إلى وجود اختلال وظيفي في الجهاز العصبي المركزي أو تأثيرات جانبية لبعض الأدوية التي تؤثر في تنظيم الحركة البصرية.}}، في حين تشمل الآثار الخطرة متلازمة ستيڤنز جونسون (Stevens-Johnson Syndrome)، وتسمم الكبد، وتثبيط نقي العظم {{تثبيط نقي العظم: (Bone Marrow Suppression) حالة مرضية تتضمن انخفاضًا في توليد خلايا الدم الأساسية مثل الكريات البيضاء، والحمراء، والصفائح الدموية داخل نقي العظم. ينجم عن ذلك زيادة في مخاطر الإصابة بالعدوى والنزيف نتيجة ضعف المناعة وانخفاض نسبة التجلط.}}.
9. بريغابالين
بريغابالين
(Pregabalin) هو دواء لعلاج آلام الأعصاب، مثل اعتلال الأعصاب السكري والصرع والألم العضلي التليفي، إذ يقلل النشاط العصبي الزائد بطريقة مشابهة للناقل العصبي غابا (GABA). يُعطى بريجابالين على شكل أقراص أو شراب بجرعات تتراوح بين 150 و300 ملّيغرامات يوميًّا، مع بدء فعاليته خلال أسابيع. ومن آثاره الجانبية الشائعة: الدوخة والتعب وجفاف الفم وزيادة الوزن، كذلك يُحذَّر من استخدامه في أثناء الحمل والرضاعة إلا عند الضرورة.
10. توبيراميت
توبيراميت (Topiramate) وهو مضاد للاختلاج، يُستخدم لعلاج نوبات الصرع والحد من أعراض الصداع النصفي لدى البالغين. يقلل الدواء النشاط العصبي المفرط في الدماغ، ما يساعد في تقليل التشنجات والصداع، وتتراوح الجرعة الموصى بها لعلاج الصرع بين 200 و 400ملّيغرام يوميًّا للبالغين، مقسمة على جرعتين، في حين يُحدد للأطفال بناءً على الوزن، وبجرعة بين 1 و3 ملّيغرام لكل كيلوغرام يوميًّا. ومن آثاره الجانبية الشائعة: فقدان الشهية والإسهال ونقص الوزن والشعور بالتعب والدوخة، والتأثير في التركيز والذاكرة، وقد يسبب أيضًا أفكارًا اكتئابية أو انتحارية لدى بعض المرضى. لا يُنصح بإيقاف الدواء فجأة، بل يجب تقليل الجرعة تدريجيًّا تحت إشراف الطبيب، لتجنب أعراض الانسحاب مثل القلق والاكتئاب وزيادة الوزن.
11. فيغابترين
ڤيغابترين (Vigabatrin) هو دواء مضاد للصرع، يُستخدم لعلاج النوبات الجزئية المركبة والتشنجات عند حديثي الولادة، ولا سيما للحالات الشديدة التي لم تستجب للعلاجات الأخرى. الجرعة المعتادة للبالغين تبدأ بـ1 غرام يوميًّا مقسمة على جرعتين، ويمكن زيادتها تدريجيًّا حتى 3 غرامات يوميًّا حسب الحاجة، في حين تتراوح جرعة الأطفال حسب الوزن. من أبرز آثاره الجانبية: الصداع والنعاس والدوار والتعب وزيادة الوزن، ومشاكل في الرؤية التي قد تصل إلى فقدان البصر الدائم، واضطرابات نفسية، مثل الاكتئاب والنزعات الانتحارية، علاوة على اضطرابات الجهاز الهضمي والتنفس. يجب الحذر عند استخدامه، وإجراء فحوصات دورية للعين، وعدم التوقف عنه فجأة من دون استشارة الطبيب.
12. زونيساميد
يستخدم الزونيساميد (Zonisamid) بوصفه علاجًا مساعدًا لنوبات الصرع الجزئي لدى البالغين والمراهقين فوق 16 عامًا، وبجرعة تبدأ من 100 ملّيغرام يوميًّا، ويمكن زيادتها تدريجيًّا حتى 400-600 ملّيغرام يوميًّا. قد يسبب آثارًا جانبية، تشمل النعاس والدوار وفقدان الشهية، واضطرابات الذاكرة وفقدان التوازن، وتغيرات مفاجئة في المزاج، علاوة على ميول انتحارية، وردود فعل تحسسية، وحصى الكلى، والحماض الاستقلابي.
يمنع استخدامه من الأشخاص الذين لديهم حساسية تجاهه أو تجاه مركبات السلفا، أو المصابين بأمراض الكبد والكلى، واضطرابات العظام، أو من يتبعون حمية الكيتو (Ketogenic Diet)، كذلك قد يكون ضارًا للجنين، لذا يُنصح باستخدام وسائل منع الحمل المناسبة.
13. حمض الڤالبرويك
يعدّ حمض الڤالبرويك (Valproic Acid) من مضادات الاختلاج واسعة النطاق، ويستخدم لعلاج الصرع الجزئي والمعمم، والصداع النصفي، واضطراب ثنائي القطب. تبدأ الجرعة بـ500 مليغرام يوميًّا، وتزداد من 1000 حتى 2000 ملّيغرام يوميًّا حسب الحاجة، ويستمر العلاج عدة سنوات حسب استجابة المريض. ومن الأعراض الجانبية زيادة الوزن والرعشة، واضطرابات الدورة الشهرية، وقد يؤثر أيضًا في وظائف الكبد.
الآثار الجانبية لها وموانع استعمالها
يمكن أن تشمل الآثار الجانبية لمضادات الصرع أعراضًا عصبية أو عامة (الجدول 1)، ومن الآثار الجانبية الشائعة: النعاس والتعب، واضطرابات الجهاز الهضمي، وزيادة الوزن أو فقدانه، والطفح الجلدي في بعض الحالات. ومن التأثيرات طويلة المدى، ضعف الإدراك والتركيز، وهشاشة العظام بسبب بعض الأدوية، وتأثيرات سلبية في وظائف الكبد والكلى[15].
[الجدول 1]
الآثار الجانبية لمضادات الصرع وموانع الاستعمال
الآثار الجانبية العصبية | الآثار الجانبية العامة | موانع الاستخدام | اسم الدواء |
|---|
النعاس والخمول، والدوخة، وازدواج الرؤية، والترنح، ومتلازمة ستيڤنز-جونسون (Stevens-Johnson syndrome)، ومتلازمة فرط التحسس الدوائي مع فرط الحمضات (Eosinophilia) والأعراض الجهازية، وتثبيط نخاع العظم، والحصار القلبي الأذيني البطيني | نقص الصوديوم في الدم، ومشاكل الجهاز الهضمي، وقلة الكريات البيض، والطفح الجلدي، وهشاشة العظام. | يمنع استخدامه مع مثبطات أحادي الأمين أكسيداز (Monoamine oxidase inhibitors, MAOIs)، ومرضى الحصار القلبي الأذيني البطيني (Atrioventricular block, AVB) من الدرجة الثانية أو الثالثة. | كاربامازيبين Carbamazepine)) |
نعاس، ودوخة، وترنح، وفقدان في الشهية، وذهان، ومتلازمة ستيڤن جونسون، ومتلازمة فرط التحسس الدوائي مع فرط الحمضات والأعراض الجهازية. | مشاكل الجهاز الهضمي، وفقدان الوزن، وقلة كريات الدم البيضاء، وفقر الدم. | يمنع استخدامه في حالة البورفيريا (Porphyria). | الإيثوسكسيميد Ethosuximide)) |
نعاس، وخمول، ودوخة، وازدواج في الرؤية، وترنح، ورعشة. | مشاكل الجهاز الهضمي، وزيادة الوزن. | يمنع استخدامه في نوبات الغياب (Absence Seizure). | غابابنتين Gabapentin)) |
نعاس، وخمول، ودوخة، وازدواج في الرؤية، وترنح، وصداع. | عدم انتظام ضربات القلب. | يمنع استخدامه في حال وجود مشاكل قلبية، وفرط الحساسية تجاهه. | لاكوساميد Lacosamide)) |
ترنح، ودوخة، وازدواج الرؤية، والتهاب السحايا العقيم، ومتلازمة ستيڤنز جونسون، ومتلازمة فرط التحسس الدوائي مع فرط الحمضات والأعراض الجهازية. | طفح جلدي، وهشاشة في العظام. | يُفضل تجنب استخدامه في الأمراض الكبدية الحادة. | لاموتريجين Lamotrigine)) |
نعاس وخمول، ودوخة، وازدواج في الرؤية، وترنح، واضطرابات في المزاج، وذهان، وأفكار انتحارية. | قلة الكريات الدموية. | يجب الحذر عند استخدامه مع المرضى الذين يعانون من مشاكل حادة في الكلى. | ليڤتيراسيتام (Levetiracetam) |
نعاس، وخمول، ودوخة، وترنح، وصداع، ومتلازمة ستيڤنز-جونسون. | نقص صوديوم الدم، ومشاكل الجهاز الهضمي | مثبطات أحادي الأمين أكسيداز، ومرضى الحصار القلبي الأذيني البطيني. | أوكسكاربازيبين (Oxcarbazepine) |
نعاس، وخمول، ودوخة، وازدواج الرؤية، وترنح، وعدوان، وذهان، واضطراب في المزاج. | الأفكار الانتحارية (Suicidal ideation) | يجب تجنبه من المرضى الذين يعانون من مشاكل كبدية حادة | بيرامبانيل (Perampanel) |
نعاس، وخمول، ودوخة، وازدواج في الرؤية، وترنح، وصداع، وطفح جلدي، وذهان، وتباطؤ في الإدراك. | هشاشة العظام، وفقر الدم. | متلازمة ستيڤنز-جونسون، ومتلازمة فرط التحسس الدوائي مع الأعراض الجهازية (Drug Reaction with Eosinophilia and Systemic Symptoms) . | الڤينوباربيتال (Phenobarbital) |
نعاس، وخمول، ودوخة، وازدواج في الرؤية، وترنح، ورعشة، وضمور مخيخي. | تضخم في اللثة، وهشاشة العظام، وتضخم العقد اللمفاوية. | مرضى الحصار القلبي الأذيني البطيني من الدرجة الثانية أو الثالثة. | فينيتوين (Phenytoin) |
نعاس، وخمول، ودوخة، وترنح. | جفاف في الفم، وزيادة في الوزن، ووذمة. | وذمة وعائية. | بريغابالين (Pregabalin) |
تباطؤ في الإدراك، ودوخة، فقدان الشهية. | فقدان الوزن، ومشاكل الجهاز الهضمي. | الجلوكوما، وفرط أمونيا الدم (Hyperammonemia)، ونقص التعرق مع ارتفاع الحرارة. | توبيراميت (Topiramate) |
دوخة، وازدواج في الرؤية، وترنح، ورعشة. | فرط الأمونيا، وقلة الصفيحات، والثعلبة، ومشاكل الجهاز الهضمي. | اضطراب دورة اليوريا، وخلل كبير في وظائف الكبد أو البنكرياس. | حمض ڤالبرويك (Valproic acid) |
النعاس، والخمول، وازدواج الرؤية، ورعشة العين، وتباطؤ الإدراك. | فقر الدم، وزيادة الوزن، وآلام المفاصل. | انقباض المجال البصري الثنائي الدائم (Permanent Bilateral Visual Field Constriction). | ڤيغاباترين (Vigabatrin) |
النعاس، والخمول، والدوخة، واضطرابات المزاج، وفقدان الشهية، وتباطؤ الإدراك. | فقدان الوزن. | متلازمة ستيفنز جونسون، ومتلازمة فرط التحسس الدوائي مع الأعراض الجهازية. | زونيساميد (Zonisamide) |
العلاج الغذائي ودوره في التحكم بالصرع
يُعدّ التدخل الغذائي أحد الأساليب العلاجية المساندة في السيطرة على الصرع، إذ تركز بعض الأنظمة الغذائية على تعديل التمثيل الغذائي للدماغ، بهدف تقليل النشاط الكهربائي غير الطبيعي، ومن بين هذه الأنظمة، يُعدّ النظام الغذائي الكيتوني من أكثر الأنظمة فعالية، ولا سيما في الحالات المقاومة للعلاج الدوائي. تعتمد الحمية الكيتونية (Ketogenic diet) على استهلاك كميات مرتفعة من الدهون، مع تقليل تناول الكربوهيدرات، ما يحفز الحالة الكيتونية (Ketosis)، إذ تُنتَج الكيتونات بوصفها مصدرًا بديلًا للطاقة في الدماغ، ما يسهم في تحسين الاستقرار العصبي وتقليل تكرار النوبات. يُستخدم هذا النظام غذائيًّا لعلاج الصرع وبعض الاضطرابات الموروثة في عملية الأيض، علاوة على ذلك، يُعتقد أن الصيام المتقطع (Intermittent fasting) يسهم في تقليل معدل النوبات، من خلال تنظيم التوازن العصبي وتقليل العمليات الالتهابية في الدماغ، ما يجعله خيارًا داعمًا في إدارة مرض الصرع.
علاوة على النظام الكيتوني، أثبتت أنظمة غذائية أخرى فعاليتها في بعض الحالات، مثل
النظام الغذائي منخفض المؤشر الغلايسيمي {{النظام الغذائي منخفض المؤشر
الغلايسيمي: (Low Glycemic Index Diet) نظام غذائي يركز على تناول أطعمة تُسبب ارتفاعًا بطيئًا ومتدرجًا في مستويات سكر الدم. مثل تناول كربوهيدرات بطيئة الامتصاص، ما قد يساعد في الحد من النوبات ويوفّر هذا النمط الغذائي فوائد واضحة في التحكم بالوزن، كما يُسهم في الوقاية من بعض الأمراض المزمنة مثل داء السكري من النوع الثاني.}} ونظام أتكينز المُعدَّل {{نظام أتكينز المُعدَّل: (Modified Atkins Diet) نظام غذائي منخفض الكربوهيدرات، يُتّبع بديلًا للحمية الكيتونية التقليدية. يتميز بأنه يسمح بمقادير أعلى نسبيًّا من البروتين والدهون مقارنة بالكربوهيدرات، ما يجعله خيارًا مفيدًا للتحكم في نوبات الصرع وتخفيض الوزن.}}، ومع ذلك، يجب تطبيق هذه الأنظمة تحت إشراف طبي متخصص لضمان تحقيق توازن غذائي مناسب، ولتجنب الآثار الجانبية المحتملة مثل نقص الفيتامينات والمعادن، ولا سيما عند الأطفال[16].
كذلك يوصى مرضى الصرع بضرورة الابتعاد عن المنبهات العصبية مثل الكافيين والكحول، إذ تؤثر هذه المواد في الجهاز العصبي المركزي، وقد تزيد من خطر حدوث النوبات.
كذلك الحد من استهلاك الأطعمة التي ترفع مستوى السكر في الدم، ولا سيما تلك التي تحتوي على كربوهيدرات ذات مؤشر غلايسيمي مرتفع، مثل الخبز الأبيض، والأرز الأبيض والبيتزا، والمشروبات الغازية، ويُنصح باستبدالها بخيارات ذات مؤشر غلايسيمي منخفض، مثل الأرز البني، والخبز المصنوع من الحبوب الكاملة، والبقوليات والبيض والخضروات الورقية، إذ تساعد هذه الأطعمة في استقرار مستويات الغلوكوز وتقليل من تذبذب الإنسولين، ما قد يكون له أثر إيجابي في التحكم بالنوبات.
كذلك ينصح بالحد من تناول الفواكه الغنية بالسكر، مثل المانغو والموز والتمر، إذ يمكن أن تؤدي إلى ارتفاع سريع في مستويات الغلوكوز في الدم، ويُفضل استبدالها بفواكه منخفضة السكر، مثل التوت والفراولة والأڤوكادو. يسهم الالتزام بهذه التوصيات الغذائية، إلى جانب المتابعة الطبية الدورية، في تحسين استقرار المرضى وتقليل تكرار النوبات، ما يعزز جودة حياة مرضى الصرع[17].
المراجع
Brodie, Martin J. “Antiepileptic Drug Therapy: The Story So Far.”
Seizure. vol. 19, no. 10 (2010). pp. 650-655.
Corrales-Hernández, María Gabriela et al. “Development of Antiepileptic Drugs Throughout History: From Serendipity to Artificial Intelligence.”
Biomedicines. vol. 11, no. 6 (2023).
Cramer, Joyce A. et al. “Adverse Effects of Antiepileptic Drugs: A Brief Overview of Important Issues.”
Expert Review of Neurotherapeutics. vol. 10, no. 6 (2010). pp. 885-891.
De Kinderen, Reina J. A. et al. “Side-Effects of Antiepileptic Drugs: The Economic Burden.”
Seizure. vol. 23, no. 3 (2014). pp. 184-190.
Ekstein, D. & S. C. Schachter. “Natural Products in Epilepsy—The Present Situation and Perspectives for the Future.”
Pharmaceuticals. vol. 3, no. 5 (2010). pp. 1426-1445.
French, J. A. & T. A. Pedley. “Clinical Practice: Initial Management of Epilepsy.”
New England Journal of Medicine. vol. 359, no. 2 (2008). pp. 166-176.
Katzung, B. G., S. B. Masters & A. J. Trevor.
Basic & Clinical Pharmacology. 12th ed. New York: The McGraw-Hill Companies, 2012.
Krasowski, M. D. “Therapeutic Drug Monitoring of the Newer Anti-Epilepsy Medications.”
Pharmaceuticals. vol. 3, no. 6 (2010). pp. 1909-1935.
Li, Cunjiang et al. “Antiepileptic Drug Combinations for Epilepsy: Mechanisms, Clinical Strategies, and Future Prospects.”
International Journal of Molecular Sciences. vol. 26, no. 9, article no. 4035 (2025).
Scheffer, I. E. et al. “ILAE Classification of the Epilepsies.”
Epilepsia. vol. 58, issue 4 (2017). pp. 512-521.
Thijs, R. D. et al. “Epilepsy in Adults.”
The Lancet. vol. 393, no. 10172 (2019). pp. 689-701.
Verrotti, Alberto et al., “Diet in the Treatment of Epilepsy: What We Know So Far.”
Nutrients. vol. 12, no. 9 (2020).
Westmark, Cara J. “Diet in the Treatment of Epilepsy.”
Nutrients. vol. 13, no. 3 (2021).
[1] B. G. Katzung, S. B. Masters & A. J. Trevor,
Basic & Clinical Pharmacology, 12th ed. (New York: The McGraw-Hill Companies, 2012); Martin J. Brodie, “Antiepileptic Drug Therapy: The Story So Far,”
Seizure, vol. 19, no. 10 (2010), pp. 650-655.
[2] María Gabriela Corrales-Hernández et al., “Development of Antiepileptic Drugs Throughout History: From Serendipity to Artificial Intelligence,”
Biomedicines, vol. 11, no. 6 (2023), p. 1632.
[3] Katzung, Masters & Trevor.
[4] J. A. French & T. A. Pedley, “Clinical Practice: Initial Management of Epilepsy,”
New England Journal of Medicine, vol. 359, no. 2 (2008), pp. 166-176.
[5] R. D. Thijs et al., “Epilepsy in Adults,”
The Lancet, vol. 393, no. 10172 (2019), pp. 689-701.
[6] Brodie.
[7] Corrales-Hernández et al.
[8] Katzung, Masters & Trevor.
[9] I. E. Scheffer et al., “ILAE Classification of the Epilepsies,”
Epilepsia, vol. 58, no. 4 (2017), pp. 512-521.
[10] Cunjiang Li et al., “Antiepileptic Drug Combinations for Epilepsy: Mechanisms, Clinical Strategies, and Future Prospects,”
International Journal of Molecular Sciences, vol. 26, no. 9, article no. 4035 (2025).
[11] Sills.
[12] Ibid.
[13] Ibid.
[14] Katzung, Masters & Trevor; Corrales-Hernández et al.; Scheffer et al.; Sills; M. D. Krasowski, “Therapeutic Drug Monitoring of the Newer Anti-Epilepsy Medications,”
Pharmaceuticals, vol. 3, no. 6 (2010), pp. 1909-1935.
[15] Joyce A. Cramer et al., “Adverse Effects of Antiepileptic Drugs: A Brief Overview of Important Issues,”
Expert Review of Neurotherapeutics, vol. 10, no. 6 (2010), pp. 885-891; Reina J. A. de Kinderen et al., “Side-Effects of Antiepileptic Drugs: The Economic Burden,”
Seizure, vol. 23, no. 3 (2014), pp. 184-190.
[16] Cara J. Westmark, “Diet in the Treatment of Epilepsy,”
Nutrients, vol. 13, no. 3 (2021), p. 917; Alberto Verrotti et al., “Diet in the Treatment of Epilepsy: What We Know So Far,”
Nutrients, vol. 12, no. 9 (2020).
[17] D. Ekstein & S. C. Schachter, “Natural Products in Epilepsy—The Present Situation and Perspectives for the Future,”
Pharmaceuticals, vol. 3, no. 5 (2010), pp. 1426-1445.